 組織工學의 원리
組織工學의 원리
組織工學
(組織工學,
英語
:
tissue engineering
)은 生物學的 組織을 改善하거나 代替하기 위해 細胞, 工學 및 材料 方法, 適切한 生化學 및 物理 化學的 要因의 組合을 使用한다. 組織工學이란 (줄기)細胞, 細胞가 附着되어 자랄 수 있는 支持體, 그리고 細胞의 成長 및 分化를 調節할 수 있는 各種 因子를 適切히 利用하여 여러 組織 再生, 및 나아가 臟器復元을 目標로 하는 硏究를 統稱하는 學問이다.
[1]
組織工學은 醫療 目的을 위한 새로운 生體 組織의 形成을 위한 발板(scaffold)의 使用을 包含한다. 한때 生體 物質(biomaterial)의 下位 分野로 分類되었지만 範圍와 重要性이 커지면서 獨立的인 分野로 看做될 수 있다.
組織工學의 大部分의 定義가 廣範圍한 應用 分野를 다루는 反面, 實際로 이 用語는 組織의 一部 또는 全體 (卽, 뼈, 軟骨
[2]
, 血管, 膀胱, 皮膚, 筋肉 等)의 改善 또는 代替하는 應用分野와 密接하게 關聯되어 있다. 種種, 關聯된 組織은 適切한 機能을 위해 특정한 機械的 및 構造的 特性을 必要로 한다. 이 用語는 人爲的으로 生成 된 支持 시스템 (예 : 人工 膵臟 또는 生物 人工 肝) 內의 細胞를 使用하여 特定 生化學 機能을 遂行하려는 努力에도 適用되었다. 再生 醫學이라는 用語는 組織工學과 同義語로 使用되는 境遇가 많지만 再生 醫學과 關聯된 用語는
줄기細胞
또는 電球 細胞(
en:progenitor cells
)를 使用하여 組織을 生産하는 데 더 重點을 둔다.
槪要
[
編輯
]
 Alcian blue로 染色 된 다양한 酸素 張力에서 C3H-10T1 / 2 細胞의 微細 質量 培養.
Alcian blue로 染色 된 다양한 酸素 張力에서 C3H-10T1 / 2 細胞의 微細 質量 培養.
랭거(Langer)
[3]
와 바캉티(Vacanti)
[4]
에 依해 一般的으로 適用되는 組織工學의 定義는 "生物學的 組織 機能 또는 全體 機關(organ)을 復元, 維持 또는 改善하는 生物學的 代替物의 開發에 對한 工學 및 生命 科學의 原理를 適用하는 學制 間(融合) 分野이다".
[5]
組織工學은 또한 "組織 成長 原理를 理解하고 臨床 適用을 위한 機能的 代替 組織을 生産하기 危害이 技術을 適用하는 것"으로 定義되어 있다.
[6]
追加 說明은 "組織工學의 基本 家庭은 시스템의 自然 生物學의 使用이 組織 機能의 代替, 改善, 維持 및 / 또는 向上을 目標로하는 治療 戰略을 開發함에 있어 더 큰 成功을 可能케 할 것이라는 點이다."
[6]
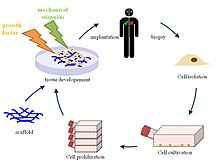
組織 工學을 簡略히 說明하면, 患者의 組織에서 分離하여 培養한 細胞들을 生分解性 高分子 物質로 만든 多孔性의 支持體(스캐폴드)에 附着시켜 移植하거나 體外에서 一定 期間 동안 培養하여 새로운 生體組織을 만드는 것이다. 細胞는 附着해서 자라려는 性質이 있기 때문에 이 環境을 提供하여 줄 支持體가 必要하다. 多孔性의 스캐폴드는 三次元的 構造物을 提供하여 細胞가 附着하고 分裂하여 새로운 組織을 形成하도록 한다. 移植된 細胞가 細胞外 氣質을 分泌하며 組織을 形成하는 동안 生分解性 高分子 物質로 만든 支持體는 分解되어 몸 밖으로 排出되어 人體組織의 成分과 같은 成分을 가진 새로운 組織이 形成된다.
組織工學을 利用해 만들어진 새로운 組織이 元來 機能을 가지기 위해서는 移植된 細胞의 遺傳子 發現이 組織形成 過程 中 適切하게 制御되어야 한다. 細胞의 遺傳子 發現은 周圍 環境과의 相互作用에 依해 調節되는데, 이 相互作用에는 細胞附着 表面과의 作用, 成長因子나 호르몬과의 作用, 그리고 物理的 刺戟과의 作用이 있다. 人體의 組織에서 콜라젠 等의 細胞外 氣質이 細胞附着 領域, 成長因子, 그리고 物理的 刺戟을 提供하듯이, 組織工學에서는 支持體가 이들 特定因子들을 移植된 細胞에 適切하게 提供하여야 한다.
[1]
細胞
[
編輯
]
組織 工學은 살아있는 細胞를 利用한다. 살아있는 細胞는 移植 後 移植물로 移動하거나, 移植 前에 細胞培養에서 매트릭스(matrix)와 聯關될 수도 있다. 이러한 細胞는 再生性되길 願하는 組織의 完全히 分化된 細胞로서 分離되거나, 다른 組織 또는 줄기細胞 供給源으로부터 分離될 때 願하는 機能을 生成하도록 操作될 수 있다.
[7]
組織工學에 利用되는 細胞에 對해 알아보면 初期에는 케라틴細胞, 纖維母細胞, 軟骨細胞 等 性體細胞를 利用하였으나 培養過程에서 細胞星霜이 바뀔 수 있고, 增殖에 限界가 있어 最近에는 다양한 分化陵과 無限한 自家再生陵을 지닌
줄기細胞
가 主로 利用되고 있다. 特히
胚芽줄기細胞
는 全分化能이 있어 모든 組織으로 分化될 수 있으나 그 不安定性과 畸形腫 發生 可能性이 問題視 된다. 骨髓組織이나 地方 組織에 있는 中胚葉性
聖體줄기細胞
는 骨細胞, 軟骨軟骨細胞, 脂肪細胞, 筋細胞 等으로 分化시킬 수 있어 組織工學 硏究에 많이 利用된다.
[8]
組織工學에 利用되는 細胞는 使用되는 供給源이 自家(autologous)인지, 同種(allogenic)인지, 李鍾成(xenogeneic)인지 區別된다. 表에서 보여주는 것처럼 各各의 長短點이 있다.
[9]
組織工學에 利用되는 細胞는 免疫拒否 反應을 避하기 위해서 自家細胞가 바람직하다.
[8]
組織工學에 利用되는 細胞 供給源
[9]
| 種類
|
|
| 自家(Autologous)
|
患者 自身의 細胞;
免疫 拒否 反應이 없지만, 宿主로부터 제공받지 않는이상 卽時 使用할 수 없음.
|
| 同種(allogeneic)
|
다른 사람의 細胞;
卽時 使用可能하지만, 免疫 拒否 反應이 있을 수도 있음.
|
| 異種(xenogeneic)
|
다른 種:
免疫 拒否 反應이 있을 수도 있을 뿐만 아니라, 動物 바이러스 傳播와 關聯이 있음.
|
줄기細胞
[
編輯
]
組織 工學의 主要 焦點은 줄기細胞 機能을 制御하는 手段으로서 適切한 特性을 機能性 갖는 重合體를 利用하는 것이다. 줄기細胞의 分化 潛在力에 기초하여, 組織 工學에 使用되는 줄기細胞는 pluripotent stem cell(全分化能 줄기細胞) 과 mutipotent stem cell(多能性 줄기細胞)의 두가지 範疇로 나눌 수 있다. 全分化能 줄기細胞에는
胚芽줄기細胞
뿐만 아니라
誘導萬能줄기細胞
를 包含한다.
[10]
스캐폴드
[
編輯
]
 組織 工學의 스캐폴드로 많이 利用되는 炭素 나노튜브
組織 工學의 스캐폴드로 많이 利用되는 炭素 나노튜브
血液 細胞와는 달리, 人間 組織 大部分의 正常 細胞들은
細胞外 氣質
(extracellular matrix, ECM)라 불리는 固體型 매트릭스와 相互作用하며 살아간다. 組織 工學 分野는 組織과 機關의 再生을 위한 適切한 環境을 提供하기 爲해 多孔性 3D 스캐폴드의 使用에 依存한다. 이 스캐폴드는 組織 形成을 爲한 鑄型으로 作用하고, 細胞 및 成長 因子들이 '심어져 있거나',
生物反應機
形態의 生體 物理的 刺戟을 받는다.
[11]
엔지니어링된 組織을 위한 最上의 스캐폴드는 本來 狀態의 타겟 組織의 細胞外 氣質이어야 한다. 그러나, 本來 組織에서의 多重 機能, 複雜한 構成 및 細胞外 氣質의 動的 性質은 正確하게 模倣하기 어렵다. 그래서 組織 工學에서 스캐폴딩의 槪念은 部分的으로 本來의 細胞外 氣質의 機能을 模倣하는 것이다. 卽, 엔지니어링된 組織에서 스캐폴드가 遂行하는 重要한 役割은 本來 組織에서 細胞外 氣質의 機能과 類似하며 建築學的, 生物學的, 機械的 特徵과 關聯이 있다.
[12]
- 生體 適合性
: 組織工學에서 스캐폴드의 첫番째 基準은 生體 適合性이어야 한다. 스캐폴드는
in vitro culture
(
人 비트로
, 試驗管 內 培養) 및
in vivo implantation
(
人 비보
, 生體 內 移植) 동안 外部에서 提供되거나
內因性
細胞(endogenous cell)李 附着, 成長 및 分化되도록 支援해야한다. 細胞는 새로운 매트릭스 아래에 놓이기 前에 附着되어야 하고, 正常的으로 기능하며, 表面 위로 移動하고, 結局 스캐폴드를 통해 增殖하기 始作해야한다. 移植 後, 스캐폴드 또는 엔지니어링된 組織 構造物은 免疫 拒否 反應을 막기 위해
[11]
스캐폴드를 製造하는데 使用된 生體 物質(biomaterial)은 宿主 組織에서 造作된 組織 및 內因性 細胞의 構成 成分과 互換的이어야 한다.
- 建築學的 特徵: 스캐폴드는 移植時 宿主 組織과의 統合을 促進하기 위해 血管生成火, 새로운 組織 形成 및 리모델링을 위한 빈 空間을 提供해야 한다. 스캐폴드를 構成하는 生體 物質들은 스캐폴드의 機械的 安定性을 크게 損傷시키지 않으면서 效率的인 營養素 및 代謝 産物 輸送을 위한 높은 多孔性의 構造를 提供하도록 加工되어야 한다. 더욱이, 生體 物質은 發生되는 組織에 依해 새롭게 만들어지는 매트릭스 生産 速度에 맞추어 移植 後 分解될 수 있어야 한다(
生分解性
).
[13]
- 生體 活性: 스캐폴드는 엔지니어링된 組織의 細胞 構成 要素와 活潑하게 相互作用하여 活動을 促進하고 調節할 수 있다. 生體 物質은 附着力을 向上시키기 위한 細胞-附着
리간드
와 같은 生物學的 信號 또는 細胞 模樣 및 整列에 影響을 주는 物理的 信號를 包含 할 수 있다. 또한 스캐폴드는 再生 速度를 높이기 위한 成長 因子와 같은 外部 成長 刺戟 信號를 위한 傳達 輸送體 또는 貯藏所로서 作用할 수 있다. 이와 關聯하여, 生體 物質은
生體分子
와 互換될 수 있어야 하며, 生體 活性이 維持된 生體分子의 放出을 制御하기 위한 캡슐化 技術을 使用할 수 있어야 한다.
- 機械的 性質: 스캐폴드는 組織 缺陷에 機械的 및 形態 安定性을 提供한다. 스캐폴딩에 使用되는 生體 物質의 固有한 機械的 特性 또는 프로세싱 後 特性은 宿主 組織의 固有한 機械的 特性과 一致해야 한다.
[12]
材料
[
編輯
]
스캐폴드를 構成하는 많은 物質들(天然 및 合成 物質, 生分解性 및 永久 物質 等)李 硏究되었다.
[14]
이들中 大部分은 이미 生體 吸收性 封合 材料로 使用되는 硏究 主題로서, 組織 工學이 登場하기 以前에 醫療 分野에서 알려져왔다. 이들 物質의 例로
콜라겐
및 一部 폴리에스테르가 있다.
폴리락트산
(PLA),
폴리글리콜山
(PGA),
폴리카프롤락톤
(PCL)과 같은 폴리 락톤과 複合體들은 生體 適合性이 優秀하기 때문에 固定物로 가장 一般的으로 使用되는 合成 生分解性 폴리머街되고 있다.
[15]
새로운 生體 物質은 理想的인 特性과 注入 可能性, 合成 製造, 生體 適合性, 免疫 適合性, 透明性, 나노 크기의 纖維, 低濃度, 再吸收率 等 機能的으로 맞춤化되도록 設計되었다. Zhang, Rich, Grodzinsky, Langer의 MIT 硏究室에서 만들어진 PuraMatrix는 現在 商用化되어 臨床 組織 工學에 影響을 미치는 새로운 生體 模倣 스캐폴드 製品群 中 하나이다.
[16]
一般的으로 使用되는 合成 物質은
폴리락트산
(PLA, polylactic acid)이다. PLA는 人體 內에서 分解되어 몸에서 쉽게 除去할 수 있는
젖酸
(lactic acid)를 形成하는 폴리 에스테르이다.
[17]
폴리글리콜山
도 多樣한 醫療 分野에서 利用되는 生分解性 脂肪族 폴리에스테르이다. 이 PGA의 모노 필라멘트들은
in vivo
(生體 內)에서 2-4週만에 分解될 수 있다.
[18]
폴리카프롤락톤은 폴리락트산에 비해 分解速度가 宏壯히 느리다. 쥐에서의 生體 內 分解가 3年동안이나 觀察되었다. 그래서 長期間 移植 및 藥물 放出 制御 應用分野에서 널리 使用되고 있으나, 느린 分解 速度 等으로 인해 組織 工學에서는 短點을 가지고 있다.
[19]
[20]
主로 쓰이는 폴리에스테르들은 生體 活性 減少로 인한 免疫 拒否 反應을 包含하여 短點이 있다. 또한 폴리락트산과 폴리글리콜産銀 加水分解에 依해 分解되면서 二酸化炭素를 生成하고 pH를 낮추어 酸性環境을 만들게 된다. 甚한 境遇 組織 壞死를 誘導할 수 있다.
[8]
이러한 限界를 克服하기 위해 最近, 폴리에스테르와 하이드로 겔 材料를 統合하여 複合 材料를 開發하고 있다. 하이드로겔은 親水性으로 물을 吸收할 수 있으며 種種 疏水性 폴리머(폴리에스테르 等)와 比較해 優秀한 生體 適合性을 보인다. 그러나, 하이드로겔은 弱한 機械的 强度를 나타내며 壓力이나 水蒸氣 條件下에서 材料가 쉽게 變形될 수 있다.
[21]
스캐폴드는 天然材料로도 構成될 수 있다. 天然 材料로는 콜라겐, 피브린, 젤라틴같은 蛋白質, 히알루로난, 아가로스, 遏止네이트, 키토산 같은 多糖類 等이 있다. 天然 材料로 만들어진 스캐폴드는 一般的으로 優秀한 生物學的 互換性을 갖지만, 機械的 安定性이 缺如되며, 天然 材料의 供給, 加工, 疾病 傳播可能性에 對한 問題가 있다.
[22]
 組織 工學을 利用해 만든 血管
組織 工學을 利用해 만든 血管
組織工學 스캐폴드로 使用될 多孔性 構造를 만들기 위한 다양한 方法들이 있다. Principles of Tissue Engineering, 3rd(Robert Lanza, Robert Langer, Joseph Vacanti)를 參考해서 作成함.
纖維 結合法(fiber bonding)
[
編輯
]
polymer fiber는 細胞 附着을 위해 훌륭한 表面的 臺 부피 比率을 보이므로 좋은 스캐폴드 材料이다. 가장 初期의 組織 工學 스캐폴드는 機械的 安定性이 缺如된 纖維 메쉬, 祕結合 PGA 테瑟 또는 펠트였다. 이 問題를 克服하기 위해 纖維 結合 技術은 纖維를 交叉點에서 서로 結合시키는 方式으로 發展했다. 纖維 스캐폴드의 一般的인 例는 PGA와 PLLA를 使用한다. PGA 纖維들은 짜여진(nonwoven) 메쉬로 配列된다. 重合體의 녹는點 以上의 溫度에서 纖維들은 纖維들끼리의 接觸點에서 結合할 것이다. 융龍 重合體(melting polymer)의 構造的 崩壞를 防止하기 爲해, PGA 纖維는 熱處理 前에 캡슐化 過程을 거친다. 鹽化 메틸렌(methylene chloride)에 溶解된 PLLA로 메쉬 纖維를 감싸고 건조시켜 PGA-PLLA 複合 매트릭스를 만든다. 熱處理 및 纖維 結合 後, PLLA를 鹽貨메틸렌으로 녹인 後, 眞空 建造에 依해 溶媒를 스캐폴드로부터 除去한다.
[24]
또다른 方法으로는 얽혀있는(nonwoven) PGA 纖維 케쉬를 원자화된 PLLA 또는 PLGA 溶液으로 噴射하면서 회전시키는 方法이 있다.
[25]
纖維 結合法으로 生成한 스캐폴드는 單純性, PGA 纖維의 特性 維持, 生體 適合性 材料만 使用, 테瑟 또는 펠트 配列에 對한 構造的 利點을 가진다는 點에서 좋은 方法이다. 그러나 氣孔率 및 氣功 크기에 對한 制御, 적합한 溶媒의 利用可能性, 溶解 狀態의 두가지 重合體의 無害性, 重合體에 必要한 相對的인 融解 溫度 等이 短點으로 나타난다.
電氣放射法(electrospinning)
[
編輯
]
 電氣放射法
電氣放射法
PGA, PLGA, PCl을 包含한 많은 生體適合性 重合體는 多孔性이 90% 以上인 나노纖維의 構造物에 電氣的 結合을 할 수 있다.
[26]
選擇한 폴리머를 適切한 溶媒(예: 클로로포름에 PCL)에 녹여 準備한다. 폴리머 溶液은 注射器에 積載된 後 注射器 펌프를 통해 일정한 比率로 金屬 毛細管을 통해 排出된다. 高電壓(10-15kv)을 毛細管에 加하여 폴리머를 接해있는 表面을 向해 輩出한다. 얇은 纖維들이 plate에 組立되면서 溶媒는 蒸發하고 짜여진(nonwoven) 多孔性 비계만 남는다. 纖維 두께, 스캐폴드 直徑 및 平均 氣功 直徑은 重合體 濃度, 溶媒의 選擇, 放出 速度, 認可 電壓, 毛細管 直徑, 毛細管과 表面 사이의 距離를 包含하는 因子에 依해 調整된다. 이러한 理由로, 電氣放射法은 많은 實驗室에서 스캐폴드 製造의 一般的인 方法이 되었다.
廉浸出法(solvent casting and particulate leaching)
[
編輯
]
廉浸出法(solvent casting and particulate leaching, SCPL)은 規則的인 多孔性을 가진 構造物을 만들 수 있지만, 이 構造物의 두께는 制限되어 있다. 重合體를 적합한 有機溶媒에 녹이고(예: 폴리 락트산을 다이클로메탄(dichloromethane)에 溶解시킬수 있음) 녹인 重合體를 적합한 氣孔誘導物質(porogen) 周圍에 캐스팅한다. 그리고 重合體를 乾燥하고 굳힌 後, 氣孔誘導物質을 浸出시켜 相互連結된 多孔性 네트워크를 가진 重合體 스캐폴드를 만들 수 있다. 이러한 氣孔誘導物質로 염화나트륨(sodium chloride)같은 武器 廉, 社카로스 決定(crystals of saccharose), 젤라틴 具體(gelatin spheres), 파라핀 具體(paraffin spheres)가 使用된다. 多孔性 스캐폴드는 氣孔誘導物質의 製作 媒介變數 및 類型, 量, 크기를 調整함으로써 맞춤 製作이 可能하다. 氣孔誘導物質의 크기는 스캐폴드 氣功의 크기에 影響을 미치는 反面, 重合體 臺 氣孔誘導物質 比率은 最終 救助의 多孔性의 量과 直接的으로 關聯된다. SCPL의 短點으로는 스캐폴드에 심어진 細胞의 損傷을 避하기 위해 使用되는 有機 溶媒를 完全히 除去해야 한다.
鎔融 成型法(melt molding)
[
編輯
]
立體 스캐폴드의 製造를 위한 다른 方法은 융龍 成型法이다. 이 技術은 重合體와 氣孔誘導物質 粒子가 몰드에서 結合되어 重合體의 有利 轉移 溫度(非結晶性 重合體의 境遇) 또는 융龍 溫度(飯 決定 重合體의 境遇) 以上으로 加熱되도록 要求한다. 重合體의 再構成 後, 複合 材料를 몰드로부터 꺼내어 冷却시키고, 適切한 液體에 浸漬시켜 誘導物質粒子를 浸出시킨다. 生成된 多孔性 스캐폴드는 틀과 同一한 外部 形象을 갖는다.
막 라미네이션(membrane lamination)
[
編輯
]
組織 工學은 種種 뼈와 軟骨과 같은 模樣 依存的 機能을 가진 단단한 組織을 위해 正確한 3次元 解剖 構造를 必要로 한다. melt molding으로 製造된 多孔性 重合體의 얇은 層은 막 라미네이션에 依해 切斷, 積層, 및 結合될 수 있다.
[27]
層들은 化學的으로 結合되지만, 2個의 隣接한 幕의 境界面에는 뚜렷한 境界가 없다. 이 方法의 核心은 願하는 스캐폴드 模樣의 3次元 等高線圖를 만드는 것이다. 스캐폴드의 各 層은 多孔性 幕에서 該當 레벨에 맞는 模樣으로 切斷된다. 클로로포름과 같은 少量의 溶媒가 界面 表面에 코딩되어 있고, 막 사이에 結合이 形成되어 있다. 이 過程은 最終 3次元 構造가 完成될 때까지 모든 後續 層에 對해 反復된다. 막 라미네이션에 使用되는 多孔性 重合體는 SCPL에 依해 形成된 PLA 및 PLGA 幕이 包含된다. 앞서 言及된 바와 같이 完成된 스캐폴드의 層들 사이에는 檢出可能한 境界가 없다. 막 라미네이션은 個別的인 膜과 同一한 벌크 特性을 갖는 3次元 解剖學的 形態를 製造하는 方法을 提供한다.
 壓出法
壓出法
壓出法(extrusion)
[
編輯
]
組織工學을 위한 重合體의 첫番째 壓出法은 PLGA 및 PLLA를 利用하여 末梢神經 再生을 위한 관형 스캐폴드를 形成한 것이다.
[28]
氣孔誘導物質로 염화나트륨을 使用하여 solvent casting을 使用하여 重合體를 膜으로 製造하였다. 製造된 막을 適切한 크기로 切斷하고 맞춤型 壓出 道具에 넣는다. 壓出機는 複合 材料에 熱과 壓力을 加하고 노즐을 통해 圓筒形 導管을 形成하도록 壓力을 加한다. 導管을 식힌 後, 물에 담가 염화나트륨을 浸出하고 眞空 건조시킨다. 溫度가 높을수록 壓力이 낮아지고 溫度가 낮을수록 壓力이 높아진다. 高壓에는 强力한 油壓 프레스가 必要할 수 있지만, 高溫은 스캐폴드의 決定도 및 多孔性, 混入된 生體 分子의 活性에 惡影響을 줄 수 있다. 壓出法 또한, 다른 方法과 마찬가지로 氣孔誘導物質 含量 및 크기는 多孔性 및 平均 氣功 直徑의 가장 重要한 媒介 變數이다. 壓出된 重合體 스캐폴드는 細胞의 移動 또는 組織 工學을 위한 成長因子를 支援하기 위해 製作할 수 있다.
凍結 乾燥法(freeze-drying)
[
編輯
]
制御 可能한 多孔性 및 平均 氣功 直徑을 가지는 스캐폴드의 迅速한 製造를 위한 方法 中 하나이다. 重合體를 適切한 溶媒(예: 폴리 락트산을 다이클로메탄(dichloromethane)에 溶解시킬수 있음)에 溶解시킨 다음 물을 重合體 溶液에 添加하고 두 液體를 混合하여 에멀젼을 얻는다.
[29]
生成된 에멀젼을 몰드에 붓고 液體 窒素로 凍結시킨다. 凍結 建造는 물과 溶媒를 除去하여 高度로 相互 連結된 氣功, 最大 90%의 氣孔率 및 15~35um의 平均 氣功 直徑의 스캐폴드를 生成한다. 이 技術은 PGA, PLLA, PLGA 및 PPF(poly(propylene fumarate)를 包含한 많은 生體 適合性 重合體와 함께 使用되었다. 에멀젼과 凍結 乾燥를 使用하는 方法은 SCPL처럼 固體 氣孔誘導物質을 使用할 必要가 없다. 또한 SCPL처럼 時間이 많이 걸리는 浸出 段階가 必要하지 않기 때문에 빠르게 準備되지만 如前히 溶媒를 使用해야 한다. 또한 만들어진 氣功 크기가 작고 氣孔率이 種種 不規則하다.
上 分離法(phase separation)
[
編輯
]
分解 可能한 組織 工學 스캐폴드로부터 藥물과 다른 生體 活性 分子를 傳達할 수 있는 可能性은 細胞 分化를 調節하고 組織 再生을 誘導하는데 유리하다. 이러한 스캐폴드는 生體 活性 分子를 有機 化學 物質이나 極限 溫度에 露出시키지 않는 賞 分離 技術에 依해 生成될 수 있다.
[30]
PLGA 또는 poly(phosphoester)와 같은 生體 適合性 重合體는 適切한 溶媒(예: 552°C에서 페놀, 63°C에서 다이獄山(dioxane), 85°C에서 나프탈렌)에 溶解된다. 흔들어 섞는 동안, 生體 活性 分子를 均質 混合物에 添加되어 分散시키고, 液狀이 分離될 때까지 溶媒 戎點 未滿으로 冷却시킨다.
[31]
重合體 및 溶媒는 液體 窒素로 急冷함으로써 2床 固體를 얻을 수 있다. 溶媒는 昇華에 依해 除去하여, 重合體 內에 生體 活性 分子가 있는 多孔性 스캐폴드를 生成한다. 多孔性 및 構造는 重合體에 對한 溶媒의 冷却 速度 및 융龍 溫度에 依해 影響을 받는다. 特定 藥물 放出 速度를 調整하고 큰 蛋白質을 包含시키는 것은 賞 分離 方法에 있어 主要 障礙物이다.
가스 포밍法(gas foaming)
[
編輯
]
SCPL에 對한 가장 큰 問題點은 有機 溶媒의 使用이다. 有機 溶媒의 殘留物은 注入 後 炎症反應을 일으킬 수 있다. 이를 避하기 위해 가스 포밍法을 使用한다. 壓縮된 重合體 디스크(예: PLGA)는 高壓 CO2로 處理된다. 壓力은 漸次 大氣 水準으로 回復된다. 壓力이 減少함에 따라, 壓力의 量과 減少 速度에 따라 重合體 매트릭스에서 核 形成 및 氣孔이 形成된다. 平均 긱洪 크기는 100um~500um의 範圍이다.
[32]
氣功은 重合體를 떠나는 CO2分子에 依해 形成되어 스펀지型 構造를 生成한다. 이 技術의 主要 問題點은 壓縮 成形동안 使用된 過度한 熱과 孔隙이 相互連結된 構造를 形成하지 않는다는 것이다.
펩타이드 自家 組立法(peptide self-assembly)
[
編輯
]
1990年代 中盤 以後, 組織 工學 스캐폴드에서는 合成 ECM에서의 펩타이드 나노 纖維 使用을 硏究한다. 콜라겐, 젤라틴 및 피브린과 같은 다른 生物學的 由來 物質은 合成 重合體와 比較하여 細胞와 友好的으로 相互作用할 수 있지만, 펩타이드 纖維는 自家 組立되어 나노 規模에서 安定的이고, 高度로 整列된 스캐폴드를 形成할 수 있다.
[33]
自家 組立 펩타이드는 疏水性 및 親水性 도메인을 번갈아 가지는 이온性 自家 相補的 序列로 構成된다.
[34]
自家 組立 펩타이드 救助는 나노 規模에서 形成되며, 附着된 細胞가 本來의 3次元 形態를 維持하게끔 하며, 一部 마이크로스케일 表面에 附着된 細胞처럼 平平해지지 않을 수 있다. 아미노산 序列에서 荷電된 疏水性 殘期의 間隔을 調節함으로써, 形成된 스캐폴드의 幾何學的 構造가 操作될 수 있다. 펩타이드 分子 內部와 그 사이의 非共有 結合 및 이온 相互作用은 合成 生物學的 시스템에서 機能的 및 動的 構造를 生成한다. 隣接한 纖維는 시스테인 殘期의 配置에 依해 이환화 結合으로 永久的으로 交叉連結될 수 있다. 自家 組立 펩타이드는 물 또는 生理學的 溶液에서 一般的으로 安定한 β-sheet를 形成한다. 兩極性 펩타이드는 시트, 莫大, 區, 디스크와 같이 더 複雜한 構造를 形成하는 것으로 나타났다. 스캐폴드 組立 및 크기는 pH, 펩타이드 濃度, 2街 이온 誘導에 依해 制御될 수 있다.
組織 培養
[
編輯
]
大多數의 境遇에, 試驗管 內(
in vitro
)에서 機能性 組織 및 生物學的 構造의 生成은 生存, 成長, 機能 誘導를 促進하기 위해 廣範圍한 培養이 必要하다. 一般的으로 細胞는 酸素, pH, 濕度, 溫度, 營養素 및 渗透壓 維持를 包含한 培養 環境을 맞추어주어야 한다. 組織 工學的 培養은 培養 條件을 維持하는데 追加的인 問題가 있다. 標準 細胞 培養에서 擴散은 營養素 및 代謝 産物 輸送의 唯一한 手段이다. 그러나, 造作된 機關 및 全體 組織의 境遇와 같이 培養물이 더 크고 複雜해지면, 組織 內에 毛細管 네트워크의 生成과 같은 다른 메커니즘을 함께 使用하여 培養물을 維持해야 한다. 組織 培養으 또 다른 問題는 機能을 誘導하는데 必要한 適切한 因子 및 刺戟을 導入하는 것이다. 大部分의 境遇, 簡單한 培養 方法(維持하는 것 等)으로는 充分하지 않다. 成長 因子, 호르몬, 特定 代謝 産物 또는 營養素, 化學的 및 物理的 刺戟이 種種 要求된다. 例를 들어, 骨格 發達(skeletal development) 中 낮은 酸素 環境이나 저산소에 適應해야 하는 軟骨細胞(chondrocytes)와 같이, 正常的인 發達過程 中 一部로서 酸素 張力의 變化에 反應해야 한다. 內皮細胞(endothelial cell)와 같은 다른 細胞들은 血管에서 마주치는 遺體 흐름으로 因한 切斷(shear) 스트레스에 反應한다. 壓力 펄스와 같은 機械的 刺戟은 心臟 瓣膜, 血管 또는 心囊과 같은 모든 種類의 心血管 組織에 이로운 것으로 보인다.
生物反應機(Bioreactor)
[
編輯
]
 血管 移植을 위한 生物反應機
血管 移植을 위한 生物反應機
生物反應機
或은 生體反應器라고도 한다. 組織 工學에서의 生物反應氣는 試驗管 內에서(
in vitro
)에서 細胞 또는 組織 成長을 促進시키기 위해 生理學的 環境을 시뮬레이션하는 裝置이다. 生理學的 環境은 溫度 및 酸素 또는 二酸化炭素 濃度와 같은 다양한 媒介 變數로 構成될 수 있지만 모든 種類의 生物學的, 化學的 또는 機械的 刺戟으로 넓혀질 수도 있다. 따라서, 2次元 또는 3次元 環境에서 組織에 힘 또는 應力, 甚至於 電流의 힘도 包含할 수 있는 시스템이다.
學術 및 産業 硏究 施設에서, 生物反應氣는 成長 中인 組織의 特定 生理的 環境을 複製하도록 開發되는 것이 一般的이다(예: 心臟 組織 成長을 위한 流動性있는 傳單)
[35]
. 여러 一般 用途와 應用 分野別 生物反應祈禱 商業的으로 使用할 수 있으며, 政敵 化學 刺戟 또는 化學的 및 機械的 刺戟의 組合을 提供할 수 있다.
3D 細胞 培養을 위해 만들어진 다양한 生物反應機가 存在한다. 작은 플라스틱 圓筒形 챔버와 有利 챔버가 있으며, 內部 濕度와 水分이 調節되어 細胞를 3次元으로 성장시키기 위해 特別히 設計되었다.
[36]
生物反應氣는 폴리에틸렌테레프탈레이트(polyethylene terephthalate) 膜과 같은 生物 活性 合成 物質을 使用하여 높은 水準의 營養分을 維持하는 環境에서 스페로이드 細胞들을 둘러싼다.
[37]
이들은 쉽게 열고 닫을 수 있어 테스트를 위해 스페로이드를 除去할 수 있지만, 챔버는 100% 濕度를 維持할 수 있다.
[38]
이 濕度는 最大 細胞 成長 및 機能을 達成하는데 重要하다. 生物反應機 챔버는 3次元에 걸쳐 各 方向에서 均一한 細胞 成長을 保障하기 위해 回轉하는 더 큰 裝置의 一部이다.
[38]
現在 싱가포르 Quintech Life Sciences가 運營하는 QuinXell Technologies는 組織 工學을 目的으로 만들어진 TisXell Biaxial Bioreactor로 알려진 生物反應氣를 開發했다. 이는 世界 最初로 兩軸 回轉이 있는 舊型 有利 챔버를 가진 生物 反應岐路, 特히 子宮 내 胎兒의 回轉을 模倣하기 爲한 것이며, 이것은 組織의 成長에 도움이 되는 環境을 提供한다.
[39]
MC2 Biotek은 가스 交換을 使用하여 細胞室 內에서 높은 酸素 水準을 維持하는 ProtoTissue
[36]
로 알려진 生物反應氣를 開發했다. 酸素 水準이 높을수록 細胞가 成長하고 正常的인 細胞 呼吸을 할 수 있다는 點이 以前의 生物反應기보다 向上된 點이다.
長纖維 生成(long fiber generation)
[
編輯
]
2013年, 도쿄 大學校에서 最大 1m 길이, 100μm 크기의 細胞 적制 纖維를 開發했다.
[40]
이 纖維는 이中 동축 層流 흐름을 形成하는 微細 流體 裝置를 使用하여 만들어졌다. 微細 流體 裝置의 各 '層'은 ECM, 하이드로겔 被服, 最終的으로 염화칼슘 溶液에 심어진 細胞들이다. 하이드로겔 被服 안에 심어진 細胞는 며칠동안 培養된 後, 이 被服은 살아남은 細胞 纖維로 除去된다. ECM core에 揷入되는 細胞의 種類는 다양하며, 筋細胞(myocytes), 內皮 細胞(endothelial cells), 神經 細胞 纖維(nerve cell fibers), 上皮 細胞 纖維(epithelial cell fibers)가 있다. 이 그룹들은 纖維를 짜는 것과 類似한 메커니즘으로 組織이나 機關을 製作하기 위해 纖維가 함께 만들어질 수 있음을 보여주었다. 纖維質 形態는 傳統的인 스캐폴드 디자인에 對한 代案을 提供한다는 點과 筋肉을 비롯한 많은 機關이 纖維質 細胞로 構成되어 있다는 것이 하나의 長點이다.
生體 人工 機關(Bioartificial organ)
[
編輯
]
人工 將棋란, 人間이 人工 臟器를 代替하기 위해 人間에게 移植되거나 統合된 人工 裝置로, 特定 機能이나 關聯 機能을 復元하여 患者가 最大限 빨리 正常的인 生活로 돌아올 수 있도록 한다. 交替된 機能이 반드시 生命 維持와 關聯이 있을 必要는 없지만 種種 關聯이 있기도 하다. 組織 工學의 窮極的인 目標는 '特別히 注文하거나 디자인 하지 않아도 되는 旣成'의 生體 人工 機關과 身體의 損傷된 組織 再生을 許容하는 것이다. 患者 줄기 細胞로부터 生體 人工 機關을 成功的으로 生成하기 위해, 硏究者들은 組織 工學에 依한 複合 組織의 生成을 持續的으로 改善하고 있다. 例를 들어, 細胞의 微細 環境에 存在하는 나노 規模 信號를 理解하기 위한 많은 硏究가 이루어지고 있다.
[41]
生體 模倣 技術(Biomimetics)
[
編輯
]
生體 模倣 技術은 自然에 存在하는 것들을 複製하는 物質 및 시스템을 生産하는 것을 目標로 하는 分野이다.
[42]
組織 工學의 脈絡에서, 이것은 엔지니어가 構造, 特性 및 生體 適合性 側面에서 本來의 組織에 匹敵하는 材料를 만들기 위해 使用하는 一般的인 接近 方式이다. 材料의 特性은 該當 材料의 物理的, 構造的 및 化學的 性質에 크게 左右된다. 結果的으로 시스템 設計에 對한 生體 模倣的 接近 方式은 材料를 합치는 過程에서 重要해질 것이며, 生物學的 過程과 相互作用에 對한 充分한 理解가 必要할 것이다. 生物學的 시스템 및 公正의 複製는 生物學的 材料를 만들기 위한 狀態를 위해 生體 刺戟 物質의 合成에 使用될 수도 있다. 따라서, 構造的·化學的으로 生體 組織과 同一한 特性을 가진 物質이 合成된다면, 이 物質은 生體 組織과 類似한 性質을 가질 것이다. 이 技術은 人間의 問題에 對한 解答으로 自然 現象에서 解答을 찾는다는 아이디어에서 始作된 廣範圍한 歷史를 가지고 있다. 航空機, 自動車, 建築, 甚至於 産業 시스템을 包含한 것들이 自然系에서 靈感을 받아 技術을 發展을 이룬 것이다. 나노 技術의 發展으로 이 技術을 組織 工學을 包含한 마이크로 및 나노 스케일 問題에 適用하기 始作했고. 合成 뼈 組織, 血管 技術, 스캐폴딩 材料 및 統合 技術, 나노 粒子를 開發하는데 使用되었다.
[42]
各州
[
編輯
]
- ↑
가
나
“:: 서울大學校 줄기細胞 및 組織工學 硏究室 ::”
. 2020年 4月 20日에 確認함
.
- ↑
Whitney G. A.; Jayaraman K.; Dennis J. E.; Mansour J. M. (2014). “Scaffold-free cartilage subjected to frictional shear stress demonstrates damage by cracking and surface peeling”. 《J Tissue Eng Regen Med.》.
doi
:
10.1002/term.1925
.
- ↑
“Langer Lab: Professor Robert Langer”
.
- ↑
“The Laboratory for Tissue Engineering and Organ Fabrication - Massachusetts General Hospital, Boston, MA”
. 2016年 12月 1日에
原本 文書
에서 保存된 文書
. 2017年 1月 19日에 確認함
.
- ↑
Langer R; Vacanti JP (May 1993).
“Tissue engineering”
. 《Science》
260
(5110): 920?6.
Bibcode
:
1993Sci...260..920L
.
doi
:
10.1126/science.8493529
.
PMID
8493529
.
- ↑
가
나
MacArthur BD; Oreffo RO (January 2005). “Bridging the gap”. 《Nature》
433
(7021): 19.
Bibcode
:
2005Natur.433...19M
.
doi
:
10.1038/433019a
.
PMID
15635390
.
- ↑
《Principles of tissue engineering》
3板. Amsterdam: Elsevier Academic Press. 2007. 4쪽.
ISBN
978-0-08-054884-5
.
- ↑
가
나
다
Kim, Woo Seob (2014).
“The principles of tissue engineering and its recent advances and future prospects”
. 《Journal of the Korean Medical Association》
57
(2): 145.
doi
:
10.5124/jkma.2014.57.2.145
.
ISSN
1975-8456
.
- ↑
가
나
《Principles of tissue engineering》
3板. Amsterdam: Elsevier Academic Press. 2007. 8-9쪽.
ISBN
978-0-08-054884-5
.
- ↑
Mashayekhan, Shohreh; Hajiabbas, Maryam; Fallah, Ali (2013年 8月 28日). Bhartiya, Deepa, 編輯.
《Stem Cells in Tissue Engineering》
(英語). InTech.
doi
:
10.5772/54371
.
ISBN
978-953-51-1192-4
.
- ↑
가
나
O'Brien, Fergal J. (2011年 3月 1日).
“Biomaterials & scaffolds for tissue engineering”
. 《Materials Today》 (英語)
14
(3): 88?95.
doi
:
10.1016/S1369-7021(11)70058-X
.
ISSN
1369-7021
.
- ↑
가
나
Chan, B. P.; Leong, K. W. (2008年 12月).
“Scaffolding in tissue engineering: general approaches and tissue-specific considerations”
. 《European Spine Journal》 (英語)
17
(S4): 467?479.
doi
:
10.1007/s00586-008-0745-3
.
ISSN
0940-6719
.
PMC
2587658
.
PMID
19005702
.
- ↑
Babensee, Julia E.; Anderson, James M.; McIntire, Larry V.; Mikos, Antonios G. (1998年 8月 3日).
“Host response to tissue engineered devices”
. 《Advanced Drug Delivery Reviews》. Tissue Engineering (英語)
33
(1): 111?139.
doi
:
10.1016/S0169-409X(98)00023-4
.
ISSN
0169-409X
.
- ↑
Wang, Qun. ([2017]).
《Smart materials for tissue engineering : fundamental principles》
. Royal Society of Chemistry.
ISBN
978-1-78262-675-6
.
- ↑
Lopes, M. Savioli; Jardini, A. L.; Filho, R. Maciel (2012年 1月 1日).
“Poly (Lactic Acid) Production for Tissue Engineering Applications”
. 《Procedia Engineering》. CHISA 2012 (英語)
42
: 1402?1413.
doi
:
10.1016/j.proeng.2012.07.534
.
ISSN
1877-7058
.
- ↑
Zhao, Xiaojun; Zhang, Shuguang; Spirio, Lisa (2005年 8月 19日).
《PuraMatrix》
. CRC Press. 217?238쪽.
ISBN
978-1-57444-521-3
.
- ↑
Chu, Constance R.; Coutts, Richard D.; Yoshioka, Makoto; Harwood, Frederick L.; Monosov, Anna Z.; Amiel, David (1995年 9月).
“Articular cartilage repair using allogeneic perichondrocyteseeded biodegradable porous polylactic acid (PLA): A tissue-engineering study”
. 《Journal of Biomedical Materials Research》 (英語)
29
(9): 1147?1154.
doi
:
10.1002/jbm.820290915
.
ISSN
0021-9304
.
- ↑
Wong, Wai Hung; Mooney, David J. (1997).
《Synthesis and Properties of Biodegradable Polymers Used as Synthetic Matrices for Tissue Engineering》
. Boston, MA: Birkhauser Boston. 51?82쪽.
ISBN
978-1-4612-8677-6
.
- ↑
Sun, Hongfan; Mei, Lin; Song, Cunxian; Cui, Xiumin; Wang, Pengyan (2006年 3月).
“The in vivo degradation, absorption and excretion of PCL-based implant”
. 《Biomaterials》
27
(9): 1735?1740.
doi
:
10.1016/j.biomaterials.2005.09.019
.
ISSN
0142-9612
.
- ↑
Hajiali, Faezeh; Tajbakhsh, Saeid; Shojaei, Akbar (2017年 6月 28日).
“Fabrication and Properties of Polycaprolactone Composites Containing Calcium Phosphate-Based Ceramics and Bioactive Glasses in Bone Tissue Engineering: A Review”
. 《Polymer Reviews》
58
(1): 164?207.
doi
:
10.1080/15583724.2017.1332640
.
ISSN
1558-3724
.
- ↑
Wang, Jin-Yang; Wang, Kai; Gu, Xi; Luo, Ying (2016年 6月 13日).
“Polymerization of Hydrogel Network on Microfiber Surface: Synthesis of Hybrid Water-Absorbing Matrices for Biomedical Applications”
. 《ACS Biomaterials Science & Engineering》
2
(6): 887?892.
doi
:
10.1021/acsbiomaterials.6b00143
.
- ↑
Ivkovic, Alan (2011).
“Regenerative medicine and tissue engineering in orthopaedic surgery”
. 《Frontiers in Bioscience》 (英語)
E3
(3): 923?944.
doi
:
10.2741/e299
.
ISSN
1945-0494
.
- ↑
《Principles of tissue engineering》
3板. Amsterdam: Elsevier Academic Press. 2007.
ISBN
978-0-08-054884-5
.
- ↑
Mikos, Antonios G.; Bao, Yuan; Cima, Linda G.; Ingber, Donald E.; Vacanti, Joseph P.; Langer, Robert (1993年 2月).
“Preparation of poly(glycolic acid) bonded fiber structures for cell attachment and transplantation”
. 《Journal of Biomedical Materials Research》 (英語)
27
(2): 183?189.
doi
:
10.1002/jbm.820270207
.
ISSN
0021-9304
.
- ↑
Mooney, D. J.; Sano, K.; Kaufmann, P. M.; McNamara, K.; Vacanti, J. P.; Langer, R. (1995).
“Integrating Cell Transplantation and Controlled Drug Delivery Technologies to Engineer Liver Tissue”
. 《MRS Proceedings》
385
.
doi
:
10.1557/proc-385-43
.
ISSN
0272-9172
.
- ↑
Yoshimoto, H.; Shin, Y.M.; Terai, H.; Vacanti, J.P. (2003年 5月).
“A biodegradable nanofiber scaffold by electrospinning and its potential for bone tissue engineering”
. 《Biomaterials》
24
(12): 2077?2082.
doi
:
10.1016/s0142-9612(02)00635-x
.
ISSN
0142-9612
.
- ↑
Mikos, Antonios G.; Sarakinos, Georgios; Leite, Susan M.; Vacant, Joseph P.; Langer, Robert (1993年 4月).
“Laminated three-dimensional biodegradable foams for use in tissue engineering”
. 《Biomaterials》 (英語)
14
(5): 323?330.
doi
:
10.1016/0142-9612(93)90049-8
.
- ↑
Widmer, Markus S.; Gupta, Puneet K.; Lu, Lichun; Meszlenyi, Rudolf K.; Evans, Gregory R.D.; Brandt, Keith; Savel, Tom; Gurlek, Ali; Patrick, Charles W. (1998年 11月).
“Manufacture of porous biodegradable polymer conduits by an extrusion process for guided tissue regeneration”
. 《Biomaterials》
19
(21): 1945?1955.
doi
:
10.1016/s0142-9612(98)00099-4
.
ISSN
0142-9612
.
- ↑
Whang, K.; Thomas, C.H.; Healy, K.E.; Nuber, G. (1995年 1月).
“A novel method to fabricate bioabsorbable scaffolds”
. 《Polymer》
36
(4): 837?842.
doi
:
10.1016/0032-3861(95)93115-3
.
ISSN
0032-3861
.
- ↑
Lo, H.; Ponticiello, M.S.; Leong, K.W. (1995年 3月).
“Fabrication of Controlled Release Biodegradable Foams by Phase Separation”
. 《Tissue Engineering》
1
(1): 15?28.
doi
:
10.1089/ten.1995.1.15
.
ISSN
1076-3279
.
- ↑
Hua, Feng Jun; Kim, Go Eun; Lee, Jong Doo; Son, Yong Keun; Lee, Doo Sung (2002).
“Macroporous poly(L-lactide) scaffold 1. Preparation of a macroporous scaffold by liquid-liquid phase separation of a PLLA-dioxane-water system”
. 《Journal of Biomedical Materials Research》
63
(2): 161?167.
doi
:
10.1002/jbm.10121
.
ISSN
0021-9304
.
- ↑
Mooney, David J.; Baldwin, Daniel F.; Suh, Nam P.; Vacanti, Joseph P.; Langer, Robert (1996年 7月 1日).
“Novel approach to fabricate porous sponges of poly(d,l-lactic-co-glycolic acid) without the use of organic solvents”
. 《Biomaterials》 (英語)
17
(14): 1417?1422.
doi
:
10.1016/0142-9612(96)87284-X
.
ISSN
0142-9612
.
- ↑
Yokoi, H.; Kinoshita, T.; Zhang, S. (2005年 6月 14日).
“Dynamic reassembly of peptide RADA16 nanofiber scaffold”
. 《Proceedings of the National Academy of Sciences》 (英語)
102
(24): 8414?8419.
doi
:
10.1073/pnas.0407843102
.
ISSN
0027-8424
.
PMC
1150805
.
PMID
15939888
.
- ↑
Zhang, Shuguang; Holmes, Todd C.; DiPersio, C.Michael; Hynes, Richard O.; Su, Xing; Rich, Alexander (1995年 12月).
“Self-complementary oligopeptide matrices support mammalian cell attachment”
. 《Biomaterials》 (英語)
16
(18): 1385?1393.
doi
:
10.1016/0142-9612(95)96874-Y
.
- ↑
Lee, Elaine L.; von Recum, Horst A. (2010).
“Cell culture platform with mechanical conditioning and nondamaging cellular detachment”
. 《Journal of Biomedical Materials Research Part A》 (英語). 9999A: NA?NA.
doi
:
10.1002/jbm.a.32754
.
- ↑
가
나
“MC2 Biotek | 3D Tissue Culture | The 3D ProtoTissue System™”
. 2012年 5月 28日. 2012年 5月 28日에
原本 文書
에서 保存된 文書
. 2020年 6月 16日에 確認함
.
- ↑
Friedrich, Juergen; Seidel, Claudia; Ebner, Reinhard; Kunz-Schughart, Leoni A (2009年 3月).
“Spheroid-based drug screen: considerations and practical approach”
. 《Nature Protocols》 (英語)
4
(3): 309?324.
doi
:
10.1038/nprot.2008.226
.
ISSN
1754-2189
.
- ↑
가
나
Marx, Vivien (2013年 4月).
“A better brew”
. 《Nature》
496
(7444): 253?258.
doi
:
10.1038/496253a
.
ISSN
0028-0836
.
- ↑
Zhang, Zhi-Yong; Teoh, Swee Hin; Chong, Woon-Shin; Foo, Toon-Tien; Chng, Yhee-Cheng; Choolani, Mahesh; Chan, Jerry (2009年 5月).
“A biaxial rotating bioreactor for the culture of fetal mesenchymal stem cells for bone tissue engineering”
. 《Biomaterials》 (英語)
30
(14): 2694?2704.
doi
:
10.1016/j.biomaterials.2009.01.028
.
- ↑
Onoe, Hiroaki; Okitsu, Teru; Itou, Akane; Kato-Negishi, Midori; Gojo, Riho; Kiriya, Daisuke; Sato, Koji; Miura, Shigenori; Iwanaga, Shintaroh (2013年 3月 31日).
“Metre-long cell-laden microfibres exhibit tissue morphologies and functions”
. 《Nature Materials》
12
(6): 584?590.
doi
:
10.1038/nmat3606
.
ISSN
1476-1122
.
- ↑
Cassidy, John W. (2014年 1月).
“Nanotechnology in the Regeneration of Complex Tissues”
. 《Bone and Tissue Regeneration Insights》
5
: BTRI.S12331.
doi
:
10.4137/btri.s12331
.
ISSN
1179-061X
.
- ↑
가
나
Choi, Jonghoon; Hwang, Jangsun; Jeong, Yoon; Park, Jeong Min; Lee, Kwan Hong; Hong, Jong Wook (2015年 9月).
“Biomimetics: forecasting the future of science, engineering, and medicine”
. 《International Journal of Nanomedicine》 (英語): 5701.
doi
:
10.2147/IJN.S83642
.
ISSN
1178-2013
.
PMC
4572716
.
PMID
26388692
.
外部 링크
[
編輯
]
 위키미디어 公用에
組織工學
關聯 미디어 分類가 있습니다.
위키미디어 公用에
組織工學
關聯 미디어 分類가 있습니다.