 人間의 胚芽줄기細胞
人間의 胚芽줄기細胞
 萬能誠意 胚芽줄기細胞는 太半을 除外하고, 어떤 類型의 細胞로도 發生할 수 있다. 그러나, 桑實胚의 胚芽줄기細胞만 全分化能을 가지며, 이는 太半을 包含하여, 어떤 類型의 細胞로도 發生할 수 있다.
萬能誠意 胚芽줄기細胞는 太半을 除外하고, 어떤 類型의 細胞로도 發生할 수 있다. 그러나, 桑實胚의 胚芽줄기細胞만 全分化能을 가지며, 이는 太半을 包含하여, 어떤 類型의 細胞로도 發生할 수 있다.
胚芽줄기細胞
(Embryonic stem cell, ES cells)는
胚盤胞
의
內部細胞怪
에서 由來한 萬能性 줄기細胞로, 初期 着想 前 胚芽이다.
[1]
[2]
修正
後 人間의
胚芽
는 4-5달 後
胚盤胞
를 形成하며, 그 때
胚芽
는 50-150個의 細胞로 構成된다. 胚盤胞의 안쪽에는 來世泡塊라고 하는 細胞들의 덩어리가 있는데, 이 細胞들은 細胞分裂과 分化를 거쳐
胚芽
를 形成하고, 胚芽는 妊娠期間을 거치면서 하나의 個體로 發生하게 된다. 이 過程에서 來世泡塊의 細胞들이 血液, 뼈, 皮膚, 肝 等 한 個體에 있는 모든 組織의 細胞로 分化하게 된다. 때문에 胚芽 段階에서 抽出한 줄기細胞는 뼈, 肝, 心臟 等 臟器로 發展할 수 있는 萬能細胞라고 불린다.
胚芽줄기細胞로 各種 難治病 治療에 쓰이는 長期 細胞를 試驗管에서 無限定 만들어 移植할 수 있다면 人類의 꿈인 無病長壽가 實現될 수 있다. 寄贈된 臟器가 不足한 現實에서 꼭 必要한 技術이다. 現在 白血病, 파킨슨病, 糖尿病 等에 걸린 患者에게 障礙가 생긴 細胞를 代身하는 正常 細胞를 外部에서 培養, 注入하여 治療하려는 試圖가 行해지고 있다.
또한 무엇보다도 不妊夫婦에게 새로운 希望을 줄 수 있다. 卽 性細胞(程子)에 問題가 있어서 正常的인 方法으로는 修正이 不可能한 夫婦를 위해 여러 가지 方法들이 講究되어 왔지만 體細胞核 移植術을 利用하면 精子가 없이도 修正이 可能하므로 이 問題를 完全히 다른 次元에서 解決할 수 있는 길이 열린다. 수核 細胞質로 어머니의 卵子를 利用하고 細胞核으로 어머니, 或은 아버지의 體細胞를 利用한다면 어머니와 꼭 닮은 딸, 或은 아버지와 꼭 닮은 아들을 낳을 수도 있는 것이다. 또 受精卵의 倍 分離 技術을 利用하면 子宮에 移植하기 前에 受精卵을 檢査하여 缺陷이 있는 것을 걸러 내거나 或은 그 遺傳子만을 矯正하여 願하는 健康한 아기를 얻을 수 있다.
쥐의 胚芽줄기細胞는 8마이크로미터에 가깝고 사람의 胚芽줄기細胞는 約 14마이크로미터이다.
[3]
屬性
[
編輯
]
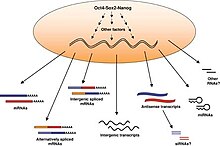 胚芽줄기細胞의 轉寫體
胚芽줄기細胞의 轉寫體
初期 哺乳類 胚芽의 배頒布 段階로부터 由來한 胚芽줄기細胞는 모든 다른 細胞 類型으로 分化할 수 있는 能力과 繁殖 能力에 依해 區別된다. 胚芽줄기細胞의 特性은 一般的인 核型을 가지고, 높은 텔러머라제 活性을 維持하며, 長期的으로 增殖할 수 있는 能力을 가진다.
[4]
萬能性
[
編輯
]
內部細胞怪疑 胚芽줄기細胞는 萬能性이며, 이는 胚芽줄기細胞가 原始外胚葉을 發生하기 위해
噴火
할 수 있고, 이는 窮極的으로
囊胚形成
동안 3가지 主要 胚葉의 派生物인 :
外胚葉
,
內胚葉
및
中胚葉
으로 分化된다. 胚芽줄기細胞는 成人 身體에 220가지 以上의 各各 細胞 類型이 있다. 萬能姓은 聖人에 있는
聖體줄기細胞
와 胚芽줄기細胞를 區別한다. 胚芽줄기細胞는 身體의 모든 細胞 類型을 發生할 수 있는 反面, 聖體줄기細胞는 多能性 줄기細胞이며, 오직 制限된 數의 細胞 類型으로만 生産할 수 있다. 胚芽줄기細胞의 萬能性을 試驗管 內에서 利用할 수 있다면, 그것은 事實上 細胞 또는 組織 形態를 導出하는 手段일지도 모른다. 이것은 年齡, 疾患 또는 외상으로 인한 組織의 損傷 또는 機能 喪失을 招來하는 條件에 對한 다양한 새로운 治療法을 提供한다.
2012年
노벨 生理學·醫學賞
은 John B. Gurdon과 Shinya Yamanaka 共同 硏究로 聖體 細胞는 萬能性으로 再프로그램 될 수 있다는 發見에 起因하였다.
[5]
增殖
[
編輯
]
게다가 定義된 條件 下에, 胚芽줄기細胞는 未分化 狀態에서 自身을 無期限으로 增殖할 수 있고, 分化하기 위해 適切한 信號가 提供될 때, 電球細胞 形成을 통해 거의 모든 聖體 細胞
表現型
으로의 能力을 가진다.
[6]
胚芽줄기細胞는 持續的인 實驗과 臨床的인 使用을 위해 自身을 無限하게 生産할 수 있기 때문에, 이는 胚芽줄기細胞가 硏究와 再生醫學 모두를 위해 有用한 道具로 使用될 수 있게 한다.
有用性
[
編輯
]
自家 再生에 對한 胚芽줄기細胞의 可塑性과 潛在的인 無限 能力 때문에, 負傷 또는 疾病 後에 胚芽줄기細胞 治療法은 再生醫學과 組織代替를 위해 提案되었다. 潛在的으로 萬能性 줄기細胞로 治療될 수 있는 疾患은 血液과 關聯된 免疫 體系의 遺傳的 疾患, 癌 및 障礙,
小兒兄 糖尿
,
파킨슨病
,
失明
및 脊椎負傷 等을 包含한다. 줄기細胞 治療의 倫理的인 問題 以外에 同種 줄기細胞 移植에 關聯된
移植編隊宿主病
의 技術的 問題點이 있다. 그러나 組織 接合性과 關聯된 이러한 問題는 自家 寄贈者 聖體줄기細胞와 治療用 複製를 使用하여 解決될 수 있다.
體細胞 核 移植
(SCNT)이라는 方法에 따라 行해져 治療 複製는 미토콘드리아 DNA (mDNA의) 變異된 疾患에 對한 유리한 境遇가 있다.
[7]
定義된 要素와 體細胞의 再프로그래밍하여 더 最近에는 細胞 銀行 또는 줄기에 利用된다. 胚芽줄기細胞는 寄贈者 組織 不足問題를 克服하고, 또한 需用者의 免疫接合性을 갖는 細胞를 만듦으로써 問題를 克服할 수 있다는 希望을 提供한다. 胚芽줄기細胞의 다른 潛在的인 使用은 初期 人間 發達의 調査, 遺傳子 疾患의 그리고 毒性 檢査를 위한 體外 實驗 시스템을 包含한다.
[4]
活用
[
編輯
]
 培養體
培養體
潛在的인 臨床的 活用(潛在的 診斷用)
[
編輯
]
2002年 PNAS 실린 記事에 따르면, “人間 胚芽줄기細胞는 다양한 細胞 類型으로 分化할 수 있는 潛在力을 가지고 있다. 그러므로, 移植 或은 組織 工學用 細胞의 源泉으로서 有用할 수 있다.”
[8]
現在 硏究는 胚芽줄기細胞를 細胞 大體 療法으로 使用하기 위해 다양한 細胞 類型으로 區別하는 것에 重點을 두고 있다(CRTs). 現在 있거나 開發 中인 細胞 類型 中 一部는 心筋 細胞(CM),
神經 細胞
,
간 細胞
, 骨髓 細胞, 섬 細胞 및 內皮 細胞를 包含한다.
[9]
그러나, 胚芽줄기細胞로부터 그러한 細胞 類型의 起源은 障礙物 없이는 不可能하다. 따라서 現在 硏究는 이 障壁을 克服하는데 重點을 두고 있다.
게다가, 未來에는 臟器 移植의 重要한 對案이 되고, 胚芽줄기細胞는 毒性學 分野 및 低分子醫藥品으로 開發될 수 있는 新物質을 밝히기 위한 細胞 檢診으로 使用되고 있다. 硏究 結果는 胚芽줄기細胞로부터 얻은 心筋細胞는 藥물 反應에 對해 實驗하고, 毒性 프로파일을 豫測하기 위해서 試驗管 모델에서 檢證된 것을 보여줬다.
[9]
胚芽줄기細胞에서 由來된 心筋細胞는 藥理學的 刺戟에 反應하는 것으로 나타났으므로, 多形性心室頻脈 같은 心臟 毒性을 評價하기 위해서 使用할 수 있다.
[10]
또한 胚芽줄기細胞에서 由來된 肝細胞는 新藥開發의 前臨床 段階에서 使用될 수 있는 有用한 모델이다. 그러나, 胚芽줄기細胞로부터 肝細胞의 發生은 어려운 것으로 밝혀졌고, 이것은 藥물代謝를 試驗하는 能力을 沮害한다. 그러므로, 現在 硏究는 安定된 段階Ⅰ과 Ⅱ 酵素 活性을 갖는 完全한 機能性 胚芽줄기細胞 由來 肝細胞를 設立하는데 焦點을 맞추고 있다.
[11]
硏究者들은 또한 胚芽줄기細胞를 파킨슨病 治療에 使用할 수 있다는 希望을 가지고
도파민
生産하는 細胞로도 區分했다.
[12]
[13]
最近 健康한 卵母細胞에 嗅覺 超聖火 細胞를 體細胞 核 置換한 後의 胚芽줄기細胞 發生은 神經變性疾患에 勸奬되었다.
[14]
胚芽줄기細胞는 또한
自然 殺害 細胞
(NK 細胞)와 뼈 組織으로 分化되어왔다.
[15]
糖尿病에 對한 代替 治療法을 提供하기 위해 胚芽줄기細胞가 包含된 硏究도 進行 中이다. 例를 들어, D’Amour
et al.
은 胚芽줄기細胞를
인슐린
生産 細胞로 分化시킬 수 있었고,
[16]
하버드 大學의 硏究者들은 胚芽줄기細胞로부터 膵臟 베타 細胞를 大量으로 生産 할 수 있었다.
[17]
遺傳 疾患 모델로서의 人間 胚芽 줄기 細胞
[
編輯
]
이 問題를 解決하기 위한 몇 가지 새로운 硏究가 始作되었다. 이것은 細胞를 遺傳的으로 造作하거나 最近에는 産前遺傳學診斷(PGD)에 依해 確認된 疾病 細胞주를 얻음으로써 行해져 왔다. 이 接近法은
脆弱 X 症候群
,
囊胞性 纖維症
및 믿을만한 모델 시스템이 없는 다른 遺傳病 같은 障礙를 硏究할 때 매우 有用할 수 있다.
胚芽와 細胞 遺傳學(遺傳子 細胞學)을 專門으로 硏究하는 러시아 系 美國人 醫學 硏究原因 Yury Verlinsky는 一般的인 羊水 檢査보다 한달 半 앞당겨 遺傳子 및 染色體 疾患을 決定하는 産前 診斷 테스트 方法을 開發했다. 이 技術은 現在 많은 妊産婦 및 豫備 父母, 特히 遺傳的 畸形 兵力이 있거나 遺傳學的으로 關聯된 疾患의 危險이 높은 35歲 以上의 女性에게 使用된다. 또한, 父母가 遺傳的 障礙가 없는 胚芽를 選擇할 수 있게 함으로써, 無病 後孫의 細胞를 使用하여 이미 類似한 障礙와 疾病을 가진 動機의 삶을 避할 수 있게 한다.
[18]
科學者들은 人間 胚芽 줄기 細胞를 誘導하는 새로운 技術을 開發했다. 桑實胚와 全體 胚盤胞를 包含한 胚芽의 다른 出處로부터 正常 胚芽줄기細胞主들이 確立되었다. 이 結果는 硏究者들이 다른 遺傳的 畸形을 가진 胚芽로부터 胚芽줄기細胞株를 만들 수 있게 한다.; 따라서, 疾病 進行을 沮害할 수 있는 分子 水準의 메커니즘을 찾을 수 있다. 遺傳的 및 染色體 畸形을 가진 胚芽에서 由來한 胚芽줄기細胞주는 遺傳的 缺陷의 經路를 理解하는데 必要한 데이터를 提供한다.
[19]
寄贈者 患者는 하나의 缺陷 遺傳子 複製本과 하나의 正常 複製物을 얻으며, 이 두 寫本 中 하나만 複製에 使用된다. 2個의 正常的인 複製本을 가지는 胚芽 줄기 細胞에서 發生한 卵子 細胞를 選擇함으로써, 硏究者들은 다양한 疾病에 對한 다양한 治療法을 發見할 수 있다. 이 理論을 테스트하기 위해 McLaughlin 博士와 그의 同僚 中 一部는 處女 生食 胚芽 줄기 細胞가 脫라세미아 媒介物이 있는 마우스 모델에서 使用될 수 있는지 與否를 調査했다. 이 疾病은 遺傳되는 血液 疾患으로서, 헤모글로빈이 不足하여
貧血
을 惹起하는 疾病이다. 使用된 마우스 모델에 缺陷이 있는 遺傳子 複製本이 하나가 있었는데, 疾病에 걸린 마우스에 있는 美修正 卵子로부터 胚芽줄기細胞를 採取하였고, 健康한 헤모글로빈 遺傳子만 包含하는 줄기細胞가 識別되었다. 健康한 胚芽 줄기 細胞주는 保菌者 마우스에 移植된 細胞로 轉換되었다. 5週 後, 移植 實驗 結果, 이 保菌者 마우스는 正常的인 血球 數와
헤모글로빈
數値를 보였다.
[20]
DNA 損傷 復舊
[
編輯
]
分化된 體細胞와 胚芽줄기細胞는 DNA 損傷을 處理하기 위해 다른 戰略을 使用한다. 例를 들어,체세포의 한 類型인 人間 包皮
纖維 芽細胞
는 모든
細胞週期
段階에서 이中 가닥 破損을 復舊하기 위한 經路로서 誤謬가 發生하기 쉬운 DNA 復舊 過程인 非常桐末端附着을 使用한다.
[21]
그 誤謬가 發生하기 쉬운 性質 때문에, 非常桐末端附着은 細胞의 複製 子孫에 突然變異를 일으키는 傾向이 있다.
胚芽줄기細胞는 이中 가닥 破損을 다루기 위해 다른 戰略을 使用한다.
[22]
胚芽줄기細胞는
生殖細胞系列
의 細胞를 包含하여 生物體의 모든 細胞 類型을 生成하기 때문에, 잘못된 DNA 復舊로 인해 胚芽줄기細胞에서 發生하는 突然變異는 分化된 體細胞에서 보다 더 深刻한 問題이다. 結果的으로, DNA 損傷을 正確하게 復舊하기 위해서는 胚芽줄기細胞에서 强力한 메커니즘이 必要하고, 復舊가 失敗하면 DNA가 損傷된 그 細胞를 除去하는 것이 必要하다. 따라서, 마우스 胚芽줄기細胞는 主로 이中 가닥 破損을 고치기 위해서 높은 正確度의 상동 再組合 回復을 使用한다.
[22]
이러한 類型의 水利는 S 段階 동안 形成되는 두 姊妹 染色體의 相互作用에 依해 決定되며, 細胞 週期의 G2 段階 동안 같이 存在한다. 상동 再組合 回復은 다른 姊妹 染色體의 穩全한 情報를 使用하여 姊妹 染色體의 二重 가닥 破損을 正確하게 復舊할 수 있다. 細胞 週期의 G1期(卽, 다음 複製 段階드 移轉이지만 中企/細胞 分裂 以後)의 細胞는 各 染色體의 單 하나의 複製本을 갖는다(즉, 姊妹 染色體는 存在하지 않는다). 마우스 胚芽줄기細胞에는 G1 關門이 없으며, DNA 損傷을 입으면 細胞週期가 停止되지 않는다.
[23]
오히려 그들은 DNA 損傷에 對한 反應으로 프로그램된
細胞 死滅
(apoptosis)을 겪는다.
[24]
細胞 死滅은 突然變異와 癌 進行을 防止하기 爲해서 DNA 損傷된 細胞를 除去하는 이中 安全 裝置 戰略으로 使用될 수 있다.
[25]
이 戰略과 一致하게, 마우스 胚芽줄기細胞는 同質 遺傳子型의 마우스 體細胞보다 突然變異 頻度가 約 100倍 낮다.
[26]
副作用
[
編輯
]
治療를 위해 胚芽줄기細胞를 患者에게 移植할 수 있다는 것에 對한 主要한 憂慮는
畸形腫
을 包含한
腫瘍
을 形成하는 能力이다.
[27]
安全 問題로 FDA는 最初의 胚芽줄기細胞
臨床試驗
(아래 參照)을 保留했으나, 腫瘍은 觀察되지 않았다.
潛在的 臨床 用途를 위해 胚芽줄기細胞의 安全性을 向上시키는 主要 戰略은 腫瘍을 誘發하는 能力을 감소시키거나 除去한 特定 細胞 類型(예 : 뉴런, 筋肉, 간 細胞)으로 分化시키는 것이다. 噴火 後, 細胞를 追加 精製하기 위해 流動 細胞 係數法에 依해 分類한다. 胚芽줄기細胞는 遺傳的으로 癌과 關聯된 c-Myc 같은 遺傳子로 變形되지 않기 때문에, 本質的으로
誘導萬能줄기細胞
보다 安全할 것으로 豫測된다. 그럼에도 不拘하고, 胚芽줄기細胞는 매우 높은 水準의 誘導萬能줄기細胞 誘導 遺傳子를 發現하며, Myc을 包含한 이 遺傳子들은 胚芽줄기細胞의 自家 再生 및 萬能城에 必須的이다.
[28]
그리고, c-Myc 發現을 除去함으로써 安全性을 向上시킬 수 있는 潛在的 戰略은 細胞의 줄기細胞陵을 保存하기 어려울 것이다. 그러나, N-Myc 및 L-Myc은 c-Myc 代身에 誘導萬能줄기細胞를 類似한 效率로 誘導하는 것으로 確認되었다.
[29]
歷史
[
編輯
]
 Martin Evans는 마우스 子宮에서 胚芽를 培養하여 胚芽줄기細胞를 誘導할 수 있는 새로운 技術을 發表했다.
[30]
Martin Evans는 마우스 子宮에서 胚芽를 培養하여 胚芽줄기細胞를 誘導할 수 있는 새로운 技術을 發表했다.
[30]
1964年 Lewis Kleinsmith and G. Barry Pierce Jr.는 生殖細胞에서 由來된 것으로 알려진 腫瘍인 畸形癌腫으로부터 한 細胞를 分離하였다.
[31]
畸形癌腫으로부터 分離한 細胞들은
細胞培養
을 통해 줄기細胞로 複製되고 자라서 只今은 胚芽癌腫(EC) 細胞로 알려져 있다.
[32]
비록
形態學
및 分化 可能性(全分化能)의 類似性은 初期 마우스 發達을 위한 試驗管 모델로서 胚芽癌腫細胞의 利用을 誘導하였지만,
[33]
胚芽癌腫細胞는 遺傳的 變異와 種種 畸形癌腫의 發生동안 蓄積된 非正常的인 核型을 가진다. 이러한 遺傳的 非正常은 內部細胞怪로부터 直接 萬能性 細胞를 培養할 必要性을 强調했다.
1981年 胚芽줄기細胞는 마우스 胚芽에서 獨집敵으로 두 그룹으로 나뉘었다. 子宮에서 마우스 胚芽를 培養하여 細胞 數를 增加시키고, 이들 胚芽의 胚芽줄기細胞를 誘導할 수 있는 새로운 技術을
케임브릿지 大學校
遺傳學과의
Martin Evans
와 Matthew Kaufman은 7月 1日에 發表하였다.
[34]
샌프란시스코
캘리포니아 大學
解剖學과의 게일 R 마틴 (Gail R. Martin)은 12 月에 그女의 論文을 發表하고 “胚芽줄기細胞”라는 用語를 만들었다.
[35]
그女는 胚芽가 試驗管 모델에서 培養될 수 있다는 것 과 胚芽줄기細胞는 이 胚芽에서 抽出할 수 있음을 보여주었다. 1998年
위스콘신-매디슨 大學
(University of Wisconsin-Madison)의 제이슨 톰슨(James Thomson)李 이끄는 硏究員들은 처음으로 細胞 培養에서 人間 胚芽 줄기 細胞를 分離 및 성장시키는 技術을 처음으로 開發했을 때, 큰 轉換點이 發生하였다.
[36]
臨床 試驗
[
編輯
]
2009年 1月 23日, 人間胚芽줄기細胞에서 派生된
稀突起膠細胞
(腦와 脊椎의 細胞 類型)를 脊髓 損傷 患者들에게 移植하는 1 段階 臨床試驗은
美國食品醫藥局
(FDA)으로부터 承認을 받았는데, 이것은 世界 最初의 人間 對象의 人間胚芽줄기細胞 實驗이다.
[37]
科學的 發展을 이끈 이 硏究는 캘리포니아 大學의 Hans Keirstead와 그 同僚들 그리고 Irvine에 依해 進行되었으며, Michael D. West 博士에 依하여 設立된 CA(California) Menlo Park의 Geron Corporation의 支援을 받았다.
[38]
1段階 臨床試驗은 瘢痕 組織이 形成되기 前에 細胞가 注入되어야 하기 때문에, 臨床試驗 始作 2週 前에 負傷을 입은 約 8 ~10名의 下半身 不隨 患者들을 登錄하도록 設計되었다. 硏究陣들은 細胞를 注入하는 것이 患者를 完治하는 것과 機動性을 復舊시키는 것이 期待되지 않는다는 것을 强調하였다.
齧齒類
實驗 結果들을 土臺로, 硏究陣들은
數秒
의 復元과 發生 할지도 모르는 移動度의 增加를 推測하였다. 이 첫 番째 實驗은 主로 이 節次의 安定性을 試驗하기 위해 考案되었고, 萬若 모든 것이 잘 進行된다면, 더 深刻한 障礙를 가진 사람들이 包含된 未來 硏究로 이어질 것으로 期待되었다.
[39]
이 實驗은 治療를 받은 여러 쥐 모델에서 少數의
囊胞
發見에 對해 美國食品醫藥局의 憂慮로 2009年에 中斷되었지만, 2010年 7月 30日에 再開되었다.
[40]
2010年 10月에 硏究陣은 애틀란타의 Shepherd Center에서 첫 番째 患者에게 ESTs를 登錄하고 管理했다.
[41]
줄기細胞 治療의 創始者 Geron Corporation은 줄기細胞가 複製되고 GRNOPC1治療가 成功 또는 失敗 與否를 評價하는데 數個月이 걸릴 것으로 推定했다.
2011年 11月 Geron은 財政的인 理由로 줄기細胞 硏究를 中斷하고 實驗을 멈췄지만, 旣存 患者들을 持續的으로 모니터링하고 그들의 硏究를 持續할 수 있는 파트너를 찾는 試圖를 繼續할 것이라고 發表했다.
[42]
2013年에 CEO Dr. Michael D. West가 運營하는 BioTime(AMEX: BTX)은 脊椎 損傷 硏究에 對한 Geron의 胚芽줄기細胞 基盤의 臨床試驗을 再開하겠다는 公式的인 醫師와 Geron의 줄기 細胞 資産을 引受하였다.
[43]
BioTime의 子會社인 Asterias Biotherapeutics (NYSE MKT: AST)는 California Institute for Regenerative Medicine (CIRM)로부터 脊髓 損傷에 對한 世界 最初의 胚芽줄기細胞基盤의 人間 臨床試驗 硏究를 再開하기 위하여, California Institute for Regenerative Medicine (CIRM)으로부터 1,430萬 달러의 戰略的 提携 額數가 承認되었다. 캘리포니아의 公的 資金의 支援을 받는 CIRM은 줄기 細胞 關聯된 硏究 開發에 最大 資金 提供者이다.
[44]
이 賞은 Asterias에게 脊髓損傷에 關한 AST-OPC1의 臨床 開發을 再開하는 것과 未來 中樞的인 硏究를 위해 타겟集團에 上昇容量의 따른 臨床試驗 擴大를 위해서 基金을 提供한다.
[44]
AST-OPC1은 稀突起膠細胞前驅體(OPCs)를 包含한 人間胚芽줄기細胞(hESCs)에서 派生된 細胞集團이다. 稀突起膠細胞前驅體와 稀突起膠細胞라고 불리는 그들의 成熟한 派生細胞는 神經 脊髓와 腦의 神經 細胞에 重要한 機能的인 支援을 提供한다. Asterias는 最近 神經學上으로 完全한 胸部脊髓損傷을 가진 患者들에게 低容量으로 AST-OPC1 投與에 對한 1段階 臨床試驗 結果를 發表하였다. 이 結果는 AST-OPC1이 脊髓 損傷 部位에 成功的으로 傳達된 것을 보여주었다. AST-OPC1 投與 後 2~3年 追跡한 患者들에게서 頻繁한 神經系 檢査 및 MRI를 包含한 詳細한 後續 評價에서 細胞와 關聯된 深刻한 副作用이 없다는 것을 보여주었다. 移植 後 一 年 동안 實驗 患者의 免疫 모니터링은 AST-OPC1에 對한 抗體 基盤 또는 細胞 免疫反應이 없음을 보여준다. 5名의 實驗 患者들 中 4名은, 2-3年 追跡 觀察 期間 동안 遂行된 連續的인 MRI 스캔은 減少된 脊髓 캐비테이션의 發生과 AST-OPC1街 脊髓 組織 惡化를 減少시키는데 肯定的인 效果가 있을지도 모른다는 것을 示唆한다. 信賴度 높고 脊髓損傷患者의 神經學的 評價方法人 International Standards for Neurological Classification of Spinal Cord Injury (ISNCSCI)의 評價에 依하면, 臨床試驗에서 5名의 患者에게서 豫想치 못한 神經의 惡化 또는 向上은 없었다.
[44]
CIRM 資金은 實驗에 對하여 FDA 承認 및 Asterias와 CIRM 間의 最終的인 合意 完了 그리고 事前 定義된 프로젝트의 特定 業績 達成에 對한 Asterias의 持續的인 進展에 달려있다.
[44]
由來와 培養 技術 및 條件
[
編輯
]
人間에서 由來
[
編輯
]
試驗管 修正은 多衆 胚芽를 生成한다. 剩餘의 胚芽는 臨床的으로 使用되지 않거나 患者에게 移植하기에 不適合하므로, 寄贈者가 同意하여 寄贈할 수 있다. 人間 胚芽 줄기 細胞는 이러한 寄贈된 胚芽로부터 由來될 수 있거나, 追加的으로 患者의 細胞 및 寄贈된 卵子를 使用하여 複製된 胚芽로부터 抽出될 수 있다.
[45]
胚芽의 배頒布 段階에서 內部細胞괴는 胚芽 外姓 組織으로 分化할 수 있는
營養外胚葉
細胞에서 分離된다. 抗體가 營養 外胚葉에 結合되고, 다른 溶液에 依해 除去되는 過程인 免疫 手術 및 機械的인 分析은 分離하기 위해 遂行된다. 生成된 內部細胞怪 細胞는 支持를 提供할 細胞에 둘러지게 된다. 內部細胞怪 細胞는 附着되고 더 擴張되어 未分化된 人間 胚芽細胞株를 形成한다. 이 細胞는 每日 營養分이 供給되고, 4-7日마다 酵素的 또는 機械的으로 分離된다. 分化가 일어나기 위해서는 人間 胚芽 줄기 細胞株가 支持 細胞에서 除去되어 培養體를 形成하고, 必要한 信號를 包含하는 血淸과 共同 培養된다.
[46]
다른 動物에서 由來
[
編輯
]
胚芽줄기細胞는 寄贈者 母體 動物로부터 採取된 初期 胚芽의
內部細胞怪
로부터 誘導된다. Martin Evans와 Matthew Kaufman은 胚芽 移植을 遲延시켜 內部細胞怪를 증가시키는 技術을 發表했다. 이 過程에는 寄贈者의
卵巢
를 除去하고,
프로게스테론
을 投與함으로써 호르몬 環境을 변화시켜 胚芽를
子宮
에서 自由롭게 維持하는 過程이 包含된다. 子宮 內 培養 4-6日 後에, 胚芽를 採取한다. 그리고, 內部細胞怪가 單一 細胞로 分離되고
mitomycin-c
로 處理한 纖維 芽細胞에 둘러싸여 “卵子 圓筒形 構造”를 形成할 때까지 體外 培養한다. (纖維 芽細胞 類似 分裂을 豫防하기 위해서) 複製 細胞주는 單一 細胞가 자라서 만들어진다. Evans와 Kaufman은 이 培養에서 成長한 細胞가 畸形腫과 培養體를 形成할 수 있고, 體外 培養에서 分化할 수 있음을 보여주었는데, 이들 모두는 細胞가 萬能性임을 나타낸다.
[34]
Gail Martin은 胚芽줄기細胞를 다르게 誘導하였다. 그女는 交尾 後 約 76 時間에 寄贈者 母體에서 胚芽를 除去하고, 血淸을 含有한 배지에서 하룻밤 동안 培養했다. 다음날, 그女는 顯微鏡手術을 使用하여 後記 胚盤胞에서 內部細胞怪를 除去했다. 抽出된 內部細胞괴는 血淸을 含有하는 배지에 mitomycin-c를 處理하고, 胚芽줄기細胞에 依해 길들여진 纖維 芽細胞에서 培養했다. 約 1週日 後, 細胞 集團이 자랐다. 이 細胞들은 배지에서 자랐으며, 畸形腫을 形成하고, 試驗管 內에서 分化하고, 培養體를 形成하는 能力에 依해 立證된 것처럼 萬能性 特徵을 立證했다. Martin은 이 細胞들을 胚芽줄기細胞로 言及했다.
[35]
培養補助細胞가 白血病 抑制 人者(LIF)을 提供하고, 血淸이 胚芽 줄기 細胞가 分化되는 것을 막는데 必要한 뼈 形成 蛋白質들(BMPs)을 提供한다는 것이 現在 알려져 있다.
[47]
[48]
이러한 要素들은 胚芽줄기細胞를 誘導하는데 매우 重要하다. 게다가, 胚芽줄기細胞를 分離하는데 여러 마우스 種類가 다른 效率을 보였다.
[49]
마우스 胚芽줄기細胞에 對한 現在의 使用은 넉아웃 마우스를 包含하여 遺傳子 移植 마우스의 發生을 包含한다. 人間 治療를 위해서는, 患者 特異的 萬能性 細胞가 必要하다. 人間 胚芽줄기細胞의 生成은 어렵고, 倫理的인 問題에 直面한다. 따라서, 人間 胚芽줄기細胞 硏究 外에도 많은 그룹이 誘導萬能줄기細胞(iPS cells)의 生成에 重點을 두고 있다.
[50]
誘導萬能줄기細胞
[
編輯
]
誘導萬能줄기細胞 技術은 2006年
日本
교토
의
Shinya Yamanaka
의 實驗室에서 開拓되었으며, 이는
戰士人者
를 코딩하는 4個의 特定 遺傳子를 導入하면 聖體 細胞를 萬能性 줄기細胞로 전환시킬 수 있다는 것이다.
[51]
그는 成熟한 細胞가 萬能性을 가지기 위해 再프로그램 될 수 있다는 事實을 發見한
John Gurdon
과 함께 2012年 노벨賞을 受賞했다.
[52]
2007年에 胚芽줄기細胞와 매우 類似한 萬能性 줄기細胞가 세 가지 遺傳子(Oct4, Sox2 및 Klf4)를 分化된 細胞에 傳達함으로써 生成될 수 있음이 밝혀졌다.
[53]
이 遺傳子의 傳達은 分化된 細胞를 萬能性 줄기 細胞로 “再프로그램”하여, 胚芽 없이 萬能性 줄기細胞를 만들 수 있게 한다. 胚芽 줄기 細胞에 關한 倫理的인 憂慮는 典型的으로 終結된 胚芽에서 由來된 것이므로, 이러한 “誘導萬能줄기細胞”(iPS 細胞)로의 再프로그램은 論難의 餘地가 덜 하다. 人間과 마우스 細胞는 모두 이 方法論에 依해 再프로그램되어 胚芽 없이 人間 萬能性 줄기細胞와 마우스 줄기 細胞를 生成할 수 있다.
[54]
이것은 潛在的으로 細胞 大體 療法에 使用될 수 있는 患者 特異的 胚芽줄기細胞注意 生成을 可能하게 할 수 있다. 또한 다양한 遺傳 疾患을 앓고 있는 患者의 胚芽줄기細胞株를 生成할 수 있으며, 이는 硏究할 수 있는 貴重한 모델을 提供할 것이다.
그러나 誘導萬能줄기細胞(iPSc) 細胞 技術이 빠른 速度로 連續的으로 새로운 治療劑로 使用될 수 있다는 첫 番째 徵候로, Rudolf Jaenisch이 主導하는 硏究팀이 매사추세츠주 케임브리지의 生物 醫學 硏究所 (Whitehead Institute for Biomedical Research)에서
鎌狀 赤血球 貧血症
人 쥐를 治療할 수 있다고 2007年 12月 6日
사이언스
저널의 온라인 판에 보고하였다.
[55]
[56]
2008年 1月 16日, 캘리포니아 基盤의 會社인 Stemagen은 成人으로부터 抽出한 單一 皮膚 細胞로부터 最初의 成熟한 複製 人間 胚芽를 만들었다고 發表했다. 이 胚芽는 胚芽 줄기 細胞와 一致하는 患者를 위해 抽出될 수 있다.
[57]
細胞 培養에 使用되는 試藥에 依한 汚染
[
編輯
]
Nature Medicine의 온라인 판에 2005年 1月 24日 硏究를 發表했다. 이 硏究는 聯邦 基金 硏究에 使用할 수 있는 人間 胚芽 줄기 細胞가 細胞를 성장시키는데 使用된 배지에서 어떤 分子로 汚染되었다고 發表했다.
[58]
活潑하게 줄기細胞를 분열시키는 萬能性을 維持하기 위해서 마우스 細胞와 다른 動物細胞를 使用하는 것이 一般的인 技術이다. 샌디에고
캘리포니아 大學
의 科學者들에 따르면, 成長 배지에 시알酸이 人間의 胚芽 줄기 細胞의 潛在的인 用途를 損傷시키는 것으로 밝혀졌다.
[59]
그러나, 2005年 3月 8日 Lancet Medical 저널의 온라인 판에 發表된 硏究는 完全히 細胞와 血淸이 없는 條件下에서 人間 胚芽에서 由來된 새로운 줄기 細胞株에 對한 情報를 詳細히 알렸다. 未分化된 增殖이 6個月 以上 持續된 後에, 이 細胞들은 試驗管 및 畸形腫 모두에서 3가지 胚葉의 誘導體를 形成할 수 있는 可能性을 證明하였다.
[60]
胚芽줄기細胞硏究의 生命倫理的 問題點
[
編輯
]
人間受精卵 및 胚芽에 對한 硏究, 特히 줄기細胞를 抽出하여 活用하고자 하는 硏究는 그 胚芽의 죽음을 前提로 한다. 胚芽 自體를 子宮에 着床시키면 穩全한 人間 個體로 發展할 수 있기 때문에, 이는 倫理的으로 深刻한 물음을 提起한다. 胚芽의 道德的 地位가 穩全한 人間과 同一하다면, 어떤 境遇에도 胚芽를 活用한 硏究나 胚芽의 使用은 倫理的으로 正當化 되기 어렵다. 受精卵 및 胚芽는 追後 人間으로 發達하기 위한 모든 潛在性(potentiality)을 갖추고 있는 存在이기 때문이다. 그러므로 人間 胚芽의 生産, 剩餘 胚芽의 硏究, 胚芽로부터의 胚芽줄기細胞 抽出을 통한 治療의 試圖 모두가 倫理的으로 正當化될 수 없는 것이라는 意見이 있다.
[61]
하지만, 胚芽의 道德的 地位가 人間과 同等하다고 볼 수 있는가? 萬一, 불 속에 胚芽 20個와 어린 女子아이가 있다면 胚芽 20個를 求하는 것이 正當化 될 수 있는가? 이는 矛盾된 結果를 招來한다. 卽, 胚芽의 道德的 地位는 人間과 穩全히 類似하다고 判斷할 수 없다. 胞胚에서부터 着想된 胚芽, 胎兒, 그리고 新生兒에 이르기까지 發達上 連續性이 存在한다고 해서 胞胚와 新生兒가 道德的으로 同一하다는 結論이 成立되지 않는다. 그렇다고 해서 胚芽를 우리가 願하는 어떤 目的으로든 使用해도 된다는 것은 아니다. 胚芽를 單純한 事物로 看做한다면 그것이 潛在的인 人間 生命體로서 갖는 意味를 無視하는 것이다. 마땅히 尊重받아야 한다는 것이 胚芽에게 人格을 附與하는 行爲는 아니다. 胚芽가 人格體라는 確信은 道德的인 二分法에서 由來된 것인데, 모든 것은 尊重받을 價値가 있는 人格體이거나 或은 마음대로 利用할 수 있는 事物로 區分된다는 것이다. 이러한 二元論은 度를 지나친 觀點이다. 따라서 胚芽줄기細胞의 硏究와 硏究用 複製를 無條件 禁止할 것이 아니라, 初期 人間의 尊嚴性을 지키기 위한 適切한 道德的 規制를 마련하는 것이 바람직하다.
[62]
現在 體外受精技術은 一般的으로 받아들여지고 있고, 그 結果 廢棄될 運命인 剩餘 倍아들이 量産되고 있기 때문에 이를 活用한 制限的인 硏究에 對한 倫理的인 反感은 比較的 덜하다고 할 수 있다. 勿論 宗敎界 一角에서는 剩餘 胚芽를 量産하는 體外受精技術부터가 倫理的으로 그릇된 것으로 看做하지만, 現實的으로 廢棄될 수 밖에 없는 剩餘 胚芽를 人間의 福祉와 健康 增進을 위해 硏究用으로 活用한다는 데는 꽤 많은 사람들이 同意하고 있으며, 이미 言及한 科學技術部 生命倫理諮問委員會의 勸告案도 이런 事實을 背景으로 하고 있다. 하지만 硏究 等의 應用 目的으로 胚芽를 創出하는 것은 특정한 目的을 위해 人間을 手段化한다는 强力한 批判을 받을 수 있다. 大部分의 境遇에 程子나 卵子를 寄贈하는 目的은 다른 方法으로는 아기를 가질 수 없는 不妊夫婦를 돕는데 있으며, 寄贈 節次上의 同意 亦是 그렇게 限定되어 있으므로 이들을 任意로 活用하여 胚芽를 創出한다면, 寄贈者의 意思를 無視하였다는 倫理的인 問題가 發生한다. 胚芽를 創出하려는 硏究의 目的으로 程子나 卵子를 寄贈하는 行爲도 받아들일 수 없는데, 이는 程子나 卵子 等의 性細胞는 그 自體로는 寄贈者의 身體 一部이고, 이것이 結合하여 修正이 되면 全혀 다른 個體(가 될 潛在性이 있는 存在)이기 때문이다. 寄贈 받은 性細胞를 利用해서 恣意的으로 受精卵, 或은 胚芽를 創出할 수 있다는 생각, 或은 그런 目的으로 쓰일 것을 알고 生殖細胞를 寄贈하는 行爲는 現在의 社會的 雰圍氣 下에서는 倫理的으로 正當化되기 어렵다.
[61]
體細胞 核置換 技術 利用
[
編輯
]
卵子의 核을 除去시킨 後 患者의 體細胞를 집어 넣어 分裂시켜 만든다. 受精卵에서 由來한 胚芽 줄기細胞의 境遇 患者에게 移植하면 免疫 拒否反應을 일으키는 反面, 體細胞 核置換 技術을 利用한 胚芽 줄기細胞를 患者에게 移植하면, 患者의 體細胞로부터 만들어진 것이기 때문에, 免疫 拒否 反應이 일어날 可能性이 매우 적다. 다만, 卵子를 제공받기 어려울 뿐만 아니라, 不法的인 方法으로 卵子를 獲得 할 境遇 倫理的 問題가 發生한다. 또한, 體細胞 核置換 技術로 만들어진 胚芽를 代理母의 子宮에 넣고 着床 시킨다면 人間 複製가 될 可能性도 있다. 參考로, 돌리는 體細胞인 젖샘 細胞를 核이 除去된 卵子에 넣은 後 代理母의 子宮에 넣어 着床 시킨 後 태어난 體細胞 複製 動物이다.
各州
[
編輯
]
- ↑
Thomson; Itskovitz-Eldor, J; Shapiro, SS; Waknitz, MA; Swiergiel, JJ; Marshall, VS; Jones, JM (1998). “Blastocysts Embryonic Stem Cell Lines Derived from Human”. 《
Science
》
282
(5391): 1145?1147.
doi
:
10.1126/science.282.5391.1145
.
PMID
9804556
.
- ↑
“NIH Stem Cell Basics. What are embryonic stem cells?”
. 2016年 8月 31日에
原本 文書
에서 保存된 文書
. 2016年 8月 19日에 確認함
.
- ↑
Thomson, James A.; Zwaka (2003年 2月 10日). “Homologous recombination in human embryonic stem cells”. 《
Nature Biotechnology
》
21
(3): 319?321.
doi
:
10.1038/nbt788
.
PMID
12577066
.
- ↑
가
나
Thomson, J. A.; Itskovitz-Eldor, J; Shapiro, S. S.; Waknitz, M. A.; Swiergiel, J. J.; Marshall, V. S.; Jones, J. M. (1998). “Embryonic Stem Cell Lines Derived from Human Blastocysts”. 《Science》
282
(5391): 1145?7.
doi
:
10.1126/science.282.5391.1145
.
PMID
9804556
.
- ↑
“The Nobel Prize in Physiology or Medicine 2012.”
. nobelprize.org.
- ↑
Ying; Nichols, J; Chambers, I; Smith, A (2003). “BMP Induction of Id Proteins Suppresses Differentiation and Sustains Embryonic Stem Cell Self-Renewal in Collaboration with STAT3”. 《Cell》
115
(3): 281?292.
doi
:
10.1016/S0092-8674(03)00847-X
.
PMID
14636556
.
- ↑
Mannan Baig, Abdul (2014). “Cloned Microglias with novel delivery systems in Multiple Sclerosis”. 《J Stem Cell Res Ther》
4
(11): 11.
doi
:
10.4172/2157-7633.1000252
.
- ↑
Levenberg, Shulamit; Golub, Justin S.; Amit, Michal; Itskovitz-Eldor, Joseph; Langer, Robert (2002年 4月 2日).
“Endothelial cells derived from human embryonic stem cells”
. 《Proceedings of the National Academy of Sciences》
99
(7): 4391?4396.
doi
:
10.1073/pnas.032074999
.
- ↑
가
나
Davila, Julio C.; Cezar, Gabriela G.; Thiede, Mark; Strom, Stephen; Miki, Toshio; Trosko, James (2004年 6月).
“Use and application of stem cells in toxicology”
. 《Toxicological Sciences: An Official Journal of the Society of Toxicology》
79
(2): 214?223.
doi
:
10.1093/toxsci/kfh100
.
ISSN
1096-6080
.
PMID
15014205
.
- ↑
Jensen, Janne; Hyllner, Johan; Bjorquist, Petter (2009年 6月).
“Human embryonic stem cell technologies and drug discovery”
. 《Journal of Cellular Physiology》
219
(3): 513?519.
doi
:
10.1002/jcp.21732
.
ISSN
1097-4652
.
PMID
19277978
.
- ↑
Soderdahl, Therese; Kuppers-Munther, Barbara; Heins, Nico; Edsbagge, Josefina; Bjorquist, Petter; Cotgreave, Ian; Jernstrom, Bengt (2007年 8月).
“Glutathione transferases in hepatocyte-like cells derived from human embryonic stem cells”
. 《Toxicology in vitro: an international journal published in association with BIBRA》
21
(5): 929?937.
doi
:
10.1016/j.tiv.2007.01.021
.
ISSN
0887-2333
.
PMID
17346923
.
- ↑
Perrier, Anselme L.; Tabar, Viviane; Barberi, Tiziano; Rubio, Maria E.; Bruses, Juan; Topf, Norbert; Harrison, Neil L.; Studer, Lorenz (2004年 8月 24日).
“Derivation of midbrain dopamine neurons from human embryonic stem cells”
. 《Proceedings of the National Academy of Sciences》
101
(34): 12543?12548.
doi
:
10.1073/pnas.0404700101
.
- ↑
Parish, Clare L.; Arenas, Ernest (2007).
“Stem-cell-based strategies for the treatment of Parkinson's disease”
. 《Neuro-Degenerative Diseases》
4
(4): 339?347.
doi
:
10.1159/000101892
.
ISSN
1660-2854
.
PMID
17627139
.
- ↑
Baig, Abdul Mannan (2014年 10月).
“Designer’s microglia with novel delivery system in neurodegenerative diseases”
. 《Medical Hypotheses》
83
(4): 510?512.
doi
:
10.1016/j.mehy.2014.08.003
.
ISSN
0306-9877
.
- ↑
Waese, Elaine Y. L.; Kandel, Rita A.; Kandel, Rita R.; Stanford, William L. (2008年 7月).
“Application of stem cells in bone repair”
. 《Skeletal Radiology》
37
(7): 601?608.
doi
:
10.1007/s00256-007-0438-8
.
ISSN
0364-2348
.
PMID
18193216
.
- ↑
D'Amour, Kevin A.; Bang, Anne G.; Eliazer, Susan; Kelly, Olivia G.; Agulnick, Alan D.; Smart, Nora G.; Moorman, Mark A.; Kroon, Evert; Carpenter, Melissa K. (2006年 11月).
“Production of pancreatic hormone-expressing endocrine cells from human embryonic stem cells”
. 《Nature Biotechnology》
24
(11): 1392?1401.
doi
:
10.1038/nbt1259
.
ISSN
1087-0156
.
PMID
17053790
.
- ↑
“Giant leap against diabetes”
. 2014年 11月 24日.
- ↑
Dr. Yury Verlinsky (2009年 7月 20日).
“Expert in reproductive technology”
. 2009年 8月 8日에
原本 文書
에서 保存된 文書.
- ↑
Verlinsky, Y.; Strelchenko, N.; Kukharenko, V.; Rechitsky, S.; Verlinsky, O.; Galat, V.; Kuliev, A. (2005年 1月).
“Human embryonic stem cell lines with genetic disorders”
. 《Reproductive Biomedicine Online》
10
(1): 105?110.
ISSN
1472-6483
.
PMID
15705304
.
- ↑
“Embryonic stem cells help deliver 'good genes' in a model of inherited blood disorder”
. 《ScienceDaily》. 2011年 2月 13日.
- ↑
Mao, Zhiyong; Bozzella, Michael; Seluanov, Andrei; Gorbunova, Vera (2008年 9月 15日).
“DNA repair by nonhomologous end joining and homologous recombination during cell cycle in human cells”
. 《Cell Cycle (Georgetown, Tex.)》
7
(18): 2902?2906.
doi
:
10.4161/cc.7.18.6679
.
ISSN
1551-4005
.
PMC
2754209
.
PMID
18769152
.
- ↑
가
나
Tichy, Elisia D.; Pillai, Resmi; Deng, Li; Liang, Li; Tischfield, Jay; Schwemberger, Sandy J.; Babcock, George F.; Stambrook, Peter J. (2010年 11月).
“Mouse embryonic stem cells, but not somatic cells, predominantly use homologous recombination to repair double-strand DNA breaks”
. 《Stem Cells and Development》
19
(11): 1699?1711.
doi
:
10.1089/scd.2010.0058
.
ISSN
1557-8534
.
PMC
3128311
.
PMID
20446816
.
- ↑
Hong, Yiling; Stambrook, Peter J. (2004年 10月 5日).
“Restoration of an absent G1 arrest and protection from apoptosis in embryonic stem cells after ionizing radiation”
. 《Proceedings of the National Academy of Sciences of the United States of America》
101
(40): 14443?14448.
doi
:
10.1073/pnas.0401346101
.
ISSN
0027-8424
.
PMC
521944
.
PMID
15452351
.
- ↑
Aladjem, M. I.; Spike, B. T.; Rodewald, L. W.; Hope, T. J.; Klemm, M.; Jaenisch, R.; Wahl, G. M. (1998年 1月 29日).
“ES cells do not activate p53-dependent stress responses and undergo p53-independent apoptosis in response to DNA damage”
. 《Current biology: CB》
8
(3): 145?155.
ISSN
0960-9822
.
PMID
9443911
.
- ↑
Bernstein, Carol; Bernstein, Harris; Payne, Claire M.; Garewal, Harinder (2002年 6月).
“DNA repair/pro-apoptotic dual-role proteins in five major DNA repair pathways: fail-safe protection against carcinogenesis”
. 《Mutation Research》
511
(2): 145?178.
ISSN
0027-5107
.
PMID
12052432
.
- ↑
Cervantes, Rachel B.; Stringer, James R.; Shao, Changshun; Tischfield, Jay A.; Stambrook, Peter J. (2002年 3月 19日).
“Embryonic stem cells and somatic cells differ in mutation frequency and type”
. 《Proceedings of the National Academy of Sciences of the United States of America》
99
(6): 3586?3590.
doi
:
10.1073/pnas.062527199
.
ISSN
0027-8424
.
PMC
122567
.
PMID
11891338
.
- ↑
Knoepfler, Paul S. (2009年 5月).
“Deconstructing stem cell tumorigenicity: a roadmap to safe regenerative medicine”
. 《Stem Cells (Dayton, Ohio)》
27
(5): 1050?1056.
doi
:
10.1002/stem.37
.
ISSN
1549-4918
.
PMC
2733374
.
PMID
19415771
.
- ↑
Varlakhanova, Natalia V.; Cotterman, Rebecca F.; deVries, Wilhelmine N.; Morgan, Judy; Donahue, Leah Rae; Murray, Stephen; Knowles, Barbara B.; Knoepfler, Paul S. (2010年 7月).
“myc maintains embryonic stem cell pluripotency and self-renewal”
. 《Differentiation; research in biological diversity》
80
(1): 9?19.
doi
:
10.1016/j.diff.2010.05.001
.
ISSN
0301-4681
.
PMC
2916696
.
PMID
20537458
.
- ↑
Wernig, Marius; Meissner, Alexander; Cassady, John P.; Jaenisch, Rudolf (2008年 1月 10日).
“c-Myc is dispensable for direct reprogramming of mouse fibroblasts”
. 《Cell Stem Cell》
2
(1): 10?12.
doi
:
10.1016/j.stem.2007.12.001
.
ISSN
1875-9777
.
PMID
18371415
.
- ↑
Cardiff University (2007年 10月).
“Sir Martin John Evans, British scientist, a co-winner of the Nobel Prize in Physiology or Medicine in recognition of his gene targeting work (2007)”
.
- ↑
Kleinsmith, L. J.; Pierce, G. B. (1964年 10月).
“MULTIPOTENTIALITY OF SINGLE EMBRYONAL CARCINOMA CELLS”
. 《Cancer Research》
24
: 1544?1551.
ISSN
0008-5472
.
PMID
14234000
.
- ↑
Andrews, P. W.; Matin, M. M.; Bahrami, A. R.; Damjanov, I.; Gokhale, P.; Draper, J. S. (2005年 12月).
“Embryonic stem (ES) cells and embryonal carcinoma (EC) cells: opposite sides of the same coin”
. 《Biochemical Society Transactions》
33
(Pt 6): 1526?1530.
doi
:
10.1042/BST20051526
.
ISSN
0300-5127
.
PMID
16246161
.
- ↑
Martin, G. R. (1980年 8月 15日).
“Teratocarcinomas and mammalian embryogenesis”
. 《Science (New York, N.Y.)》
209
(4458): 768?776.
ISSN
0036-8075
.
PMID
6250214
.
- ↑
가
나
Evans, M. J.; Kaufman, M. H. (1981年 7月 9日).
“Establishment in culture of pluripotential cells from mouse embryos”
. 《Nature》
292
(5819): 154?156.
ISSN
0028-0836
.
PMID
7242681
.
- ↑
가
나
Martin, G. R. (1981年 12月).
“Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells”
. 《Proceedings of the National Academy of Sciences of the United States of America》
78
(12): 7634?7638.
ISSN
0027-8424
.
PMC
349323
.
PMID
6950406
.
- ↑
Thomson, J. A.; Itskovitz-Eldor, J.; Shapiro, S. S.; Waknitz, M. A.; Swiergiel, J. J.; Marshall, V. S.; Jones, J. M. (1998年 11月 6日).
“Embryonic stem cell lines derived from human blastocysts”
. 《Science (New York, N.Y.)》
282
(5391): 1145?1147.
ISSN
0036-8075
.
PMID
9804556
.
- ↑
“FDA approves human embryonic stem cell study”
. 2009年 1月 23日.
- ↑
Keirstead, Hans S.; Nistor, Gabriel; Bernal, Giovanna; Totoiu, Minodora; Cloutier, Frank; Sharp, Kelly; Steward, Oswald (2005年 5月 11日).
“Human embryonic stem cell-derived oligodendrocyte progenitor cell transplants remyelinate and restore locomotion after spinal cord injury”
. 《The Journal of Neuroscience: The Official Journal of the Society for Neuroscience》
25
(19): 4694?4705.
doi
:
10.1523/JNEUROSCI.0311-05.2005
.
ISSN
1529-2401
.
PMID
15888645
.
- ↑
Steven Reinberg (2009年 1月 23日).
“FDA OKs 1st Embryonic Stem Cell Trial”
. The Washington Post.
- ↑
“Geron comments on FDA hold on spinal cord injury trial.”
. 2009年 8月 27日. 2011年 2月 12日에
原本 文書
에서 保存된 文書.
- ↑
Vergano, Dan (2010年 10月 11日).
“
"
Embryonic stem cells used on patient for first time
"
”
.
- ↑
“Geron exits stem cell research”
. LA Times. 2011年 11月 15日.
- ↑
“Great news: BioTime Subsidiary Asterias Acquires Geron Embryonic Stem Cell Program”
. iPScell.com. 2013年 10月 1日.
- ↑
가
나
다
라
“California Institute of Regenerative Medicine.”
. BioTime, Inc. 2017年 10月 24日에
原本 文書
에서 保存된 文書.
- ↑
Mountford, J. C. (2008年 2月).
“Human embryonic stem cells: origins, characteristics and potential for regenerative therapy”
. 《Transfusion Medicine (Oxford, England)》
18
(1): 1?12.
doi
:
10.1111/j.1365-3148.2007.00807.x
.
ISSN
1365-3148
.
PMID
18279188
.
- ↑
Thomson, J. A.; Itskovitz-Eldor, J.; Shapiro, S. S.; Waknitz, M. A.; Swiergiel, J. J.; Marshall, V. S.; Jones, J. M. (1998年 11月 6日).
“Embryonic stem cell lines derived from human blastocysts”
. 《Science (New York, N.Y.)》
282
(5391): 1145?1147.
ISSN
0036-8075
.
PMID
9804556
.
- ↑
Smith, A. G.; Heath, J. K.; Donaldson, D. D.; Wong, G. G.; Moreau, J.; Stahl, M.; Rogers, D. (1988年 12月 15日).
“Inhibition of pluripotential embryonic stem cell differentiation by purified polypeptides”
. 《Nature》
336
(6200): 688?690.
doi
:
10.1038/336688a0
.
ISSN
0028-0836
.
PMID
3143917
.
- ↑
Williams, R. L.; Hilton, D. J.; Pease, S.; Willson, T. A.; Stewart, C. L.; Gearing, D. P.; Wagner, E. F.; Metcalf, D.; Nicola, N. A. (1988年 12月 15日).
“Myeloid leukaemia inhibitory factor maintains the developmental potential of embryonic stem cells”
. 《Nature》
336
(6200): 684?687.
doi
:
10.1038/336684a0
.
ISSN
0028-0836
.
PMID
3143916
.
- ↑
Ledermann, B.; Burki, K. (1991年 12月).
“Establishment of a germ-line competent C57BL/6 embryonic stem cell line”
. 《Experimental Cell Research》
197
(2): 254?258.
ISSN
0014-4827
.
PMID
1959560
.
- ↑
Takahashi, Kazutoshi; Tanabe, Koji; Ohnuki, Mari; Narita, Megumi; Ichisaka, Tomoko; Tomoda, Kiichiro; Yamanaka, Shinya (2007年 11月 30日).
“Induction of pluripotent stem cells from adult human fibroblasts by defined factors”
. 《Cell》
131
(5): 861?872.
doi
:
10.1016/j.cell.2007.11.019
.
ISSN
0092-8674
.
PMID
18035408
.
- ↑
Takahashi, Kazutoshi; Yamanaka, Shinya (2006年 8月 25日).
“Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors”
. 《Cell》
126
(4): 663?676.
doi
:
10.1016/j.cell.2006.07.024
.
ISSN
0092-8674
.
PMID
16904174
.
- ↑
“
"
The Nobel Prize in Physiology or Medicine ? 2012 Press Release".”
. Nobel Media AB. 2012年 10月 8日.
- ↑
Wernig, Marius; Meissner, Alexander; Foreman, Ruth; Brambrink, Tobias; Ku, Manching; Hochedlinger, Konrad; Bernstein, Bradley E.; Jaenisch, Rudolf (2007年 7月 19日).
“In vitro reprogramming of fibroblasts into a pluripotent ES-cell-like state”
. 《Nature》
448
(7151): 318?324.
doi
:
10.1038/nature05944
.
ISSN
1476-4687
.
PMID
17554336
.
- ↑
“
"
Embryonic stem cells made without embryos".”
. 2007年 11月 21日.
- ↑
“
"
Scientists Cure Mice Of Sickle Cell Using Stem Cell Technique: New Approach Is From Skin, Not Embryos".”
. The Washington Post. pp. A02. 2007年 12月 7日.
- ↑
Hanna, Jacob; Wernig, Marius; Markoulaki, Styliani; Sun, Chiao-Wang; Meissner, Alexander; Cassady, John P.; Beard, Caroline; Brambrink, Tobias; Wu, Li-Chen (2007年 12月 21日).
“Treatment of sickle cell anemia mouse model with iPS cells generated from autologous skin”
. 《Science (New York, N.Y.)》
318
(5858): 1920?1923.
doi
:
10.1126/science.1152092
.
ISSN
1095-9203
.
PMID
18063756
.
- ↑
“
"
US team makes embryo clone of men
"
”
. BBC. pp. A01. 2008年 1月 17日.
- ↑
Ebert, Jessica (2005年 1月 24日).
“Human stem cells trigger immune attack”
. 《news@nature》 (英語).
doi
:
10.1038/news050124-1
.
ISSN
1744-7933
.
- ↑
Martin, Maria J.; Muotri, Alysson; Gage, Fred; Varki, Ajit (2005年 2月).
“Human embryonic stem cells express an immunogenic nonhuman sialic acid”
. 《Nature Medicine》
11
(2): 228?232.
doi
:
10.1038/nm1181
.
ISSN
1078-8956
.
PMID
15685172
.
- ↑
Klimanskaya, Irina; Chung, Young; Meisner, Lorraine; Johnson, Julie; West, Michael D.; Lanza, Robert (2005).
“Human embryonic stem cells derived without feeder cells”
. 《Lancet (London, England)》
365
(9471): 1636?1641.
doi
:
10.1016/S0140-6736(05)66473-2
.
ISSN
1474-547X
.
PMID
15885296
.
- ↑
가
나
권복규 (2005年 4月 27日).
“줄기細胞 硏究의 倫理的 問題點”
. 《細胞應用硏究事業團 倫理委員會》.
- ↑
마이클 센델 (2016). 《完璧에 對한 反論》. 198쪽.