藥물 大使
(藥物代謝,
英語
:
drug metabolism
)는 一般的으로 특별한
酵素
시스템을 통해, 살아있는
有機體
가
藥物
을
代謝 分解
하는 過程이다. 보다 一般的인 用語로
生體異物 大使
(生體異物代謝,
英語
:
xenobiotic metabolism
,
그리스어
로 '낯선 것'이라는 뜻의 xenos와 '살아 있는 存在와 關聯됨'이라는 뜻의 'biotic'에서 由來)는
毒
이나 約 같은
生體異物
의 化學 構造를 변화시키는 一連의
大使經路
이다. 이러한 經路는 모든 主要 有機體 그룹에 存在하는
生體 內 變換
의 한 形態이며 古代부터 存在했던 것으로 여겨진다. 이러한 反應은 種種 毒性 化合物을
解毒
하는 役割을 한다. 一部에서는 生體異物 大使의
중간체
自體가 毒性 效果를 일으킬 수도 있다. 藥물 大使에 對한 硏究를
藥物動態學
(藥東學)이라고 한다.
醫藥品
의 大使는
藥理學
과
醫學
의 重要한 主題이다. 例를 들어
新陳代謝
速度는 藥물의 藥理 作用의 持續 時間과 强度를 決定한다. 또한 藥물 大使는
感染
으로 인한 疾患이나
癌
에 對한
化學療法
에서
多藥劑 耐性
에 影響을 미치며, 一部 藥物이 生體異物 代謝에 關與하는 酵素의
氣質
이나
抑制劑
로서 作用하면 危險한
藥물 相互作用
의 原因이 되기 쉽다. 이러한 經路는
環境科學
에서도 重要하다.
微生物
의 生體異物 大使는 汚染 物質이
生物的 環境淨化
中에 分解될지, 環境에
殘留
할지 與否를 決定한다. 生體異物 大使의 酵素, 特히
글루타티온 S-傳達酵素
는
農藥
과
除草劑
에 對한 抵抗性을 만들 수 있기 때문에 農業에서도 重要하다.
藥물 大使는 세 段階(上, phase)로 나뉜다. 1段階에서
시토크롬 P450
酸化酵素와 같은 酵素는 生體異物에 反應性, 또는 極盛期를 導入한다. 이렇게 變形된 化合物은 以後 2段階 反應에서 極性 化合物에 接合된다. 이러한 反應은
글루타티온 S-傳達酵素
와 같은
傳達酵素
에 依해 觸媒된다. 마지막으로, 接合된 生體異物은 3段階에서
流出 輸送體
에 依해 認識되고 펌프를 통해 細胞 밖으로 내보내지기 前에 追加로 處理될 수 있다. 藥물 大使는 種種
親油性
化合物을 더 쉽게
排泄
되는
親水性
物質로 전환시킨다.
透過性 障壁과 解毒
[
編輯
]
有機體가 露出되는 正確한 化合物은 大體로 豫測할 수 없으며, 露出될 때마다 크게 다를 수 있다. 이것은 生體外 毒性 스트레스의 主要 特徵이다.
[1]
生體異物 解毒 시스템이 直面하는 主要 課題는 正常的인
新陳代謝
에 關與하는 複雜한 化學 物質로 이루어진 混合物에서 거의 無限한 數의 生體異物 化合物을 除去할 수 있어야 한다는 것이다. 이 問題를 解決하기 위해 進化한 解決法은 物理的 障壁과 낮은 特異性을 가진
酵素
시스템의 組合이다.
모든 有機體는
細胞膜
을 疏水性, 透過性 障壁으로 使用하여 外部 生體異物이 內部 環境에 對한 接近하는 것을 制御한다. 極性 化合物은 이러한
細胞膜
을 가로질러
擴散
될 수 없으며 有用한 分子를 吸收하는 過程은 細胞外 混合物에서 氣質을 特異的으로 選擇하는
輸送 蛋白質
을 통해 媒介된다. 大部分의
親水性
分子가 特定 輸送體에 依해 認識되지 않기 때문에, 細胞에 들어갈 수 없고, 따라서 外部 物質이 選擇的으로 들어오게 된다.
[2]
反對로 이러한 障壁을 통해서
疏水性
化合物의 擴散은 制御할 수 없으며, 따라서 有機體는 細胞膜 障壁만 가지고는
脂溶性
生體異物을 排除할 수 없다.
그러나 透過性 障壁이 存在하므로, 막 透過性 生體異物은 共通的으로 疏水性이다. 그러므로 有機體는 이 疏水性을 利用하는 解毒 시스템을 進化시킬 수 있다. 따라서 有機體의 解毒 시스템은 거의 모든 無極性 化合物을 臺詞하는 廣範圍한 氣質 特異性을 통해 特異性 問題를 解決한다.
[1]
有用한 代謝 産物은 極盛이고 一般的으로 하나 以上의 電荷를 띄는 氣를 包含하기 때문에 解毒 시스템의 廣範圍한 氣質 特異性에서 除外된다.
위에서 言及된 解毒 시스템은 頂上 大使의 反應性 副産物을 解讀할 수는 없다. 이러한 反應性 副産物은 正常 細胞 構成 要素에서 由來했고, 一般的으로 極盛이기 때문이다. 그러나 이러한 化合物의 數는 적기 때문에 特定 酵素가 이를 認識하고 除去할 수 있다. 이러한 特定 解毒 시스템의 例로는 反應性
알데하이드
메틸글리옥살을 除去하는
글리옥살레이스 시스템
[3]
과,
活性 酸素種
을 除去하는 다양한 抗酸化 시스템이 있다.
[4]
解讀의 段階
[
編輯
]
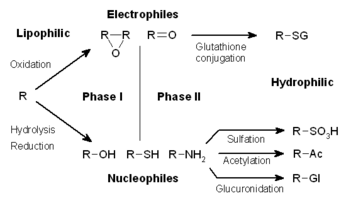 親油性 生體異物 大使의 1段階, 2段階(1床, 2床).
親油性 生體異物 大使의 1段階, 2段階(1床, 2床).
生體異物 大使는 變形, 結合, 排泄의 3段階로 區分되는 境遇가 많다. 이러한 反應은 生體異物을 解讀하고 細胞에서 除去하기 위해 함께 作用한다.
1段階 ? 變形
[
編輯
]
1段階에서는 다양한 酵素가 基質에 反應性, 極盛期를 導入하는 役割을 한다. 가장 一般的인 變形 中 하나는
시토크롬 P-450
依存的 混合 機能 酸化酵素 시스템에 依해 觸媒되는
하이드錄失火
이다. 이러한 酵素 複合體는 酸素 原子를 비활성화된 炭化水素에 統合하는 役割을 하며, 이로 因해
하이드록시機
가 導入되거나 氣質의 N-, O- 및 S-
脫알킬화
를 일으킬 수 있다.
[5]
P-450 酸化酵素의 反應 메커니즘은 다음 反應式에 따라 사이토크롬 結合 酸素의 還元과 高反應性 옥시페릴 種의 生成을 통해 進行된다.
[6]
- O
2
+ NADPH + H
+
+ RH → NADP
+
+ H
2
O + ROH
1段階 反應(비合成 反應이라고도 函)은 種種 肝에서 混合 機能 酸化酵素에 依해 遂行되는
酸化
,
還元
,
加水分解
,
고리火
, 脫稿李花, 酸素 添加, 水素 除去에 依해 發生할 수 있다. 이러한 酸化 反應에는 一般的으로
시토크롬 P450
모노옥시第네이스(種種 CYP로 縮約됨), NADPH, 酸素가 包含된다. 臺詞를 위해 이 方法을 使用하는 醫藥品 種類에는
페노티아진
,
派라세타몰
, 스테로이드가 있다. 1段階 反應의 代謝産物이 充分히 極盛이면 이 地點에서 쉽게 排泄될 수 있다. 그러나 많은 1段階 生成物은 빠르게 除去되지 않고
內因性
氣質
이 새로 導入된 作用基와 結合하여 劇性이 높은 接合體를 形成하는 後續 反應(2段階, 2床)을 겪는다.
一般的인 1段階의 酸化 反應은 CH 結合을 C-OH로 轉換하는 過程을 包含한다. 이 反應은 때때로 藥理學的으로 非活性人 化合物(
戰區藥物
)을 藥理學的으로 活性人 것으로 轉換한다. 같은 理由로 1段階에서는 無毒性 分子를 오히려 有毒性 分子로 바꿀 수 있다. 위에서 單純 加水分解는 一般的으로 無害한 反應이지만 例外가 있다. 例를 들어, 1段階 大使는
아세토나이트릴
을 HOCH
2
CN으로 變換하고, 이 物質은
폼알데히드
와
사이安和 水素
로 빠르게 解離된다.
[7]
非酵素 觸媒를 使用하여 實驗室에서 藥물 候補의 1段階 大使를 시뮬레이션해 볼 수 있다.
[8]
生體模倣
反應의 이런 例示는 種種 1段階 代謝物質을 包含하는 生成物을 生成하는 傾向이 있다. 例를 들어, 制約에서
트리메부틴
의 主要 代謝産物인 데스메틸트리메부틴(노르-트리메부틴)은 市販되는 藥물의 試驗管 內(in vitro) 酸化에 依해 效率的으로 生成될 수 있다. N-메틸기의 水酸化反應은
폼알데히드
分子의 放出로 이어지는 反面, O-메틸기의 酸化는 덜 일어난다.
酸化
[
編輯
]
還元
[
編輯
]
시토크롬 P450 還元酵素는 細胞 안
小胞體
로의 電子 傳達에 必要한 막 結合 酵素이다. POR/P450 시스템에서 一般的인 電子 흐름은 다음과 같다. NADPH → FAD → FMN → P450 → O
2
還元 反應 동안 化學 物質은 無益한 循環(futile cycling)에 들어갈 수 있다. 이 循環에서 物質은 自由 라디칼 電子를 얻은 다음 卽時
酸素
로 내어 주고, 酸素는
過酸化物 陰이온
을 形成한다.
加水分解
[
編輯
]
2段階 ? 接合
[
編輯
]
이어지는 2段階 反應에서는 1段階 反應으로 인해 活性化된 生體外 代謝産物이
글루타티온
(GSH),
黃酸鹽
,
글라이신
,
글루쿠론산
과 같은 電荷를 띄는 物質과 接合된다. 藥물의 接合 反應이 일어나는 部位에는
카복실機
(-COOH),
하이드록시機
(-OH),
아미노기
(NH
2
),
티올기
(-SH)가 있다. 接合 反應의 生成物은 種種
活性 代謝物質
을 生成하는 1段階 反應과 달리 分子量이 增加하고, 器質보다 덜 活性을 띄는 傾向이 있다. 큰 陰이온 그룹(예: GSH)을 追加하면 反應性
親展自體
를 解毒하며, 膜을 가로질러 擴散할 수 없는 極盛 代謝産物을 더 많이 生成하므로 活潑하게 輸送될 수 있다.
이러한 反應은 廣範圍한 特異性을 가지는 轉移酵素 그룹에 依해 觸媒되며, 이 轉移酵素는 結合하여 親核性, 親前者性 作用基를 包含하는 거의 모든 疏水性 化合物을 代謝할 수 있다.
[1]
이 轉移酵素 그룹의 가장 重要한 酵素 中 하나는
글루타티온 S-轉移酵素
(GST)이다.
| 器具
|
關聯 酵素
|
補助 人者
|
位置
|
出處
|
| 메틸화
|
메틸기轉移酵素
|
S-아데노실-L-메티오닌
|
肝, 腎臟, 肺, CNS
|
[9]
|
| 黃酸鹽
|
설抛트랜스퍼레이스
|
3'-抛스포아데노신-5'-포스鋪設페이트
|
肝, 腎臟, 所長
|
[9]
|
| 아세틸化
|
- N-아세틸트랜스퍼레이스
- 膽汁酸-CoA: 아미노산 N-아실트랜스퍼레이스
|
아세틸-CoA
|
肝, 肺, 脾臟, 胃 粘膜,
赤血球
, 림프球
|
[9]
|
| 글루쿠론火
|
UDP-글루쿠로노실트랜스퍼레이스
|
UDP-글루쿠론산
|
肝, 腎臟, 腸, 肺, 皮膚, 前立샘, 腦
|
[9]
|
| 글루타티온 接合
|
글루타티온 S-트랜스퍼레이스
|
글루타티온
|
肝, 腎臟
|
[9]
|
| 글라이신 接合
|
- XM-라이게이스 (異種 生物的 아실-CoA 形成)
- 글리신 N-아실트랜스퍼레이스 (글리신 接合體 形成)
|
글라이신
|
肝, 腎臟
|
|
3段階 ? 追加 變形과 排泄
[
編輯
]
生體異物 接合體는 2段階 反應 以後에도 追加로 代謝될 수 있다. 一般的인 例示로는 글루타티온 接合體를
아세틸시스테인
(메르캅투르산) 接合體로 加工하는 것이다.
[10]
여기에서 글루타티온 分子의
γ-글壘打메이트
와
글라이신
殘期는
감마-글壘打밀 傳達 酵素
와
다이펩티데이스
에 依해 除去된다. 마지막 段階에서 接合體의
시스테인
殘期는
아세틸化
된다.
接合體와 그 代謝産物은 3段階 大事 中 細胞에서 排泄될 수 있으며 陰이온氣는
P-糖蛋白質
(多重藥物 耐性 蛋白質, MRP) 系列의 다양한 막 輸送體에 對한
表紙蛋白質
役割을 한다.
[11]
이 蛋白質들은
ABC輸送體
系列에 屬하며 매우 다양한 疏水性 陰이온의 ATP 依存性 輸送을 촉매할 수 있다.
[12]
, 따라서 2段階 臺詞에서 生成된 物質을 細胞 밖으로 除去하는 作用을 한다. 細胞 밖으로 나온 뒤 生成物들은 追加로 大使되거나 排泄될 수 있다.
[13]
內因性 毒素
[
編輯
]
過酸化物
이나 反應性
알데하이드
와 같은 內因性(몸 안에서 生成된) 反應性 代謝 産物의 害毒은 種種 위에서 說明한 시스템으로는 達成할 수 없다. 內因性 代謝 産物은 該當 種의 正常的인 細胞 構成 要素에서 派生되고, 一般的으로 極性을 가진다. 그러나 이러한 化合物은 그 數가 적기 때문에 酵素 시스템이 特定 分子를 認識하여 除去하는 것이 可能하다. 이러한 分子는 有用한 代謝 産物과도 類似한데, 따라서 內因性 毒素의 各 그룹을 臺詞하는 데에는 一般的으로 서로 다른 解毒 酵素가 必要하다. 이러한 特異的인 解毒 시스템의 例로는 反應性 알데하이드
메틸글리옥살
을 處理하는 役割을 하는
글리옥살레이스 시스템
과,
活性 酸素種
을 除去하는 多樣한
抗酸化
시스템이 있다.
大使 場所
[
編輯
]
모든
組織
은 藥물을 臺詞하는 能力이 있지만, 量的으로 重要한 機關은
肝細胞
의
매끈小胞體
이다. 藥물 臺詞에 肝이 重要한 理由는 肝이 큰 機關이고,
腸
에서 吸收된 化學 物質이
肝門脈界
를 통해 最初로 貫流되며, 다른 機關에 비해 大部分의 藥물 代謝 酵素 시스템이 매우 높은 濃度로 存在하기 때문이다. 藥물이 胃腸管으로 吸收된 後
肝門脈
을 통해 肝으로 들어가면 많은 種類의 藥물이 臺詞되어
初回 通過 效果
가 發生한다.
藥물 臺詞가 일어나는 다른 部位에는
胃腸管
,
肺
,
콩팥
,
皮膚
의
上皮 細胞
等이 있다. 이러한 部位들은 一般的으로 局所的인 毒性 反應을 擔當한다.
藥물 代謝에 影響을 미치는 要因
[
編輯
]
大部分의 親油性 藥물의 藥理學的 作用의 持續 時間과 强度는 非活性 産物로 代謝되는 速度에 依해 決定된다.
시토크롬 P450
시스템은 이런 藥물 臺詞에서 가장 重要한 經路이다. 一般的으로 藥理學的 活性 代謝 産物의 代謝 速度를 증가시키는 모든 것(예:
酵素誘導
)은 藥物 作用의 持續 時間과 强度를 감소시킨다.
酵素抑制
와 같은 反對의 境遇는 持續 時間과 强度를 증가시킨다. 그러나 酵素가 戰區藥물을 藥物로 臺詞하는 役割을 하는 境遇 酵素誘導는 이러한 轉換 速度를 높이고 藥물 濃度를 증가시켜 潛在的으로 毒性을 誘發할 수 있다.
다양한 生理學的, 病理學的 要因도 藥물 代謝에 影響을 줄 수 있다. 藥물 代謝에 影響을 줄 수 있는 生理學的 要因에는 年齡, 個人差(
藥物誘電體學
的인 原因),
腸肝循環
,
營養
,
腸內 細菌무리
,
性別 差異
가 있다.
一般的으로 藥물은
成人
보다
胎兒
,
新生兒
,
老人
에서 더 천천히 代謝된다.
遺傳的 變異(
多形性
)는 藥物 效果의 可變性을 一部 說明한다.
시토크롬 P450
모노옥시第네이스 시스템의 酵素도 個人에 따라 다를 수 있으며, 民族的 背景에 따라 1~30%의 사람들에게서 缺乏이 發生한다.
藥물의 容量, 頻度, 投與 經路, 組織 分布,
蛋白質 結合
도 代謝에 影響을 미친다.
間
,
콩팥
,
心臟
疾患 같은 病理學的 要因도 藥물 代謝에 影響을 줄 수 있다.
In silico
모델링 및 시뮬레이션 方法을 使用하면 人間을 對象으로 한 臨床 硏究를 遂行하기 前에 假想 患者 集團에서 藥물 大使를 豫測할 수 있다.
[14]
이 方法은 副作用으로 인해 가장 危險한 사람을 識別하는 데 使用할 수 있다.
歷史
[
編輯
]
사람들이 攝取한 物質을 어떻게 몸 안에서 變形시키는지에 對한 硏究는 19世紀 中盤에 化學者들이
벤즈알데하이드
와 같은 有機 化學 物質이 酸化되어 人體의
아미노산
과 結合될 수 있다는 것을 發見하면서 始作되었다.
[15]
以後 19世紀의 나머지 期間 동안
메틸화
,
아세틸化
,
설폰火
와 같은 몇 가지 다른 基本的인 解讀 反應이 發見되었다.
20世紀 初盤에는 이러한 臺詞 産物의 生産을 擔當하는 酵素와 經路에 對한 硏究가 進行되었다. 이 分野는 1947年
리처드 테크윈 윌리암스
(Richard Tecwyn Williams)가 "Detoxication mechanisms"라는 冊을 出版하면서 別途의 硏究 分野로 定義되었다.
[16]
이 現代的인 生化學的 硏究는 1961年 글루타티온
S-
傳達 酵素의 同情,
[17]
1962年 시토크롬 P450의 發見,
[18]
1963年 生體異物 臺詞에서 글루타티온 P450의 中樞的 役割을 發見하는 成果로 이어졌다.
[19]
[20]
같이 보기
[
編輯
]
各州
[
編輯
]
追加 資料
[
編輯
]
外部 링크
[
編輯
]