鹽素酸 칼륨
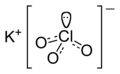 The structure of the ions in potassium chlorate The structure of the ions in potassium chlorate
|
 The crystal structure of potassium chlorate The crystal structure of potassium chlorate
|
|

|
| 이름
|
| 別稱
Potassium chlorate(V), Potcrate
|
| 識別子
|
|
|
|
|
|
|
| ChemSpider
|
|
| ECHA InfoCard
|
100.021.173
|
| EC 番號
|
|
|
|
|
| RTECS 番號
|
|
| UNII
|
|
| UN 番號
|
1485
|
|
|
|
InChI=1S/ClHO3.K/c2-1(3)4;/h(H,2,3,4);/q;+1/p-1
 예 예
Key: VKJKEPKFPUWCAS-UHFFFAOYSA-M
 예 예
InChI=1/ClHO3.K/c2-1(3)4;/h(H,2,3,4);/q;+1/p-1
Key: VKJKEPKFPUWCAS-REWHXWOFAC
|
|
|
| 性質
|
|
|
KClO
3
|
| 몰 質量
|
122.55 g mol
?1
|
| 겉보기
|
white crystals or powder
|
| 密度
|
2.32 g/cm
3
|
| 녹는點
|
356 °C (673 °F; 629 K)
|
| 끓는點
|
400 °C (752 °F; 673 K) decomposes
[1]
|
|
|
3.13 g/100 mL (0 °C)
4.46 g/100 mL (10 °C)
8.15 g/100 mL (25 °C)
13.21 g/100 mL (40 °C)
53.51 g/100 mL (100 °C)
183 g/100 g (190 °C)
2930 g/100 g (330 °C)
[2]
|
| 溶解度
|
soluble in
glycerol
negligible in
아세톤
and liquid
ammonia
[1]
|
| glycerol
에서의
溶解度
|
1 g/100 g (20 °C)
[1]
|
|
|
−42.8·10
?6
cm
3
/mol
|
|
|
1.40835
|
| 救助
|
|
|
monoclinic
|
| 熱化學
|
|
|
100.25 J/mol·K
[1]
|
|
|
142.97 J/mol·K
[3]
[1]
|
|
|
?391.2 kJ/mol
[3]
[1]
|
|
|
-289.9 kJ/mol
[1]
|
| 危險
|
| 物質 安全 保健 資料
|
ICSC 0548
|
| GHS 그림文字
|
   [4] [4]
|
| 信號어
|
危險
|
|
|
H271
,
H302
,
H332
,
H411
[4]
|
|
|
P220
,
P273
[4]
|
| NFPA 704
(파이어 다이아몬드)
|
|
| 半修 致死量 또는 半修 致死濃度 (LD, LC):
|
|
|
1870 mg/kg (oral, rat)
[5]
|
| 關聯 化合物
|
|
|
Potassium bromate
Potassium iodate
Potassium nitrate
|
|
|
Ammonium chlorate
Sodium chlorate
Barium chlorate
|
關聯 化合物
|
Potassium chloride
Potassium hypochlorite
Potassium chlorite
Potassium perchlorate
|
달리 明示된 境遇를 除外하면,
標準狀態
(25 °C [77 °F], 100 kPa)에서 物質의 情報가 提供됨.
|

鹽素酸 칼륨
(?素酸kalium, potassium chlorate) 또는 鹽素酸 포타슘은 KClO
3
分子式을 지닌 化合物로,
칼륨
,
鹽素
,
酸素
原子가 包含되어 있다. 純粹 形態에서는 흰 結晶 物質이다. 産業用으로 가장 흔한
鹽素酸鹽
이다. 光澤이 있는 無色의 單斜晶系 決定이며 混合爆藥으로 쓰일 程度로 摩擦과 衝擊에 銳敏해 잘 暴發한다. 더 加熱하면 酸素를 放出하고 全部 염화칼륨이 된다. 이 反應은 二酸化亡家니즈 MnO
2
와 같은 金屬酸化物을 加하면 促進되어 70°C에서 酸素를 發生하기 始作하므로, 實驗室 等에서 酸素를 얻기 위해 利用된다. 但, 有機物·黃·炭素 等이 混入되면 爆發하므로 注意해야 한다. 吸濕性은 없다. 물에 녹고, 알코올에도 少量 녹는다. 中性 및 알칼리성 溶液에서는 酸化作用이 없으나, 酸性 溶液에서는 剛한 酸化劑가 된다.
| 化學式
|
KClO
3
|
| 分子量
|
122.55g/mol
|
| 녹는點
|
368°C
|
| 끓는點
|
400°C (分解)
|
| 比重
|
2.326 (39°C)
|
| 非熱容量
|
100.25J/(mol·K)
|
| 溶解度
|
8.15g/100mL
|
利用
[
編輯
]
 雪糖을 태우는 鹽素酸 칼륨
雪糖을 태우는 鹽素酸 칼륨
다음의 用途로 쓰인다.
酸化劑로서 성냥·연화·爆藥 等의 原料가 되고, 漂白劑·染料·醫藥品 等의 製造에도 使用된다. 長期間 保存한 것은 亞鹽素酸칼륨을 含有하여, 乾燥 狀態에서는 有機物·因·黃 等 可燃性 物質과 接觸하기만 해도 暴發한다. 摩擦·衝擊 等에 銳敏하여, 爆發事故를 잘 일으키며, 津한 黃酸이나 津한 窒酸과 接觸해도 잘 暴發한다. 混合爆藥으로 쓰이기도 하며, 劇藥이다. 빛이 遮斷되는 密閉된 容器에 保管한다.
準備
[
編輯
]
- 3 NaOCl → 2NaCl + NaClO3
- KCl + NaClO3 → NaCl + KClO3
- 3Cl2(g) + 6KOH (aq) → KClO3 (aq) + 5KCl (aq) + 3H2O(l)
各州
[
編輯
]
- ↑
가
나
다
라
마
바
社
“potassium chlorate”
. 2015年 7月 9日에 確認함
.
- ↑
Seidell, Atherton; Linke, William F. (1952).
《Solubilities of Inorganic and Organic Compounds》
. Van Nostrand
. 2014年 5月 29日에 確認함
.
- ↑
가
나
Zumdahl, Steven S. (2009). 《Chemical Principles 6th Ed.》. Houghton Mifflin Company. A22쪽.
ISBN
0-618-94690-X
.
- ↑
가
나
다
“Potassium chlorate”
. 2012年 9月 22日에
原本 文書
에서 保存된 文書
. 2015年 7月 9日에 確認함
.
- ↑
Michael Chambers.
“ChemIDplus - 3811-04-9 - VKJKEPKFPUWCAS-UHFFFAOYSA-M - Potassium chlorate - Similar structures search, synonyms, formulas, resource links, and other chemical information.”
. 2015年 7月 9日에 確認함
.
- ↑
Manochai, P.; Sruamsiri, P.; Wiriya-alongkorn, W.; Naphrom, D.; Hegele, M.; Bangerth, F. (2005年 2月 12日).
“Year around off season flower induction in longan (Dimocarpus longan, Lour.) trees by KClO3 applications: potentials and problems”
. 《Scientia Horticulturae》 (Department of Horticulture, Maejo University, Chiang Mai, Thailand; Department of Horticulture, Chiang Mai University, Chiang Mai, Thailand; Institute of Special Crops and Crop Physiology, University of Hohenheim, 70593 Stuttgart, Germany)
104
(4): 379?390
. 2010年 11月 28日에 確認함
.
外部 링크
[
編輯
]
 위키미디어 公用에
鹽素酸 칼륨
關聯 미디어 分類가 있습니다.
위키미디어 公用에
鹽素酸 칼륨
關聯 미디어 分類가 있습니다.
같이 보기
[
編輯
]