| Vann
|
|---|
|
| Identifikatorer
|
| CAS-nummer
| 7732-18-5
|
|---|
| Kjemiske egenskaper
|
| Formel
| H
2
O
|
|---|
| Molar masse
| 18,01528
g/mol
|
|---|
| Utseende
| Gjennomsiktig væske
|
|---|
| Tetthet
| 997,0474
kg/m
3
|
|---|
| Smeltepunkt
| 0
°C
|
|---|
| Kokepunkt
| 99,98
°C
|
|---|
| Damptrykk
| 3.1690 kPa
|
|---|
| p
K
a
| 13,995
|
|---|
| p
K
b
| 13,995
|
|---|
| λ
| 0,6065 W/(m·K) W/mK
|
|---|
| n
D
| 1,3330 (20 °C)
|
|---|
| Viskositet
| 0.890 cP
|
|---|
| Dipolmoment
| 1,8546 D
|
|---|
| Struktur
|
| Krystallstrukt.
| Heksagonal
|
|---|
| Termokjemiske egenskaper
|
Dannelsesentalpi
Δ
f
H
o
298
| Δ
f
H
0
gass
?241,83
kJ
/
mol
Δ
f
H
0
flytende
?285,83 kJ/mol
Δ
f
H
0
fast
-291,83 kJ/mol
|
|---|
Molar entropi
S
o
298
| S
0
gass
188,84 J/mol·K
S
0
flytende
69,95 J/mol·K
S
0
fast
41 J/mol·K
|
|---|
| Varmekapasitet
, C
| 4,2
kJ
/(
kg
K
)
|
|---|
| Farer
|
| Fare for huden
| Langvarig nedsenkelse i vann kan føre til avskalling.
|
|---|
| Fare for øyne
| Ufarlig.
|
|---|
| Innandingsfare
| Ugiftig. Kvelning i vann kalles
drukning
.
|
|---|
| Fare ved svelging
| Livsnødvendig
. Overdrevet inntak kan føre til
vannforgiftning
.
|
|---|
| Relatert
|
| Andre
kationer
| Hydrogen sulfid
,
Hydrogen selenid
,
Hydrogen tellurid
,
Hydrogen polonid
,
Hydrogen peroksid
|
|---|
- For ≪et vann≫, se
innsjø
.
 En foss
En foss
Vann
, eller
vatn
[1]
(fra
norrønt
vatn
), er en
kjemisk forbindelse
og et
polart molekyl
. Det er flytende under
STP
-forhold. Dens
kjemiske formel
er
H
2
O
, som betyr at et
molekyl
vann bestar av to hydrogenatomer og ett
oksygenatom
.
Vann finnes nesten overalt pa
Jorden
og er livsnødvendig for alt kjent
liv
. Omtrent 70 % av Jordens overflate er dekket av apent vann (hav, innsjøer og elver).
En
vannmasse
eller
vassmasse
er et uttrykk for et
osean
,
hav
,
innsjø
,
elv
,
bekk
,
kanal
,
dam
eller lignende.
Ordet ≪vann≫ kommer via
norrønt
vatn
, videre fra
indoeuropeisk
, som igjen er utviklet fra
urindoeuropeisk
fra roten *
wes
. Det
skandinaviske
ordet ≪
vinter
≫, de
engelske
ordene ≪
water
≫ og ≪
wash
≫, med flere, det
tyske
ordet ≪
Wasser
≫ og de
russiske
ordene ≪вода,
voda
≫ og ≪водка,
vodka
≫ har samme opphav. Avledet fra urindoeuropeisk *
ud-ro
kommer ogsa
greske
hydro
(≪vann≫) og
hydra
, mens det
latinske
aqua
kommer fra urindoeuropeisk *
agwjo
.
Vann i fast form er kjent som
is
og i gassform som
damp
. Temperaturskalaen
celsius
er definert ut fra vannets smelte- og fordampningspunkt, der vannet fryser ved 0 °C og koker ved 100 °C, og en grad stigning tilsvarer 1/100 av forskjellen mellom disse punktene. Temperaturskalen
Kelvin
har samme stigningstall. Mellom smeltepunktet og kokepunktet, inkludert i
STP
-forhold, er vannet i flytende tilstand (ved normalt trykk).
Temperaturenhetene (tidligere celsius og na kelvin) er definert ut i fra
trippelpunktet
til vann, 273,16 K (0,01 C) og 611,2
Pa
. Under dette trykket og denne temperaturen kan fast, flytende og gassformen av vann eksistere samtidig i likevekt. Vann viser ganske merkelig atferd, som a kunne eksistere som glassaktig is, en ikke-krystallisk fast form av vann.
Under temperaturer større enn 647
K
og trykk større enn 22,064
Mpa
, vil en samling av vannmolekyler anta en
superkritisk
tilstand, der væskelignende grupper flyter inni en gasslignende fase.
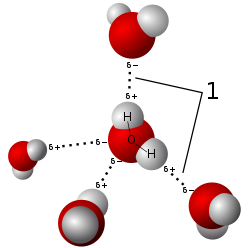 Modell av vannmolekyler med hydrogenbindinger mellom seg (1).
Modell av vannmolekyler med hydrogenbindinger mellom seg (1).
En viktig egenskap ved vann er dets
polare
egenskap. Vannmolekylet H
2
O er vinklet, med
oksygen
i spissen og
hydrogenatomer
ytterst. Siden oksygen har høyere
elektronegativitet
enn hydrogen, har oksygenatomets side delvis negativ ladning i forhold til hydrogensiden. Et molekyl med en slik ladningsforskjell kalles en
dipol
. Spenningsforskjellene gjør at vannmolekylene tiltrekkes av hverandre (den negative siden trekkes til et annets molekyl positive side) og til andre polare molekyler. Dette kalles
hydrogenbinding
. Denne kraften er relativt svak, men det høye antallet
hydrogenbindinger
fører til at vann har en rekke spesielle fysiske egenskaper.
Vann har, pa grunn av hydrogenbindingene, et veldig høyt
kokepunkt
, siden det trengs mye
energi
for a bryte disse bindingene mellom molekylene.
Grunnstoffet
svovel
som ligger under
oksygen
i
periodesystemet
, og dets tilsvarende kjemiske forbindelse
hydrogensulfid
(H
2
S), har ikke disse hydrogenbindingene og er en
gass
ved romtemperatur selv om det har dobbelt sa høy
molekylvekt
som vann. Hydrogenbindinger gir ogsa vann høy
varmekapasitet
, det vil si at det trengs mye energi for a varme opp vann.
Hydrogenbindinger gir samtidig vann spesielle egenskaper nar det fryser. Som de fleste andre materialer blir vannets tetthet større ved lavere temperatur. Men nar vann blir kjølt ned til nær
frysepunktet
fører hydrogenbindingene til – mens vannmolekylene flytter pa seg for a minimalisere sin energi ? at det dannes en struktur som faktisk har lavere tetthet. Dermed vil vann utvide seg nar det fryser og is vil flyte i vann, mens de fleste andre materialer krymper og synker nar de gar over til fast form.
Flytende vann har sin høyeste tetthet ved 3,98 °C. Dette har en interessant konsekvens for livet i vannet om vinteren. Vann som blir avkjølt ved overflaten blir tyngre og synker, og danner
konveksjonsstrømmer
som avkjøler hele vannet. Nar overflaten kjøles under 4 °C blir den imidlertid lettere, konveksjonsstrømmene opphører, og overflaten fryser til is som danner en isolerende hinne som kan hindre videre nedkjøling og bunnfrysing. Dermed kan fisk og andre organismer leve videre i vannet som holder ca. 4 °C pa bunnen. (Grunt vann vil likevel bunnfryse ved sterk kulde.)
 Salt (
NaCl
) løser seg i vann.
Salt (
NaCl
) løser seg i vann.
Vann er ogsa et godt
løsemiddel
pa grunn av sin polaritet. Egenskapene som løsemiddel er livsviktige i
biologi
, fordi mange biokjemiske reaksjoner forekommer kun i vannholdige
løsninger
, for eksempel reaksjoner i
celleslimet
og
blodet
. I tillegg brukes vann til a transportere
biologiske molekyler
.
Nar en ionisk eller polar forbindelse kommer i kontakt med vann blir den omringet av vannmolekyler. Siden vannmolekylene er relativt sma kan de omringe helt et molekyl av det oppløste. De delvis negative dipolene til vann blir tiltrukket av de positivt ladde delene av det oppløste, og motsatt for de positive dipolene.
Et eksempel pa en ionisk løsning er
bordsalt
; natriumklorid, NaCl, vil dele seg opp i Na
+
?
kationer
og Cl
?
?
anioner
. Hvert ion vil bli omringet av vannmolekyler. Ionene blir da lett fraktet ut av sitt krystallgitter og inn i løsningen. Et eksempel pa en ikke-ionisk løsning er
sukker
. Dipolene til vann vil hydrogenbinde seg til de dipolare omradene pa sukkermolekylet og frakter det ut i løsningen.
Generelt løser ioniske og polare substanser som
syrer
,
alkoholer
og
salter
seg lett med vann, mens ikke-polare substanser som fett gjør ikke det. Ikke-polare molekyler holder seg sammen i vann fordi det er energisk mer gunstig for vannmolekylene a hydrogenbinde seg med hverandre enn a anta
van der Waals forbindelser
med ikke-polare molekyler.
Selv om vann er essensielt for menneskekroppen, kan sterkt overdrevet vanninntak kan føre til en potensielt livstruende tilstand kjent som
vannforgiftning
. Arsaken er at vannet fører til en lavere konsentrasjon av blant annet elektrolytter i blodet.
 Kapillærkrefter,
kohesjon
og adhesjon, fører til at vann beveger seg oppover, mot tyngdekraften. Her sammenlignet med kvikksølv.
Kapillærkrefter,
kohesjon
og adhesjon, fører til at vann beveger seg oppover, mot tyngdekraften. Her sammenlignet med kvikksølv.
De sterke hydrogenbindingene gir høy
kohesjon
, og dermed
overflatespenning
. Dette ses tydelig hvis man har vann pa en overflate som ikke er løselig i vann. Vannet holder seg samlet i draper. Denne evnen er viktig nar plantene frakter vann gjennom stengelen; de sterke intramolekylære kreftene holder vannet sammen og motvirker
harrørskreftene
. Andre
væsker
vil ha langt større tendens til a danne luftlommer,
vakuum
og dermed stoppe væsketilførselen.
Rent vann er en
isolator
, men likevel er det vanlig a se pa vann som et elektrisk ledende, eller konduktivt, stoff. Hvis et
salt
løses i vann, vil denne
saltløsningen
(elektrolytten) kunne lede elektrisk strøm. Denne ledeevnen skyldes
redoksreaksjonen
som oppstar i løsningen. Det er altsa ikke selve vannet som leder strømmen. Se
Elektrolyse
nedenfor.
Vann kan deles opp i sine bestanddeler, hydrogen og oksygen, ved a la en strøm ga gjennom det. Denne prosessen kalles
elektrolyse
. Vannmolekyler skiller seg naturlig til H
+
- og OH
-
-ioner som trekkes henholdsvis mot
anoden
og
katoden
. Ved katoden vil to H
+
-ioner ta opp elektroner og danne H
2
-gass. Ved anoden gar fire OH
?
-ioner sammen og danner O
2
-gass og avgir fire elektroner. Gassene som blir dannet bobler opp til overflaten og kan bli samlet opp.
Vann kan oppføre seg som bade
syre
og
base
; det kan bade avgi og motta
protoner
(H
+
), en reaksjon som kalles
protolyse
. Vann protolyserer med seg selv etter følgende likevektsreaksjon:
H
2
O + H
2
O ↔ H
3
O
+
+ OH
-
Vann reagerer med
syrer
og
baser
og lager sure og basiske løsninger, etter hvor sterke syrene/basene er. Hvor sur eller basisk en løsning er, males med
pH
(eller
pOH
). pH er et mal pa konsentrasjonen av
oksoniumioner
(H
3
O
+
) i en løsning, mens pOH er et mal pa konsentrasjonen av
hydroksidioner
(OH
?
). Jo lavere pH, jo høyere er konsentrasjonen av H
3
O
+
. I vann ved romtemperatur er
produktet
av konsentrasjonene av H
3
O
+
og OH
?
alltid 10
?14
(mol/l)
2
; summen av pH og pOH er 14. Ved pH 7 er konsentrasjonen av H
3
O
+
og OH
?
lik, og løsningen er nøytral. Hvis denne
likevekten
forstyrres, blir løsningen sur (lavere pH; mer H
3
O
+
) eller basisk (høyere pH; mer OH
?
).
Det systematiske syrenavnet for vann er hydroksisyre, mens det systematiske basenavnet er hydrogenhydroksid. Det bør imidlertid nevnes at vann alene er verken syre eller base, men kan altsa opptre som en svak syre eller en svak base i nærvær av hhv. en sterk base eller en sterk syre.
I teorien har rent vann pH 7, men i praksis er rent vann svært vanskelig a fremstille. Vann som er i kontakt med
luft
over en viss tid opptar raskt
karbondioksid
og danner en løsning av karbonsyre (
kullsyre
) med en likevekt-pH pa ca. 5,7.
[2]
Rent vann er farget i en veldig lys blafarge
[3]
, men oppfattes som oftest som fargeløst, og viser som regel fargen pa stoffene bak eller rundt, eller reflekterer lyset som treffer vannoverflaten. Havet er faktisk blatt i seg selv og ikke bare fordi det reflekterer himmelen. Under visse lysforhold kan regn eller lignende vannfall vise en
regnbue
.
Rent vann har ingen lukt eller smak, men siden vann er et meget godt løsemiddel vil det ofte være
salter
og andre forurensinger til stede. Nar man refererer til ≪smaken≫ pa vann fra ulike kilder, er det tilstedeværelsen av disse forurensningene man egentlig sikter til.
 Modell av et vannmolekyl.
Modell av et vannmolekyl.
Kjemisk formel: H
2
O,
dihydrogenmonoksid
.
Kjemikere
omtaler tidvis vann spøkefullt som
dihydrogenmonoksid
eller
DHMO
, molekylets systematisk kovalente navn, særlig i
parodier
pa kjemisk forskning som krever forbud mot dette ≪farlige kjemikaliet≫.
[4]
I byen Aliso Viejo i
California
ble
isoporkopper
nesten bannlyst da det ble kjent at DHMO var brukt i produksjonen.
[5]
 Vannets kretsløp; hvordan vannet beveger seg rundt pa jorden.
Vannets kretsløp; hvordan vannet beveger seg rundt pa jorden.
 Det meste av vannet pa jorden befinner seg i de store havbassengene. Her fra kysten utenfor California.
Det meste av vannet pa jorden befinner seg i de store havbassengene. Her fra kysten utenfor California.
- Se ogsa:
hydrologi
,
vannets kretsløp
Vann eksisterer i mange former omtrent overalt pa jorden, til og med dypt under de store ørkenene. Mesteparten av vannet befinner seg i
verdenshavene
og som
polaris
, men en del finnes ogsa som skyer og vanndamp, regnvann, elver, vassdrag og is. Vannet forandrer stadig aggregattilstand, drevet av sollyset, og sirkulerer dermed rundt, og har pa den maten en kontinuerelig bevegelse,
vannets kretsløp
. Gjennom
fordampning
,
nedbør
og
avrenning
, avgjør vannet temperaturen og klimaet over hele jorden.
Den totale vannmengden pa jordkloden anslas til a være ca.
1 384 120 000 km³
. Mesteparten av dette finnes i havet, ca. 97,2 %. Resten, ca. 2,8 % er ferskvann. 2,15 % av dette finnes i frossen tilstand som breer og innlandsis, 0,63 % befinner seg under bakkeniva som grunnvann. Bare 0,02 % befinner seg i vassdrag, elver og innsjøer, og ikke mer enn 0,001 % som vanndamp i atmosfæren.
Vannet har høyest
densitet
ved 4 °C, hvilket gjør at det kalde vannet, og det av vannet som har frosset til is, legger seg som et isolerende lag over det varmere vannet. Dette gjør at større vannansamlinger veldig sjeldent bunnfryser, hvilket gir godt grunnlag for liv i innsjøer, elver og i havet.
Vann som har fordampet og kondensert, faller ? dersom ansamlingen er tung nok ? ned til jorden som nedbør. Dette er avgjørende for
jordbruk
og for mennesker generelt. Mennesker har derfor en mengde ord for a beskrive de ulike formene nedbør, for eksempel
regn
,
hagl
,
snø
,
take
og
dugg
.
Pa samme mate har hvordan vannet renner stor betydning for menneskenes tilholdssteder.
Elver
og oppsamling av vann er viktige forutsetninger for vart jordbruk, og
havene
gir muligheter for
fiske
, samt for
reise
,
handel
og
transport
. Gjennom
erosjon
former vannet
kontinentene
og
landskapet
. De fleste mennesker lever i
daler
og ved
elvedeltaer
.
Vannet trenger inn i jorden og blir
jordvann
. Dette
grunnvannet
tar seg opp til jordens overflate igjen, gjennom naturlige vannkilder og menneskenes brønner, eller som
varme kilder
og
geysirer
.
Økt etterspørsel etter vann pavirker ogsa investeringsnivaet. FN venter at det globalt vil investeres for nærmere 800 milliarder dollar i aret frem mot 2020.
[6]
Tidevann er en periodisk variasjon i vannstanden i havet, hvor havet stiger og synker, fordi manen og solen med sin tyngdekraft trekker vannet i havet mot seg. Forandringer kommer av at manen og solen forandrer posisjon i forhold til jorden, kombinert med jordens rotasjon og lokalt
batymetri
. Dette forarsaker forandringer mht. hvor høyt vannet star, spesielt ved kysten, og skaper ogsa varierende strømmer, kjent som tidevannsstrøm. Økologisk er landstripen som vises ved lavvann er en viktig sone.
Mye av universets vann er et biprodukt av
stjernedannelse
. En stjernes fødsel involverer sterke ytre vinder som inneholder gass og støv. Nar denne utstrømningen av materialer til slutt pavirker det omkringliggende gassen vil sjokkbølgene som oppstar komprimere og varme opp gassene. I denne oppvarmede, tette gassen produseres vann
[7]
Den 22. juli 2011 ble det publisert en rapport om oppdagelsen av en gigantisk sky av vanndamp, som inneholder ≪140 billioner ganger mer vann enn alle verdens hav til sammen≫ rundt en
kvasar
12 milliarder
lysar
fra Jorden. Ifølge forskerne viser funnet at ≪vann har vært utbredt i universet nesten siden universets begynnelse≫.
[8]
[9]
Vann er pavist i
interstellare skyer
i var egen
galakse
,
Melkeveien
. Sannsynligvis finnes vann i overflod i andre galakser siden vannets komponenter, hydrogen og oksygen, er blant de vanligste elementene i universet. Over tid vil de interstellare skyene kondensere til
solskyer
og
solsystemer
som vart eget.
Vanndamp er til stede i
Flytende vann er til stede pa
- Jorden: 71 % av overflaten
- Europa
: 100 km dypt undergrunnshav
Mye tyder pa at flytende vann er til stede like under overflaten av Saturns mane
Enceladus
.
Is er til stede pa
Vann i form av is kan være til stede pa
Ceres
og
Tethys
. Vann og andre
volatiler
utgjør sannsynligvis mye av de indre strukturene i
Uranus
og
Neptun
og vannet i de dypere lagene kan være i form av
ionisk vann
som molekylene bryter ned til en suppe av hydrogen- og oksygenioner, og dypere nede
superionisk vann
der oksygen krystalliseres mens hydrogenionene flyter fritt rundt inne i oksygenkrystallene.
[14]
 Mennesker som foretar hinduistiske seremonier ved en av
ghats
-ene ved
Ganges
, i
Varanasi
.
Mennesker som foretar hinduistiske seremonier ved en av
ghats
-ene ved
Ganges
, i
Varanasi
.
Vann blir ansett som rensende i de fleste religioner. Rituell vask inngar i flere større religioner, blant annet innen
kristendom
,
hinduisme
,
rastafaribevegelsen
,
islam
,
shintoisme
,
taoisme
og
jødedom
. Nedsenking av en person i vann er et sentralt sakrament i kristendommen (hvor det er kalt
dap
); det er ogsa en del av praksisen i andre religioner, som jødedom (
mikvah
) og
sikhisme
(
Amrit Sanskar
). I tillegg blir døde badet i rent vann i mange religioner, inkludert jødedom og islam. Innen islam kan de fem daglige bønnene som regel gjennomføres etter a ha vasket visse deler av kroppen med rent vann (
wudu
). I shintoisme blir vann brukt i nesten alle ritualer for a vaske en person eller et omrade, for eksempel i
misogi
-ritualet.
Noen trossamfunn bruker vann spesielt forberedt for religiøs bruk (
hellig vann
innen kristendommen,
amrita
i sikisme og hinduisme). Mange religioner anser ogsa visse vannkilder eller vannansamlinger som hellige eller i det minste gunstige, for eksempel
Lourdes
i
Den romersk-katolske kirke
,
Jordan
(i det minste symbolsk) i noen kristne samfunn,
Zamzam
i islam og elva
Ganges
(blant mange andre) i hinduismen.
Vann er ofte ansett a ha spirituell makt. Innen
keltisk mytologi
er
Sulis
den lokale gudinnen for varme kilder, og i hinduismen er
Ganges
ogsa personifisert som gudinne, mens
Saraswati
har blitt referert til som gudinne i
Vedaene
. Vann er ogsa en av hinduismens elementer, sammen
ild
,
jord
,
rom
og
luft
. Guder kan ogsa være beskyttere for visse kilder, elver eller sjøer: For eksempel var den greske og romerske guden
Peneus
en elvegud, en av tre tusen
okeanider
. I islam gir ikke vann bare liv, men livet selv har kommet fra vannet.
Den greske filosofen
Empedokles
ansa vann som en av de fire
klassiske elementene
, sammen
ild
,
jord
og
luft
. Det ble ogsa ansett som
ylem
, en basisk substans av universet. Vann ble ansett som kaldt og vatt. I teorien om de
fire kroppsvæsker
forbindes vannet med slim. Vann var ogsa en av de fem elementene innen tradisjonell kinesisk filosofi, sammen med jord, ild, tre og metall.
UNESCOs
internasjonale vannforskningsprogram og deres
World Water Development Report
(2003) anslar at verden i løpet av de neste 20 arene star foran en mangel pa
drikkevann
uten sidestykke i historien. Mengden av alment tilgjengelig, brukbart vann antas a minske med 30 prosent i denne perioden. Arsakene er
forurensning
,
global oppvarming
og politiske stridigheter.
40 prosent av verdens befolkning har for lite vann til et minimum av
hygieniske
formal. Mer enn 2,2 millioner mennesker døde av sykdommer knyttet til inntak av forurenset vann i ar
2000
.
Rapporten oppgir store globale forskjeller i volumet av tilgjengelig vann pr. person, fra 10 000 liter arlig i
Kuwait
til mer enn 810 000 000 liter arlig i
Fransk Guyana
. Imidlertid kan rike land som Kuwait lettere enn fattige land handtere et relativt vannunderskudd.
Verdens vanndag
er en internasjonal FN-merkedag den 22. mars hvert ar for a sette fokus pa mangel pa rent drikkevann.
Vannforbruket pr. individ er høyt, men varierer med levestandard. FN har beregnet at et menneske trenger 20?50 liter vann om dagen for a dekke grunnleggende behov for drikke, personlig hygiene og renhold.
[15]
En gjennomsnittlig nordmann forbruker likevel 200 liter vann om dagen.
[16]
Rundt 10 liter gar til drikke og matlaging, mens det øvrige gar til andre formal, som renhold, hygiene, klesvask, toalettspyling m.m. Vann- forsyningen dekker ogsa behovene til andre enn husholdningene, som næringsliv, brannvesen, skoler, barnehager og helseinstitusjoner.
- ^
https://ordbok.uib.no/perl/ordbok.cgi?OPP=vatn&ant_bokmaal=5&ant_nynorsk=5&bokmaal=+&ordbok=bokmaal
- ^
Kendall J. (1916):
Journal of the American Chemical Society
,
38
(11), 2460-2466.
- ^
≪The visible and UV spectra of liquid water≫
. Arkivert fra
originalen
27. juli 2017
. Besøkt 6. januar 2010
.
- ^
≪Dihydrogen Monoxide≫
,
DHMO
- ^
≪Local officials nearly fall for H2O hoax≫
,
MSNBC
- ^
World Water Assessment Programme 2013
≪Arkivert kopi≫
. Arkivert fra
originalen
6. september 2013
. Besøkt 11. oktober 2013
.
- ^
Melnick, Gary, Harvard-Smithsonian Center for Astrophysics og Neufeld, David, Johns Hopkins University sitert i:
≪Discover of Water Vapor Near Orion Nebula Suggests Possible Origin of H20 in Solar System (sic)≫
(engelsk)
. The Harvard University Gazette. 23. april 1998. Arkivert fra
originalen
. Besøkt 26. mai 2012
.
≪Arkivert kopi≫
. Archived from the original on 16. januar 2000
. Besøkt 26. mai 2012
.
≪Space Cloud Holds Enough Water to Fill Earth's Oceans 1 Million Times≫
(engelsk)
. Headlines@Hopkins, JHU. 9. april 1998.
≪Water, Water Everywhere: Radio telescope finds water is common in universe≫
. The Harvard University Gazette. 25. februar 1999.
(linked 4/2007)
- ^
Clavin, Whitney; Buis, Alan (22. juli 2011).
≪Astronomers Find Largest, Most Distant Reservoir of Water≫
(engelsk)
.
NASA
. Arkivert fra
originalen
24. juli 2011
. Besøkt 25. juli 2011
.
- ^
Staff (22. juli 2011).
≪Astronomers Find Largest, Oldest Mass of Water in Universe≫
(engelsk)
.
Space.com
. Besøkt 23. juli 2011
.
- ^
≪MESSENGER Scientists 'Astonished' to Find Water in Mercury's Thin Atmosphere≫
(engelsk)
. Planetary Society. 3. juli 2008. Arkivert fra
originalen
7. juli 2008
. Besøkt 5. juli 2008
.
≪Arkivert kopi≫
. Arkivert fra
originalen
7. juli 2008
. Besøkt 26. mai 2012
.
- ^
Water Found on Distant Planet
Arkivert
16. juli 2007 hos
Wayback Machine
. 12. juli 2007, av Laura Blue,
Time
(engelsk)
- ^
Water Found in Extrasolar Planet's Atmosphere
? Space.com
(engelsk)
- ^
a
b
Sparrow, Giles (2006).
The Solar System
. Thunder Bay Press.
- ^
Weird water lurking inside giant planets
, New Scientist, 1. september 2010, Magazine issue 2776
(engelsk)
- ^
FN 2013
≪Arkivert kopi≫
. Arkivert fra
originalen
17. mai 2013
. Besøkt 8. mai 2013
.
- ^
Norsk Legeforeningen 2003
http://tidsskriftet.no/article/935089/
- Tvedt, Terje (2011): "Vann. Reiser i vannets fortid og fremtid", Kagge forlag,
ISBN 978-82-489-1033-6
.
- Kroglund, Nina Drolsum (2008):
Vann ? kilde til konflikt eller samarbeid? : Jordanvassdragets historie
. Kolofon Oslo.
ISBN 978-82-300-0450-0
- Jones, O. A.; Lester, J. N.; & Voulvoulis, N. (2005): ≪Pharmaceuticals: a threat to drinking water?≫
TRENDS in Biotechnology
23(4): 163
- Franks, F. (red) (1972?1982):
Water, A comprehensive treatise
, Plenum Press, New York
- Gleick, P.H. et al.:
The World's Water: The Biennial Report on Freshwater Resources
. Island Press, Washington, D.C. (utgitt hvert andre ar fra og med 1998.)
- Marks, William E. (November 2001):
The Holy Order of Water: Healing Earth's Waters and Ourselves
. Bell Pond Books, Great Barrington, MA.
ISBN 0-88010-483-X
.
- Debenedetti, P. G., & Stanley, H. E. (2003):
≪Supercooled and Glassy Water≫
(PDF) i:
Physics Today
56
(6), s. 40–46.
- Tvedt, Terje (1997):
En reise i vannets historie. Fra regnkyst til Muscat
. J.W. Cappelen Forlag as.
ISBN 82-02-16404-4
.
- Gleick, Peter H. (2006):
The World's Water: The Biennial Report on Freshwater Resources
. Washington: Island Press.
ISBN 978-1-59726-105-0
.
- Maude Barlow, Tony Clarke (2003):
Blue Gold: The Fight to Stop the Corporate Theft of the World's Water
. The New Press.
ISBN 978-1565848139
- Miriam R. Lowi (1995):
Water and Power: The Politics of a Scarce Resource in the Jordan River Basin
. Cambridge Middle East Library
- Postel, Sandra (1997:
Last Oasis: Facing Water Scarcity
. New York: Norton Press. 2. utg.
- Tollan, Arne (1977):
Vann ? en naturressurs
. Universitetsforlaget. 107 s.
ISBN 82-00-02408-3
- Økland, Jan og Karen Anna (1995):
Vann og vassdrag 1. Ressurser og problemer
. Vett og Viten.
ISBN 82-412-0151-6
- Økland, Jan og Karen Anna (1996):
Vann og vassdrag 2. Økologi
. Vett og Viten.
ISBN 82-412-0160-5
- Økland, Jan og Karen Anna (2006):
Vann og vassdrag 3. Kjemi, fysikk og miljø
. Vett og Viten, 2. utg.
ISBN 82-41-20635-6
- Økland, Jan og Karen Anna (1999):
Vann og vassdrag 4. Dyr og planter: Innvandring og geografisk fordeling
. Vett og Viten.
ISBN 82-412-0165-6
- Ward, Diane Raines (2002):
Water Wars: Drought, Flood, Folly and the Politics of Thirst
,
ISBN 1573222291