레티날

|

|
| 이름
|
| IUPAC
이름
(2
E
,4
E
,6
E
,8
E
)-3,7-Dimethyl-9-(2,6,6-trimethylcyclohexen-1-yl)nona-2,4,6,8-tetraenal
|
別稱
- Retinene
- Retinaldehyde
- Vitamin A aldehyde
- RAL
|
| 識別子
|
|
|
|
|
|
|
| ChemSpider
|
|
| ECHA InfoCard
|
100.003.760
|
|
|
|
| UNII
|
|
|
|
|
InChI=1S/C20H28O/c1-16(8-6-9-17(2)13-15-21)11-12-19-18(3)10-7-14-20(19,4)5/h6,8-9,11-13,15H,7,10,14H2,1-5H3/b9-6+,12-11+,16-8+,17-13+
Key: NCYCYZXNIZJOKI-OVSJKPMPSA-N
|
CC1=C(C(CCC1)(C)C)/C=C/C(=C/C=C/C(=C/C=O)/C)/C
|
| 性質
|
|
|
C
20
H
28
O
|
| 몰 質量
|
284.443
g·mol
?1
|
| 겉보기
|
Orange crystals from
petroleum ether
[1]
|
| 녹는點
|
61 to 64 °C (142 to 147 °F; 334 to 337 K)
[1]
|
|
|
Nearly insoluble
|
| fat에서의
溶解度
|
Soluble
|
| 關聯 化合物
|
關聯 化合物
|
retinol
;
retinoic acid
;
beta-carotene
;
dehydroretinal
; 3-hydroxyretinal; 4-hydroxyretinal
|
달리 明示된 境遇를 除外하면,
標準狀態
(25 °C [77 °F], 100 kPa)에서 物質의 情報가 提供됨.
|
 前(全)-trans-레티날
前(全)-trans-레티날
레티날
(
英語
:
retinal
)은
레티넨
의 한 種類로,
레티날데하이드
(
英語
:
retinaldehyde
) 或은
비타민 A 알데하이드
(
英語
:
vitamin A aldehyde
)라고도 한다.
[2]
[3]
種
마다 다양한 形態의
비타민 A
가 存在하는데, 레티날 亦是 비타민 A의 한 形態이다. 레티날은 폴리엔(
polyene
)
發色團
으로,
옵신
이라는 蛋白質에 結合하고 動物의
時刻
과 關聯이 있다. 레티날은 또한 第1型
로돕신
蛋白質에 結合하여 特定한
微生物
이 빛을 大使 에너지로 轉換하도록 한다.
脊椎動物
이 레티날을 얻는 方法으로는 고기를 攝取하거나,
카로틴
(
α-카로틴
,
β-카로틴
)으로부터 生産하거나,
葉黃素
의 一種인
β-크립토盞틴
이라는 또 다른 카로티노이드로부터 合成한다. 原料인 카로틴이나 葉黃素는 植物이나 其他
光合成
生物에서 얻어야 한다. 다른
카로티노이드
는 動物이 레티날로 轉換할 수 없고, 몇몇 肉食動物은 카로티노이드를 아예 레티날로 轉換하지 못한다. 비타민 A의 主要 形態 中
레티놀
과 部分的 活性型인
레티盧山
은 레티날에서 合成될 수 있다.
昆蟲
이나
오징어
等
無脊椎動物
은 하이드록시型 레티날을 시각계에서 使用한다. 이들은 다른 葉黃素를 轉換하여 레티날을 얻는다.
비타민 A 代謝
[
編輯
]
生物은 카로티노이드를 切斷하는 非可逆的 酸化反應을 통하여 레티날을 生産한다.
[4]
이 反應은 β-카로틴 15,15'-모노옥시저네이스
[5]
또는 β-카로틴 15,15'-다이獄시저네이스가
[6]
觸媒作用한다.
- β-카로틴
+ O
2
→ 2 retinal
카로티노이드가 레티날의 前驅體인 것처럼 레티날은 다양한 形態의
비타민 A
의 前驅體이다. 레티날은
레티놀
로 或은 反對로 轉換될 수 있다. 레티놀은 貯藏 및 輸送型 비타민 A이며, 비타민 A 알코올이라고도 하고, 簡單히 비타민 A라고 하기도 한다. 이 反應은 레티놀 脫水素酵素
[7]
와 알코올 脫水素酵素
[8]
가 觸媒作用한다.
- 레티날 +
NADPH
+ H
+
 레티놀 + NADP
+
레티놀 + NADP
+
- 레티놀 +
NAD
+
 레티날 + NADH + H
+
레티날 + NADH + H
+
레티날은 酸化되어
레티盧山
으로 酸化될 수도 있다.
- 레티날 + NAD
+
+ H
2
O → 레티盧山 + NADH + H
+
(레티날 脫水素酵素
[9]
가 觸媒)
- 레티날 + O
2
+ H
2
O → 레티盧山 + H
2
O
2
(레티날 酸化酵素
[10]
가 觸媒)
레티날 脫水素酵素는 레티날데하이드 脫水素酵素(RALDH)라고도 한다.
[8]
레티盧山은 비타민 A 山이라고도 불리며, 脊椎動物에서 信號 分子와
호르몬
役割을 한다.
時刻
[
編輯
]
 發色團
內의 레티날
發色團
內의 레티날
時刻은 레티날이 빛에 依하여 異性質體로 變하면서(
photoisomerization
) 始作된다. 11-시스-레티날 發色團이
光子
를 吸收하면 全(全)-트랜스形 異性質體로 變한다. 發色團의 吸收 스펙트럼은 發色團이 結合하고 있는
옵신
과 相互作用에 따라 決定된다. 卽, 옵신의 種類가 다르면 吸收 스펙트럼이 달라진다.
옵신
[
編輯
]
옵신은 蛋白質이고 레티날이 結合하고 있는 視角 色素이다.
눈
의
網膜
에 있는
광受容機 細胞
에 있다. 옵신은 幕貫通
알파 나선
일곱 個가 고리 여섯 個로 連結된 形態이다.
莫大細胞
에 있는 옵신 分子는 細胞 內에 있는 圓盤의 膜에 묻혀있다. 옵신 分子의 N-末端 머리는 圓盤 안에 뻗어 있고, C-末端 꼬리는 細胞質에 뻗어 있다.
圓뿔細胞
에서 圓盤은 細胞의 原形質膜으로 區分되기 때문에, N-末端 머리는 細胞 바깥으로 뻗어 있는 꼴이다. 레티날은 C-末端에 가장 가까운 幕通過 나선의
라이신
殘氣에
쉬프 鹽基
連結을 통하여 共有的으로 結合한다. 쉬프 鹽基 連結을 통하여 레티날에서
酸素
原子를, 라이신의 琉璃 아미노기에서
水素
原子 두 個를 除去하여
물
을 生成한다. 레티날에서 酸素 原子를 除去하고 形成된 2街 作用基를
레티닐리딘
(
retinylidene
)이라고 하므로, 옵신은 레티닐리딘 蛋白質이라고 불렸다.
옵신은
G 蛋白質 連結 受容體
(GPCR)에 屬한다.
[11]
소의
로돕신
은
X線 結晶學
으로 構造가 밝혀진 最初의 GPCR이다.
[12]
348個 아미노산 殘氣로 이루어져 있고, 레티날 發色團은 Lys
296
에 結合한다.
哺乳動物
은 옵신 發色團으로 거의 大部分 레티날을 使用하지만, 其他 動物은 레티날과 密接한 關聯이 있는 네 種類의 發色團을 使用한다. 3,4-다이디하이드로레티날, (3
R
)-3-하이드록시레티날, (3
S
)-3-하이드록시레티날, (4
R
)-4-하이드록시레티날이 그것이다.
魚類
와
兩棲類
는 디하이드로레티날이라고도 하는 3,4-다이디하이드로레티날을 使用한다. 흔히 파리라고 하는
쌍시류
의 亞目人 가락지감針파리亞目(
Cyclorrhapha
)을 除外하고
昆蟲
은 大部分 3-하이드록시레티날의 (
R
)-
光學異性質體
를 使用한다.
醋파리
를 包含하여 가락지감針파리亞目에 屬하는 무리는 (3
S
)-3-하이드록시레티날을 使用한다.
[13]
[14]
반딧불오징어(
Watasenia scintillans
)는 (4
R
)-4-하이드록시레티날을 使用한다.
時刻週期
[
編輯
]
 時刻週期
時刻週期
빛 情報를 傳達하는 信號傳達體系는 循環하는 酵素 經路로 이루어져 있고, 11-
시스
-레티날을 再生性한다. 哺乳動物 莫大細胞의 時刻週期는 아래와 같다.
- 前(全)-
트랜스
-레티닐 에스터 + H
2
0 → 11-
시스
-레티놀 + 脂肪酸 (酵素는
RPE65
아이소머로加水分解酵素)
[15]
- 11-
시스
-레티놀 + NAD
+
→ 11-
시스
-레티날 + NADH + H
+
(酵素는 11-
시스
-레티놀 脫水素酵素)
- 11-
시스
-레티날 + 芽胞로돕신 → 로돕신 + H
2
O (
라이신
에
쉬프 鹽基
連結이 形成된다. -CH=N
+
H-,
- 로돕신 + hν → 메타로돕신 II; 11-
시스
가 前-
트랜스
로 狂異性質體化된다.
- 로돕신 + hν → 포토로돕신 → 바토로돕신 → 루미로돕신 → 메타로돕신 I → 메타로돕신 II,
- 메타로돕신 II + H
2
O → 芽胞로돕신 + 前-
트랜스
-레티날
- 前-
트랜스
-레티날 + NADPH + H
+
→ 前-
트랜스
-레티놀 + NADP
+
(酵素는 전-
트랜스
-레티놀 脫水素酵素)
- 前-
트랜스
-레티놀 + 脂肪酸 → 前-
트랜스
-레티닐 에스터 + H
2
O (酵素는 레시틴 레티놀 아실轉移酵素(LRATs))
[16]
3, 4, 5, 6段階는
莫大細胞
의 바깥 分節에서 일어난다. 1, 2, 7段階는
網膜 色素 上皮細胞
에서 일어난다.
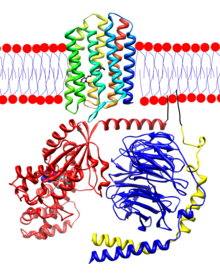 第2型
로돕신
(무지개色)李
지질 二重層
에 묻혀있다. 로돕신의
N-末端
은 빨간色이고 C-末端은 파란色이다. 로돕신 아래에는
트랜스듀新
(G
t
)이 膜에 固定되어 있다(검은색). G
t
α 小段位는 빨간色, G
t
β는 파란色, G
t
γ는 노란色으로 標示하였다. G
t
α 小段位에는
GDP
가 結合하고 로돕신에는
레티날
(검은色)李 結合하고 있다.
第2型
로돕신
(무지개色)李
지질 二重層
에 묻혀있다. 로돕신의
N-末端
은 빨간色이고 C-末端은 파란色이다. 로돕신 아래에는
트랜스듀新
(G
t
)이 膜에 固定되어 있다(검은색). G
t
α 小段位는 빨간色, G
t
β는 파란色, G
t
γ는 노란色으로 標示하였다. G
t
α 小段位에는
GDP
가 結合하고 로돕신에는
레티날
(검은色)李 結合하고 있다.
RPE65 아이소머로加水分解酵素는 베타카로틴 모노옥시第네이스와 상동이다.
[4]
醋파리
Drosophila
에 있는 ninaB 酵素 上胴體는 레티날을 形成하는 카로티노이드 옥시第네이스 活性과 前-
트랜스
兄을 11-
시스
刑으로 轉換하는 異性質化酵素 活性을 모두 가지고 있다.
[17]
第1型 로돕신
[
編輯
]
前(全)-
트랜스
-레티날은 微生物에 있는 第1型 옵신을 構成하는 主要 成分이기도 하다. 第1型 옵신에는
박테리오로돕신
,
채널로돕신
,
黠虜로돕신
等이 있다. 이들 分子가 빛을 받으면 전-
트랜스
-레티날이 13-
시스
레티날로 變하고
[18]
다시 어두운 狀態에서는 전-
트랜스
-레티날로 되돌아온다.
歷史
[
編輯
]
美國의 生化學者
조지 월드
와 同僚들은 1958年 時刻週期를 大略的으로 밝혔고, 그 功勞로
핼던 케퍼 하틀라인
과
랑나르 그라니트
와 함께 1967年
노벨 生理學·醫學賞
을 受賞하였다.
[19]
같이 보기
[
編輯
]
各州
[
編輯
]
- ↑
가
나
Merck Index
, 13th Edition,
8249
- ↑
MORTON, R. A.; GOODWIN, T. W. (1944年 4月 1日). “Preparation of Retinene in Vitro”. 《Nature》
153
(3883): 405?406.
doi
:
10.1038/153405a0
.
- ↑
BALL, S; GOODWIN, TW; MORTON, RA (1946). “Retinene1-vitamin A aldehyde.”. 《The Biochemical Journal》
40
(5-6): lix.
PMID
20341217
.
- ↑
가
나
von Lintig J, Vogt K (2000). “Filling the Gap in Vitamin A Research: Molecular Identification of An Enzyme Cleaving Beta-carotene to Retinal”. 《Journal of Biological Chemistry》 (ASBMB)
275
(16): 11915?11920.
doi
:
10.1074/jbc.275.16.11915
.
PMID
10766819
.
- ↑
Woggon, Wolf-D. (2002). “Oxidative cleavage of carotenoids catalyzed by enzyme models and beta-carotene 15,15´-monooxygenase”. 《Pure and Applied Chemistry》 (IUPAC)
74
(8): 1397?1408.
doi
:
10.1351/pac200274081397
.
- ↑
Kim YS, Kim NH, Yeom SJ, Kim SW, Oh DK (2009).
“In Vitro Characterization of a Recombinant Blh Protein from an Uncultured Marine Bacterium as a β-Carotene 15,15′-Dioxygenase”
. 《Journal of Biological Chemistry》 (ASBMB)
284
(23): 15781?93.
doi
:
10.1074/jbc.M109.002618
.
PMC
2708875
.
PMID
19366683
.
- ↑
Liden M Eriksson U (2006). “Understanding Retinol Metabolism: Structure and Function of Retinol Dehydrogenases”. 《Journal of Biological Chemistry》 (ASBMB)
281
(19): 13001?13004.
doi
:
10.1074/jbc.R500027200
.
PMID
16428379
.
- ↑
가
나
Duester, G (2008年 9月).
“Retinoic Acid Synthesis and Signaling during Early Organogenesis”
. 《Cell》
134
(6): 921?31.
doi
:
10.1016/j.cell.2008.09.002
.
PMC
2632951
.
PMID
18805086
.
- ↑
Lin M, Zhang M, Abraham M, Smith SM, Napoli JL. (2003). “Mouse Retinal Dehydrogenase 4 (RALDH4), Molecular Cloning, Cellular Expression, and Activity in 9-cis-Retinoic Acid Biosynthesis in Intact Cells”. 《Journal of Biological Chemistry》 (ASBMB)
278
(11): 9856?9861.
doi
:
10.1074/jbc.M211417200
.
PMID
12519776
.
- ↑
“KEGG ENZYME: 1.2.3.11 retinal oxidase”
. 2009年 3月 10日에 確認함
.
- ↑
Lamb, T D (1996).
“Gain and kinetics of activation in the G-protein cascade of phototransduction”
. 《Proceedings of the National Academy of Sciences》
93
(2): 566?570.
Bibcode
:
1996PNAS...93..566L
.
doi
:
10.1073/pnas.93.2.566
.
PMC
40092
.
PMID
8570596
.
- ↑
Palczewski K, Kumasaka T,; Behnke CA, Motoshima H, Fox BA, Le Trong I, Teller DC, Okada T, Stenkamp RE, Yamamoto M, Miyano M (2000). “Crystal Structure of Rhodopsin: A G Protein-Coupled Receptor”. 《Science》 (AAAS)
289
(5480): 739?745.
doi
:
10.1126/science.289.5480.739
.
PMID
10926528
.
- ↑
Seki T, Isono K, Ito M, Katsuta Y (1994). “Flies in the Group Cyclorrhapha Use (3S)-3-Hydroxyretinal as a Unique Visual Pigment Chromophore”. 《European Journal of Biochemistry》 (Wiley)
226
(2): 691?696.
doi
:
10.1111/j.1432-1033.1994.tb20097.x
.
PMID
8001586
.
- ↑
Seki T, Isono K, Ozaki K, Tsukahara Y, Shibata-Katsuta Y, Ito M, Irie T, Katagiri M (1998). “The metabolic pathway of visual pigment chromophore formation in Drosophila melanogaster: All-trans (3S)-3-hydroxyretinal is formed from all-trans retinal via (3R)-3-hydroxyretinal in the dark”. 《European Journal of Biochemistry》 (Wiley)
257
(2): 522?527.
doi
:
10.1046/j.1432-1327.1998.2570522.x
.
PMID
9826202
.
- ↑
Moiseyev G, Chen Y, Takahashi Y, Wu BX, Ma J (2005).
“RPE65 is the isomerohydrolase in the retinoid visual cycle”
. 《Proceedings of the National Academy of Sciences》
102
(35): 12413?12418.
Bibcode
:
2005PNAS..10212413M
.
doi
:
10.1073/pnas.0503460102
.
PMC
1194921
.
PMID
16116091
.
- ↑
Jin M, Yuan Q, Li S, Travis GH (2007).
“Role of LRAT on the Retinoid Isomerase Activity and Membrane Association of Rpe65”
. 《Journal of Biological Chemistry》 (ASBMB)
282
(29): 20915?20924.
doi
:
10.1074/jbc.M701432200
.
PMC
2747659
.
PMID
17504753
.
- ↑
Oberhauser V, Voolstra O, Bangert A, von Lintig J, Vogt K (2008).
“NinaB combines carotenoid oxygenase and retinoid isomerase activity in a single polypeptide”
. 《Proceedings of the National Academy of Sciences》
105
(48): 19000?5.
Bibcode
:
2008PNAS..10519000O
.
doi
:
10.1073/pnas.0807805105
.
PMC
2596218
.
PMID
19020100
.
- ↑
Chen DL, Wang G, Xu B, Hu KS (2002). “All-trans to 13-cis retinal isomerization in light-adapted bacteriorhodopsin at acidic pH”. 《Journal of Photochemistry and Photobiology B: Biology》
66
(3): 188.
doi
:
10.1016/S1011-1344(02)00245-2
.
- ↑
“The Nobel Prize in Physiology or Medicine 1967”
. Nobelprize.org
. 2014年 12月 22日에 確認함
.
外部 링크
[
編輯
]
|
|---|
| 細胞 外
| |
|---|
| 細胞 內
| | 核 受容體
| |
|---|
| 2次 傳達者
|
- 一般:
아라키돈산
- 다이글리세라이드
(
蛋白質 키네이스 C
,
TRPC
)
- 이노시톨 1,4,5-三重因山
(
이노시톨 1,4,5-三重因山 受容體
,
리아盧딘 受容體
)
- 포스파티드山
- 抛스포이노시타이드:
포스파티딜이노시톨 4,5-二重因山
(
內部 整流 칼륨 通路
)
- 포스파티딜이노시톨 3,4,5-三重因山
(
蛋白質 키네이스 B
,
브루톤 티로신 키네이스
,
抛스포이노시타이드 依存性 키네이스-1
)
- 포스파티딜이노시톨 3,4-二重因山
(
蛋白質 키네이스 B
,
抛스포이노시타이드 依存性 키네이스-1
), 스핑告知질:
세라마이드 1-因山
- 세라마이드
(
세라마이드 活性化 蛋白質 因山加水分解酵素
,
KSR1
,
蛋白質 키네이스 C 제타
,
카텝신 D
)
- 글루코세레브로사이드
- 스핑孤辰 1-因山
- 스핑孤辰
(
스핑孤辰 依存性 蛋白質 키네이스 1
,
蛋白質 키네이스 H
,
酵母 蛋白質 키네이스
)
|
|---|
|
|---|
| 前驅體
| |
|---|