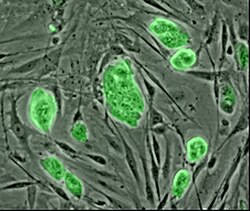
 Embryonale stamcellen van een
muis
Embryonale stamcellen van een
muis
 Ontwikkeling vanaf bevruchting
Ontwikkeling vanaf bevruchting
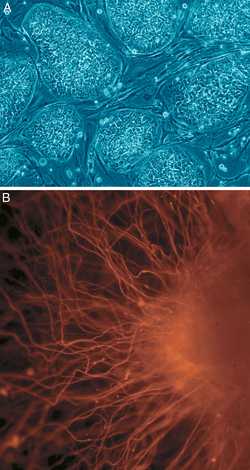 A: Menselijke
embryonische
stamcellen (celkolonies die nog niet gedifferentieerd zijn).
A: Menselijke
embryonische
stamcellen (celkolonies die nog niet gedifferentieerd zijn).
B:
Zenuwcellen
Een
stamcel
of
cellula praecursoria
, is een
cel
die ook in staat is om in een ander celtype te veranderen of
differentieren
.
In tegenstelling tot
dieren
, kunnen
planten
, dankzij hun
meristeem
, voortdurend nieuwe organen, zoals
bladeren
,
bloemen
,
stengels
en
wortels
, vormen uit aanwezig blijvende stamcellen.
Diktegroei
van stengels en
bomen
is mogelijk, door de aanwezigheid van het
secundaire meristeem
.
Afhankelijk van het type stamcel, heeft deze meer of minder mogelijkheden om tot verschillende celtypes te differentieren. Naar afnemende veelzijdigheid, worden vier differentiatiegraden van stamcellen onderscheiden:
- toti
potente stamcellen
- pluri
potente stamcellen
- multi
potente stamcellen
- uni
potente stamcellen
Een
embryo
bestaat aanvankelijk enkel uit totipotente stamcellen. Later gaan deze zich specialiseren, en vormen ze cellen met elk een eigen functie. Deze gespecialiseerde cellen kunnen daarna geen andere functies meer vervullen (uitzondering:
plasticiteit
van
zenuwcellen
) en ze kunnen ook niet teruggaan in hun ontwikkeling, om opnieuw stamcellen te vormen. Als de
celfunctie
deling toestaat, worden door
deling
alleen soortgelijke, of nog sterker gespecialiseerde cellen gevormd.
In een gewone
(somatische) cel
worden de
telomeer
-sequenties van de
dochtercellen
bij elke deling een stukje korter omdat, bij afwezigheid van het enzym
telomerase
, het laatste stukje chromosoom bij de deling verloren gaat. Wanneer er na een aantal celdelingen uiteindelijk niets meer van de telomeren van de opgedeelde
moedercel
over is, gaan de gevormde dochtercellen in
delingsrust
, of sterven af (
apoptose
). Als de telomeren op zijn, zou immers bij verdere celdeling een stukje cruciaal DNA verdwijnen. Stamcellen beschikken echter wel over het enzym telomerase, dat in staat is na elke deling het verloren stukje telomeer weer bij te maken.
De volgende indeling is gebaseerd op de verschillen tussen
embryonale stamcellen
en
volwassen stamcellen
.
[noten 1]
Wanneer een
zaadcel
versmelt met een
eicel
ontstaat een
zygote
. Een zygote is een voorbeeld van een totipotente stamcel. Deze cel is in staat om, in het juiste milieu, uit te groeien tot een compleet
individu
: alle meer dan 220 verschillende soorten cellen die samen de verschillende
weefsels
vormen, inclusief het extra-embryonaal weefsel, zoals de
placenta
. De acht
blastomeren
, die ontstaan door
klievingdelingen
van de zygote, zijn ook nog totipotent.
Totipotentie is heel moeilijk aan te tonen bij humane stamcellen. Bij muizencellen is dit gemakkelijker: men injecteert een
blastocyste
met een vermoedelijk totipotente stamcel, die een zichtbare of een eenvoudig te detecteren
genetische afwijking
heeft, bijvoorbeeld
albinisme
. Wanneer het blastocyst zich door celdeling verder ontwikkelt tot een compleet individu, kan men gemakkelijk achterhalen of de geinjecteerde stamcel is uitgegroeid tot verschillende soorten weefsel, en dus totipotent was. Een dergelijke,
genetisch gemanipuleerde
muis noemt men een
chimere
muis; het spreekt voor zich dat het creeren van een chimere mens uit
ethische overwegingen
ongewenst is.
Pluripotente stamcellen
kunnen differentieren tot cellen van alle drie de kiemlagen van het embryo, maar niet meer tot extra-embryonaal weefsel, zoals
amnion
en
chorion
(zie ook
celdifferentiatie
). Er zijn verschillende bronnen mogelijk voor pluripotente stamcellen:
 Blastocyst
Blastocyst
 Regulatie van de kern- en uitgebreide pluripotentienetwerken in
embryonale stamcellen
van muizen
Regulatie van de kern- en uitgebreide pluripotentienetwerken in
embryonale stamcellen
van muizen
 Celsignaleringen die de omschakeling tussen zelfvernieuwing en differentiatie in embryonale stamcellen van muizen te weegbrengen
Celsignaleringen die de omschakeling tussen zelfvernieuwing en differentiatie in embryonale stamcellen van muizen te weegbrengen
Na de bevruchting begint de zygote zich te delen, die eerste delingen zijn klievingen. Na drie dagen bestaat de celklomp uit acht niet-gedifferentieerde cellen: het
morulastadium
. Deze cellen delen echter verder; wanneer ze het 32-cellige morulastadium bereiken, wijken de cellen uiteen waardoor een holte ontstaat, de
blastula
. De buitenste cellaag rondom de blastulaholte noemt men de
trofoblast
. Het geheel noemen we de blastocyst. De trofoblast ontwikkelt zich later tot de ondersteunde weefsels zoals de placenta. Later is in die celmassa de
kiemschijf
met drie kiemlagen te onderscheiden: het
ectoderm
,
mesoderm
en het
endoderm
. Hiermee begint de orgaanvorming of de organogenese. Cellen ontstaan uit de eerste klievingen van de zygote, differentieren en nadat ze eenmaal het blastulastadium bereikt hebben, zijn ze hun totipotente karakter verloren.
In
1998
isoleerde Dr. Thomson (
Universiteit van Wisconsin
) voor het eerst embryonale stamcellen uit de binnenste celmassa van menselijke embryo’s in het blastocyststadium. Dr. Thomson werkte met restembryo’s afkomstig van
ivf
-klinieken. Door de geisoleerde cellen in het laboratorium te laten delen cultiveerde hij een 'stamcellijn': de eerste
cellijn
op basis van pluripotente stamcellen.
Sindsdien zijn er wereldwijd meer dan 400 verschillende stamcellijnen geisoleerd. Deze embryonale stamcellijnen (
embryonic stem cells
of ES) hebben twee bijzondere eigenschappen. Afhankelijk van de kweekcondities kunnen de cellen zich vernieuwen (proliferatie) of specialiseren (differentiatie). Totipotente en pluripotente stamcellen hebben de unieke mogelijkheid om te differentieren (specialiseren) tot alle cellen van het organisme. Dit kan in het laboratorium getest worden door de stamcellen op een andere manier te kweken. Dit kan ook worden getest door de cellen in de testes (teelbal) van laboratoriummuizen te plaatsen waar ze uitgroeien tot grote tumoren:
teratomen
of
teratocarcinomen
. Teratoma’s bevatten cellen van de drie kiemlagen, georganiseerde weefsels (zoals haren en tanden) en cellen die erg lijken op embryonale cellen.
Het gebruik van humane ES-cellen voor onderzoek is in bepaalde landen (o.a Amerika en Duitsland) sterk gelimiteerd vanwege
ethische
bezwaren.
In
1998
vond Dr. Gearhart van de
Johns Hopkins University
een tweede bron van pluripotente stamcellen. Hij nam
primordiale kiemcellen
(voorlopers van de geslachtscellen) weg uit foetaal weefsel van afgebroken zwangerschappen. Deze EG of
embryonic germ cells
kunnen zich ook differentieren tot cellen uit de drie kiemlagen (
ectoderm
,
mesoderm
en
endoderm
). Hun proliferatie is echter wel beperkt, ze verdubbelen zich maximaal tachtig keer. EC (
embryonal carcinoma
), EG en ES hebben dezelfde eigenschappen: ze zijn morfologisch gelijkaardig, ze brengen veel dezelfde genen tot expressie, vereisen gelijkaardige groeicondities en ze kunnen differentieren tot cellen van alle drie de kiemlagen.
[1]
Een derde bron om pluripotente cellen te isoleren is het gebruik van de somatische
celkerntransplantatie
of therapeutisch klonen. Hierbij wordt in een eicel (of eventueel in een pluripotente stamcel) een
somatische
celkern van de patient geplaatst. Daardoor bezit deze cel exact dezelfde genetische informatie (tenminste wat
nucleair DNA
betreft) als de patient, wat problemen met afstoting na transplantatie vermijdt. Deze cel zou men dan kunnen laten differentieren en implanteren. Deze techniek is echter nog lang niet uitgewerkt. Zo is er de kwestie van het
mitochondriaal DNA
, dat datgene van de eicel blijft.
Daarnaast hebben Takahashi en
Yamanaka
in 2006 gedifferentieerde cellen teruggeprogrammeerd in stamcellen. Deze cellen worden
induced Pluripotent Stem Cells
(iPSC's) genoemd. Het voordeel van deze "stamcellen" is dat ze makkelijk te verkrijgen zijn, maar recent (2012) is ontdekt dat iPSC's niet zo ongedifferentieerd zijn als embryonale stamcellen. Als de epigenetische code van de iPSC's veranderd zou kunnen worden, zouden de mogelijkheden van iPSC's even groot zijn als die van embryonale stamcellen.
[2]
Voor deze ontdekking verkreeg Yamanaka in 2012 samen met
John Gurdon
de
Nobelprijs voor de Fysiologie of Geneeskunde
.
Multipotente stamcellen zijn cellen die tot een beperkt aantal celtypes kunnen differentieren. Hun differentiatie en proliferatiemogelijkheden zijn nog meer beperkt daar ze enkel tot cellen van een kiemlaag kunnen differentieren.
De meeste multipotente stamcellen zijn volwassen stamcellen (
adult stem cells
of AS). Een volwassen stamcel is een nog niet gedifferentieerde of een niet-gespecialiseerde cel die na de geboorte voorkomt in een gedifferentieerd en gespecialiseerd weefsel van een organisme. Ze kunnen aanleiding geven tot alle rijpe cellen van het betrokken weefsel. Ze zijn nodig in het lichaam om bepaalde cellen met een korte levensduur te verversen. Voorbeelden van AS zijn de hematopoetische (bloedvormende) stamcellen, neurale stamcellen uit hersenweefsel, stamcellen in huid- en vetweefsel. Aanvankelijk was men er vast van overtuigd dat de AS zeer geringe differentiatie- en proliferatiemogelijkheden had. Maar recent onderzoek van de Belgische onderzoekster Catherine Verfaillie bewees het tegendeel. Ze slaagde erin AS toch te laten differentieren tot cellen van een ander kiemblad .
De aandacht voor AS nam vooral toe met de opkomst van ethische implicaties over het gebruik van ES en EG (Boogaerts, 2005). Nu gaat men ervan uit dat in elk orgaan van een volwassen persoon een hoeveelheid volwassen stamcellen aanwezig is (Allemeersch, 2002). De oorsprong van AS is echter nog niet achterhaald maar wetenschappers vermoeden het bestaan van een universele stamcel die aanwezig zou zijn in de bloedbaan. Het feit dat AS in een orgaan dicht bij een bloedvat genesteld zijn, versterkt dit vermoeden. AS zijn onderling echter ook erg verschillend, zo zijn hematopoetische stamcellen erg actief terwijl in de meeste organen adulte stamcellen vooral rustend aanwezig zijn. Om stamcellen van de patient zelf te kunnen gebruiken voor behandeling moeten ze eerst worden geisoleerd en in grotere aantallen worden gegenereerd. Voor acute ziekten ontbreekt echter dan de tijd om voldoende cellen te kunnen kweken en ziekten veroorzaakt door een genetisch defect zijn wellicht niet geschikt doordat de genetische fout ook in de stamcel aanwezig is.
Weefselbanken vormen voor deze patienten in de toekomst misschien wel een oplossing. Dat zijn banken waarin hoeveelheden gedifferentieerd weefsel opgeslagen zijn, met verschillende
HLA-typeringen
, om bij zo veel mogelijk patienten een transplantatie zonder afstoting mogelijk te maken. Deze weefselhoeveelheden kunnen eventueel afkomstig zijn van (embryonale) stamcellijnen.
Volwassen stamcellen hebben in ieder geval meer genetische afwijkingen door de inwerking van giftige stoffen en zonlicht maar ook door de fouten die ontstaan zijn in de celdeling. Stamcellen zijn moeilijk te herkennen, te isoleren en in vitro te vermenigvuldigen. Navelstrengbloed vormt ook een bron van multipotente stamcellen. Ze bieden talrijke voordelen namelijk dat er geen risico is voor de donor bij het oogsten. Navelstrengbloed kan gemakkelijk ingevroren worden. Een nadeel is het lage aantal aanwezige hematopoetische stamcellen. Ook is er geen tweede transplantatie mogelijk. Navelstrengbloed heeft vooral zijn toepassing bij hematologische ziekten (zoals acute leukemie).
Unipotente stamcellen zijn in staat welbepaald een type gedifferentieerde cel te maken.
Bronnen, noten en/of referenties
Noten
- ↑
Een andere indeling is mogelijk volgens de leeftijd van derivatie (afname).
Referenties
|