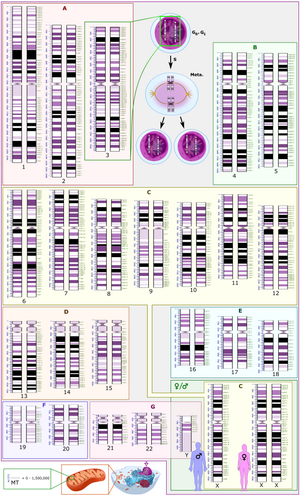
 Representacion grafica del cariotipo humano normal.
Representacion grafica del cariotipo humano normal.
El
Proyecto Genoma Humano
(PGH) fue un proyecto internacional de investigacion cientifica con el objetivo fundamental de determinar la secuencia de pares de bases quimicas que componen el
ADN
e identificar y cartografiar todos los
genes
de un
genoma humano
promedio desde un punto de vista fisico y funcional, incluyendo tanto los genes que codifican proteinas como
los que no
.
En el ano 2003, se completo la secuencia del genoma humano, aunque no se conoce la funcion del todo.
El proyecto, dotado con 3000 millones de
dolares
, fue fundado en 1990 en el
Departamento de Energia
y los
Nacionales de la Salud de los Estados Unidos
, bajo la direccion del doctor
Francis Collins
, quien lideraba el grupo de investigacion publico, conformado por multiples cientificos de diferentes paises, con un plazo de realizacion de 15 anos. Debido a la amplia colaboracion internacional, a los avances en el campo de la genomica, asi como los avances en la tecnologia computacional, un borrador inicial del genoma fue terminado en el ano 2000 (anunciado conjuntamente por el expresidente
Bill Clinton
y el ex primer ministro britanico
Tony Blair
el 26 de junio de 2000),
[
1
]
[
2
]
finalmente el genoma completo fue presentado en abril del 2003, dos anos antes de lo esperado. Un proyecto paralelo se realizo fuera del gobierno por parte de la
Corporacion Celera
. La mayoria de la secuenciacion se realizo en las universidades y centros de investigacion de
Estados Unidos
,
Canada
,
Nueva Zelanda
,
Reino Unido
y
Espana
.
Conocer la secuencia completa del
genoma humano
puede tener mucha relevancia cuanto a los estudios de biomedicina y genetica clinica, desarrollando el conocimiento de enfermedades poco estudiadas, nuevas medicinas y diagnosticos mas fiables y rapidos. Sin embargo descubrir toda la secuencia genica de un organismo no nos permite conocer su
fenotipo
. Como consecuencia, la ciencia de la genomica no podria hacerse cargo en la actualidad de todos los problemas eticos y sociales que ya estan empezando a ser debatidos. Por eso el PGH necesita una regulacion legislativa basada en la etica.
El Proyecto Genoma Humano tiene una extension que es el
Proyecto Microbioma Humano
.
[
3
]
Este intenta caracterizar las comunidades microbianas encontradas en diversas localizaciones del cuerpo humano para determinar las posibles correlaciones entre los cambios del microbioma y el estado de salud.
Se consideraria al microbioma como el ultimo organo humano por investigar.
[
4
]
Historia del Proyecto Genoma Humano
[
editar
]
En 1984 comenzaron las actividades propias del PGH, coincidiendo con la idea de fundar un instituto para la secuenciacion del
genoma humano
por parte de Robert Sinsheimer, en ese momento Rector de la
Universidad de California
. De forma independiente el
Departamento de Energia de Estados Unidos (DOE)
se intereso por el proyecto, al haber estudiado los efectos que las actividades de sus programas nucleares producian en la genetica y en las mutaciones. Entonces se conocia como ≪Proyecto
HUGO
≫.
En su comienzo, el Proyecto Genoma Humano, enfrento a dos tipos de cientificos: de un lado, los biologos moleculares universitarios y del otro, biologos de institutos de investigacion del Instituto Nacional de Salud, organismo estatal que percibia grandes sumas economicas federales destinadas a la investigacion. Si bien el enfrentamiento se baso en la preocupacion de ambos cientificos por la magnitud y los costes de la empresa a llevar a cabo, existian sobre todo discrepancias para definir las vias mas adecuadas a la hora de lograr los objetivos fijados. Solo debemos observar los 28.2 millones de dolares destinados al periodo 88-89 para ubicarnos ≪materialmente≫. Por su parte, Estados Unidos se comprometieron a destinar parte de los fondos economicos del proyecto al estudio de los aspectos eticos y sociales del PGH.
James Watson asumio en 1988 la direccion ejecutiva de la Investigacion del Genoma Humano en el NIH (Instituto Nacional de Salud). Al asumir el cargo, firmo un acuerdo de cooperacion con el Departamento de Energia de Estados Unidos mediante el cual ambas instituciones se ayudarian mutuamente. De esta forma el PGH comenzo con el liderazgo del NIH en lugar del Departamento de Energia. El interes internacional por el proyecto crecio de forma notable, motivado fundamentalmente por no quedar por detras de Estados Unidos en un tema de tanta importancia. Para evitar repeticiones y solapamientos en los logros, se creo
HUGO
(Organizacion del Genoma Humano) para coordinar los trabajos de investigacion.
Antes de los ochenta ya se conocia la secuencia de genes sueltos de algunos organismos, como tambien se conocian los genomas de entidades subcelulares, tales como virus y
plasmidos
. En mayo de 1985, Robert Sinsheimer organizo un taller en la
Universidad de California en Santa Cruz
, para debatir la viabilidad de construir un
genoma de referencia
sistematico utilizando tecnologias de secuenciacion genetica.
[
5
]
Sin embargo, no fue hasta 1986 cuando la Oficina de Investigacion Sanitaria y Medioambiental del
Departamento de Energia de los Estados Unidos
(DOE) concreto institucionalmente el Proyecto Genoma Humano (PGH) durante un congreso en Santa Fe organizado por
Charles DeLisi
y David Smith.
[
6
]
Al mismo tiempo,
Renato Dulbecco
, presidente del
Instituto Salk de Estudios Biologicos
, propuso por primera vez el concepto de
secuenciacion del genoma
completo en un ensayo publicado en
Science
.
[
7
]
El trabajo publicado, titulado "Un punto de inflexion en la investigacion del cancer: Secuenciacion del genoma humano", se acorto a partir de la propuesta original de utilizar la secuencia para comprender las bases geneticas del cancer de mama.
[
8
]
James Watson
, uno de los descubridores de la forma de doble helice del ADN en los anos 70, le siguio dos meses despues con un taller celebrado en el
Laboratorio Cold Spring Harbor
. Asi pues, la idea de obtener una secuencia de referencia tuvo tres origenes independientes: Sinsheimer,
Dulbecco
y
DeLisi
. En ultima instancia, fueron las acciones de
DeLisi
las que pusieron en marcha el proyecto.
[
9
]
[
10
]
[
11
]
[
12
]
El PGH contaba con una buena suma economica y seria utilizado para estudiar los posibles efectos de las radiaciones sobre el ADN. Al siguiente ano, en el congreso de biologos en el
Laboratorio Cold Spring Harbor
, el Instituto Nacional de la Salud (NIH) quiso participar del proyecto al ser otro organismo publico con mucha mas experiencia en el campo de la biologia, si bien no tanta en la organizacion de proyectos de esta magnitud. El debate publico que suscito la idea capto la atencion de los responsables politicos, no solo porque el Proyecto Genoma Humano era un gran reto tecnocientifico, sino por las tecnologias de vanguardia que surgirian, asi como porque el conocimiento obtenido aseguraria la superioridad tecnologica y comercial del pais. Antes de dar luz verde a la iniciativa del PGH se necesito por un lado el informe de 1988 de la Oficina de Evaluacion Tecnologica del Congreso (OTA) y el del Consejo Nacional de Investigacion (NRC). Ese ano se inauguro
HUGO
(Organizacion del Genoma Humano) y
James D. Watson
fue nombrado alto cargo del proyecto. Seria reemplazado por
Francis Collins
en abril de 1993, en gran parte por su enemistad con Bernadine Healy que era su jefe por aquel entonces. Tras esto el nombre del Centro cambio a Instituto Nacional de Investigaciones del Genoma Humano (NHGRI).
En 1990 se inauguro definitivamente el Proyecto Genoma Humano calculandose quince anos de trabajo. Sus objetivos principales en una primera etapa eran la elaboracion de mapas geneticos y fisicos de gran resolucion, mientras se ponian a punto nuevas tecnicas de secuenciacion, para poder abordar todo el
genoma
. Se calculo que el Proyecto Genoma Humano estadounidense necesitaria unos 3000 millones de dolares y terminaria en 2005. En 1993 los fondos publicos aportaron 170 millones de dolares, mientras que la industria gasto aproximadamente 80 millones. Con el paso de los anos, la inversion privada cobro relevancia y amenazo con adelantar a las financiaciones publicas.
Contribucion de empresas privadas
[
editar
]
En 1999
Craig Venter
funda, con un financiamiento mixto, el Instituto para la Investigacion Genetica (TIGR) que se dio a conocer publicamente en 1995 con el descubrimiento de la secuencia nucleotidica del primer organismo completo publicado, la bacteria
Haemophilus influenzae
con cerca de 1740 genes (1.8 Mb). En mayo de 1998 surgio la primera empresa relacionada con el PGH llamada
Celera Genomics
. La investigacion del proyecto se convirtio en una carrera frenetica en todos los laboratorios relacionados con el tema, ya que se intentaba secuenciar trozos de cromosomas para rapidamente incorporar sus secuencias a las bases de datos y atribuirse la prioridad de pantera.
Resultados del proyecto
[
editar
]
 La primera presentacion impresa del
genoma humano
fue entregada en una serie de libros, desplegados en la Coleccion Wellcome,
Londres
.
La primera presentacion impresa del
genoma humano
fue entregada en una serie de libros, desplegados en la Coleccion Wellcome,
Londres
.
El 6 de abril de 2000 se anuncio publicamente la terminacion del primer borrador del genoma humano secuenciado que localizaba a los genes dentro de los cromosomas. Los dias 15 y 16 de febrero de 2001, las dos prestigiosas revistas cientificas estadounidenses,
Nature
y
Science
, publicaron la secuenciacion definitiva del Genoma Humano, con un 99,9 % de fiabilidad y con un ano de antelacion a la fecha presupuesta. Sucesivas
secuenciaciones
condujeron finalmente al anuncio del
genoma
esencialmente completo en abril de 2003, dos anos antes de lo previsto.
[
13
]
En mayo de 2006 se alcanzo otro hito en la culminacion del proyecto al publicarse la secuencia del
ultimo cromosoma
humano en la revista
Nature
.
Una extension del Proyecto Genoma Humano es el del
microbioma humano
,
[
3
]
que intenta caracterizar las comunidades microbianas encontradas en diversas localizaciones del cuerpo humano para determinar las posibles correlaciones entre los cambios de dicho microbioma y el estado de salud. Algunos autores consideran al microbioma humano el ultimo organo por investigar.
[
4
]
En junio de 2021 se dio a conocer que un consorcio internacional habia secuenciado por primera vez el genoma completo de un ser humano. El libro de instrucciones de una persona tiene 3.055 millones de letras, segun la nueva lectura, que incluye un 8 % del ADN que permanecia oculto por falta de tecnologia.
[1]
Objetivos Principales
[
editar
]
Desde el principio de la investigacion, se propuso desarrollar el PGH a traves de dos vias independientes, pero relacionadas y ambas esenciales:
- Secuenciacion:
se trataba de averiguar la posicion de todos los nucleotidos del genoma (cada una de las cuatro posibles bases nitrogenadas tipicas del ADN).
- Cartografia o mapeo genetico:
consistia en localizar los genes en cada uno de los 23 pares de cromosomas del ser humano.
Identificacion de los genes en el genoma humano
[
editar
]
El
genoma humano
esta compuesto por aproximadamente 30 000 genes, cifra bastante proxima a la mencionada en el borrador del proyecto, publicado en el ano 2000, ocasion en la que los genes oscilaban entre 26 000 a 38 000. Otra peculiaridad del
genoma humano
es que la cifra de genes es solo dos o tres veces mayor que la encontrada en el genoma de
Drosophila
, y cualitativamente hablando, existen genes comunes a los de bacterias y que no han sido hallados en nuestros ancestros.
Determinacion de la secuencia de bases nitrogenadas que forman el ADN humano
[
editar
]
Los humanos poseen poco mas de 3000 millones de bases nitrogenadas, similar al tamano de genomas de otros vertebrados.
Mantenimiento a resguardo de la informacion creando bases de datos
[
editar
]
En estos momentos son una realidad las bases de datos donde se almacena toda la informacion surgida del Proyecto Genoma Humano. Si accedemos a Internet podremos conocer libremente aspectos de alto interes en la comparacion entre genomas de distintas especies de animales y plantas. Gracias al uso libre de este conocimiento es posible determinar la funcion de los genes, asi como averiguar como las mutaciones influyen en la sintesis de proteinas.
Aprovisionamiento de herramientas multimedia para el analisis de datos
[
editar
]
Se ha inducido un gran desarrollo tecnologico a partir de la creacion de herramientas de analisis de datos generadas en el Proyecto Genoma Humano. Este desarrollo facilitara y hara posible definir los temas de estudio futuros con vistas a las tareas pendientes. Entre las tecnologias gracias al PGH figuran las de manejo computacional de datos, las que permiten la generacion de las anteriores, tecnicas de biologia molecular relacionadas con la secuenciacion de trozos de ADN automaticamente y aquellas que permiten ampliar la cantidad de material genetico disponible como la RCP pero no es posible realizar esta accion porque esta fuera de las leyes universales propuestas por la ONU en cualquier parte del globo terrestre.
Transferencia de tecnologia relacionada con el tema al sector privado
[
editar
]
Se ha producido importante corriente de liberacion de derechos que anteriormente estaban en manos del Estado, en relacion con la transferencia de tecnologias al sector privado. Esta medida ha suscitado aplausos y criticas. Por un lado se amplia el acceso libre a los datos del Proyecto con lo que muchas mas personas pueden seguir estudiando este campo, pero por otro esto puede suponer el incremento de poder de ciertos sectores que a su vez, aumentaran su influencia en la sociedad.
Supervision de los temas eticos, legales y sociales derivados del Proyecto
[
editar
]
Para terminar, se puede afirmar que el objetivo relacionado con el estudio de la etica del PGH es un tema de gran controversia actual, y ha necesitado de grandes sumas de dinero estatales asi como de un importante trabajo de laboratorios e investigadores. Todo esto ha provocado un deterioro del apoyo a otros proyectos de investigacion no menos importantes, que se han visto muy afectados o incluso cancelados.
Donantes de genoma
[
editar
]
El PGH e IHGSC internacional ( sector publico) recogieron el semen de hombres y la sangre de mujeres de muchos donantes diferentes, pero solo unas pocas de estas muestras fueron estudiadas despues realmente. Asi se garantizo que la identidad de los donantes estuviera salvaguardada de modo que nadie supiera que ADN seria el secuenciado. Tambien han sido utilizados clones de ADN de varias bibliotecas, la mayoria de las cuales fueron creadas por el Dr. J. Pieter de Jong. Se comunico de manera informal, pero es bien conocido por la comunidad en general, que gran parte del
ADN
secuenciado provenia de un unico donante anonimo de Buffalo, Nueva York, su nombre en clave era
RP11
. Los cientificos encargados utilizaron principalmente los globulos blancos de dos hombres y dos mujeres elegidos aleatoriamente.
[
14
]
carlos
Ventajas
[
editar
]
El trabajo sobre la interpretacion de los datos del genoma se encuentra todavia en sus etapas iniciales. Se preve que un conocimiento detallado del
genoma humano
ofrecera nuevas vias para los avances de la medicina y la biotecnologia. Por ejemplo, un numero de empresas, como Myriad Genetics ha empezado a ofrecer formas sencillas de administrar las pruebas geneticas que pueden mostrar la predisposicion a una variedad de enfermedades, incluyendo cancer de mama, los trastornos de la hemostasia, la fibrosis quistica, enfermedades hepaticas y muchas otras. Ademas, la etiologia de los canceres, la enfermedad de Alzheimer y otras areas de interes clinico se consideran susceptibles de beneficiarse de la informacion sobre el genoma y, posiblemente, pueda a largo plazo conducir a avances significativos en su gestion.
Hay tambien muchos beneficios tangibles para los biologos. Por ejemplo, un investigador de la investigacion de un determinado tipo de cancer puede haber reducido su busqueda a un determinado gen. Al visitar la base de datos del genoma humano en la World Wide Web, este investigador puede examinar lo que otros cientificos han escrito sobre este gen, incluyendo (potencialmente) la estructura tridimensional de su producto; su/s funcion/es; sus relaciones evolutivas con otros genes humanos, o genes de ratones, levaduras, moscas de la fruta; las posibles mutaciones perjudiciales; las interacciones con otros genes; los tejidos del cuerpo en el que este gen es activado; las enfermedades asociadas con este gen u otro tipo de datos. Ademas, la comprension mas profunda de los procesos de la enfermedad en el ambito de la biologia molecular puede determinar nuevos procedimientos terapeuticos. Dada la importancia del ADN en biologia molecular y su papel central en la determinacion de la operacion fundamental de los procesos celulares, es probable que la ampliacion de los conocimientos en este ambito facilite los avances medicos en numerosas areas de interes clinico que puede no haber sido posible por otros metodos.
El analisis de las similitudes entre las secuencias de ADN de diferentes organismos es tambien la apertura de nuevas vias en el estudio de la evolucion. En muchos casos, las cuestiones de evolucion ahora se pueden enmarcar en terminos de biologia molecular y, de hecho, muchos de los grandes hitos evolutivos (la aparicion de los ribosomas y organulos, el desarrollo de planes de embriones con el cuerpo, el sistema inmune de vertebrados) pueden estar relacionados con el nivel molecular. Muchas de las preguntas acerca de las similitudes y diferencias entre los seres humanos y nuestros parientes mas cercanos (los primates, y de hecho los otros mamiferos) se espera que sean iluminados por los datos de este proyecto.
El Proyecto Diversidad del Genoma Humano (PDGH), derivado de investigaciones dirigidas a la asignacion del ADN humano - que varia entre los grupos etnicos - que se rumorea que ha sido detenido, realmente continua y hasta la fecha ha arrojado nuevas conclusiones. En el futuro, el PGH podria exponer nuevos datos en la vigilancia de las enfermedades, el desarrollo humano y la antropologia. El PGH podria desbloquear secretos y crear nuevas estrategias para combatir la vulnerabilidad de los grupos etnicos a ciertas enfermedades. Tambien podria mostrar como las poblaciones humanas se han adaptado a estas vulnerabilidades.
Ademas, el PGH tiene una consecuencia muy importante, y es que se pueden conocer la base molecular de ciertas enfermedades hereditarias y que se puede realizar un diagnostico de las mismas:
Conocer las bases moleculares de las enfermedades hereditarias
[
editar
]
Una de las aplicaciones mas directas de conocer la secuencia de genes que componen el
genoma humano
es que se puede conocer la base molecular de muchas enfermedades geneticas y se puede realizar un diagnostico adecuado. Algunas de estas enfermedades son las siguientes:
- Enfermedad de Gaucher
: esta enfermedad es producida por una mutacion recesiva en el gen que codifica la enzima glucocerebrosidasa, que se localiza en el cromosoma 1. Esta enzima se encarga de metabolizar los glucocerebrosidos (un tipo de lipidos). En los enfermos de Gaucher, estos lipidos no pueden ser descompuestos y se acumulan principalmente en el higado, en el bazo y en la medula osea. Los sintomas de la enfermedad de Gaucher incluyen fuertes dolores, fatiga, ictericia, danos oseos, anemia y muerte. Gracias al PGH se pudo realizar la primera terapia efectiva contra esta enfermedad, inyectandose la enzima sintetizada en
escherichia coli
en el torrente sanguineo de los enfermos. Esto detiene el avance de los sintomas y en muchos casos los revierte.
- Enfermedad de Alzheimer
: Esta enfermedad es una enfermedad degenerativa que destruye el cerebro, haciendo que los enfermos pierdan la memoria y el juicio, y que finalmente impide que se puedan valer por si solos. El unico metodo seguro para diagnosticar la
enfermedad de Alzheimer
se encuentra en la autopsia, pero actualmente, mediante resultados obtenidos con la resonancia magnetica y tomografia por emision de positrones de las proteinas beta amiloide y tau, los investigadores pueden detectar cambios cerebrales asociados a la fase preclinica (hasta 20 anos antes de los primeros sintomas) de la enfermedad. El Alzheimer esporadico es el mas comun y de origen multifactorial, aunque el mayor factor de riesgo sea la edad, mientras que el Alzheimer de origen genetico ronda en un 1 % de los casos. Gracias al PGH se han localizado marcadores para el Alzheimer de origen genetico en los cromosomas 1, 14, 19 y 21.
- Enfermedad de Huntington
: Esta enfermedad es tambien una enfermedad degenerativa y conduce a un deterioro mental que termina en demencia. Normalmente comienza a aparecer entre los 30 y los 50 anos y presenta sintomas tales como cambios en la personalidad y en el estado de animo, depresion y perdida gradual del control sobre los movimientos voluntarios, causando espasmos primero y grandes movimientos al azar posteriormente. Esta enfermedad presenta una herencia autosomica dominante, es decir, si uno de los padres la posee, sus hijos tienen el 50 % de probabilidad de padecerla tambien. La Enfermedad de Huntington no se salta generaciones. Si no se hereda el gen, no se puede transmitir a la descendencia. Del mismo, modo, si se hereda el gen, inevitablemente se padecera la enfermedad, mas tarde o mas temprano. En 1993 se consiguio aislar el gen que provoca esta enfermedad, localizado en el cromosoma 4, y en lo que se han ido desarrollando las investigaciones posteriores, ha sido fundamentalmente en conocer las razones que hacen que la Enfermedad de Huntingnton se manifieste de forma tardia, y muchas lineas de investigacion estan dirigidas a encontrar un tratamiento y una cura.
- Sindrome de Marfan
: Es una enfermedad congenita del tejido conectivo que afecta a numerosos organos y sistemas, incluyendo el esqueleto, los pulmones, los ojos, el corazon y los vasos sanguineos. Esta enfermedad se caracteriza por un crecimiento anormal de las extremidades (especialmente de los dedos), una dislocacion parcial del cristalino (en el 50 % de los pacientes), anormalidades cardiovasculares (la arteria aorta suele ser mas ancha y mas fragil que en las personas normales) y otras deformaciones. El sindrome de Marfan es tambien una enfermedad autosomica dominante, por lo que los descendientes de personas afectadas poseen el 50 % de posibilidades de padecerla. La enfermedad esta asociada al gen FBN1, localizado en el cromosoma 15. El FBN1 codifica una proteina llamada fibrilina, que es esencial para la formacion de fibras elasticas del tejido conectivo. Sin el soporte estructural de las fibras elasticas, muchos tejidos presentan una debilidad que puede conducir los sintomas comentados anteriormente.
Diagnosticos de enfermedades posibles gracias al PGH
[
editar
]
Estos son algunos ejemplos de enfermedades que se han podido diagnosticar gracias, de una u otra manera, al conocimiento de las secuencias geneticas tras la secuenciacion del genoma por el Proyecto Genoma Humano. El diagnostico de cierta enfermedad, gracias al PGH se puede realizar de manera presintomatica y prenatal.
El conocimiento de la base molecular de las enfermedades permite realizar el
diagnostico presintomatico
y gracias a el tomar medidas preventivas, como alteraciones en el estilo de vida, evitar la exposicion a factores de riesgo, realizar un seguimiento continuo del individuo o realizar intervenciones puntuales, para poder tratar la enfermedad aunque todavia no haya aparecido.
En cuanto al
diagnostico prenatal
, este consiste en un conjunto de tecnicas que sirven para conocer la adecuada formacion y el correcto desarrollo del feto antes de su nacimiento, para poder conocer posibles malformaciones desde los primeros estadios de desarrollo del embrion. La tecnica mas comun de diagnostico prenatal es la
amniocentesis
, que consiste en el analisis del liquido amniotico que rodea al feto durante el embarazo. Las celulas desprendidas del feto y que flotan en dicho liquido sirven para obtener un recuento exacto de cromosomas y para detectar cualquier estructura cromosomica anormal. El diagnostico prenatal conlleva una importante polemica. Las mujeres cuyo hijo se observe que presentan caracteristicas de padecer cierta enfermedad o que presentan malformaciones en sus cromosomas, decidiran abortar, lo que para los detractores del aborto es una aberracion. La polemica esta tambien alimentada por el hecho de que se pueden conocer tanto enfermedades que se desarrollen desde el primer dia de vida del individuo como enfermedades que pueden aparecer a su edad avanzada, como el Alzheimer, por ejemplo. En ese caso, ¿abortariamos a un feto que puede presentar la Enfermedad de Alzheimer casi al final de su vida, privandole de una vida previa normal? Esto conlleva tambien a realizar un baremo de que enfermedades podrian considerarse suficientes para realizar el aborto, poniendose por ejemplo, el daltonismo.
Por otra parte, y como consecuencia del desarrollo de las tecnicas de la fecundacion in vitro, hoy en dia se puede realizar el conocido como
diagnostico genetico preimplantacional
(DGPI). Este permite testar los embriones desde un punto de vista genetico y cromosomico para asi elegir el que se encuentre sano e implantarlo en el utero de la madre. El DGPI evita la gestacion de un nino afectado genetica o cromosomicamente, y conlleva la decision de los padres de realizar, en su caso, un aborto terapeutico.
Terapia genica, terapia farmacologica y medicina predictiva
[
editar
]
Una vez que se conocen que genes producen que enfermedades, y las caracteristicas para diagnosticar una enfermedad conociendo la secuencia de bases, es necesario realizar una terapia para acabar con esa enfermedad, ya que de ser de otra manera, el diagnostico de una enfermedad no es mas que una carga emocional que el paciente tiene que soportar de la mejor manera posible, conviviendo con la impotencia y la ansiedad que le puede suponer a un paciente el saber que en un determinado lapso de tiempo es posible que padezca una enfermedad. Una consecuencia, por tanto, del PGH es desarrollar terapias contra las enfermedades que ha diagnosticado. Se conocen la terapia genica, la terapia farmacologica y la medicina predictiva:
- La
terapia genica
es una consecuencia directa del PGH y supone la probabilidad de curar las enfermedades hereditarias cartografiadas por este, insertando copias funcionales de genes defectivos o ausentes en el genoma de un individuo para tratar dicha enfermedad. Las tecnicas actuales de terapia genica no pueden asegurar que el gen se inserte en un lugar apropiado del genoma, existe la posibilidad de que interfiera con el funcionamiento de un gen importante o incluso que active un oncogen, provocando asi un cancer en el paciente. Sin embargo, estas tecnicas solo se utilizan con pacientes que ya corren peligro inminente de muerte, por lo que la posibilidad de contraer un cancer en un futuro incierto no constituye un impedimento muy grave para aceptar el tratamiento.
- El primer caso que se conoce de terapia genica tuvo lugar en los NIH (
National Institutes of Health
. En espanol: Institutos Nacionales de la Salud), en
Bethesda, Maryland
. Consistio en la inoculacion de globulos blancos geneticamente modificados a una nina que padecia
inmunodeficiencia severa combinada
(deficiencia de
adenosina-desaminasa
o ADA). Esta enfermedad es una
enfermedad rara
, y la carencia de
ADA
se puede tratar con trasplantes de medula osea. Sin embargo, el trasplante solo es posible si el paciente tiene un hermano que no este afectado por la enfermedad y que sea compatible. Otra posibilidad es inyectar la proteina directamente, pero las inyecciones no llegan inmediatamente al lugar necesario y constituyen un mal sucedaneo de los sutiles mecanismos que controlan y dirigen la produccion de
ADA
en circunstancias normales. La operacion consistio en la extraccion de linfocitos T de la paciente, su modificacion genetica y su reimplantacion. Con esto las celulas comenzaron a producir la
ADA
.
- Cuando se realizo esta primera intervencion, los doctores de los NIH estudiaron las implicaciones eticas que podia tener esta operacion y llegaron a la conclusion de que no existia diferencia moral con respecto a cualquier tipo de trasplante de tejidos o de organos. Esta comparacion residia en que los genes trasplantados solo afectaban a las celulas somaticas del individuo, de modo que solo afectaban a la nina misma y que no lo harian por tanto a su descendencia. Podemos diferenciar entonces dos tipos de terapia genica, en linea somatica y en linea germinal. Esta ultima consiste en introducir genes nuevos, biologicamente funcionales, en
celulas germinales
(
ovulos
y/o
espermatozoides
) antes de que se produzca la
fecundacion
. El
embrion
que surge tras la fecundacion partira de una unica celula modificada geneticamente, por lo que todas sus celulas posteriores presentaran la misma modificacion, incluyendo las futuras celulas germinales que producira, pudiendo transmitir sus caracteristicas a las generaciones futuras.
- Todos los estudios nacionales han rechazado la terapia en linea germinal, de momento, ya que opinan que todavia no se dispone de los suficientes conocimientos para evaluar los riesgos que supone este tipo de terapia y que es necesario realizar un estricto examen etico antes de comenzar a aplicarla, si esto se acabara produciendo.
- La
terapia farmacologica
se ve tambien facilitada por el PGH ya que este permite encontrar alteraciones en la secuencia del ADN de genes especificos y esto conlleva a que se realice el tratamiento con medicamentos de una manera dirigida, neutralizando las alteraciones y modificando favorablemente el curso de la enfermedad de forma mas efectiva que los tratamientos de la medicina actual, que estan generalmente dirigidos a aliviar los sintomas.
- El PGH permite ademas, en relacion con la farmacologia, modificar los medicamentos para que se ajusten a las caracteristicas geneticas del paciente y asi poder metabolizar el farmaco de la mejor manera posible, lo que en consecuencia, elimina o minimiza los efectos secundarios indeseables del mismo. Gracias al PGH el medico tendra un perfil genetico del paciente antes de iniciar el tratamiento.
- La
medicina predictiva
permite diagnosticar enfermedades, gracias a los conocimientos del genoma, que aun no se han desarrollado en el paciente. Se distinguen dos tipos de enfermedades que se pueden diagnosticar mediante la medicina predictiva. Las monogenicas, que se pueden identificar facilmente ya que se conocen perfectamente las leyes deterministas que las regulan; y las poligenicas, para cuyo buen estudio es necesario realizar sondeos poblacionales. Por ejemplo se pueden encontrar los genes que regulan el nivel de colesterol en la sangre (unos veinte). Determinadas combinaciones de variedades de estos genes situan al sujeto en un grupo de riesgo de padecer enfermedades tempranas de las arterias coronarias y ataques cardiacos. Si ademas el sujeto lleva una dieta rica en grasas animales y una vida sedentaria (tambien influyen por tanto agentes externos como puede ser el modo de vida y la alimentacion), es muy posible que muera de infarto antes de los cincuenta anos. La meta es conocer exactamente que combinaciones de genes son especialmente peligrosas y en esto tiene un papel muy importante el Proyecto Genoma Humano. La medicina predictiva tambien causa una importante controversia en la sociedad ya que los estudios poblaciones que se realizan para estudiar las enfermedades poligenicas se pueden utilizar para discriminar a ciertas personas o grupos, lo que se llamaria discriminacion genetica. Este tema se tratara en el apartado Aspectos Eticos.
Aspectos eticos y controversia
[
editar
]
Aunque la medicina proporciona la base para la evolucion de la bioetica, actualmente somos testigos de su aplicacion a la investigacion cientifica relacionada. Asi pues, el PGH ha dado lugar a una de las areas de conocimiento biologico con mayor crecimiento. Los conocimientos genomicos derivados del Proyecto Genoma Humano, se utilizan para mejores y mas rapidos diagnosticos basados en el analisis directo del ADN, e incluso para el diagnostico prenatal en aquellos casos en los que se sospecha que el bebe tenga alteraciones morfologicas, funcionales o ponga en peligro la vida de su madre. Tambien es posible aplicar este conocimiento a personas asintomaticas para averiguar si han heredado de algun progenitor una mutacion causal de una enfermedad genetica que pueda desarrollarse en el futuro.
Asi planteado el tema, se percibe entonces una importante brecha entre la capacidad diagnostica y predictiva del conocimiento genomico por un lado, y la falta de intervenciones preventivas y terapeuticas por otro, lo que lleva a conflictos eticos surgidos del Proyecto Genoma Humano. Ademas hay determinadas areas como el asesoramiento a parejas en riesgo de transmitir enfermedades geneticas a su descendencia, que han suscitado mucho interes y para las que se han dictado una serie de principios eticos:
- Respeto a la dignidad individual y a la inteligencia basica de las personas, asi como a sus decisiones medicas y reproductivas (libre eleccion de interrumpir o continuar un embarazo con riesgo).
- Informar objetivamente al paciente sin tener en cuenta los valores subjetivos del profesional medico.
- Proteccion a la privacidad de la informacion genetica.
- Desmitificacion del Proyecto Genoma Humano, aclarando verdaderamente su alcance con acciones especificas en educacion.
Otro problema de gran importancia es la obtencion de patentes de genes por parte de companias biotecnologicas, gobiernos y centros de investigacion universitarios, para una posterior venta o explotacion comercial, sin tener en cuenta que parte de los fondos empleados en el PGH era de los contribuyentes. Tambien debemos observar el PGH contextualizado social e historicamente, atendiendo a la desigualdad social y economica entre paises, que va a producir una inequidad en el acceso a los beneficios que se extraigan de la investigacion.
Una solucion a todas estas tensiones podria ser la formacion de profesores de ciencias o la ensenanza directa a estudiantes como una forma de abrir las mentes y aclarar definitivamente el alcance del Proyecto Genoma Humano en la sociedad. Pero es imprescindible incorporar temas de bioetica a los programas de ensenanza.
Tanto en Estados Unidos como en la Union Europea se han desarrollado programas para contemplar las consecuencias eticas y sociales de la investigacion cientifica y que no se produzcan conflictos. En Estados Unidos se encuentra el ELSI y fuera de ellos se encuentra la Declaracion Universal sobre el Genoma Humano y los Derechos Humanos, promovida por la UNESCO
El ELSI es el
Programa Etico, Legal y Social
(Ethical, Legal and Social Implications Research Program, en ingles) que desarrollo el
Instituto Nacional de Investigacion del Genoma Humano
de Estados Unidos en 1990. Este programa permite un acercamiento a la investigacion cientifica teniendo en cuenta las implicaciones eticas, legales y sociales que esta supone, al mismo tiempo que se esta investigando para, de esta manera, poder identificar los posibles futuros problemas y solucionarlos antes de que la informacion cientifica se extienda.
El programa de investigacion ELSI tiene un papel muy importante en todo lo relacionado con el PGH, y se encarga de analizar las implicaciones eticas y sociales de la investigacion genetica de la siguiente manera:
- Examinando las ediciones que rodean la terminacion de la secuencia humana del ADN y del estudio de la variacion genetica humana.
- Examinando las ediciones llevadas a cabo por la integracion de tecnologias e informacion genetica para el cuidado medico y actividades de la salud publica.
- Explorando las maneras en las cuales el nuevo conocimiento genetico puede actuar reciprocamente con una variedad de perspectivas eticas, filosoficas y teologicas.
- Explorando como influyen en el uso e interpretacion de la informacion genetica, de la utilizacion de servicios geneticos y del desarrollo de la politica, los factores y los conceptos socioeconomicos de la raza y de la pertenencia etnica.
Para alcanzar estas metas, las actividades y la investigacion del programa de ELSI se centran en cuatro areas del programa:
- Aislamiento e imparcialidad en el uso y la interpretacion de la informacion genetica.
- Integracion clinica de las nuevas tecnologias geneticas.
- Ediciones que rodean la investigacion de la genetica.
- Educacion publica profesional.
El ELSI tambien ha iniciado una serie de emprendimientos educacionales que estan dirigidos a entrenar a profesionales de la salud para que puedan interpretar los nuevos tests diagnosticos basados en el ADN que comenzaran a surgir mas y mas frecuentemente gracias a la informacion obtenida del PGH. Ademas de esta formacion de profesionales de la salud tambien se necesita que los politicos y el publico en general tengan un criterio suficiente sobre algunos asuntos criticos relacionados con las pruebas geneticas. Por ello, es necesario extender la informacion genetica en las escuelas, los medios de comunicacion, alentar la discusion publica sobre el tema y suministrar tambien informacion a los politicos. Una de las iniciativas es el establecimiento de la Coalicion Nacional para la Educacion de los Profesionales de la Salud en Genetica (NCHPEG), tambien en EE. UU., pero rapidamente se queda insuficiente ya que solo abarca a los profesionales de la Salud.
Declaracion Universal sobre el Genoma Humano y los Derechos Humanos
[
editar
]
Asi como Estados Unidos tiene un programa para regular las implicaciones sociales y eticas que tienen las investigaciones cientificas para tratar de regularlas y que no haya conflictos, la
UNESCO
redacto en 1997 la
Declaracion Universal sobre el Genoma Humano y los Derechos Humanos
, cuyo prefacio es el siguiente:
- La Declaracion Universal sobre el Genoma Humano y los Derechos Humanos, aprobada el 11 de noviembre de 1997 por la Conferencia General en su 29ª reunion por unanimidad y por aclamacion, constituye el primer instrumento universal en el campo de la biologia. El merito indiscutible de ese texto radica en el equilibrio que establece entre la garantia del respeto de los derechos y las libertades fundamentales, y la necesidad de garantizar la libertad de la investigacion. La Conferencia General de la UNESCO acompano esa Declaracion de una resolucion de aplicacion, en la que pide a los Estados Miembros que tomen las medidas apropiadas para promover los principios enunciados en ella y favorecer su aplicacion. El compromiso moral contraido por los Estados al adoptar la Declaracion Universal sobre el Genoma Humano y los Derechos Humanos es un punto de partida: anuncia una toma de conciencia mundial de la necesidad de una reflexion etica sobre las ciencias y las tecnologias. Incumbe ahora a los Estados dar vida a la Declaracion con las medidas que decidan adoptar, garantizandole asi su perennidad.
Federico Mayor, 3 de diciembre de 1997.
Esta compuesta por 25 articulos que se dividen en las siguientes areas, destacando en cada una de ellas un determinado articulo:
- La dignidad humana y el genoma humano.
Contiene los 4 primeros articulos y establece la base la declaracion y su objeto, el ser humano y el genoma humano. Cabe destacar el articulo 1:
El genoma humano es la base de la unidad fundamental de todos los miembros de la familia humana y del reconocimiento de su dignidad intrinseca y su diversidad. En sentido simbolico, el genoma humano es el patrimonio de la humanidad.
- Derechos de las personas interesadas.
Esta compuesta por los articulos desde el 5 al 9 y presenta los derechos que tienen las personas como portadoras de los genes y sus consecuencias sociales. Cabe destacar el articulo 6 porque esta relacionado con la discriminacion genetica, que sera tratada mas adelante:
Nadie podra ser objeto de discriminaciones fundadas en sus caracteristicas geneticas, cuyo objeto o efecto seria atentar contra sus derechos humanos y libertades fundamentales y el reconocimiento de su dignidad.
- Investigaciones sobre el genoma humano.
Formada por los articulos 10, 11 y 12. Trata la imposicion de la dignidad humana sobre cualquier tipo de investigacion relativa al genoma humana, el derecho de todas las personas a acceder a los progresos de la biologia y a la orientacion de la investigacion en el campo de la biologia, genetica y medicina hacia un alivio del sufrimiento y una mejora de la salud del individuo y de toda la humanidad. Se puede destacar el articulo 10 que alienta a los Estados miembros a actuar sobre posibles conductas contrarias a la declaracion:
No deben permitirse las practicas que sean contrarias a la dignidad humana, como la clonacion con fines de reproduccion de seres humanos. Se invita a los Estados y a las organizaciones internacionales competentes a que cooperen para identificar estas practicas y a que adopten en el plano nacional o internacional las medidas que correspondan, para asegurarse de que se respetan los principios enunciados en la presente Declaracion.
- Condiciones de ejercicio de la actividad cientifica.
Contiene los articulos del 13 al 16 y en ellos se otorga a los Estados miembros la potestad de regular las actividades relacionadas con la investigacion y de crear organismos para regular las consecuencias eticas y sociales causadas por ella, como declarar el articulo 16:
Los Estados reconoceran el interes de promover, en los distintos niveles apropiados, la creacion de comites de etica independientes, pluridisciplinarios y pluralistas, encargados de apreciar las cuestiones eticas, juridicas y sociales planteadas por las investigaciones sobre el genoma humano y sus aplicaciones.
- Solidaridad y cooperacion internacional.
Esta parte esta formada por los articulos 17, 18 y 19 y se refiere a la cooperacion y solidaridad tanto entre los individuos que forman los Estados miembros como entre los Estados mismos, refiriendose en primer lugar a casos como enfermedades geneticas y en el segundo a compartir conocimientos cientificos sobre el genoma humano entre paises que tengan una gran investigacion desarrollada y otros que la tengan menos, como dice el articulo 18:
Los Estados deberan hacer todo lo posible, teniendo debidamente en cuenta los principios establecidos en la presente Declaracion, para seguir fomentando la difusion internacional de los conocimientos cientificos sobre el genoma humano, la diversidad humana y la investigacion genetica, y a este respecto favoreceran la cooperacion cientifica y cultural, en particular entre paises industrializados y paises en desarrollo.
- Fomento de los principios de la Declaracion.
Son los articulos 20 y 21 e impulsan a los Estados miembros de la UNESCO a fomentar y extender los principios entre los individuos que los forman, tambien entre los politicos, y ademas comprometerse a favorecer el debate abierto y la libre expresion de corrientes socioculturales, religiosas o filosoficas. El articulo 20 tambien impulsa la informacion desde la educacion:
Los Estados tomaran las medidas adecuadas para fomentar los principios establecidos en la Declaracion, a traves de la educacion y otros medios pertinentes, y en particular, entre otras cosas, la investigacion y formacion en campos interdisciplinarios y el fomento de la educacion en materia de bioetica, en todos los niveles, particularmente para los responsables de las politicas cientificas.
- Aplicacion de la Declaracion.
Los articulos del 22 al 25 se refieren a la obligacion de los Estados de fomentar el respeto frente a los enunciados de la Declaracion, difundirlos y hacerse cargo de que se realicen correctamente. Asi, el articulo 23 declara:
Los Estados tomaran las medidas adecuadas para fomentar mediante la educacion, la formacion y la informacion, el respeto de los principios antes enunciados y favorecer su reconocimiento y su aplicacion efectiva. Los Estados deberan fomentar tambien los intercambios y las redes entre comites de etica independientes, segun se establezcan, para favorecer su plena colaboracion.
Discriminacion genetica y patente de genes
[
editar
]
Entramos ahora en los que posiblemente sean los dos puntos mas importantes de la controversia causada por el PGH, que se pasan a explicar a continuacion:
Discriminacion genetica
[
editar
]
El
ELSI
tiene un papel muy importante en el campo de la discriminacion genetica. Cuando se dieron los primeros pasos del PGH, los cientificos tuvieron muy claro desde el principio que era necesario realizar un estudio etico y social, inicialmente a pequena escala y si era necesario, a mayor; sobre alguna enfermedad que pudiera tener lugar en la sociedad, para evitar cualquier tipo de discriminacion genetica. Un ejemplo interesante de discriminacion genetica tuvo lugar en Estados Unidos durante los anos setenta y relacionada con una campana que realizo el gobierno para detectar portadores del gen de la
anemia de celulas falciformes
.
 Capilares sanguineos en los que se pueden observar eritrocitos falciformes.
Capilares sanguineos en los que se pueden observar eritrocitos falciformes.
La anemia de celulas falciformes, ademas, tiene un componente relacionado con la
raza
muy importante, ya que es la enfermedad genetica mas frecuente entre la poblacion negra. Se trata de una enfermedad
recesiva
bastante cruel ya que los que la sufren no pueden realizar esfuerzos, ya que corren un grave riesgo de sufrir una
insuficiencia respiratoria aguda
que les ocasione repentinamente la muerte. Pues bien, la discriminacion genetica aparece cuando el gobierno realizo un estudio poblacional para detectar individuos que portaran este gen. La anemia de celulas falciformes no tiene cura y por tanto, si alguien era diagnosticado de anemia de celulas falciformes no poseia la mas minima esperanza de curacion. El problema se hizo patente cuando el gobierno declaro obligatorio en varios estados realizar la prueba de deteccion a los recien nacidos y a los escolares, sin seguir un programa paralelo de orientacion genetica que pudiera ofrecer consejo a las familias afectadas, y cuando el publico comenzo a confundir a las personas portadoras (
heterocigoticas
) con las enfermas, debido a la completa falta de una campana informativa. Por si esto fuera poco,
Linus Pauling
, que habia descubierto el metodo de analisis de la
hemoglobina
, realizo unas desafortunadas declaraciones en las que sugeria que se marcara de alguna manera a los portadores para que no se mezclaran y no tuvieran hijos entre si. La informacion que se recogio en este estudio paso a formar parte del historial medico de los ninos que estaban afectados. Las companias de seguros comenzaron entonces a negarse a formalizar el seguro si conocian que su posible cliente padecia anemia de celulas falciformes, e incluso si era simplemente portador del gen. Tambien el mercado de trabajo comenzo a discriminar a los enfermos y portadores. A las personas de color que portaban el gen se les negaba por ejemplo el trabajo en companias aereas porque se pensaba que su sangre reaccionaria mal al encontrarse a bajas presiones causados por la altura del avion (algo que es erroneo).
Un gran problema que tuvo el caso de la anemia de celulas falciformes en los anos setenta fue que no se conocian metodos de estudio del feto y que tampoco estaba permitido el aborto. Esto se ha podido superar actualmente y es un problema menor para el programa
ELSI
, ya que ahora si existe la posibilidad de detectar la enfermedad en el feto y, ademas de que ya esta permitido, el aborto terapeutico tiene una aceptacion social casi mayoritaria.
En definitiva, es necesario realizar un estudio social y etico y dar la informacion necesaria a la opinion publica para que no se produzcan casos de discriminacion genetica, si ya no tan llamativos como el de la anemia de celulas falciformes en EE. UU., pero si a menor escala como puede ser la predisposicion hacia enfermedades cardiacas o a las discapacidades mentales, por ejemplo.
Patente de genes
[
editar
]
El concepto de ≪patente de genes≫ aparece tambien con la secuenciacion del genoma producida por el PGH. Y es que resulta necesario compatibilizar las expectativas terapeuticas y de avance cientifico con las expectativas de aspecto economico, procurando encontrar un equilibrio razonable entre el altruismo que unos buscan en el conocimiento publico de la informacion proporcionada por el PGH y otros que encuentran esta informacion suficiente para sacarle provecho economico. Es necesario combinar la moralidad con el interes economico. El elemento fundamental de todo esto se encuentra en las empresas privadas que realizan investigaciones en el
genoma humano
. Como tales empresas privadas, necesitan obtener un beneficio que supla las grandes inversiones que hacen en investigaciones para obtener posteriormente productos farmaceuticos, desarrollar terapias clinicas u otras aplicaciones. Para esto, necesitan proteger sus hallazgos para que nadie se aproveche de su esfuerzo. La cuestion reside en determinar cual es el marco juridico apropiado para garantizar debidamente esas expectativas de beneficio. Es, por tanto, logico que se tratara de amparar bajo la proteccion de las patentes a los descubrimientos relacionados con la descodificacion y aislamiento del ADN, considerandolo una sustancia o estructura que, como otras, se encuentra en la naturaleza y de cuyo conocimiento se puede derivar algun uso diagnostico y con el fin de compensar las inversiones economicas realizadas. De este modo, los investigadores o instituciones que patentaran la secuencia parcial o total de cierto gen podrian ser acreedores de los derechos que se derivaran de ella para la obtencion de farmacos. Por otro lado, hay gente que piensa que las patentes no hacen mas que impedir el desarrollo biotecnologico y que la informacion que se encuentra en los genes deberia ser de acceso publico.
Las patentes sobre secuencias totales o parciales de genes continuan estando en una importante controversia y se pueden encontrar tres posiciones diferentes:
- La postura de la UNESCO
: afirma que el Genoma Humano es patrimonio de la Humanidad y que debe quedar excluido de cualquier apropiacion publica o privada.
- La postura estadounidense
: representada por los NIH y
Craig Venter
(dueno de la empresa
Celera Genomics
, empresa biotecnologica involucrada en el estudio del Genoma Humano). Parten de que los genes, por muy esenciales que sean para la vida, no son vida humana, y tampoco pueden clasificarse como materia exclusivamente humana ya que los compartimos con otras especies. Opinan que no hay nada que choque contra los criterios de patentabilidad impuestos por la USPTO (
http://en.wikipedia.org/wiki/USPTO_registration_examination
), por lo que nada deberia impedirles proteger la informacion obtenida y conseguir beneficios para poder avanzar en sus investigaciones.
- La postura europea:
se encuentra en una posicion intermedia. Niega la patentabilidad de cualquier genoma individual completo pero admite que se puedan patentar los genes humanos individualmente si han sido aislados. Tambien mantiene clausulas de moralidad que permitan rechazar administrativa o jurisdiccionalmente determinadas solicitudes de patente. (Directiva Europea 98/44/CE Art. 5
https://web.archive.org/web/20160304212509/http://www.cgcom.org/sites/default/files/54_Directiva_98_44_CE.pdf
). La Directiva europea pretende solucionar los problemas de las patentes estableciendo una distincion de planos. Por un lado se encontrarian los genes “tal y como se encuentran en la naturaleza”, que actuarian como patrimonio comun de la humanidad y a los que se debe proteger, y por otro lado se encontrarian los genes “que han sido aislados de su medio natural por procedimientos tecnicos”, sobre los que si podria implantarse una patente al haberse modificado su naturaleza a traves del procedimiento tecnico.
Proyecto Genoma Humano
[
editar
]
El Proyecto Genoma Humano permite obtener informacion de la estructura genetica de un individuo, pero en principio solo se queda ahi. Esa informacion estructural permite conocer la base molecular de muchas enfermedades y, sobre esa base, realizar el mejor diagnostico posible. Pero, desde un punto de vista biologico, el PGH es la antesala de un proyecto mucho mas interesante y dinamico, y es el
proyecto proteoma humano
. Gracias a la
proteomica
se puede conocer como la secuencia genetica se transforma en una
proteina
que va a desarrollar cierta funcion.
Cifras y datos
[
editar
]
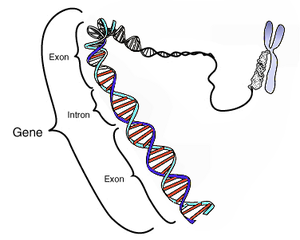 Este diagrama esquematico muestra un gen en relacion a su estructura fisica (doble helice de ADN) y a un cromosoma (derecha). Los intrones son regiones frecuentemente encontradas en los genes de eucariotas, que se transcriben, pero son eliminadas en el procesamiento del ARN (ayuste) para producir un ARNm formado solo por exones, encargados de traducir una proteina. Este diagrama es en exceso simplificado ya que muestra un gen compuesto por unos 40 pares de bases cuando en realidad su tamano medio es de 20 000-30 000 pares de bases).
Este diagrama esquematico muestra un gen en relacion a su estructura fisica (doble helice de ADN) y a un cromosoma (derecha). Los intrones son regiones frecuentemente encontradas en los genes de eucariotas, que se transcriben, pero son eliminadas en el procesamiento del ARN (ayuste) para producir un ARNm formado solo por exones, encargados de traducir una proteina. Este diagrama es en exceso simplificado ya que muestra un gen compuesto por unos 40 pares de bases cuando en realidad su tamano medio es de 20 000-30 000 pares de bases).
- El Consorcio Internacional, integrado por 20 grupos de diferentes paises y por otro lado la empresa privada Celera, hicieron publico, el 12 de febrero de 2001, el mapa provisional del genoma humano (GH) que aporta una extraordinaria informacion acerca de las bases geneticas del ser humano.
- El Consorcio Internacional ha calculado que el genoma humano contiene 20 500 genes.
- De los 300 000 clones de partida fueron validos 30 000 clones que representan un total de 3200 megabases. Estos resultados alcanzados en octubre del 2000, representan el 90 % del genoma. La secuencia obtenida es de enorme trascendencia y son muchos y variados los puntos de interes pudiendo destacarse algunos datos:
- El humano tiene solo el doble de genes que la mosca del vinagre, un tercio mas que el gusano comun y apenas 5000 genes mas que la planta
Arabidopsis
.
- 3200 millones de pares de bases forman genes, repartidos entre los 23 pares de cromosomas. Los cromosomas mas densos (con mas genes codificadores de proteinas) son el 17, 19 y el 22. Los cromosomas X, Y, 4, 18 y 13 son los mas aridos.
- El equipo de Celera Genomics utilizo para secuenciar el genoma humano muestras de ADN de tres mujeres y dos hombres (un afroamericano, un chino, un asiatico, un hispanomexicano y un caucasiano). El equipo de Celera utilizo ADN perteneciente a doce personas. Cada persona comparte un 99,99 por ciento del mismo codigo genetico con el resto de los seres humanos. Solo 1250 nucleotidos separan una persona de otra.
- Hasta ahora se han encontrado 223 genes humanos que resultan similares a los genes bacterianos.
- Solo un 5 % del genoma codifica proteinas. El 25 % del genoma humano esta casi desierto, existiendo largos espacios libres entre un gen y otro.
- Se calcula que existen entre 250 000 y 300 000 proteinas distintas. Por tanto cada gen podria estar implicado por termino medio en la sintesis de unas diez proteinas.
- Algo mas del 35% del genoma contiene secuencias repetidas. Lo que se conoce como ADN basura.
- Se han identificado un numero muy elevado de pequenas variaciones en los genes que se conocen como
polimorfismos nucleotidos unicos
, SNP de su acronimo ingles. Celera ha encontrado 2,1 millones de SNP en el genoma y el Consorcio 1,4 millones. La mayoria de estos polimorfismos no tienen un efecto clinico concreto pero de ellos depende, por ejemplo, el que una persona sea sensible o no a un determinado farmaco y la predisposicion a sufrir una determinada enfermedad.
Finalizacion de la secuenciacion del genoma
[
editar
]
Telomere-to-Telomere (T2T)
[
editar
]
El
Telomere-to-Telomere Consortium
en 2022 anuncio que habian descubierto las secuencias finales de ADN del genoma humano, tras 32 anos de estudio.
[
15
]
El Proyecto Genoma Humano finalizo en 2003, describiendo alrededor del 92% de la secuencia. Esta ultima etapa se pudo completar tras el desarrollo de herramientas computacionales mas complejas, ya que genoma humano consta de unos 3 mil millones de bases en un orden preciso, que no se puede leer de un extremo a otro. Por lo que primero se debio determinar la secuencia de secciones aleatorias de ADN (de hasta diez mil bases diferentes) y luego usar esas secuencias para rearmar toda la secuencia del
genoma
.
[
16
]
La secuencia descrita por T2T incluye algunos genes y ADN repetitivo, que reside cerca de los
telomeros
repetitivos y los
centromeros
.
[
17
]
(Para acceder al mapeado del genoma humano, revisar
Human Genome Resources at NCBI
)
Referencias
[
editar
]
- ↑
≪Cientificos de todo el mundo anuncian el primer borrador del genoma humano≫
.
El Mundo
. 27 de junio de 2000
. Consultado el 3 de mayo de 2020
.
- ↑
Meilan, J.; Allende, I. (26 de junio de 2000).
≪El conocimiento del genoma revolucionara la medicina y la biologia del ser humano≫
.
La Voz de Galicia
(Londres/Nueva York)
. Consultado el 3 de mayo de 2020
.
- ↑
a
b
≪HMP (Proyecto de Microbioma Humano)≫
.
Observatorio de la Microbiota Intestinal de la Sociedad Europea de Neurogastroenterologia y Motilidad
. 26 de febrero de 2015
. Consultado el 2 de mayo de 2020
.
- ↑
a
b
Baquero, Fernando
;
Nombela, Cesar
(18 de julio de 2012).
≪The microbiome as a human organ≫
.
The microbiome as a human organ.
(en ingles)
.
PMID
22647038
.
doi
:
10.1111/j.1469-0691.2012.03916.x
.
- ↑
Sinsheimer RL (November 1989). ≪The Santa Cruz Workshop ? May 1985 and≫.
Genomics
5
(4): 954-956.
PMID
2591974
.
doi
:
10.1016/0888-7543(89)90142-0
.
- ↑
DeLisi C (October 2008). ≪Meetings that changed the world: Santa Fe 1986: Human genome baby-steps≫.
Nature
455
(7215): 876-877.
Bibcode
:
2008Natur.455..876D
.
PMID
18923499
.
S2CID
41637733
.
doi
:
10.1038/455876a
.
- ↑
Dulbecco R (March 1986). ≪A turning point in cancer research: sequencing the human genome≫.
Science
231
(4742): 1055-1056.
Bibcode
:
1986Sci...231.1055D
.
PMID
3945817
.
doi
:
10.1126/science.3945817
.
- ↑
Cook-Deegan, Robert M. (1994).
The Gene Wars: Science, Politics, and the Human Genome
. New York: W.W. Norton. pp.
108
.
- ↑
≪President Clinton Awards the Presidential Citizens Medals≫
.
clintonwhitehouse5.archives.gov
.
- ↑
≪File:Plaque commemorating the Human Genome Project, outside Charles DeLisi's former office at DOE.png ? Wikimedia Commons≫
.
- ↑
Bevatron's Encyclopedia of Inventions: a compendium of technological leaps, ground break discoveries and scientific breakthroughs that changed the world. The Human Genome Project, Charles DeLisi, pp. 360?362.
- ↑
Origins of the Human Genome Project: A Political History ? Bob Cook-Deegan
https://www.youtube.com/watch?v=-opMu4Ld21Q&t=3885s
- ↑
Noble, Ivan; Personal cientifico de BBC News Online (14 de abril de 2003).
≪Human genome finally complete≫
.
BBC NEWS
. Consultado el 22 de julio de 2006
.
- ↑
≪Terminacion del Proyecto Genoma Humano: Preguntas mas frecuentes≫
.
Instituto Nacional de Investigacion del Genoma Humano
. 13 de octubre de 2011
. Consultado el 3 de mayo de 2020
.
- ↑
≪Telomere-to-Telomere≫
.
www.genome.gov
(en ingles)
. Consultado el 19 de enero de 2024
.
- ↑
≪Completing the human genome sequence≫
.
www.genome.gov
(en ingles)
. Consultado el 19 de enero de 2024
.
- ↑
Green, Eric D.
≪Completing the Human Genome Sequence (Again)≫
.
Scientific American
(en ingles)
. Consultado el 19 de enero de 2024
.
Vease tambien
[
editar
]
Enlaces externos
[
editar
]