 Magenkrebs in fortgeschrittenem Stadium
Magenkrebs in fortgeschrittenem Stadium
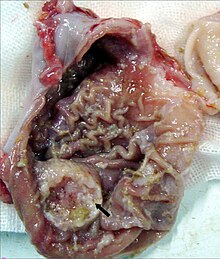 Ein
ulzerierendes
Magenkarzinom (siehe Pfeil) bei einem
Weißen Neuseelander
(Kaninchen).
Ein
ulzerierendes
Magenkarzinom (siehe Pfeil) bei einem
Weißen Neuseelander
(Kaninchen).
Ein
Magenkarzinom
(Synonym:
Magenkrebs
) ist eine
Krebserkrankung
des
Magens
. Im Gegensatz zu den meisten anderen Krebsarten hat die Anzahl an Neuerkrankungen pro Jahr in den westlichen Landern seit Jahren kontinuierlich abgenommen. Hauptrisikofaktoren fur die Entstehung eines Magenkarzinoms sind eine
nitrosaminreiche
Ernahrung sowie eine chronische Infektion mit
Helicobacter pylori
. Zentrale Bedeutung in der Diagnostik des Magenkrebses hat die Magenspiegelung (
Gastroskopie
). Mittels kleiner Gewebeproben, die im Rahmen einer solchen Untersuchung gewonnen werden, kann die Diagnose genau vom
Pathologen
gestellt werden. Beim Fehlen von
Metastasen
(Tochtergeschwulsten) ist die Therapie der Wahl die operative Entfernung des Magens (
Gastrektomie
), verknupft mit einer Entfernung der lokalen Lymphknoten (
Lymphadenektomie
). In Abhangigkeit vom Tumorstadium erfolgt bei lokalem Tumorstadium eventuell zusatzlich eine
Chemotherapie
vor der Operation, eine sogenannte
neoadjuvante Chemotherapie
, oder im Anschluss an die Operation (
adjuvante Chemotherapie
). Bei Vorliegen von Fernmetastasen ist keine heilende Therapie mehr moglich. In diesem Stadium wird bei Hinweis auf Behinderung der Magenpassage eine Umgehungsoperation (palliative Gastrektomie) durchgefuhrt. Fehlt diese Symptomatik, so wird in Abhangigkeit vom
Allgemeinzustand
des Patienten eine
palliative
Chemotherapie durchgefuhrt.
Weltweit stellt das Magenkarzinom den zweithaufigsten Tumor des Menschen dar.
[1]
In
Deutschland
macht Magenkrebs nur rund 5 % aller malignen Erkrankungen aus.
[2]
Das Auftreten variiert regional erheblich. Lander mit hohem Auftreten sind
Japan
,
Chile
,
Costa Rica
,
Kolumbien
,
China
,
Portugal
,
Russland
und
Bulgarien
. In diesen Staaten ist das Auftreten rund vier- bis sechsfach im Vergleich zu Landern mit niedrigem Risiko erhoht. In der westlichen Welt geht die Krebsart mittlerweile im Vergleich zu anderen Krebsarten zuruck. So war sie 1930 die haufigste Krebstodesursache in den
USA
, heute ist Magenkrebs nur noch fur rund 2,5 % der Krebstoten verantwortlich. Dies lasst sich durch ein besseres Langzeituberleben der Patienten erklaren, ist aber vor allem der Abnahme der
Neuerkrankungsrate
zu verdanken. Diese fiel von 38:100.000 in den 1930er-Jahren auf rund 5:100.000 im 21. Jahrhundert. In den meisten Staaten sind Manner gegenuber Frauen doppelt so oft von der Krankheit betroffen.
[1]
Im Jahr 2002 wurden in Deutschland knapp 20.000 Falle diagnostiziert. Dort erkranken seither jedes Jahr uber 15.000 Menschen neu an Magenkrebs, davon uber 9.000 Manner.
[3]
Manner sind etwas haufiger als Frauen betroffen (Verhaltnis etwa 3:2). Der Haufigkeitsgipfel liegt jenseits des 50. Lebensjahres.
 Lage des Magens im Verdauungstrakt
Lage des Magens im Verdauungstrakt
Zu den umweltbedingten Risikofaktoren zahlen die Infektion mit
Helicobacter pylori
, bestimmte Ernahrungsweisen und gesellschaftliche Faktoren. Eine chronische Infektion mit Helicobacter pylori, einem Bakterium, das in der
Magensaure
uberleben kann und auch
Magengeschwure
begunstigt, steigert das Risiko von Magenkrebs um den Faktor funf bis sechs. Zwar fuhrt nicht jede Infektion zum Krebs, aber in fast allen Karzinomen vom intestinalen Typ kann eine Infektion nachgewiesen werden. Eisenmangel erhoht das Risiko, dass aus einer Helicobacter-Infektion ein Karzinom entsteht.
[4]
Eine Ernahrung mit hohem Gehalt an
Nitrat
und
Nitrit
, das in schlecht aufbereitetem Trinkwasser oder
Konservennahrung
vorkommen kann, fordert auch die Krebsentstehung. Ebenso kann mit der Nahrung aufgenommenes
Benzo[
a
]pyren
zur Entartung beitragen. Auch
Rauchen
erhoht uber einen bisher unbekannten Mechanismus das Risiko, an einem Magenkarzinom zu erkranken. Da diese Risikofaktoren vor allem bei Personen mit geringem sozio-okonomischen Status vorhanden sind, tritt Magenkrebs in dieser Bevolkerungsgruppe gehauft auf.
[1]
Ferner gilt auch Alkoholgenuss als wahrscheinlicher Risikofaktor, in der Entstehung von Magenkarzinomen.
[5]
[6]
Außerdem gibt es zahlreiche patientenbezogene Risikofaktoren, die Magenkrebs begunstigen. Eine chronische
Magenschleimhautentzundung
senkt auf die Dauer den Saurespiegel und macht so den Magen verwundbar fur die Besiedlung mit Helicobacter. Ebenso fuhrt sie durch die andauernde
Entzundungsreaktion
zu einer
Umwandlung der Schleimhaut
, bei der Magenschleimhaut durch Schleimhaut, die der des Darms ahnelt, ersetzt wird. Diese
Lasionen
gelten als Vorlaufer eines Karzinoms vom intestinalen Typ. Patienten, bei denen eine teilweise
Magenentfernung
durchgefuhrt wurde, haben auch ein erhohtes Risiko zu erkranken. Dies wird auf den Fluss basischer Gallenflussigkeit und Dunndarmsekret zuruckgefuhrt.
Adenome
des Magens sind auch als Vorlaufer von Magenkrebs anzusehen. Bei 40 % der entfernten Adenome findet sich ein Karzinom. Außerdem hat rund ein Drittel der Patienten mit Adenomen ein Karzinom an einer anderen Stelle des Magens.
[1]
Das
Menetrier-Syndrom
, bei dem Schleimhaut des Magens generell verdickt ist, wird als
Krebsvorstufe
des Magens angesehen.
[7]
Auch genetische Risikofaktoren fordern die Entstehung von Magenkrebs. So haben Patienten mit
Blutgruppe
A ein erhohtes Risiko zu erkranken. Ebenso kommt es im Rahmen des autosomal-dominant erblichen Tumorsyndroms
HNPCC
gehauft zu Magenkrebsfallen.
[8]
Falle von Magenkrebs in der Familie erhohen generell das individuelle Risiko des Patienten, selbst an Magenkrebs zu erkranken. Außerdem gibt es ein familiares Magenkarzinomsyndrom, das auf einer Mutation von
Cadherin
beruht.
[1]
Chronische Magengeschwure entarten nur selten maligne (in bis zu 3 % der Falle), hinter einem chronischen, nicht abheilenden Magengeschwur kann sich allerdings auch ein unerkannter Magenkrebs verbergen.
Ein hoher Obst- und Gemuseverzehr konnte vor
Lungenkrebs
und Krebs des oberen
Verdauungstraktes
(u. a.
Magen
) schutzen. Vor allem Manner mit ursprunglich geringerem Konsum profitierten in der EPIC-EURGAST-Studie (2006) von einer Erhohung auf 300 g Obst und Gemuse am Tag. Ein Zusammenhang mit anderen Krebsentitaten ist nicht belegt. Je hoher der
Vitamin-C
-Spiegel im Blut war, desto geringer das Magenkrebsrisiko. Dies galt vor allem bei hohem Fleisch- und Wurstkonsum.
[9]
Die Diagnose des Magenkarzinoms wird dadurch erschwert, dass Karzinome, die noch klein sind und operativ vollkommen entfernt werden konnten, in der Regel keinerlei Symptome verursachen. Erst spat zeigen sich fur den Patienten Symptome wie ein Vollegefuhl im Oberbauch, das bei weiterem Wachstum in dauerhafte Schmerzen ubergehen kann. Appetitlosigkeit, oft zusammen mit Ubelkeit und Brechreiz, ist ein haufiges Spatsymptom, fuhrt aber selten zur Vorstellung beim Arzt. Schluckstorungen sind ein Symptom fortgeschrittener Tumoren am Mageneingang. Brechreiz und Ubelkeit werden eher bei Tumoren des Magenausgangs beobachtet.
[7]
Seltene mit einem Magenkarzinom vergesellschaftete Symptome sind
Thrombosen oberflachlicher Venen
,
hamolytische
Anamien
mit
Mikroangiopathie
und
Acanthosis nigricans
.
[7]
Teilweise werden Metastasen im
Eierstock
, auch
Krukenberg-Tumor
genannt, vor dem eigentlichen Magentumor entdeckt.
 Histologisches Praparat
eines gering differenzierten Adenokarzinomes des Magens.
Histologisches Praparat
eines gering differenzierten Adenokarzinomes des Magens.
Bei der korperlichen Untersuchung des Patienten ist insbesondere auf vergroßerte Lymphknoten oberhalb des linken
Schlusselbeins
zu achten (
Virchow-Lymphknoten
). Seltenere Orte einer lymphogenen Metastasierung sind die Region um den Bauchnabel und die linke Achselhohle. Ebenso ist auf Zeichen von
Aszites
zu achten; - dies ist ein Zeichen von Tumoraussaat in das
Bauchfell
. Außerdem sollte eine Tastuntersuchung der Leber durchgefuhrt werden, da dies den haufigsten Absiedlungsweg von Magenkarzinomen darstellt. Eine Vergroßerung kann einen Hinweis darauf geben.
[10]
Die gebrauchlichste Methode zur Diagnose eines Magenkarzinoms ist die
Magenspiegelung
. Im Rahmen dieser Untersuchung sind
Gewebeproben
zu entnehmen, da nur eine
histologische
Untersuchung Art und Dignitat des Tumors sicher feststellen kann. Um diese Methode zu verbessern, wurden mehrere Farbstoffe entwickelt, die auf die Magenschleimhaut aufgetragen werden konnen. Der Farbstoff Methylenblau wird von Oberflachenzellen des Darmes aufgenommen. Der Nachweis von Darmschleimhaut im Magen oder der Speiserohre ist ein Hinweis auf einen bosartigen Prozess oder eine Vorstufe dessen. Die Farbstoffe Indigokarmin und Kresylviolett verstarken den Kontrast des Schleimhautreliefs und lassen so Unregelmaßigkeiten leichter erkennen. Des Weiteren ist mittlerweile die Zoomendoskopie verfugbar, bei der die Schleimhaut unter 15 bis 150-facher Vergroßerung beurteilt werden kann. Eine weitere Technik ist das Narrow-Band-Imaging. Dabei wird durch einen Filter der Blauanteil des Lichts erhoht, so dass auch Unregelmaßigkeiten in der Schleimhaut besser gesehen werden konnen.
[10]
Bei vorhandenem Tumor muss dessen Ausbreitung festgestellt werden (
Staging
). Ein Mittel des Stagings ist die
Endosonographie
. Hierbei wird wie bei einer Magenspiegelung ein Endoskop in den Magen eingefuhrt. Aus dem Magen heraus wird mit Hilfe eines Ultraschallkopfs das umliegende Gewebe beurteilt. Eine weitere Untersuchung zur Suche von Tumorabsiedlungen ist eine Ultraschalluntersuchung des Bauch- und Beckenraumes. Die
Computertomographie
bietet eine weitere Moglichkeit, nach Metastasen zu suchen; - allerdings erfasst sie keine Absiedlungen, die kleiner als funf Millimeter sind. In 20 bis 30 % der CT-Untersuchungen zeigt sich ein unauffalliges Bild, obwohl Absiedlungen ins Bauchfell vorliegen. Zur Diagnose dieser Metastasen ist die
Laparoskopie
die
sensitivste
Methode. Allerdings birgt sie als operativer Eingriff Risiken fur den Patienten. In 3?5 % treten Komplikationen auf. In rund 0,1 % der Untersuchungen verstirbt der Patient an den Folgen des Eingriffs.
[10]
Tumormarker
weisen bei der Diagnostik des Magenkarzinoms eine Sensitivitat von 9 bis 30 % auf und stellen somit keine sinnvolle Maßnahme zur Entdeckung des Tumors dar.
[10]
Die Mehrheit der Karzinome zeigt unter dem
Mikroskop
Siegelringzellen
. In den Zellen ist der
Zellkern
an den Rand gedrangt, und sie reagieren stark mit der PAS-Farbung. Seltener treten Karzinome auf, die den Drusen des Darmes ahneln. Es sind auch Gallertkarzinome beschrieben, bei denen außerhalb der Krebszellen Massen von PAS-positivem Schleim liegen, sowie entdifferenzierte Karzinome, deren Herkunft sich nur durch
immunhistochemische
Methoden klaren lasst. Neben diesen Tumoren, die vom
Epithel
des Magens ausgehen, sind auch
neuroendokrine Tumoren
beschrieben.
[11]
Man unterscheidet je nach der Form des Tumorwachstums vier Typen von
Adenokarzinomen
des Magens. Das polypoide Adenokarzinom wachst wie ein
Polyp
von der Mageninnenseite in das Magen
lumen
ein. Das ulzerierende Adenokarzinom zeichnet sich durch die Bildung einer Schleimhautschadigung im Sinne eines Geschwurs aus. Gegenuber gutartigen Magengeschwuren zeigt das Karzinom unregelmaßigere Rander. Beide Typen machen je ein Drittel der Magenkarzinome aus. Rund ein Zehntel aller Magenkarzinome sind vom diffusen Typ. Diese Tumoren wachsen nicht in das Lumen ein, sondern infiltrieren das Gewebe des Magens. Die Tumorzellen induzieren eine
Fibrose
in der Schleimhaut- und der Muskelschicht des Magens, was zu einer Wandverdickung fuhrt. Der diffuse Typ ist mit einer besonders schlechten Prognose assoziiert. Als Fruhkarzinom des Magens bezeichnet man einen Tumor, der auf die Schleimhaut oder die
Submukosa
beschrankt bleibt. Obwohl rund 20 % der Fruhkarzinome bei Diagnosestellung bereits metastasiert haben, besitzen sie im Vergleich zu den anderen Arten eine relativ gute Prognose.
[12]
Viel seltener als Adenokarzinome sind adenosquamose Karzinome,
Plattenepithelkarzinome
und undifferenzierte Karzinome.
Molekularbiologische Befunde werden fur die Einschatzung der Prognose und fur die Wahl der Therapie immer wichtiger. 2014 wurde auf Basis genetischer Untersuchungen eine Klassifikation in vier Typen vorgeschlagen:
- EBV
-positive Tumoren
- MSI
-Tumoren
- genomisch ? stabile Tumoren
- Chromosomen ? instabile Tumoren
[13]
Aus dem TCGA-Projekt (The Cancer Genome Atlas) standen genetische und molekularbiologische Analysen von 295 Adenokarzinomen des Magens zur Verfugung. Die Gewebeproben der Tumoren wurden mit 6 verschiedenen molekularen Plattformen untersucht:
- array-based somatic copy number analysis: Verfahren zur Bestimmung der Anzahl somatischer DNA ? Kopien
- whole-exome sequencing:
Sequenzierung der DNA
- array-based DNA methylation profiling: Analyse der
DNA-Hypermethylierung
- messenger RNA sequencing: Sequenzierung der
mRNA
- microRNA (miRNA) sequencing: Sequenzierung der
microRNA
- reverse-phase protein array (RPPA): Analyse der gebildeten
Proteine
Das
Epstein-Barr-Virus
konnte in 9 % der Falle aufgespurt werden. EBV-positive Tumoren hatten haufig eine extrem starke DNA-Hypermethylierung. Sie wiesen oft eine PIK3CA-Mutation auf und amplifizierten
JAK
2,
PD-L1
und PD-L2, d. h. diese Proteine wurden uber-normal stark gebildet. Diese Tumoren waren potentielle Kandidaten fur eine Immuntherapie mit
PD-L1-Inhibitoren
. Bisher sind sie fur das Magenkarzinom allerdings noch nicht zugelassen. Klinische Studien brachten bisher keinen Erfolg.
[14]
64 Tumoren wiesen eine sehr starke Mutationsrate auf. Es kommt zur Mikrosatelliten-Bildung. Die Abkurzung MSI steht fur ?MikroSatellit Instabil“. Das Mismatch-Reparatur-Protein MLH1 wird haufig nicht exprimiert, wodurch bestimmte DNA-Schaden nicht erfolgreich repariert werden konnen. Das fuhrt zur Ausbildung zahlreicher Mutationen, die eventuell Ziel fur eine Target-Therapie werden konnten. Durch eine Hypermethylierung des MLH1-
Promotors
wird die Produktion dieses DNA-Reparaturmolekuls abgeschaltet.
Die verbliebenen Tumoren wurden nach dem Vorhandensein oder Fehlen extensiver somatischer Aberrationen der Kopienzahl(engl. somatic copy-number aberrations = SCNA), d. h. der Veranderung der Genaktivitat in genomisch-stabile und chromosomeninstabile unterteilt. 58 Tumoren zeigten ein stabiles Genomen mit wenig Mutationen. Histologisch waren es haufig diffus wachsenden Magenkarzinome. Gene von Proteinen fur die Zellmigration waren haufig aktiviert. Besonders haufig waren Mutationen von CDH1 und RHOA. Ferner wurde eine Fusion von CLDN18- und ARHGAP-Genen nachgewiesen.
Die ubrigen 147 Tumoren gehorten der verbleibenden chromosomeninstabilen Gruppe (CIN) mit vielen Mutationen an. Histologisch waren sie meistens intestinal differenziert. Besonders haufig war eine Mutation von TP53 anzutreffen, welches das Protein
p53
kodiert. Ferner fand sich eine Aktivierung von RTK-
RAS
.
Die
TNM-Klassifikation
dient der Stadieneinteilung der Tumorausbreitung (sogenanntes Staging). TNM ist eine Abkurzung fur
- T = Tumor: Ausdehnung des Primartumors
- N = Nodus: Lymphknoten, Fehlen oder Vorhandensein von regionaren
Lymphknotenmetastasen
- M = Metastasen: Fehlen oder Vorhandensein von Fernmetastasen
Derzeit gultig ist die 7. Auflage der Kriterien nach
AJCC staging system
(American Joint Committee on Cancer).
[15]
TNM-Klassifikation
| TX
|
Primartumor kann nicht bestimmt werden.
|
| T0
|
Keine Evidenz fur einen Primartumor
|
| Tis
|
Carcinoma in situ: Intraepithelialer Tumor ohne Invasion der Lamina propria
|
| T1
|
Infiltration der
Lamina propria
oder der
Tela submucosa
(Synonym:
Fruhkarzinom
)
|
| T1a
|
Infiltration der
Lamina propria
oder
Lamina muscularis mucosae
|
| T1b
|
Infiltration der
Tela submucosa
|
| T2
|
Infiltration der
Tunica muscularis
|
| T3
|
Infiltration des subserosen Bindegewebes ohne Invasion des visceralen Peritoneums oder benachbarter Strukturen. T3 schließt auch Tumoren ein, welche sich entlang des gastrocolischen oder gastrohepatischen Ligaments ausbreiten, sowie das Omentum majus oder minus erreichen, ohne Durchdringung des visceralen Peritonuems, welche diese Strukturen umgibt.
|
| T4
|
Infiltration von Nachbarorganen (
Milz
,
Colon
transversum,
Leber
,
Zwerchfell
,
Pancreas
,
Bauchwand
,
Nebenniere
,
Niere
,
Dunndarm
oder
Retroperitoneum
)
|
| T4a
|
Infiltration der Serosa (viszerales Peritoneum)
|
| T4b
|
Infiltration von Nachbarorganen (Milz, Colon transversum, Leber, Zwerchfell, Pancreas, Bauchwand, Nebenniere, Niere, Dunndarm oder Retroperitoneum)
|
| NX
|
Befall lokaler Lymphknoten nicht beurteilbar
|
| N0
|
Keine lokalen Lymphknoten befallen
|
| N1
|
Metastasen in ein bis zwei lokalen Lymphknoten
|
| N2
|
Metastasen in drei bis sechs lokalen Lymphknoten
|
| N3
|
Metastasen in sieben oder mehr lokalen Lymphknoten
|
| M0
|
Keine Fernmetastasen nachgewiesen
|
| M1
|
Fernmetastasen
|
Ubersicht zur Therapie des Magenkarzinoms
(Details dazu im Text)
| TNM-Stadium
|
Therapie
|
uT1aN0M0*
(Mucosakarzinom, Magenfruhkarzinom)
|
Endoskopische Resektion (EMR, ESD)
|
| alle Stadien ≥ uT1b* (operabel)
|
Operation (komplette oder Teil-Gastrektomie
mit D2-Lymphadenektomie)
|
| Stadien uT3 und uT4* (operabel)
|
zusatzlich vorgeschaltet zur o. g. Operation:
Neoadjuvante Chemotherapie mit Cisplatin
und Fluorouracil (bzw. Oxaliplatin, Capecitabin);
Stellenwert der adjuvanten (Radio-)Chemotherapie
ist umstritten, wird bisher nicht empfohlen
|
| lokal inoperabel oder metastasiert (M1)
|
Palliative Chemotherapie auf Basis der o. g. Substanzen,
bei HER2-Positivitat moglichst mit Trastuzumab
|
| *
der Buchstabe 'u' bei der TNM-Formel steht fur durch
U
ltraschall, d. h. endosonografisch gewonnene Befunde
|
Die wichtigste Behandlungsmaßnahme ist seit dem Ende des 19. Jahrhunderts
[16]
die operative Entfernung des Tumors, moglichst vollstandig, mit einem Sicherheitsabstand von 5 cm beim intestinalen Typ bzw. 8 cm beim diffusen Typ. Daraus ergibt sich je nach Lokalisation eine teilweise (4/5) oder vollstandige
Magenentfernung
, evtl. unter Mitnahme von Teilen der
Speiserohre
oder des
Zwolffingerdarmes
. Eine 4/5 Resektion nach Billroth ist ausschließlich beim intestinalen Typ in Verbindung mit einer Lokalisation im untersten Teil des Magens, dem Antrum, moglich. In allen anderen Fallen muss bei Aussicht auf Heilung eine Gastrektomie mit einer nach Y-Roux ausgeschalteten Jejunalschlinge erfolgen. Die umgebenden
Lymphknoten
werden mitentfernt, bei Infiltration auch die
Milz
oder Teile der
Leber
. Anschließend wird das verbleibende Magen- oder Speiserohrenende wieder mit dem Zwolffingerdarm verbunden (Operationstechnik nach
Billroth
I oder II).
Falls ein Magenkarzinom nur auf die Schleimhaut begrenzt ist (?Mukosakarzinom“ im Stadium T1aN0M0, dies lasst sich mit hoher Sicherheit durch die endosonografische Untersuchung feststellen) besteht die Therapie aus einer lokalen endoskopischen Abtragung. Zwei verschiedene Techniken finden hier Anwendung: die
endoskopische Mukosaresektion
(EMR), bei der die Lasion zunachst mit steriler Kochsalzlosung unterspritzt und anschließend mit einer Schlinge abgetragen wird, oder die
endoskopische submukosale Dissektion
(ESD), bei der die Lasion mikrochirurgisch abgetragen wird. Letztere hat den Vorteil, dass die Lasion en bloc abgetragen werden kann, was die spatere histopathologische Beurteilung erleichtert. Allerdings ist die ESD wohl auch mit etwas hoheren Komplikationsraten verbunden.
[17]
In den operablen Stadien T1b, T2, T3, T4 ist eine endoskopische Abtragung nicht mehr moglich oder sinnvoll. Stattdessen soll eine Operation (komplette oder partielle
Gastrektomie
[18]
) mit sogenannter Lymphknotendissektion (Mitentfernung der ableitenden Lymphwege mit Lymphstationen) erfolgen.
Bei den operablen Magenkarzinomen im Stadium T3 oder T4 empfehlen die deutschen Leitlinien grundsatzlich die Durchfuhrung einer
neoadjuvanten
Chemotherapie, d. h. einer Chemotherapie vor der Operation um den Tumor zu verkleinern und damit das Operationsergebnis zu verbessern. Zwei große Therapiestudien haben einen Uberlebensvorteil fur derartig behandelten im Vergleich zu chemotherapeutisch unbehandelten Patienten gezeigt, zum einen die britische MAGIC-Studie, bei der Patienten mit einer Kombination aus Epirubicin, Cisplatin und Fluorouracil (?ECF“) behandelt wurden,
[19]
zum anderen die franzosische FNCLCC/FFCD-Studie, bei der die Patienten Cisplatin und Fluorouracil erhielten.
[20]
Statt Fluorouracil und Cisplatin werden wegen besserer Vertraglichkeit heute vielfach
Capecitabin
und
Oxaliplatin
genommen. Eine weitere vielversprechende Kombination ist
Docetaxel
? Oxaliplatin ? Fluorouracil.
[17]
Der Stellenwert einer
adjuvanten
Chemotherapie oder Radiochemotherapie (d. h. Chemotherapie evtl. kombiniert mit
Strahlentherapie
nach der erfolgten Operation) wird zurzeit noch unterschiedlich beurteilt. Nach deutschen Leitlinien (Stand 15. Dezember 2012)
[21]
wird im Allgemeinen
keine
adjuvante Therapie empfohlen. Einzige Ausnahme bildet die Situation, wenn der Tumor nicht komplett operativ entfernt werden konnte. In asiatischen Landern wird das anders beurteilt und gehandhabt und eine adjuvante Therapie vielfach durchgefuhrt, z. B. mit Capecitabin und Oxaliplatin.
[17]
Falls der Tumor primar inoperabel ist (z. B. weil er in der Nahe großer Blutgefaße liegt, ?lokal fortgeschrittenes Karzinom“) oder mehrere Fernmetastasen zeigt, ist in der Regel keine Heilung mehr moglich. Die Therapie erfolgt dann nicht mehr mit kurativer (?heilender“), sondern mit palliativer (?lindernder“) Zielsetzung. Mit den o. g. Chemotherapeutika lasst sich in den meisten Fallen eine Beschwerdelinderung und Verlangerung der Uberlebenszeit erreichen. Falls der Tumor histopathologisch
HER2
-positiv ist, sollte wenn moglich
Trastuzumab
(Herceptin®) zum Einsatz kommen.
[22]
Nach einer Voll- oder Teilentfernung des Magens kann es bei den Patienten zu verschiedenen Storungen kommen, welche eigene Maßnahmen zur Erhohung der Lebensqualitat des Patienten nach der Operation benotigen. So fuhrt das totale oder teilweise Entfernen des Magens zu einer schnelleren Passage der Nahrung in den Dunndarm. Dadurch kann ein
Dumping-Syndrom
entstehen, welches beim Patienten zu einer
osmotischen
Schwellung des Dunndarms und vasomotorischen Storungen mit Blutdruckabfall bis zur
Synkope
direkt nach der Nahrungsaufnahme fuhren kann. Dies wird als Fruhdumping bezeichnet. Die andere Seite des Krankheitsbilds, das sogenannte Spatdumping, beruht darauf, dass leicht verdauliche
kohlenhydratreiche
Nahrung zu schnell resorbiert wird. Dies fuhrt zu einem
zu hohen Blutzucker
, den der Korper durch eine uberschießende Ausschuttung von
Insulin
zu beherrschen versucht. Da aber meist zu viel Insulin ausgeschuttet wird, kommt es einige Stunden nach der Nahrung zur
Unterzuckerung
, was fur den Patienten sehr belastend ist. Das Dumpingsyndrom kann durch
diatetische
Maßnahmen wie kleinere, aber haufigere Mahlzeiten, das Vermeiden von Flussigkeitsaufnahme mit dem Essen oder Liegen nach den Mahlzeiten gebessert werden.
[23]
Nach einer teilweisen Magenentfernung kann sich eine
Refluxosophagitis
ausbilden, wenn
proximale
Teile des Magens entfernt wurden. Ebenso kann basisches Duodenalsekret in den Restmagen oder die Speiserohre gelangen und dort Schmerzen, Ubelkeit oder eine chronische Entzundung auslosen. Diese Probleme konnen durch Hochlagern des Bettkopfendes oder auch durch medikamentose Behandlung behoben werden.
[23]
Auch die Fettverdauung kann den Patienten Probleme bereiten, da die Nahrung nicht mehr im Magen gespeichert werden kann und somit die Zeit sinkt, welche die
Bauchspeicheldruse
fur die Sekretion von Fett verdauenden
Enzymen
hat. Als Therapie kann der Fettanteil der Nahrung reduziert werden; auch konnen die Enzyme exogen zugefuhrt werden. Bei vielen Patienten treten
Malassimilationssyndrome
auf, bei denen Nahrungsmittelbestandteile nicht in ausreichendem Umfang verdaut oder resorbiert werden konnen. Deshalb ist der Patient auf eine ausreichende Zufuhr von
Nahrungsenergie
und eine ausreichende Zufuhr von Vitaminen und Mineralstoffen hinzuweisen und entsprechend zu schulen. Ebenso entwickeln fast alle Patienten mit einer vollstandigen Magenentfernung einen Mangel an
Vitamin B12
. Dieser verursacht mit einer Latenz von drei bis funf Jahren eine
Anamie
. Infolgedessen ist bei jedem Patienten eine Substitution des Vitamins indiziert. Ebenso treten bei Patienten nach der Operation Storungen des Knochenstoffwechsels auf, die
Osteoporose
sehr stark begunstigen. Einerseits wird dies auf verminderte
Kalziumaufnahme
zuruckgefuhrt, da die meisten Patienten nach der Operation keine Milchprodukte mehr vertragen. Andererseits findet sich haufig ein
Vitamin-D-Mangel
. Kalzium und Vitamin D konnen exogen zugefuhrt werden. Daruber hinaus stellen die Krebserkrankung und der operative Eingriff fur die Patienten in der Regel eine starke psychische Belastung dar. Die Fahigkeit des Patienten, mit seiner Erkrankung umzugehen, sollte infolgedessen wenn notig durch psychologische Betreuung unterstutzt werden.
[23]
Es konnte bisher nicht gezeigt werden, dass Nachsorgeuntersuchungen zu einer Fruherkennung von Rezidiven und damit zu einem besseren Uberleben fuhren. Deswegen sind die Empfehlungen zur spezifischen Nachsorge in den aktuellen Leitlinien zuruckhaltend.
[21]
Es werden dort keine routinemaßigen diagnostischen Untersuchungen wie z. B. Magenspiegelung, Sonografie, Thorax-Rontgen oder Computertomographie empfohlen. Etwas anderes ist es naturlich, wenn der in Nachsorge befindliche Patient spezifische Beschwerden hat, die durch ein Rezidiv verursacht sein konnten. Hier muss dann naturlich entsprechende Diagnostik durchgefuhrt werden, wobei allerdings die Prognose von Patienten mit einem symptomatischen (= Beschwerden verursachenden) Rezidiv als generell schlecht gilt.
[17]
Da das Ernahrungsprofil viele Risikofaktoren abdeckt, andererseits auch die protektive Wirkung von Obst und Gemuse bekannt ist, sollten ungesunde Essgewohnheiten grundsatzlich umgestellt werden. Vor allem haufiger Verzehr von Fleisch und gepokelter Nahrung sollte reduziert werden. Raucherentwohnung ist der Gesundheit prinzipiell zutraglich.
Bei nachgewiesenem Befall mit
Helicobacter pylori
ist deren
Eradikation
(medikamentose Beseitigung) anzustreben. Sollte Magenkrebs in der Familie verbreitet sein oder eine chronische Gastritis vorliegen, empfiehlt sich eine regelmaßige Magenspiegelung.
Beim
Deutschen Krebsforschungszentrum
geht man davon aus, dass der registrierte Ruckgang (zwischen 1977 und 1997 um rund ein Viertel) der Magenkrebserkrankungen auf die massenhafte Verbreitung von Kuhlschranken und die ganzjahrige Bereitstellung von frischem Obst und Gemuse und einem damit verbundenen Ruckgang der Konservierung mittels
Pokeln
und
Rauchern
zuruckzufuhren ist.
Je fruher der Magentumor erkannt wird, desto erfolgreicher kann er behandelt werden.
Da Magenkrebs in der Regel erst in weit fortgeschrittenen Stadien diagnostiziert wird (70 % aller Falle werden in Tumorstadien III und IV erkannt), ist die Sterberate insgesamt relativ hoch. Bei fruhzeitiger Erkennung (Stadium I) betragt die 5-Jahresuberlebensrate 65 bis 80 %, bei fortgeschrittenen Krebsstadien sinkt sie dramatisch. Fur den westeuropaischen Raum betragen die 5-Jahresuberlebensraten nach Sammelstatistiken 65 % im Stadium I, 22 % im Stadium II und 5 % im Stadium III. Im Tumorstadium IV ist eine 5-Jahres-Uberlebenszeit nicht zu erwarten.
[24]
Sollte man die ersten funf Jahre uberleben, besteht eine 50- bis 90-prozentige Chance auf dauerhafte Heilung.
- Die Blauen Ratgeber
.
Nr. 7: Magenkrebs, Deutsche Krebshilfe und
Deutsche Krebsgesellschaft
, Januar 2014.
- M. Moehler, S.-E. Al-Batran u. a.:
S3-Leitlinie Magenkarzinom
In:
Zeitschrift fur Gastroenterologie.
49, 2011, S. 461?531,
doi:10.1055/s-0031-1273201
.
- S3-
Leitlinie
Magenkarzinom ? Diagnostik und Therapie der Adenokarzinome des Magens und osophagogastralen Ubergangs
der Deutschen Gesellschaft fur Verdauungs- und Stoffwechselkrankheiten (DGVS) und der Deutschen Krebsgesellschaft (DKG). In:
AWMF online
- Hans-Joachim Meyer, Hansjochen Wilke:
Behandlungsstrategien beim Magenkarzinom
. In:
Dtsch Arztebl Int
.
Nr.
108(41)
, 2011,
S.
698?706
(
Ubersichtsarbeit
).
- M. Tomoda, T. J. Kejiri:
Fruhdiagnose und Therapie des Magenkrebses.
In:
Der Chirurg.
Band 33, 1962, S. 495 ff.
- ↑
a
b
c
d
e
Chen Liu, James Crawford:
The Gastrointestinal Tract.
In: Vinag Kumar, Abul Abbas, Nelson Fausto (Hrsg.):
Pathologic Basis of Disease.
7. Auflage. Philadelphia 2005, S. 823?826.
- ↑
C. Thomas:
Histopathologie.
Stuttgart, 2006, S. 139.
- ↑
Deutsche Krebshilfe
, aktuelle Statistik 2013.
- ↑
J. M. Noto, J. A. Gaddy u. a.:
Iron deficiency accelerates Helicobacter pylori-induced carcinogenesis in rodents and humans.
In:
The Journal of clinical investigation.
Band 123, Nummer 1, Januar 2013, S. 479?492,
ISSN
1558-8238
.
doi:10.1172/JCI64373
.
PMID 23257361
.
PMC 3533289
(freier Volltext).
- ↑
Ke Ma, Zulqarnain Baloch, Ting-Ting He, Xueshan Xia:
Alcohol Consumption and Gastric Cancer Risk: A Meta-Analysis
. In:
Medical Science Monitor : International Medical Journal of Experimental and Clinical Research
.
Band
23
, 14. Januar 2017,
ISSN
1234-1010
,
S.
238?246
,
doi
:
10.12659/MSM.899423
,
PMID 28087989
,
PMC 5256369
(freier Volltext).
- ↑
Risks and causes of stomach cancer | Cancer Research UK.
Abgerufen am 12. Marz 2022
.
- ↑
a
b
c
Robert Mayer:
Gastrointestinal Tract Cancer.
In: Anthony Fauci u. a. (Hrsg.):
Harrison’s Principles of Internal Medicine.
Band 1, New York 2008, S. 571?573.
- ↑
Frank Mitros, Emanuel Rubin:
The Gastrointestinal Tract.
In: Raphael Rubin, David Strayer u. a. (Hrsg.):
Rubin’s Pathology.
5. Auflage. Philadelphia 2008, S. 569.
- ↑
Abgewandelt zitiert nach:
Was schutzt vor Krebs und Diabetes?
In:
MMW-Fortschr. Med.
Nr. 24 / 2007 (149. Jg.), S. 16, dort zitiert nach
EPIC-Symposium
, Berlin, 25. April 2007.
- ↑
a
b
c
d
Ch. Englisch-Fritz u. a.:
Diagnostik beim Magenkarzinom.
In:
Der Onkologe.
14, 2008, S. 332?338.
- ↑
C. Thomas:
Histopathologie.
Stuttgart 2006, S. 139.
- ↑
Frank Mitros, Emanuel Rubin:
The Gastrointestinal Tract.
In: Raphael Rubin, David Strayer u. a. (Hrsg.):
Rubin’s Pathology.
5. Auflage. Philadelphia 2008, S. 571.
- ↑
The Cancer Genome Atlas Research Group:
Comprehensive molecular characterization of gastric adenocarcinoma.
In:
Nature
2014; Band 513: S. 202?209
doi:10.1038/nature13480
- ↑
Julia Borsch:
Hoffnungstrager Avelumab erreicht Endpunkt nicht.
In:
deutsche-apotheker-zeitung.de.
29. November 2017,
abgerufen am 26. Juni 2019
.
- ↑
K. Washington:
7th edition of the AJCC cancer staging manual: stomach.
In:
Ann Surg Oncol
.
17, 2010, S. 3077?3079.
- ↑
Vgl. etwa
Johann von Mikulicz
:
Beitrage zur Technik der Operation des Magenkarzinoms.
In:
Verhandlungen der Deutschen Gesellschaft fur Chirurgie.
27. Kongress, 1898, S. 252 ff.
- ↑
a
b
c
d
G. Woeste,
Salah-Eddin Al-Batran
, J. Albert, J. Trojan:
Diagnostik und Therapie des Magenkarzinoms.
In:
Onkologe.
2014; 20, S. 1139?1152.
doi:10.1007/s00761-014-2792-1
- ↑
Vgl. etwa Rudolf Haring, H. Franke:
Gastrektomie und Kardiaresektion beim Magenkarzinom.
Thieme, Stuttgart 1970.
- ↑
D. Cunningham, W. H. Allum, S. P. Stenning, J. N. Thompson, C. J. Van de Velde, M. Nicolson, J. H. Scarffe, F. J. Lofts, S. J. Falk, T. J. Iveson, D. B. Smith, R. E. Langley, M. Verma, S. Weeden, Y. J. Chua, MAGIC Trial Participants:
Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer.
In:
N Engl J Med.
2006;355(1), S. 11?20.
PMID 16822992
.
doi:10.1056/NEJMoa055531
- ↑
M. Ychou, V. Boige, J. P. Pignon, T. Conroy, O. Bouche, G. Lebreton, M. Ducourtieux, L. Bedenne, J. M. Fabre, B. Saint-Aubert, J. Geneve, P. Lasser, P. Rougier:
Perioperative chemotherapy compared with surgery alone for resectable gastroesophageal adenocarcinoma: an FNCLCC and FFCD multicenter phase III trial.
In:
J Clin Oncol.
2011;29(13), S. 1715?1721.
PMID 21444866
.
doi:10.1200/JCO.2010.33.0597
- ↑
a
b
Magenkarzinom - Diagnostik und Therapie der Adenokarzinome des Magens und osophagogastralen Ubergangs.
AWMF online,
abgerufen am 8. Dezember 2014
(Stand der Leitlinie:15. Dezember 2012, zum Zeitpunkt des Abrufs Gultigkeit bis zum 31. Dezember 2015).
- ↑
Y. J. Bang, E. Van-Cutsem, A. Feyereislova, H. C. Chung, L. Shen, A. Sawaki, F. Lordick, A. Ohtsu, Y. Omuro, T. Satoh, G. Aprile, E. Kulikov, J. Hill, M. Lehle, J. Ruschoff, Y. K. Kang; ToGA Trial Investigators:
Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial.
In:
Lancet.
2010;376(9742), S. 687?697.
PMID 20728210
.
doi:10.1016/S0140-6736(10)61121-X
.
- ↑
a
b
c
H. Delbruck, H. Wilke:
Rehabilitation von Patienten mit Magenkarzinomen.
In:
Der Onkologe.
6, 2000, S. 6?13.
- ↑
Leitlinie Magenkarzinom
(
Memento
vom 13. Juli 2015 im
Internet Archive
) (PDF)
Dieser Artikel behandelt ein Gesundheitsthema. Er dient
nicht
der Selbstdiagnose und ersetzt
nicht
eine Diagnose durch einen Arzt. Bitte hierzu den
Hinweis zu Gesundheitsthemen
beachten!
Onkologische
Krankheiten, topographisch nach
ICD-O-3
Nr. C00?C80,
Quelle:
[1]
mit morphologischen Eintragen erganzt