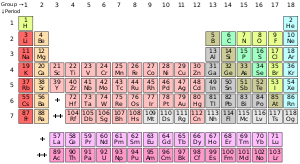
 Tabelul periodic al elementelor chimice
Tabelul periodic al elementelor chimice
Prin no?iunea de
element chimic
se in?elege o specie de
atomi
identici, adic? de atomi avand acela?i num?r de
protoni
in nucleul atomului, respectiv un num?r identic de
electroni
in
inveli?ul electronic
al atomului. Defini?ia nu se refer? la num?rul de
neutroni
din nucleu, ceea ce inseamn? c? no?iunea de
element chimic
include to?i
izotopii
acelui element chimic.
Savantul rus
Dimitri I. Mendeleev
a descoperit
legea periodicit??ii elementelor chimice
?i a conceput o reprezentare grafic? a interdependen?ei sofisticate a tuturor speciilor unice de atomi,
tabelul periodic al elementelor
.
Sunt identificate 118
elemente
, dintre care primele 94 apar natural pe
P?mant
, restul fiind elemente sintetice.
[1]
Exist? 80 de elemente care au cel pu?in un
izotop
stabil ?i 38 care au exclusiv
radionuclizi
, care se descompun in timp in alte elemente.
Fierul
este cel mai abundent element (ca mas?) care formeaz? P?mantul, in timp ce
oxigenul
este cel mai frecvent element din crusta P?mantului.
Elementele chimice constituie toat? materia obi?nuit? a
universului
. Cu toate acestea, observa?iile astronomice sugereaz? c? materia observabil? obi?nuit? reprezint? doar aproximativ 15% din materia din univers: restul este
materia intunecat?
; compozi?ia acestei materii este necunoscut?, dar nu este compus? din elemente chimice. Cele dou? elemente mai u?oare,
hidrogen
?i
heliu
, au fost formate in cea mai mare parte in
Big Bang
?i sunt cele mai comune elemente din univers. Urm?toarele trei elemente (
litiu
,
beriliu
?i
bor
) au fost formate in mare parte prin spalarea cu
radia?ie cosmic?
(
nucleosintez?
) ?i, prin urmare, sunt mai rare decat elementele mai grele. Formarea elementelor de la 6 pan? la 26 de
protoni
a ap?rut ?i continu? s? apar? in stelele secven?ei principale prin nucleosintez? stelar?. Abunden?a mare de
oxigen
,
siliciu
?i
fier
pe P?mant reflect? produc?ia lor obi?nuit? in astfel de
stele
. Elementele cu mai mult de 26 de protoni se formeaz? prin nucleosinteza in
supernove
, care, atunci cand explodeaz?, arunc? aceste elemente ca r?m??i?e departe in spa?iu, unde pot ajunge incorporate in
planete
atunci cand sunt formate.
Termenul "
element
" este utilizat pentru
atomii
cu un num?r dat de
protoni
(indiferent dac? sunt sau nu
ioni
sau lega?i chimic, de exemplu,
hidrogenul
din
ap?
), precum ?i pentru o
substan?? chimic?
pur? care const? dintr-un singur element (de exemplu, hidrogen gazos). Pentru al doilea sens, au fost sugera?i termenii "substan?? elementar?" ?i "substan?? simpl?", dar nu s-au bucurat de mult? acceptare in literatura chimic? englez?, in timp ce in alte limbi echivalentul lor este utilizat pe scar? larg?. Un singur element poate forma mai multe substan?e care difer? in structura lor; ele sunt numite
alotropi
ai elementului.
[2]
Atunci cand diferite elemente sunt combinate chimic, cu atomii de?inu?i impreun? prin
leg?turi chimice
, ele formeaz? compu?i chimici. Numai o mic? parte a elementelor se g?se?te nemodificat? ca
minerale
relativ pure. Printre elementele native mai frecvente se num?r?
cuprul
,
argintul
,
aurul
,
carbonul
(sub form? de
c?rbune
,
grafit
sau
diamante
) ?i
sulful
. Toate, cu excep?ia catorva dintre cele mai inerte elemente, cum ar fi
gazele nobile
?i metalele nobile]], se g?sesc de obicei pe P?mant in form? combinat? chimic, ca ?i compu?i chimici. In timp ce aproximativ 32 de elemente chimice apar pe P?mant in forme necombinate native, cele mai multe dintre acestea apar ca amestecuri. De exemplu,
aerul
atmosferic este in primul rand un amestec de
azot
,
oxigen
?i
argon
, iar elementele solide native apar in
aliaje
, cum ar fi cele de
fier
?i
nichel
.
Istoria descoperirii ?i utiliz?rii elementelor a inceput cu societ??i primitive umane care au g?sit elemente native precum
carbon
,
sulf
,
cupru
?i
aur
. Civiliza?iile ulterioare au extras din
minereurile
lor, prin topire, cupru, staniu, plumb ?i fier, prin utilizarea
c?rbunelui
.
Alchimi?tii
?i chimi?tii au identificat ulterior mult mai multe; aproape toate elementele naturale au fost cunoscute pan? in 1900.
Propriet??ile elementelor chimice sunt rezumate in
tabelul periodic al elementelor
, care organizeaz? elementele prin cre?terea num?rului atomic pe randuri ("perioadele") in care coloanele ("grupurile") au propriet??i fizice ?i chimice recurente ("periodice"). Cu excep?ia elementelor radioactive instabile cu timpi de injum?t??ire scur?i, toate elementele sunt disponibile din punct de vedere industrial, majoritatea in grade sc?zute de impurit??i.
[2]
Conceptul de atom (in
greaca veche
a
tomos
, adic?
in
divizibil) poate fi intalnit in lucr?rile filosofilor greci antici
Leucip
?i
Democrit
. Din punct de vedere pur abstract, speculativ, f?r? ca ?tiin?a ?i tehnica timpului lor s? le fi oferit sprijin experimental, Leucip ?i Democrit ajung la concluzia
logic?
?i
filozofic?
c? exist? o limit? inferioar? de divizare a materiei, ?i anume, aceast? limit? se opre?te la o particul?, extrem de mic?, dar indivizibil?, pe care au numit-o atom.
Cele mai u?oare elemente chimice sunt
hidrogenul
?i
heliul
[1]
, ambele create de
nucleosinteza
Big Bang
in primele 20 de minute ale
universului
[3]
in intr-un raport de aproximativ 3: 1 in mas? (sau 12: 1 in num?r de
atomi
)
[4]
[5]
, impreun? cu urme minuscule ale urm?toarelor dou? elemente,
litiu
?i
beriliu
.
[6]
Aproape toate celelalte elemente g?site in natur? au fost create prin diferite metode naturale de
nucleosintez?
[7]
. Pe p?mant, cantit??i mici de atomi noi sunt produse in mod natural in reac?ii nucleogene sau in procese cosmogene, cum ar fi spalarea cu raze cosmice. Atomii noi sunt, de asemenea, produ?i natural pe P?mant ca
izotopi
radiogeni ai fiilor proceselor de
dezintegrare radioactiv?
in curs de desf??urare, cum ar fi
dezintegrarea alfa
,
dezintegrarea beta
,
fisiunea
spontan?, dezintegrarea clusterului ?i alte moduri mai rare de dezintegrare.
Dintre cele 94 de elemente naturale, cele cu numere atomice de la 1 la 82 au fiecare cel pu?in un izotop stabil (cu excep?ia
techne?iului
, elementul 43, ?i
prome?iu
, elementul 61, care nu au
izotopi
stabili). Izotopii considera?i stabili sunt aceia pentru care nu a fost inc? observat?
dezintegrarea radioactiv?
. Elementele cu numerele atomice de la 83 pan? la 94 sunt instabile pan? la punctul in care se poate detecta dezintegrarea radioactiv? a tuturor izotopilor. Unele dintre aceste elemente, in special
bismut
(num?r atomic 83),
toriu
(num?r atomic 90) ?i
uraniu
(num?r atomic 92), au unul sau mai mul?i izotopi cu jum?t??i de via?? suficient de lungi pentru a supravie?ui ca r?m??i?e ale nucleosintezei stelare explozive care au produse metale grele inainte de formarea
sistemului nostru solar
. Cu peste 1,9×10
19
ani, de peste un miliard de ori mai mare decat varsta estimat? a universului,
bismutul
-209 (num?rul atomic 83) are cel mai lung timp de injum?t??ire la
dezintegrarea alfa
fa?? de oricare element natural, ?i este aproape intotdeauna considerat la egalitate cu cele 80 de elemente stabile
[8]
[9]
. Elementele cele mai grele (cele dincolo de
plutoniu
, elementul 94) sufer? dezintegrare radioactiv?, cu jum?t??i de via?? atat de scurte incat nu se g?sesc in natur? ?i trebuie sintetizate.
Incepand cu anul 2010, exist? 118 elemente cunoscute
[10]
[11]
(in acest context, "cunoscut" inseamn? observat suficient de bine, chiar din doar cateva produse de dezintegrare, care au fost diferen?iate de alte elemente)
[12]
[13]
. Dintre aceste 118 elemente, 94 apar natural pe P?mant. ?ase dintre acestea apar in cantit??i extreme:
techne?iu
, num?r atomic 43;
prome?iu
, num?rul 61;
astatiniu
, num?rul 85;
franciu
, num?rul 87;
neptuniu
, num?rul 93; ?i
plutoniu
, num?rul 94. Aceste 94 de elemente au fost detectate in univers in general, in spectrul stelelor ?i supernovelor, unde sunt create elemente radioactive cu durat? scurt? de via??. Primele 94 de elemente au fost detectate direct pe P?mant ca
nuclizi
primordiali prezen?i din formarea sistemului solar sau ca produse de
fisiune
sau
transmuta?ie
ap?rute in mod natural de
uraniu
?i
toriu
.
Celelalte 24 de elemente mai grele r?mase, care nu se g?sesc ast?zi nici pe P?mant, nici in spectrul astronomic, au fost produse artificial: toate acestea sunt radioactive, cu jum?t??i foarte scurte de via??; dac? exist? vreun atom al acestor elemente la formarea P?mantului, este extrem de probabil, pan? la punct de certitudine, c? au fost deja dezintegrate ?i, dac? sunt prezente in
nove
, au fost in cantit??i prea mici pentru a fi observate.
Techne?iul
a fost primul element sintetizat, care nu a fost natural, in 1937, de?i in natur? s-au g?sit urme de techne?iu (?i, de asemenea, elementul a fost descoperit in mod natural in 1925)
[14]
. Acest model al produc?iei artificiale ?i descoperirea natural? ulterioar? a fost repetat cu mai multe alte elemente rare, radioactive, naturale.
[15]
Izotopii sunt specii de atomi cu acela?i Z (
num?r atomic
), dar cu num?r de
mas?
(A) diferit?, sau specii de atomi cu aceea?i sarcin? nuclear? ?i num?r diferit de neutroni. Exemplul hidrogenului:
| PROTIU (H)
|
DEUTERIU (D)
|
TRITIU (T)-radioactiv
|
| Z=1, A=1
|
Z=1, A=2
|
Z=1, A=3
|
| 1 proton
|
1 proton
|
1 proton
|
| 0 neutroni
|
1 neutron
|
2 neutroni
|
| 1 electron
|
1 electron
|
1 electron
|
Izobarii sunt specii de atomi care apar?in unor elemente chimice diferite, dar care au acela?i num?r de nucleoni. Izobarii au num?r atomic (Z) diferit, dar au acela?i num?r de mas? (A). Ca exemplu poate servi seria izobaric? 40, care cuprinde atomi cu cate 40 de nucleoni, dup? cum se observ? in tabelul de mai jos:
Izotonii sunt specii de atomi cu acela?i num?r de neutroni (n), dar cu num?r diferit de protoni (Z).
- ^
a
b
?Elemente chimice”
.
SetThings.com
.
. Accesat in
.
- ^
a
b
Sfetcu, Nicolae (
).
Materia: Solide, Lichide, Gaze, Plasma - Fenomenologie
. MultiMedia Publishing.
ISBN
978-606-9016-12-1
.
- ^
Oganessian, Yu. Ts.; Utyonkov, V.; Lobanov, Yu.; Abdullin, F.; Polyakov, A.; Sagaidak, R.; Shirokovsky, I.; Tsyganov, Yu.; et al. (
).
?Evidence for Dark Matter”
(PDF)
.
Physical Review C
.
74
(4): 044602.
Bibcode
:
2006PhRvC..74d4602O
.
doi
:
10.1103/PhysRevC.74.044602
. Arhivat din
original
(PDF)
la
. Accesat in
.
- ^
lbl.gov (
).
?The Universe Adventure Hydrogen and Helium”
.
Lawrence Berkeley National Laboratory
U.S. Department of Energy. Arhivat din
original
la
.
- ^
astro.soton.ac.uk (
).
?Formation of the light elements”
. University of Southampton. Arhivat din
original
la
.
- ^
?Elemente chimice”
.
SetThings.com
.
. Accesat in
.
- ^
foothill.edu (
).
?How Stars Make Energy and New Elements”
(PDF)
. Foothill College.
- ^
Dume, B. (
).
?Bismuth breaks half-life record for alpha decay”
.
Physicsworld.com
. Bristol, England: Institute of Physics
. Accesat in
.
- ^
de Marcillac, P.; Coron, N.; Dambier, G.; Leblanc, J.; Moalic, J-P (
). ?Experimental detection of alpha-particles from the radioactive decay of natural bismuth”.
Nature
.
422
(6934): 876?8.
Bibcode
:
2003Natur.422..876D
.
doi
:
10.1038/nature01541
.
PMID
12712201
.
- ^
Glanz, J. (
).
?Scientists Discover Heavy New Element”
.
The New York Times
.
- ^
Oganessian, Yu. Ts.; Abdullin, F. Sh.; Bailey, P. D.; Benker, D. E.; Bennett, M. E.; Dmitriev, S. N.; Ezold, J. G.; Hamilton, J. H.; Henderson, R. A.; Itkis, M. G.; Lobanov, Yu. V.; Mezentsev, A. N.; Moody, K. J.; Nelson, S. L.; Polyakov, A. N.; Porter, C. E.; Ramayya, A. V.; Riley, F. D.; Roberto, J. B.; Ryabinin, M. A.; Rykaczewski, K. P.; Sagaidak, R. N.; Shaughnessy, D. A.; Shirokovsky, I. V.; Stoyer, M. A.; Subbotin, V. G.; Sudowe, R.; Sukhov, A. M.; Tsyganov, Yu. S.; et al. (aprilie 2010). ?Synthesis of a New Element with Atomic Number Z=117”.
Physical Review Letters
.
104
(14): 142502.
Bibcode
:
2010PhRvL.104n2502O
.
doi
:
10.1103/PhysRevLett.104.142502
.
PMID
20481935
.
- ^
Sanderson, K. (
).
?Heaviest element made ? again”
.
News@nature
.
doi
:
10.1038/news061016-4
.
- ^
Schewe, P.; Stein, B. (
).
?Elements 116 and 118 Are Discovered”
.
Physics News Update
.
American Institute of Physics
. Arhivat din
original
la
. Accesat in
.
- ^
United States Environmental Protection Agency.
?Technetium-99”
. epa.gov
. Accesat in
.
- ^
Harvard?Smithsonian Center for Astrophysics
.
?Origins of Heavy Elements”
. cfa.harvard.edu
. Accesat in
.
| Elemente chimice
|
|
|
| Metale alcaline
|
|

|
|
|
| Metale alcalino-p?mantoase
|
|
|
|
| Metale tranzi?ionale
|
|
|
|
| Metale post-tranzi?ionale
|
|
|
|
| Metaloizi
|
|
|
|
| Nemetale
|
|
|
|
| Halogeni
|
|
|
|
| Gaze nobile
|
|
|
|
| Lantanide
|
|
|
|
| Actinide
|
|
|
|
| Superactinide
|
|
|