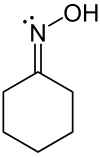
 Dalam sikloheksanon
oksima
, atom
nitrogen
mempunyai tiga ikatan valens dan oleh itu mempunyai valens tiga.
Dalam sikloheksanon
oksima
, atom
nitrogen
mempunyai tiga ikatan valens dan oleh itu mempunyai valens tiga.
Dalam
kimia
,
valens
(
bahasa Inggeris
:
valence
,
bahasa Latin
:
valentia
terbitan kata
valens
"kuat"
[1]
) juga dikenali sebagai
valensi
atau
nombor valens
ialah tahap kemampuan suatu
atom
sesebuah
unsur
mengikat gabung dengan satu atau lebih atom yang lain membentuk sebatian atau molekul lebih besar. Bagi kebanyakan unsu , bilangan ikatan boleh berubah-ubah. Takrifan
IUPAC
mengehadkan valens kepada
bilangan tertinggi atom valens tunggal yang boleh bergabung dengan satu atom
, yakni bilangan tertinggi ikatan valens yang boleh dihasilkan oleh sesuatu unsur.
[2]
Valens satu unsur bergantung kepada bilangan
elektron valens
yang boleh terlibat dalam penghasilan ikatan valens. Atom, ion atau kumpulan
univalen
(valens tunggal) mempunyai valens satu dan oleh itu boleh menghasilkan satu
ikatan kovalen
.
Entiti molekul
dwivalen
mempunyai valens dua dan boleh membentuk dua
ikatan sigma
dengan dua atom berbeza, atau satu ikatan sigma dan satu
ikatan pi
kepada satu atom tunggal.
[3]
Kumpulan alkil
dan ion
hidroksil
adalah contoh-contoh univalen;
ligand okso
adalah dwivalen.
Dalam abad yang lalu, konsep valens berkembang kepada pelbagai cara untuk menjelaskan ikatan kimia, seperti
struktur Lewis
(1916),
teori ikatan valens
(1927),
orbital molekul
(1928),
teori penolakan pasangan elektron petala valens
(1958) dan semua kaedah rumit
kimia kuantum
.
 Kombinasi zarah-zarah unggul
William Higgins
(1789)
Kombinasi zarah-zarah unggul
William Higgins
(1789)
Pada 1789,
William Higgins
menerbitkan satu pandangan yang dianggap beliau kombinasi zarah-zarah "unggul" yang membayangkan konsep
ikatan valens
.
[4]
Menurut Higgins, jika, misalnya, daya antara zarah-zarah unggul oksigen dan nitrogen ialah 6, maka kekuatan daya itu akan dibahagikan sama rata, dan begitu juga halnya bagi gabungan zarah-zarah unggul lain (lihat ilustrasi).
Pada tahun 1852, kertas kerja oleh
Edward Frankland
menggabungkan teori
radikal bebas
dan "teori jenis" dengan memasukkan anggapan
afiniti kimia
untuk menunjukkan bahawa sesetengah unsur mempunyai kecenderungan untuk bergabung dengan unsur-unsur lain untuk membentuk sebatian dengan 3, seperti mana dalam kumpulan tiga atom (contohnya
NO
3
,
NH
3
,
NI
3
dll.) atau 5, seperti mana dalam kumpulan lima atom (contohnya
NO
5
,
NH
4
O
,
PO
5
dll.) persamaan unsur-unsur yang bergabung. Menurut Frankland, cara inilah boleh memuaskan afiniti unsur-unsur. Mengikut contoh-contoh dan postulat-postulat ini, Frankland menyatakan betapa jelasnya bahawa:
[5]
A tendency or law prevails (here), and that, no matter what the characters of the uniting atoms may be, the
combining power
of the attracting element, if I may be allowed the term, is always satisfied by the same number of these atoms.
("Satu kecenderungan atau hukum diamalkan [di sini], dan bahawa, tidak kira apa ciri-ciri atom-atom yang bergabung itu,
kuasa penggabungan
unsur-unsur yang menarik, jika saya boleh menggunakan istilah tersebut, sentiasa dipuaskan oleh jumlah atom ini yang sama.")
"Kuasa penggabungan" ini kemudiannya diungkapkan sebagai
Quantivalenz
("kuantivalens" atau "berapa kuat") oleh
August Wilhelm von Hofmann
[4]
sebelum akhirnya dipendekkan lanjut dalam sebuah rencana makalah mengenai ikatan fosforus ditulis ahli kimia Jerman Hermann Wichelhaus (
bahasa Jerman
:
Valenz
) tahun 1868 memutakhirkan pengungkapan idea ini.
[6]
Konsep kovalens dibangunkan pada pertengahan abad ke-19 sebagai percubaan untuk merasionalkan
formula
sebatian-sebatian kimia
yang berbeza. Pada tahun 1919,
Irving Langmuir
telah meminjam istilah yang digunakan untuk menjelaskan model
atom kiub
Gilbert N. Lewis
dengan menyatakan yang "bilangan pasangan
elektron
yang mana-mana atom kongsi dengan atom bersebelahan dinamakan
kovalens
atom itu". Imbuhan awalan
co-
membawa maksud "bersama-sama", maka ikatan ko-valen bermaksud atom-atom itu berkongsi valens. Oleh itu, sekiranya satu atom mempunyai valens +1, ia mempunyai satu elektron lebih daripada
petalanya
yang lengkap, dan jika ia mempunyai valens -1, ia kekurangan satu elektron dan memerlukan satu elektron untuk melengkapkan petala luarannya. Ikatan antara kedua-dua atom ini boleh terjadi kerana kedua-dua atom akan menyeimbangkan dengan berkongsi kecenderungan valens masing-masing yang tidak seimbang. Kini, istilah
ikatan kovalen
lebih kerap digunakan daripada "valens", yang semakin kurang digunakan dalam kajian-kajian tahap tinggi dengan kemajuan dalam teori ikatan kimia, tetapi istilah "valens" masih lagi digunakan secara meluas dalam pembelajaran tahap rendah yang memerlukan pengenalan heuristik bagi subjek ini.
Bagi unsur-unsur dalam
kumpulan
utama
jadual berkala
(kumpulan dalam blok s dan p), valensnya adalah daripada satu hingga tujuh, tetapi biasanya unsur-unsur ini membentuk beberapa ikatan daripada satu hingga empat. Bilangan ikatan yang dihasilkan oleh suatu unsur dahulu dianggap sebagai satu ciri kimia yang tetap. Sebenarnya, dalam banyak keadaan hal ini tidak benar. Misalnya,
fosforus
selalunya memiliki valens tiga, tetapi boleh juga memiliki valens-valens lain.
Walau bagaimanapun, banyak unsur kimia mempunyai valens yang serupa mengikut kedudukannya dalam jadual berkala, mengikut
hukum oktet
. Unsur-unsur dalam
kumpulan 1
(logam alkali) dan
17
(halogen) biasanya mempunyai valens 1; unsur-unsur dalam
kumpulan 2
(logam alkali bumi) dan
16
(kalkogen) mempunyai valens 2; unsur-unsur
kumpulan 13
(kumpulan boron) dan
15
(kumpulan nitrogen) memiliki valens 3; unsur dalam
kumpulan 14
(kumpulan karbon) mempunyai valens 4.
Polivalens
atau
multivalens
merujuk kepada
spesis kimia
yang tidak terhad kepada satu nombor
ikatan
valens. (Spesis yang mempunyai satu valens sahaja digelar monovalen atau univalen). Misalnya,
kation
Cs
+
ialah kation monovalen, manakala kation Ca
2+
pula ialah kation dwivalen, polivalen atau multivalen dan kation Fe
3+
pula ialah ikatan trivalen, polivalen atau multivalen.
- ^
"v?l?ns, entis". K. Prent, J. Adisubrata, W. J. S. Poerwadarminta (1969).
Kamus Latin-Indonesia
. Jogjakarta: Penerbitan Jajasan Kanisius. m/s. 907.
- ^
Takrifan
IUPAC Gold Book
:
valence
- ^
The Free Dictionary:
valence
- ^
a
b
Partington, J.R. (1989).
A Short History of Chemistry
. Dover Publications, Inc.
ISBN
0-486-65977-1
.
- ^
Frankland, E. (1852). Phil. Trans., vol. cxlii, 417.
- ^
Constable, Edwin C.; Housecroft, Catherine E. (Jun 2020). "Chemical Bonding: The Journey from Miniature Hooks to Density Functional Theory".
Molecules
.
25
(11): 2635?6.
doi
:
10.3390/molecules25112623
.