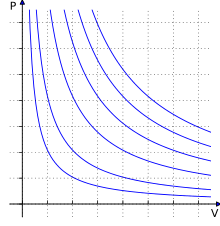
 Isoterme
di un
gas ideale
Isoterme
di un
gas ideale
L'
equazione di stato dei gas perfetti
(o ideali), nota anche come
legge dei gas perfetti
, descrive le condizioni fisiche di un "
gas perfetto
" o di un gas "ideale", correlandone le
funzioni di stato
. Venne formulata nel
1834
da
Emile Clapeyron
. La sua forma piu semplice ed elegante e:

dove le variabili sono in ordine: la
pressione
, il
volume
, la
quantita di sostanza
, la
costante dei gas
e la
temperatura assoluta
del gas perfetto.
L'equazione di stato dei gas perfetti descrive bene il comportamento dei gas reali per pressioni non troppo elevate e per temperature non troppo vicine alla temperatura di liquefazione del gas. Una migliore descrizione del comportamento dei gas reali e dato dall'
equazione di stato di Van der Waals
.
L'equazione di stato dei gas perfetti e stata inizialmente formulata come sintesi dalle leggi empiriche di
Avogadro
,
Boyle
,
Charles
e
Gay-Lussac
.
Trascurando in un primo momento la
legge di Avogadro
, si consideri un volume di gas
 in
condizioni standard
ad uno stato iniziale caratterizzato da:
in
condizioni standard
ad uno stato iniziale caratterizzato da:

Si consideri una
trasformazione isobara
(a pressione costante) applicata a questo volume di gas. Il volume alla fine della trasformazione sara, secondo la
legge di Charles
:

Il parametro
 e detto
coefficiente di dilatazione termica
e ha le dimensioni dell'inverso della temperatura perche il prodotto
e detto
coefficiente di dilatazione termica
e ha le dimensioni dell'inverso della temperatura perche il prodotto
 e adimensionale. La temperatura
e adimensionale. La temperatura
 e espressa in
gradi Celsius
(°C).
e espressa in
gradi Celsius
(°C).
Se poi si fa andare il volume cosi ottenuto incontro ad una
trasformazione isoterma
otterremo, secondo la
legge di Boyle-Mariotte
:

ovvero:

Quindi la legge in questa prima forma si esprime:

dove
 e una costante caratteristica del tipo di gas, cioe il prodotto di pressione, volume e del reciproco della
temperatura assoluta
e costante nelle varie trasformazioni fisiche a cui il
gas perfetto
venga sottoposto. Ha le dimensioni di energia per unita di massa e di temperatura.
e una costante caratteristica del tipo di gas, cioe il prodotto di pressione, volume e del reciproco della
temperatura assoluta
e costante nelle varie trasformazioni fisiche a cui il
gas perfetto
venga sottoposto. Ha le dimensioni di energia per unita di massa e di temperatura.
Questa formulazione, che non sfrutta la legge di Avogadro collega direttamente la densita alla pressione e alla temperatura, ma dipende implicitamente dal gas scelto, ed e necessario calcolare prima la costante caratteristica del gas in esame. Quindi e ancora utile da un punto di vista tecnico quando si devono ripetere calcoli con lo stesso gas, non quando si devono confrontare gas a diversa massa molecolare media.
La relazione che meglio descrive il comportamento di una sostanza in fase gassosa e:
 , dove
, dove
 e il
volume molare
e
e il
volume molare
e
 e il
fattore di comprimibilita
, che esprime lo scostamento del comportamento ideale da quello reale.
e il
fattore di comprimibilita
, che esprime lo scostamento del comportamento ideale da quello reale.
Siccome la massa
 del gas e legata alla sua
quantita di sostanza
del gas e legata alla sua
quantita di sostanza
 dalla
massa molecolare
media del gas
dalla
massa molecolare
media del gas
 :
:

o sul piano locale:
 ,
,
dove la massa molecolare media si puo calcolare come
media ponderata
sulla composizione molecolare
 (in at%):
(in at%):

allora ridefinendo una costante molare dei gas (per unita di quantita di sostanza anziche per unita di massa):

si puo rienunciare la relazione ottenuta come:

Per esempio per l'aria (qui si considera per semplicita l'aria tecnica costituita da due componenti: 79 at% azoto e 21 at% ossigeno), la massa molecolare vale:
 .
.
Quindi se la costante di gas ideale dell'aria vale
 ,
,
si puo prevedere una costante molare per l'aria pari a
 .
.
In realta Avogadro confrontando vari gas scopri che la costante molare non dipende piu neanche dal tipo di gas considerato (percio viene chiamata
costante universale dei gas
): arrivo cioe empiricamente alla
legge di Avogadro
.
Quindi la equazione di stato dei gas ideali si riscrive tenendo conto della legge di Avogadro come
[1]
:

o in forma locale, dividendo per il volume:

in cui
 e il valore della pressione del gas;
e il valore della pressione del gas;
 e il volume occupato dal gas;
e il volume occupato dal gas;
 e la
densita molare
del gas;
e la
densita molare
del gas;
 e la
costante universale dei gas
, il cui valore varia in funzione delle unita di misura adottate per esprimere le altre grandezze nell'equazione;
e la
costante universale dei gas
, il cui valore varia in funzione delle unita di misura adottate per esprimere le altre grandezze nell'equazione;
 e la temperatura assoluta del gas, espressa in
kelvin
.
[2]
e la temperatura assoluta del gas, espressa in
kelvin
.
[2]
Il valore della costante universale nel
Sistema internazionale
e:

a volte nei calcoli, specialmente in chimica, si utilizza il valore (approssimato) di:

Infine se
 e la densita molare (mol/m
3
), moltiplicando e dividendo per il
numero di Avogadro
:
e la densita molare (mol/m
3
), moltiplicando e dividendo per il
numero di Avogadro
:

si ottiene la
densita numerica
 (in molecole/m
3
). In questo modo emerge una nuova costante dimensionale, detta
costante di Boltzmann
:
(in molecole/m
3
). In questo modo emerge una nuova costante dimensionale, detta
costante di Boltzmann
:

In questo modo nelle unita elementari si e gia passati da due costanti dimensionali ad una sola.
Il valore esatto e:
[3]
