A
peptidoglikan
, mas neven
murein
cukrokbol es
aminosavakbol
allo
polimer
, ami a
bakteriumok
sejtmembranjan
kivul haloszer? peptidoglikanreteget alkot, amely a legtobb bakteriumra (
Bacteria
domen)
[1]
[2]
:
66?67
jellemz?. A cukorkomponens felvaltva all β-(1,4)-kotott
N
-acetilglukozaminbol
(NAG) es
N
-acetilmuraminsavbol
(NAM). Az
N
-acetilmuraminsavhoz harom-ot aminosavbol allo peptidlanc kapcsolodik. A peptidlanc egy masik szal peptidlancaval keresztkoteseket alkothat, igy letrehozva a terhalos szerkezetet.
[2]
[3]
A peptidoglikan a bakterium sejtfalanak szerkezeteben fontos szerepet jatszik: meger?siti azt, es a
sejtplazma
ozmozisnyomasat
ellensulyozza. A peptidoglikan a bakteriumsejtek
osztodasaban
is szerepet jatszik. Ez az ismetl?d? kapcsolodas s?r? peptidoglikan-reteget eredmenyez, ami fontos a sejt alakjanak meg?rzesehez es a magas ozmozisnyomasnak valo ellenallashoz, es folyamatosan cserel?dik a peptidoglikan-termel?des reven. A peptidoglikan-hidrolizis es -szintezis ket folyamat, amelyek a sejtnovekedeshez es -osztodashoz szuksegesek, amely a meglev? anyag felosztasabol, az uj anyag beilleszteseb?l es a meglev? anyag uj anyaghoz valo koteseb?l allo folyamat.
[4]
A peptidoglikan-reteg sokkal vastagabb Gram-pozitiv bakteriumokban (20-80 nm), mint a Gram-negativakban (7-8 nm).
[5]
A pH-ertekt?l fugg?en a peptidoglikan a sejtfal szaraz tomegenek 40-90%-at alkotja Gram-pozitiv bakteriumokban, de csak mintegy 10%-at Gram-negativakban. Igy a peptidoglikan magas szintje alapjan megallapithato, hogy a bakterium Gram-pozitiv.
[6]
A Gram-pozitiv torzsekben fontos szerepet jatszik a csatolasban es a
szerotipusok
elkulonitesehez.
[7]
Mind Gram-pozitiv, mind Gram-negativ bakteriumok eseten athaladhatnak a peptidoglikanon kb. 2 nm-es reszecskek.
[8]
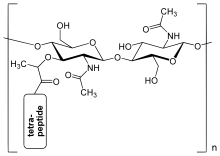 Peptidoglikan
Peptidoglikan
A bakterium sejtfalanak peptidoglikan-retege egy ket aminocukorbol (
N
-acetilglukozaminbol (GlcNAc vagy NAGA) es
N
-acetilmuraminsavbol (MurNAc vagy NAGA)) allo reteg. A cukrokat β-(1,4)-
glikozidos kotes
koti ossze. A MurNAc rovid (4?5 tagu) aminosavlanchoz csatlakozik, mely
l
-
alanint
,
d
-
glutaminsavat
,
mezo-diaminopimelinsavat
es
d
-alanint tartalmaz a Gram-negativ
Escherichia coli
eseten, illetve
l
-alanint,
d
-
glutamint
,
l
-lizint es
d
-alanint tartalmaz a tetrapeptidek kozti 5
glicines
hiddal a Gram-pozitiv
Staphylococcus aureus
eseten.
Az aminosavak kozti
keresztkoteseket
a kulonboz? linearis aminocukorlancokban a
DD-transzpeptidaz
hozza letre, er?s, rideg terszerkezetet eredmenyezve. Az aminosav-sorozat es molekularis szerkezet fajrol fajra valtozik.
[9]
A membran elzarasaval a peptidoglikan megvedi a sejtet
turgornyomasa
okozta
liziset?l
. A sejtfal alakjat meg?rzi novekedesekor, mivel a frissen hozzaadott anyag felgomb alaku falla valik az utodsejtekben.
[10]
A peptidoglikan tipusairol es taxonomiai kovetkezmenyeikr?l beszamoltak K. H. Schleiferek.
[11]
A peptidoglikan monomerei a
citoszolban
szintetizalodnak, majd egy szallitomembranhoz, a
baktoprenolhoz
kapcsolodnak. A baktoprenol a sejtmembranon keresztul szallitja a monomereket, ahol a meglev? peptidoglikanhoz kapcsolodnak.
[12]
- A peptidoglikan szintezisenek els? lepeseben a
glutamin
aminocsoportot ad at a
fruktoz-6-foszfatnak
.
[13]
Ez a reakcio, melyet az
EC 2.6.1.16
(GlmS) katalizal, a fruktoz-6-foszfatot
glukozamin-6-foszfatta
alakitja.
- A masodik lepesben egy acetilcsoport kerul at az
acetil-CoA
-rol a glukozamin-6-foszfat aminocsoportjara, igy
N
-acetil-glukozamin-6-foszfat
keletkezik.
[14]
- A harmadik lepesben az
N
-acetil-glukozamin-6-foszfat izomerizalodik, igy az atalakul
N-acetil-glukozamin-1-foszfatta
.
[14]
- A negyedik lepesben az
N
-acetil-glukozamin-1-foszfat az
UTP
-hez kot?dik. Az
uridin-trifoszfat
energiaforraskent is tud m?kodni. Ebben a reakcioban egy szervetlen pirofoszfat eltavozik, helyere a monofoszfat kerul, igy keletkezik az UDP-
N
-acetil-glukozamin (2,4) (ha
UDP
az energiaforras, szervetlen foszfat tavozik). E kezdeti szakasz soran keletkezik az NAG prekurzora a peptidoglikanban.
- Az otodik lepesben nehany UDP-
N
-acetil-glukozamin (UDP-GlcNAc) atalakul UDP-MurNAc-va (UDP-
N
-acetilmuraminsav) egy laktilcsoport hozzaadasaval a glukozaminhoz. Szinten e reakcioban a C3-hidroxilcsoport eltavolit egy foszfatot a
foszfoenolpiruvat
α-szenatomjarol. Ez egy enolszarmazekot hoz letre.
- Az enol laktil-molekulareszlette alakul a hatodik lepesben.
[14]
- A hetedik lepesben az UDP?MurNAc UDP-MurNAc-pentapeptidde alakul 5 aminosav hozzaadasaval, jellemz?en a
d
-alanil-
d
-alanin dipeptid felhasznalasaval.
[14]
Minden ilyen reakcio ATP-t igenyel.
[14]
Ezt nevezik az els? szakasznak.
A masodik szakasz a citoplazmatikus membranban tortenik. Ez a membranon belul van, ahol a baktoprenol peptidoglikan-prekurzorokat szallit a sejtmembranon keresztul
- Az
undekaprenil-foszfat
megtamadja az UDP-MurNAc pentat, a PP-MurNac pentat, egy lipidet (
lipid I
) letrehozva.
- Az UDP-GlcNAc ezutan a MurNAC-hoz kerul, igy egy diszacharid keletkezik, a Lipid-PP-MurNAc penta-GlcNAc (
lipid II
), ami szinten a peptidoglikan prekurzora.
[14]
- A lipid II-t a
flippaz
(MurJ) szallitja, melyet 2014-ben fedeztek fel.
[15]
Ekkor a glikanlanchoz adja hozza a
peptidoglikan-glikoziltranszferaz
(GTaz, EC 2.4.1.129). Ez a folyamat a transzglikozilacio. Ekkor A GlcNAc hidroxilcsoportja a glikan MurNAc-jahoz kot?dik, amely a lipid-PP-t eltavolitja a glikanlancrol.
[14]
- Vegul a
DD-transzpeptidaz
(TPaz, EC 3.4.16.4) keresztkoteseket hoz letre a glikanlancok kozt. E feherje ismert meg penicillinkot? feherjekent is. Nehany valtozata glikoziltranszferazkent is m?kodik, mig masok kulon enzimnek hagyjak ezt.
[13]
Immunrendszer altali felismerese
[
szerkesztes
]
A peptidoglikan-felismeres az evolucio soran allando folyamat.
[16]
Az egyes bakteriumfajok eseten a szerkezet hasonlo, de bizonyos elteresek novelhetik a diverzitast. Ezek koze tartozik a cukorpolimerek hosszanak, szerkezetenek elterese, a keresztkotesek elterese vagy az aminosavak valtozasa (f?kepp a 3. helyen).
[16]
[17]
Ezek celja a sejtfal tulajdonsagainak megvaltozasa, mely fontos szerepet jatszik a
patogenezisben
.
[16]
A peptidoglikanokat szamos enzim (peldaul
lizozim
, glukozaminidaz,
endopeptidaz
) kepes lebontani,
[16]
immunstimulalo toredekeket (mas neven muropeptideket) letrehozva,
[18]
amik fontosak a
gazda?patogen interakcio
letrehozasaban,
[17]
ilyen peldaul az MDP (
muramil-dipeptid
, NAG (
N-acetilglukozamin
vagy az iE-DAP (γ-
d
-glutamil-
mezo
-diaminopimelinsav).
[16]
[18]
A belbakteriumok peptidoglikanja fiziologias korulmenyek kozt is athalad a belfalon.
[18]
A peptidoglikanok es toredekeik athaladasa lehet kozvetlen (hordozofuggetlen) es kozvetett (hordozofugg?), illetve bakteriummedialt (szekrecios rendszerek,
membranvezikulum-forgalom
) vagy gazdasejtmedialt (receptormedialt, peptidtranszporterek).
[18]
A
bakterialis szekrecios rendszerek
a virulenciafaktorok a bakterium sejthartyajan keresztul a kuls? kornyezetbe torten? szallitasara feherjekomplexek.
[19]
Az intracellularis bakterialis patogenek az eukariota sejteket tamadjak (ami
fagolizoszoma
-keletkezeshez vagy
autofagiahoz
vezethet, vagy a bakteriumokat bekebelezik a
fagocitak
(
makrofagok
,
monocitak
,
neutrofilek
. A bakteriumtartalmu
fagoszoma
egyesulhet
endoszomakkal
vagy
lizoszomakkal
, igy a bakterium lebomlik, es peptidoglikan-toredekek es muropeptidek keletkeznek.
[18]
Az immunrendszer erzekeli a megmaradt peptidoglikant es peptidoglikan-toredekeket PRR-ekkel (
mintafelismer? receptorok
), amik kivalasztodnak, sejten belul vagy a sejtfelszinen fejez?dnek ki.
[16]
Peptidoglikan-felismer? feherjek
[
szerkesztes
]
A
PGLYRP
-k allandoak a
rovaroktol
az
eml?sokig
.
[18]
Az eml?sok 4 oldekony peptidoglikan-felismer? feherjet (
PGLYRP-1
,
PGLYRP-2
,
PGLYRP-3
,
PGLYRP-4
) valasztanak ki, amik felismerik a muramil-penta- vagy tetrapeptidet.
[16]
Ezek
lipopoliszacharidokhoz
es mas molekulakhoz is kot?dhetnek a peptidoglikan-kot? helyen kivuli kot?helyeken.
[19]
A peptidoglikan felismerese utan a PGLYRP-k aktivaljak a
polifenol-oxidazokat
(PPO), a Toll- vagy az immunhiany- (IMD) jelz? utvonalakat. Ez
antimikrobialis peptidek
(AMP) termelesehez vezet.
[19]
Minden eml?s PGLYRP-je egyedi kifejez?desi mintazattal rendelkezik. A PGLYRP-1 jellemz?en a neutrofilek es eozinofilek granulaiban fejez?dik ki.
[16]
A PGLYRP-3 es 4 feherjeket tobbek kozt a b?r, a verejtekmirigyek, a szemek es a belrendszer fejezik ki.
[18]
A PGLYRP-1, 3 es 4 diszulfidkotott
homo-
es
heterodimereket
alkotva fejtik ki baktericid hatasukat.
[18]
A bakteriumsejtfal peptidoglikanjaival valo kotes a bakterium sejthalalat okozhatja a kulonboz? bakterialis transzkripcios szabalyzofeherjekre valo hatasa miatt.
[16]
A PGLYRP-k segithetik a bakterium eloleset mas PRR-ekkel valo egyuttm?kodessel, igy javitva a bakteriumok fagocitak altali felismereset.
[16]
A PGLYRP-2-t els?sorban a
maj
fejezi ki es valasztja ki a verkeringesbe.
[16]
Ezenkivul kifejez?dhet a b?r
keratinocitaiban
, valamint a szaj es a belek
epitelsejtjeiben
.
[18]
Szemben a tobbi PGLYRP-vel, a PGLYRP-2 nem rendelkezik kozvetlen baktericid aktivitassal. Peptidoglikan-amidazkent m?kodik, hidrolizalja a laktil-amid kotest a MurNAc es a peptidoglikan alappeptidjenek 1. aminosava kozt.
[16]
[18]
Feltetelezesek szerint a PGLYRP-2 celja a tulzott immunvalasz, a gyulladas okozta szovetkarosodas megakadalyozasa a
NOD2
ligandumokra, mivel e muropeptideket mar nem ismeri fel a NOD2 a peptid es a MurNAc szetvalasztasa utan.
[18]
Sok tanulmany szerint a peptidoglikan-felismer? feherjecsalad tagjai fontosak a bel epitelsejtjeinek
toleranciajaban
a kommenzalista bakteriumok fele.
[19]
[20]
Kimutattak, hogy a PGLYRP-2 es -4 kifejez?dese befolyasolhatja a belbakteriumok osszetetelet.
[19]
2020-ban felfedeztek, hogy a PGLYRP-ket es a NOD-tipusu receptorokat es peptidoglikan-transzportereket a fejl?d? egeragy nagymertekben kifejezi.
[21]
A PGLYRP-2-t szamos agyi resz
neuronjai
kifejezik, peldaul a
prefrontalis kereg
, a
hippokampusz
es a
kisagy
, igy lehetnek kozvetlen hatasai a peptidoglikannak a neuronokra. A PGLYRP-2-t ezenkivul a kisgyermekek nagyagya is kifejezi, de a legtobb erett kergi szovet nem. A PGLYRP-1-et is kifejezi az agy, ez azonban feln?ttkorban is kifejez?dik.
[21]
NOD-tipusu receptorok
[
szerkesztes
]
A peptidoglikan egyik legismertebb receptorai a
NOD-tipusu receptorok
(NLR-ek), ezen belul f?kepp a
NOD1
es a
NOD2
. A NOD1 receptor iE-DAP (γ-
d
-glutamil-
mezo
-diaminopimelinsav) kotesekor aktivalodik, mig a NOD2 az MDP-t ismeri fel az
LRR domenekkel
.
[19]
Az aktivacio onoligomerizaciohoz vezet, ami ket jelz?sorozat aktivaciojahoz vezet. Az egyik az
NF-κB
-t aktivalja a RIP2-n,
TAK1
-en es
IKK
-n keresztul,
[22]
a masik a
MAPK
-sorozatot inditja el. Ezen utvonalak aktivacioja
citokin
- es
kemokintermelest
okoz.
[16]
A NOD1-et szamos sejttipus kifejezi, peldaul a mieloid fagocitak, az epitel-
[16]
es az idegsejtek.
[21]
A NOD2-t a monocitak, makrofagok, belepitel-,
Paneth-
,
dendrites
,
csontsejtek
,
oszteoblasztok
,
keratinocitak
es mas epitelsejttipusok fejezik ki.
[17]
Citoszolszenzorokkent
a NOD1-nek es NOD2-nek vagy citoszolba lep? bakteriumokat kell eszlelnie, vagy a peptidoglikannak kell a citoszolba lep? toredekekre bomlania, amik a szenzorok m?kodesbe lepeset el?idezik.
[16]
2020-ban kimutattak, hogy az
NLRP3
-at a NOD1-t?l es NOD2-t?l fuggetlen mechanizmussal aktivalja a peptidoglikan.
[18]
A makrofagokban a peptidoglikan bomlasabol kepz?d? N-acetilglukozaminrol kimutattak, hogy gatolja a hexokinazaktivitast, es annak felszabaditasat okozza a
mitokondrium
membranjan at, es hogy segiti az NLRP3
inflammaszoma
aktivalasat egy megnovekedett mitokondrialis membranpermeabilitas okozta mechanizmus reven.
[18]
Az
NLRP1
-et is citoplazmatikus peptidoglikanszenzornak tekintik. Erzekeli az MDP-t es
IL-1
-szekreciot er?sit a NOD2-hoz kot?dve.
[19]
[17]
C-tipusulektin-receptorok (CLR-ek)
[
szerkesztes
]
A
C-tipusu lektinek
nagyreszt
Ca
2+
-fugg? feherjek, melyek szamos
szenhidrathoz
kot?dnek, beleertve a peptidoglikan glikanvazat), es nem specifikus immunreceptorokkent funkcionalnak.
[18]
A peptidoglikanhoz kot?d? CLR-ek koze tartoznak az MBL (
mannozkot? lektin
), a
fikolinok
, a
Reg3A
(regeneraciosgen-csaladbeli feherje 3A) es a PTCLec1.
[19]
Az eml?sokben ?k inditjak be a
komplementsorozat
lektinutvonalat
.
[18]
Toll-tipusu receptorok
[
szerkesztes
]
A
TLR
-ek funkcioja a kozvetlen peptidoglikan-felismeresben vitatott.
[16]
Egyes tanulmanyok szerint a peptidoglikant a TLR2 erzekeli.
[23]
De ezt okozhatjak a sejtfali
lipoproteinek
es
lipoteichoinsavak
, amik gyakran egyutt valasztodnak ki a peptidoglikannal. Ezenkivul a peptidoglikan szerkezetenek elteresei is okozhatjak az elter? eredmenyeket.
[16]
[18]
Vakcinakent vagy adjuvanskent
[
szerkesztes
]
A peptidoglikan immunologiailag aktiv, ami az immunsejteket megnovekedett citokinexpressziora es az antitestfugg? specifikus immunvalasz segitesere sarkallhatja vakcinaval egyutt vagy
adjuvanskent
.
[19]
A peptidoglikan alapegyseget, az MDP-t hasznaltak eredetileg a
Freund-adjuvans
aktiv komponensekent.
[19]
A
Staphylococcus aureus
peptidoglikanjat egereket ved? vakcinakent hasznalva kimutattak, hogy a vakcinainjekcio utan 40 hetig megnovekedett a
S. aureus
halalos dozisa
.
[24]
Inhibicio es bontas
[
szerkesztes
]
Nehany
antibiotikum
, peldaul a
penicillin
hat a peptidoglikan-termelesre a
penicillinkot? feherjekhez
vagy
DD-transzpeptidazokhoz
kot?dve,
[7]
amelyek a peptidoglikanban az oligopeptidek kozti koteseket letrehozzak. Egy bakterium
kettehasadassal
valo szaporodasahoz tobb mint egymillio peptidoglikan-alegysegnek (NAM-NAG+oligopeptid) kell kapcsolodnia a meglev? egysegekhez.
[25]
A transzpeptidazkodolo genek antibiotikummal valo csokkent kolcsonhatast okozo mutacioi fontos okai az
antibiotikum-rezisztencia
megjelenesenek.
[26]
A muraimicinek a foszfo-N-acetilmuramoil-pentapeptid-transzlokazt (MraY) UDP-MurNAc-pentapeptiddel (UM5A) kompetitiven gatoljak.
[27]
A peptidoglikan-szintezis mas lepesei is megcelozhatok. A
bacitracin
peldaul a
C55-izoprenil-pirofoszfat
-felhasznalast celozza. A
lantibiotikumok
, amik koze a
nizin
is tartozik, a
lipid II
-t tamadjak.
[28]
A konnyekben talalhato
lizozim
, a nem specifikus immunrendszer resze antibakterialis hatasat a β-(1,4)-glikozidos kotesek felszakitasaval eri el (lasd fentebb). A lizozim sokkal hatekonyabb a Gram-pozitiv bakteriumokban, ahol a peptidoglikan sejtfal szabad, mint a negativakban, ahol azt
lipopoliszacharid
veszi korul.
[22]
Nehany peptidoglikan-modosulat lizozim-rezisztenciat okozhat. A bakteriumok bomlekonysagat befolyasolhatja az antibiotikumoknak valo kitettseg is. A kitett bakteriumok rovidebb cukrokat tartalmazo peptidoglikant allitanak el?, keves keresztkotessel, amit konnyebben bont a lizozim.
[19]
Pszeudopeptidoglikan
[
szerkesztes
]
Az
archeak
nem rendelkeznek peptidoglikannal,
[29]
helyettuk egyes fajaik sejtjei korul
pszeudopeptidoglikan
(mas neven pszeudomurein) talalhato, ahol a szenhidratok β-(1,3)-kotott
N
-acetilglukozamin es
N
-acetiltaloszaminuronsav
. Ez a sejtfalaikat ellenallova teszi a
lizozimmel
szemben.
[30]
- ↑
(1990. junius 1.) ?Towards a natural system of organisms: proposal for the domains Archaea, Bacteria, and Eucarya”.
Proceedings of the National Academy of Sciences of the United States of America
87
(12), 4576?4579. o.
DOI
:
10.1073/pnas.87.12.4576
.
PMID 2112744
.
- ↑
a
b
Brock Biology of Microorganisms
, 14, Boston: Pearson Education Limited,
66
?67. o. (2015).
ISBN 978-1-292-01831-7
- ↑
Animation of Synthesis of Peptidoglycan Layer
.
PharmaXChange.info
, 2011. marcius 20.
- ↑
(2013. junius 1.) ?Elasticity and biochemistry of growth relate replication rate to cell length and cross-link density in rod-shaped bacteria”.
Biophysical Journal
104
(12), 2607?2611. o.
DOI
:
10.1016/j.bpj.2013.04.028
.
PMID 23790368
.
- ↑
Purcell A:
Bacteria
. Basic Biology, 2016. marcius 18.
- ↑
Bacteria
,
Encyclopedia of Earth
. Washington DC: National Council for Science and the Environment (2014. oktober 12.)
- ↑
a
b
szerk.: Baron S: Structure,
Structure.
In:
Baron's Medical Microbiology
, 4th, Univ of Texas Medical Branch (1996).
ISBN 978-0-9631172-1-2
- ↑
Demchick PH, Koch AL (1996. februar 1.). ?
The permeability of the wall fabric of Escherichia coli and Bacillus subtilis
”.
Journal of Bacteriology
178
(3), 768?73. o.
DOI
:
10.1128/jb.178.3.768-773.1996
.
PMID 8550511
.
- ↑
Sherris Medical Microbiology
, 4, McGraw Hill (2004).
ISBN 978-0-8385-8529-0
- ↑
(2008. december 1.) ?Cell shape and cell-wall organization in Gram-negative bacteria”.
Proceedings of the National Academy of Sciences of the United States of America
105
(49), 19282?19287. o.
DOI
:
10.1073/pnas.0805309105
.
PMID 19050072
.
- ↑
(1972. december 1.) ?Peptidoglycan types of bacterial cell walls and their taxonomic implications”.
Bacteriological Reviews
36
(4), 407?477. o.
DOI
:
10.1128/MMBR.36.4.407-477.1972
.
PMID 4568761
.
- ↑
II. THE PROKARYOTIC CELL: BACTERIA
. [2010. julius 26-i datummal az
eredetib?l
archivalva]. (Hozzaferes: 2011. majus 1.)
- ↑
a
b
(2018. januar 1.) ?Peptidoglycan in obligate intracellular bacteria”.
Molecular Microbiology
107
(2), 142?163. o.
DOI
:
10.1111/mmi.13880
.
PMID 29178391
.
- ↑
a
b
c
d
e
f
g
White, D..
The physiology and biochemistry of prokaryotes
, 3rd, NY: Oxford University Press Inc. (2007)
- ↑
L. T. Sham, E. K. Butler, M. D. Lebar, D. Kahne, T. G. Bernhardt, N. Ruiz (2014. julius). ?Bacterial cell wall. MurJ is the flippase of lipid-linked precursors for peptidoglycan biogenesis”.
Science
345
(6193), 220?222. o.
DOI
:
10.1126/science.1254522
.
PMID 25013077
.
- ↑
a
b
c
d
e
f
g
h
i
j
k
l
m
n
o
p
q
A. J. Wolf, D. M. Underhill (2018. aprilis). ?Peptidoglycan recognition by the innate immune system”.
Nature Reviews. Immunology
18
(4), 243?254. o.
DOI
:
10.1038/nri.2017.136
.
PMID 29292393
.
- ↑
a
b
c
d
K. L. Bersch, K. E. DeMeester, R. Zagani, S. Chen, K. A. Wodzanowski, S. Liu, S. Mashayekh, H. C. Reinecker, C. L. Grimes (2021. aprilis). ?Bacterial Peptidoglycan Fragments Differentially Regulate Innate Immune Signaling”.
ACS Central Science
7
(4), 688?696. o.
DOI
:
10.1021/acscentsci.1c00200
.
PMID 34056099
.
- ↑
a
b
c
d
e
f
g
h
i
j
k
l
m
n
o
p
P. A. Bastor, R. Wheeler, I. G. Boneca (2021. januar). ?Uptake, recognition and responses to peptidoglycan in the mammalian host”.
FEMS Microbiology Reviews
45
(1), fuaa044. o.
DOI
:
10.1093/femsre/fuaa044
.
PMID 32897324
.
- ↑
a
b
c
d
e
f
g
h
i
j
k
Q. Sun, X. Liu, X. Li (2022. februar). ?Peptidoglycan-based immunomodulation”.
Applied Microbiology and Biotechnology
106
(3), 981?993. o.
DOI
:
10.1007/s00253-022-11795-4
.
PMID 35076738
.
- ↑
(2022. december 1.) ?Peptidoglycan recognition protein SC (PGRP-SC) shapes gut microbiota richness, diversity and composition by modulating immunity in the house fly Musca domestica”.
Insect Molecular Biology
32
(2), 200?212. o.
DOI
:
10.1111/imb.12824
.
PMID 36522831
.
- ↑
a
b
c
(2020. augusztus 1.) ?
Bacterial Peptidoglycans from Microbiota in Neurodevelopment and Behavior
”.
Trends in Molecular Medicine
26
(8), 729?743. o.
DOI
:
10.1016/j.molmed.2020.05.003
.
PMID 32507655
.
- ↑
a
b
Janeway's immunobiology
, Casey Weaver, Charles Janeway, 9th, 45, 96?98. o. (2017).
ISBN 978-0-8153-4505-3
.
OCLC
933586700
- ↑
A. Yoshimura, E. Lien, R. R. Ingalis, E. Tuomanen, R. Dziarski, D. Golenbock (1999. julius 1.). ?
Cutting edge: recognition of Gram-positive bacterial cell wall components by the innate immune system occurs via Toll-like receptor 2
”.
Journal of Immunology
163
(1), 1?5. o.
DOI
:
10.4049/jimmunol.163.1.1
.
PMID 10384090
.
- ↑
(2011. december 1.) ?The Staphylococcus aureus peptidoglycan protects mice against the pathogen and eradicates experimentally induced infection”.
PLOS ONE
6
(12), e28377. o.
DOI
:
10.1371/journal.pone.0028377
.
PMID 22145040
.
- ↑
Bauman R.
Microbiology with Diseases by Taxonomy
, 2nd, Benjamin Cummings (2007).
ISBN 978-0-8053-7679-1
- ↑
Spratt BG (1994. aprilis 1.). ?
Resistance to antibiotics mediated by target alterations
”.
Science
264
(5157), 388?93. o.
DOI
:
10.1126/science.8153626
.
PMID 8153626
.
- ↑
Saeid Malek Zadeh (2020. szeptember 2.). ?
Theoretical Study of Intermolecular Interactions between Critical Residues of Membrane Protein MraYAA and Promising Antibiotic Muraymycin D2
”.
ACS Omega
5
(36), 22739?22749. o.
DOI
:
10.1021/acsomega.0c01551
.
PMID 32954121
.
- ↑
(2017. marcius 1.) ?A review on cell wall synthesis inhibitors with an emphasis on glycopeptide antibiotics”.
MedChemComm
8
(3), 516?533. o.
DOI
:
10.1039/c6md00585c
.
PMID 30108769
.
- ↑
(1977. majus 1.) ?Lack of peptidoglycan in the cell walls of Methanosarcina barkeri”.
Archives of Microbiology
113
(1?2), 57?60. o.
DOI
:
10.1007/BF00428580
.
PMID 889387
.
- ↑
(1998. aprilis 1.) ?
Cell wall polymers in Archaea (Archaebacteria)
”.
Cellular and Molecular Life Sciences
54
(4), 305?308. o.
DOI
:
10.1007/s000180050156
.
PMID 9614965
.
Ez a szocikk reszben vagy egeszben a
Peptidoglycan
cim? angol Wikipedia-szocikk
ezen valtozatanak
forditasan alapul.
Az eredeti cikk szerkeszt?it annak laptortenete sorolja fel. Ez a jelzes csupan a megfogalmazas eredetet es a szerz?i jogokat jelzi, nem szolgal a cikkben szerepl? informaciok forrasmegjelolesekent.
Tovabbi informaciok
[
szerkesztes
]