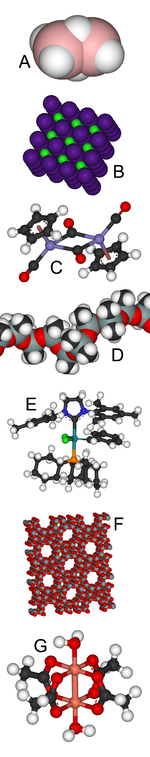
 Diversos compostos inorganicos que mostran unha gran variedade de estruturas.
Diversos compostos inorganicos que mostran unha gran variedade de estruturas.
Quimica inorganica
ou
quimica mineral
e a rama da
quimica
que estuda os
elementos quimicos
e as
substancias
da natureza que non posuen o
carbono
ordenado en cadeas; Como parte da quimica, investiga as estruturas, propiedades e a explicacion do mecanismo das reaccions e transformacions dos elementos non organicos, e dicir, os que non posuen enlaces carbono-hidroxeno, que pertencen ao campo da
quimica organica
.
[
1
]
Esta separacion, non obstante, non e sempre clara, como por exemplo na
quimica organometalica
que e unha superposicion de ambas.
[
2
]
Os materiais inorganicos comprenden cerca do 5% das substancias existentes no planeta
Terra
.
As areas de estudo en quimica inorganica son a
taboa periodica dos elementos
, e o estudo da quimica de cada elemento e os seus compostos.
Diferencianse tres grandes grupos:
O nome ten a sua orixe na epoca en que todos os compostos do carbono se obtinan de seres vivos; por iso a quimica do carbono foi denominada
quimica organica
. A quimica de compostos sen carbono, foi, polo tanto, chamada quimica inorganica.
Actualmente obtenense compostos organicos no
laboratorio
, de forma que a separacion e artificial. Algunhas das substancias con carbono que entran no campo da quimica inorganica incluense nalgun destes grupos:
Moitos materiais inorganicos e alguns nutrientes xa eran conecidos na antiguidade: a obtencion de metais (
ouro
,
prata
,
cobre
,
estano
,
ferro
,
chumbo
ou
mercurio
) a partir de minerais, a industria
ceramica
, a preparacion de
vidro
en
Exipto
, a producion de
porcelana
na
China
, os colorantes minerais (
acetato de cobre (II)
,
albaialde
,
cinabrio
,
auripigmento
), o uso do
xofre
, o
cal
para argamasas empregadas en construcions, ademais de sales como o
sal comun
para o preparacion de alimentos, o
natron
para a producion de vidro e
xabons
e o
alume
.
Durante o periodo da
alquimia
, os metodos de preparacion de
acido sulfurico
,
acido clorhidrico
,
acido nitrico
e
auga rexia
(mestura de clorhidrico e nitrico usada para disolver o ouro) xa eran conecidos polos arabes. O proceso de fabricacion de acidos foi posteriormente mellorado de xeito significativo por
Johann Rudolph Glauber
a mediados do seculo XVI.
Robert Boyle
desenvolveu a sua obra magana
The Sceptical Chymist
, abandonando as teorias aristotelicas da alquimia e contemplando a pescuda experimental e as conclusions con base en experimentos.
Georg Ernst Stahl
e
Johann Joachim Becher
desenvolveron, en 1700, a
teoria do floxisto
. Esta teoria, que se mantivo durante 80 anos ata ser refutada, afirmaba que as substancias susceptibeis de sufrir combustion continan floxisto, e que o proceso de combustion consistia basicamente na perda desta substancia. A causa da mala interpretacion da teoria era o desconecemento da existencia do
oxixeno
.
Joseph Priestley
, estudando a composicion do ar, percibiu a existencia dunha substancia no ar que participaba dos procesos respiratorios e promovia reaccions de
oxidacion
de metais. A teoria de elementos de Boyle consideraba que un elemento quimico era unha pluralidade de atomos identicos e indivisibeis.
John Dalton
foi o primeiro que tabulou un conxunto de pesos atomicos de elementos e
Jons Jacob Berzelius
desenvolveu a linguaxe de formulas cunha ou duas letras latinas para os elementos quimicos.
 Unha das principais tarefas da
quimica inorganica
no
seculo XIX
foi a clasificacion e descubrimento de
elementos quimicos
. O quimico ruso
Dmitri Mendeleiev
foi quen os clasificou na
taboa periodica
e mesmo previu a existencia dalguns desconecidos no seu tempo. Na imaxe o monumento a taboa periodica na Facultade de Quimica e Tecnoloxia dos Alimentos da Universidade Eslovaca de Tecnoloxia en
Bratislava
.
Unha das principais tarefas da
quimica inorganica
no
seculo XIX
foi a clasificacion e descubrimento de
elementos quimicos
. O quimico ruso
Dmitri Mendeleiev
foi quen os clasificou na
taboa periodica
e mesmo previu a existencia dalguns desconecidos no seu tempo. Na imaxe o monumento a taboa periodica na Facultade de Quimica e Tecnoloxia dos Alimentos da Universidade Eslovaca de Tecnoloxia en
Bratislava
.
O periodo seguinte foi a busca de novos elementos quimicos, a determinacion dos seus pesos atomicos exactos e a sua caracterizacion mediante reaccions con outras substancias, sendo esta unha das tarefas mais importantes da quimica inorganica.
Lothar Meyer
e
Dmitri Mendeleev
ordenaron os elementos quimicos polo seu peso atomico e con base na capacidade de facer enlaces quimicos, orixinando a
taboa periodica
.
Svante Arrhenius
,
Jacobus Henricus van't Hoff
e
Wilhelm Ostwald
estimaron a
constante de disociacion
dos sales, os acidos e as bases en solucions acuosas.
Alfred Werner
cuestionou a validez das teorias e modelos aceptados na quimica organica, estruturando a nova quimica inorganica en termos dos conceptos de coordinacion e de
estereoquimica
. A quimica inorganica passou por un periodo de menor actividade, que se estendeu ata despois de 1940. Entre tanto, ese foi un periodo de renovacion conceptual, marcado polo xurdimento das teorias cuanticas. Coa
segunda guerra mundial
, o mundo ingresou na era atomica, marcada polo descubrimento dos elementos transuranicos e polos avances na
radioquimica
. A disponibilizacion de
isotopos
permitiu a realizacion de experimentos importantes sobre o comportamento cinetico e mecanistico dos compostos inorganicos, o que foi racionalizado por
Henry Taube
, en 1949, con base nas teorias de enlace. O entendemento loxico do caracter labil/inerte dos compostos de coordinacion lanzou a semente dos mecanismos de transferencia de electrons, propostos por Taube en 1953, definitivamente consagrados co premio Nobel que se lle outorgou en 1983.
A quimica inorganica descritiva centrase na clasificacion dos compostos en funcion das suas propiedades. En parte, a clasificacion centrase na posicion na
taboa periodica
do elemento mais pesado (o elemento co maior peso atomico) do composto, en parte agrupando os compostos polas suas similitudes estruturais. Ao estudar compostos inorganicos, adoitan clasificarse dentro das diferentes partes da quimica inorganica (un composto organometalico caracterizase pola sua quimica de coordinacion e a sua vez pode mostrar interesantes propiedades en estado
solido
).
Unha perspectiva alternativa na area da quimica inorganica comeza co
modelo
do atomo de
Bohr
e, empregando as ferramentas e modelos da
quimica teorica
e a
quimica computacional
, expandese cara a formacion de enlaces en moleculas simples e logo mais complexas. As descricions precisas da mecanica cuantica para as especies multielectronicas, que constituen o ambito da quimica inorganica, son dificiles. Este desafio xerou moitos enfoques semicuantitativos ou semiempiricos que incluen a
teoria dos orbitais moleculares
e a
teoria do campo dos ligantes
. Paralelamente a estas descricions teoricas, empreganse metodoloxias aproximadas, incluida a
teoria do funcional da densidade
.
As excepcions as teorias, cualitativas e cuantitativas, son extremadamente importantes no desenvolvemento deste campo. Por exemplo, o
Cu
II
2
(OAc)
4
(H
2
O)
2
e case diamagnetico por debaixo da temperatura ambiente, mentres que a
teoria do campo cristalino
predi que a molecula teria que ter dos electrons non pareados. O desacordo entre a teoria cualitativa (paramagnetica) e a observacion (diamagnetica) conduciu ao desenvolvemento de modelos para o "acoplamento magnetico". Estes modelos mellorados levaron ao desenvolvemento de novos materiais magneticos e novas tecnoloxias.
Na quimica inorganica existen catro grupos funcionais:
oxidos
,
acidos
,
bases
e
sales
.
[
3
]
A sua diferenciacion e simple: a partir de catro criterios descobrese a sua funcion.
[
3
]
- - O primeiro elemento do composto e un hidroxeno, H_ ,sendo enton un
acido
. (ex:
HCl
,
HF
)
[
3
]
- - Posue OH como ultimo elemento do composto, _OH , sendo enton unha
base
. (ex:
NaOH
,
AgOH
)
[
3
]
- - E un composto diatomico (dous elementos), no que o ultimo e oxixeno, _O , sendo enton un
oxido
. (ex:
CO
,
CaO
)
- - O primeiro elemento e un metal e o segundo elemento e un non-metal, sendo enton un
sal
.(ex:
NaCl
,
AgF
[
3
]
As principais ramas da quimica inorganica incluen:
- Minerais
, como o
sal
, o
amianto
, os
silicatos
etc.
- Metais
e as suas
aliaxes
, como o
ferro
, o
cobre
, o
aluminio
, o
laton
, o
bronce
etc.
- Compostos que estan formados por elementos non-metalicos, como o
silicio
, o
fosforo
, o
cloro
ou o
oxixeno
, por exemplo a
auga
.
- Compostos de coordenacion
que incluen metais de transicion e especies doadoras de
electrons
.
A quimica inorganica inclue:
 Imaxe dun microchip ou
circuito integrado
ampliado 2.400 veces. Os
semicondutores
inorganicos como o
silicio
son fundamentais para a sua fabricacion.
Imaxe dun microchip ou
circuito integrado
ampliado 2.400 veces. Os
semicondutores
inorganicos como o
silicio
son fundamentais para a sua fabricacion.
Hai moitos
compostos
e
substancias
inorganicas de grande importancia, comercial e bioloxica. Entre eles:
A quimica inorganica esta baseada na
fisico-quimica
e forma a base para a
mineraloxia
. Frecuentemente posue elementos comuns coa
xeoquimica
, a
quimica analitica
, a
quimica ambiental
e a
quimica organometalica
.
O abano da quimica inorganica inclue compostos moleculares, os cales poden existir como
moleculas
discretas, e
cristais
(estudados pola
cristalografia
e a
quimica do estado solido
).