 Si ce bandeau n'est plus pertinent, retirez-le. Cliquez ici pour en savoir plus.
Si ce bandeau n'est plus pertinent, retirez-le. Cliquez ici pour en savoir plus.
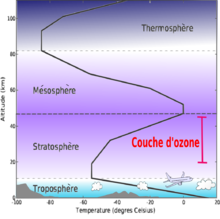 Les differentes couches de l'
atmosphere terrestre
.
Les differentes couches de l'
atmosphere terrestre
.
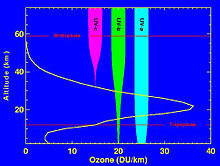 Filtration des UV par la stratosphere.
Filtration des UV par la stratosphere.
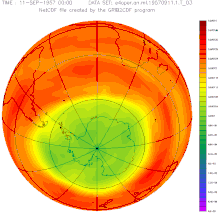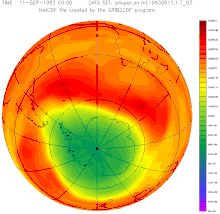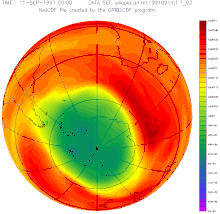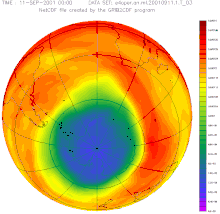 Concentration et ≪
trou d'ozone
≫ au-dessus de l'hemisphere sud.
Concentration et ≪
trou d'ozone
≫ au-dessus de l'hemisphere sud.
 Modelisation de la disparition de la couche d'ozone :
Ce qui serait arrive si les CFC n'avaient pas ete interdits
Modelisation de la disparition de la couche d'ozone :
Ce qui serait arrive si les CFC n'avaient pas ete interdits
La
couche d'ozone
ou
ozonosphere
est la partie de la
stratosphere
de la
Terre
qui contient une quantite relativement importante d'
ozone
(concentration de l'ordre de un pour cent mille). A haute altitude, la couche d'ozone est utile : elle absorbe la plus grande partie du
rayonnement solaire
ultraviolet
dangereux pour les
organismes
. Elle a donc un role protecteur pour les
etres vivants
et les
ecosystemes
.
Cette couche est distincte de l'
ozone tropospherique
de plus basse altitude, qui est un
gaz a effet de serre
et un
polluant
.
L'existence de la couche d'ozone a ete demontree en 1913 par les physiciens francais
Henri Buisson
et
Charles Fabry
grace a leur
interferometre optique
. Cet ozone est produit par l'action des
UV
, du rayonnement solaire, sur les molecules de
dioxygene
a haute altitude
[
N 1
]
.
Sydney Chapman
propose le mecanisme de formation en 1930. Elle renvoie les rayons solaires et n'en laisse penetrer que 50 % dans la
troposphere
.
A la fin des annees 1970, notamment grace aux campagnes de mesures par ballon-sondes, les scientifiques mettent en evidence une diminution periodique de l'ozone antarctique, phenomene alors baptise ≪ trou de la couche d'ozone ≫. Ce trou grandit au printemps dans l'Antarctique (a la fin de la
nuit polaire
) durant plusieurs mois avant de se reduire, jusqu'au printemps suivant ou il s'etend a nouveau. D'autres etudes a partir de
ballons
evoluant a haute
altitude
et d'
observation satellitaire
et
meteorologiques
revelent que la proportion d'ozone arctique est aussi en diminution.
Cette decouverte est a l'origine de la creation du
GIEC
et de la signature en 1987 du
Protocole de Montreal
visant a bannir la creation par l'industrie de substances chimiques chlorees aboutissant a la
destruction de la couche d'ozone
. Ces substances sont principalement les
CFC
utilises dans les systemes de refroidissements (refrigerateurs, climatiseurs…).
Ozone (utile ou nocif selon son altitude)
[
modifier
|
modifier le code
]
Selon son altitude, on considere l'ozone comme :
- ≪ bon ozone ≫, quand il est present dans la stratosphere
[
N 2
]
:
bon
, car il nous protege des rayons
UV-C
(ultraviolet) et de leurs effets ;
- le ≪
mauvais ozone
≫, quand il se forme dans la
troposphere
(couche basse de l'atmosphere
[
N 3
]
) :
mauvais
, car c'est celui que toutes les especes animales, dont l'homme, sont amenees a inhaler et qui presente, selon sa concentration, une certaine toxicite (voir
Normes de qualite de l'air
).
Sans la couche d'ozone dans la haute atmosphere, la vie telle que la planete l'a connue depuis la fin de l'
Archeen
, n'aurait ete possible que dans les
oceans
[ref. necessaire]
, a une profondeur suffisante de la surface des eaux (les UV ne penetrant qu'a quelques metres sous la surface). Ce fut le cas au cours de l'
eon
Archeen, lorsque l'
atmosphere de la Terre
etait depourvue de dioxygene (et donc de couche d'ozone).
Il se forme et persiste entre 20 et 40
km
d'altitude. Il est cependant en realite tres dilue dans l'atmosphere locale : sa teneur est de l'ordre de quelques ppm a quelques dizaines de ppm dans la couche d'ozone elle-meme qui est un melange gazeux a faible pression.
En fait si cet ozone etait regroupe en une couche a l'etat pur, il aurait dans les
conditions normales de temperature et de pression
(c'est-a-dire les conditions moyennes a la surface de la Terre) une epaisseur de seulement 3
mm
, soit 300
unites Dobson
(DU)
[
N 4
]
.
 Lancement d'un ballon sonde pour des mesures dans la couche d'ozone.
Lancement d'un ballon sonde pour des mesures dans la couche d'ozone.
L'ozone est produit a partir du
dioxygene
, compose de deux
atomes
d'
oxygene
(O
2
). Aux altitudes superieures a 30
km
, le
rayonnement solaire
possede encore une
energie
suffisante pour casser une partie des
molecules
de dioxygene et liberer les atomes. Un atome d'oxygene tendant a ne pas rester seul pour des raisons de stabilite, doit se recombiner a un autre
element
; il interagit donc avec une autre molecule de dioxygene (O
2
) presente pour former une nouvelle molecule, composee de trois atomes d'oxygene : l'ozone (O
3
).
O
2
+ rayonnement solaire → O + O et O + O
2
→ O
3
Cette
reaction chimique
est la seule qui, dans la
stratosphere
, produise de l'ozone. Mais puisque tout l'oxygene n'est pas transforme en ozone dans ce processus, il existe donc un facteur limitant sa concentration. Primitivement, une certaine quantite d'ozone est apparue, il y a plus de deux milliards d'annees, lorsque l'oxygene est devenu permanent avec une concentration de l'ordre du pour cent. La concentration observee aujourd'hui resulte d'un equilibre entre la production d'ozone par le rayonnement solaire, et certains processus de destruction : en temps normal, tout l'ozone produit en ≪ trop plein du reservoir ≫ est detruit. C'est ce que l'on appelle un
equilibre dynamique
.
Le jour, a haute altitude, le rayonnement solaire peut dissocier la molecule d'ozone en une molecule de dioxygene et un atome d'oxygene :
O
3
+ rayonnement → O
2
+ O
Durant la nuit et en particulier la
nuit polaire
, cette reaction n'existe pas puisqu'il n'y a plus de rayonnement solaire. Une autre reaction devient alors preponderante : la recombinaison d'un atome d'oxygene et d'une molecule d'ozone pour donner deux molecules de dioxygene :
O
3
+ O → 2 O
2
C'est ce que l'on appelle la decomposition spontanee de l'ozone. Mais l'ensemble de ces deux reactions ne peut rendre compte que de 20 % de la destruction naturelle de l'ozone, alors que pour parvenir a un equilibre il faut que la perte soit egale a la production. Ce probleme met en evidence la fragilite de l'equilibre de l'ozone. En effet, si les deux reactions ci-dessus avaient pu suffire a compenser la surproduction d'ozone, l'equilibre de ce dernier ne dependrait que de la quantite de dioxygene present dans la haute atmosphere, et cet equilibre aurait ete difficilement perturbable, mais les
composes chlores
perturbent cet equilibre. Les composes
bromes
, et les
oxydes d'azote
(NOx) contribuent egalement a cette destruction.
Parvenues dans la stratosphere, les molecules de composes chlores sont decomposees par le
rayonnement solaire
, les produits de cette decomposition detruisant les molecules d'ozone par le jeu de
reactions catalytiques
[
N 5
]
.
Une source naturelle abondante de
chlore
organique est le
chlorure de methyle
, principalement produit dans les
oceans
par les
micro-organismes
et les
algues
[
1
]
. La concentration ne depasse pas 0,6 milliardieme, limite naturelle du taux de chlore organique dans l'atmosphere.
Inventes dans les annees 1930, les
chlorofluorocarbures
(C.F.C.) ont connu un developpement important a partir des annees 1950 a cause de leurs proprietes remarquables (ininflammables, facilement compressibles, non solubles) et, comme ils n'ont qu'une faible reactivite chimique, on les croyait peu toxiques pour l'
environnement
. Utilises principalement dans l'
industrie du froid
, dans les bombes
aerosols
comme propulseur, en solvants pour l'industrie
electronique
, dans les mousses synthetiques et les agents extincteurs ; ils sont essentiellement dus a l'activite humaine. La production des CFC est tres importante. Pour les deux principaux, le
trichlorofluoromethane
(CFC 11) et le
dichlorofluoromethane
(R 21), la production est passee de 50 000 a 100 000
t
au debut des annees 1960 jusqu'a 500 000
t
en 1999. Cela represente une croissance de 5 a 6 % par an, soit pratiquement un doublement de la quantite tous les dix ans.
Les vents brassent l'atmosphere en permanence :
- horizontalement, avec un temps moyen de transport d'un
pole
a l'autre de l'ordre de deux ou trois ans ;
- verticalement, avec une homogeneisation de l'atmosphere jusqu'a 80
km
d'
altitude
.
En deux ou trois ans, les CFC se retrouvent donc dans l'atmosphere sous toutes les
latitudes
, aussi bien a l'
equateur
qu'aux poles. Puis, en 15 ans, ils montent dans la haute atmosphere.
A cela s'ajoute un autre effet, les CFC presents dans la stratosphere en 1997 sont ceux qui ont ete produits entre 1977 et 1982, ce qui ne represente que 40 % de ce qui a ete produit jusqu'a ce jour. Les 60 % restants sont encore en train de se melanger et de monter. Du fait de ce retard, les effets des CFC produits ces dernieres annees se feront encore sentir dans 60 ans.
Ainsi, la quantite de chlore organique naturellement presente dans la stratosphere est d'environ 0,6 milliardieme, alors qu'aujourd'hui la proportion totale de chlore organique atteint 3,5 milliardiemes. Elle a ete multipliee par 5 en 20 ans, ce qui a entraine une rupture de l'equilibre dynamique.
En hiver, la destruction d'ozone est limitee a sa destruction spontanee. Au printemps, elle devient tres importante car il y a deja des UV, beaucoup de cristaux de glace dans la
stratosphere
et parce que la circulation atmospherique, le
vortex
polaire autour de l'Antarctique, empeche le remplacement de l'ozone detruit par de l'ozone provenant du nord de l'Antarctique.
Des la fin du printemps, l'amincissement est moins important parce que la quantite de cristaux de glace diminue, et aussi parce que la circulation atmospherique change : il y a alors un melange entre l'air antarctique et l'air venu du nord qui apporte de l'ozone. Enfin, et surtout, la generation de l'ozone a partir de l'oxygene a repris avec l'allongement de l’ensoleillement diurne.
 Carte du trou d'ozone au-dessus de l'Antarctique le 15 octobre 1987.
Carte du trou d'ozone au-dessus de l'Antarctique le 15 octobre 1987.
La couche d'ozone est aujourd'hui, observee par un reseau de stations au sol tel la station Halley, a 76° S, ou des observations de l’ozone sont effectuees depuis 1956. Plus recemment, la precision des observations s'est amelioree grace aux satellites artificiels construits, entre autres, par la NASA (USA).
Les variations pluriannuelles depuis 1957 de l'epaisseur de la couche d'ozone peuvent aussi etre mesurees par le taux de
flavonoides
contenus dans des
mousses
(notamment
Bryum argenteum
) conservees dans des herbiers
[
2
]
. Cependant, les observations serieuses de la couche d'ozone n'ont ete realises que depuis une soixantaine d'annees
[
3
]
.
C'est en 1985 que l'alerte a ete donnee avec la decouverte d'une diminution importante de la concentration d'ozone au cours des mois de septembre et d'octobre au-dessus du continent
Antarctique
. Une reduction de pres de 50 % du contenu total d'ozone etait observee, se produisant au cours du printemps austral et couvrant toute la surface de l'Antarctique.
Depuis la fin des annees 1970, l'epaisseur de l'ozone est passee, en certains endroits, de l'equivalent de 3
mm
a 2 et meme 1,5
mm
aujourd'hui, en moyenne pour le mois d'octobre.
C'est cette
diminution relative de l'epaisseur de la couche d'ozone stratospherique
(par rapport a son epaisseur standard ou initiale de 300 DU), que l'on nomme ≪ trou d'ozone ≫ ou ≪ trou dans la couche d'ozone ≫. Le protocole de Montreal en 1987, a permis a la communaute internationale de realiser une prise de conscience , aboutissant a des mesures concretes pour limiter la propagation humaine des gaz CFC.
En 2000, 2001 et 2003, le trou dans la couche d'ozone a atteint une superficie jamais observee avant 2000, alors que celui de 2002 etait le plus petit qui ait ete observe depuis 1998.
En effet, a la fin de l'ete 2003, le trou a de nouveau atteint un record de superficie… pour diminuer rapidement durant le mois d'octobre. En 2006, un nouveau record a ete enregistre au-dessus de l'Antarctique.
En 2006, l'
ONU
et les experts alertent sur le fait que la couche d'ozone se reconstitue moins vite que prevu, en raison probablement de l'utilisation persistante de gaz interdits, de type CFC.
L'utilisation d'un modele a permis d'attribuer la pause observee en 2015 a l'eruption du volcan chilien
Calbuco
et de montrer que la baisse des concentrations de
chlore
et de
brome
etait bien responsable de l'amelioration observee sur le long terme
[
4
]
.
Dans l'
ocean
Arctique, l'ampleur du phenomene n'atteint pas encore celle qui est observee dans l'hemisphere sud.
Le fait que la perte d'ozone, si importante en
Antarctique
, soit moindre au-dessus de l'
Arctique
decoule des differences climatiques entre ces deux regions. Le refroidissement de la stratosphere polaire est en effet moins intense au nord ou, en moyenne, les
temperatures
sont de 15 a
20
°C
superieures a celles observees au
pole Sud
.
Cette difference entre les deux poles est d'origine
geographique
: le continent antarctique est isole au milieu des oceans dans l'hemisphere sud. Dans l'hemisphere nord, au contraire, une alternance de continents et d'oceans, de zones de hautes et de basses
pressions atmospheriques
contribue a creer un mouvement continu des masses d'air tel que le pole Nord ne reste jamais totalement isole. L'air des latitudes moyennes, plus chaud, arrive donc toujours au pole, y augmentant ainsi les temperatures moyennes.
En exploitant des donnees fournies par un satellite de la
NASA
charge de la recherche de la haute atmosphere, les chercheurs ont remarque que les
nuages
stratospheriques de l'Antarctique ont une duree de vie deux fois plus longue que ceux situes au-dessus de l'Arctique.
Le satellite
MetOp-A
a observe le trou d'ozone en 2007.
En 2011, le trou dans la couche d'ozone a atteint des valeurs record dans l'Arctique, avec une perte de 80 % de l'ozone, entre 15 et
20
km
d'altitude, dans la periode d'hiver 2010 - printemps 2011
[
5
]
.
Toutefois, en 2014, un rapport de L’Union meteorologique mondiale et du Programme des Nations unies pour l’environnement faisait etat d’une stabilisation et meme d’un debut de resorption sous les latitudes moyennes de l’hemisphere nord
[
6
]
. En juin 2016, une etude dirigee par Susan Salomon et publiee dans la revue
Science
concluait a une reduction du trou dans la couche d'ozone en Antarctique de plus de 4 millions de kilometres carres depuis 2000, soit environ la moitie de la superficie des Etats-Unis. Selon les chercheurs, cette amelioration, qui restait a confirmer, s’expliquait pour partie par la diminution des emissions de gaz chlores (les CFC notamment) et bromes ; mais aussi par
l'effet de serre anthropique
. En effet, le rechauffement induit par les gaz a effet de serre (CO
2
, methane, etc.) provoque paradoxalement un refroidissement de la stratosphere. Or comme l’explique Slimane Bekki, chercheur au CNRS : ≪ ce refroidissement ralentit les reactions chimiques qui detruisent l’ozone ≫
[
7
]
.
En 2018, l'ONU indique que la couche d'ozone est en voie de guerison
[
8
]
. Neanmoins, une etude publiee dans Science revele que le rythme de reduction des emissions de CFC-11 s'est ralenti de 50?% depuis 2012, traduisant une nouvelle production de CFC-11 non declaree a l'encontre du protocole de Montreal
[
9
]
. Cette production est suspectee de provenir d'industriels chinois
[
10
]
,
[
11
]
.
Effets des ultraviolets sur les organismes vivants
[
modifier
|
modifier le code
]
Les
ultraviolets
sont des agents
mutagenes
: ils deteriorent l'
ADN
des cellules, ce qui deregle leurs activites biologiques (
ex. :
cancer
) ou les detruit (
coup de soleil
).
Le
, au sud du
Chili
, la couche d'ozone qui avait perdu 50 % de son epaisseur habituelle, offrait si peu de protection contre les ultraviolets que ce jour-la, il suffisait de passer cinq minutes dehors sans protection pour attraper un coup de soleil
[ref. necessaire]
. Le sud du Chili n'est pas la seule zone atteinte, d'autres regions de l'
Australie
et de la
Nouvelle-Zelande
ont egalement connu des episodes semblables. De plus, les rayons ultraviolets perturbent les
divisions cellulaires
des
micro-organismes
aquatiques, ce qui a de graves consequences sur la vie aux poles
[
N 6
]
. En plus des
cancers
de la peau, on observe aussi un affaiblissement general du
systeme immunitaire
.
Sur la
planete Mars
, trois couches d'ozone distinctes ont ete identifiees dans
son atmosphere
. Une couche est situee en dessous de 30
km
d'altitude, une autre est presente durant le printemps et l'ete de l'hemisphere nord martien (entre 30 et 60
km
) et une autre au-dessus du pole sud entre 40 et 60
km
. La couche presente au-dessus du pole sud n'a pas d'equivalent au pole nord
[
12
]
.
Le
Protocole de Montreal
, signe en septembre 1987 puis revise a
Londres
,
Copenhague
,
Montreal
et
Pekin
jusqu'en 1999, a preconise une diminution des emissions de CFC de 50 % en dix ans. Sa ratification universelle (196 pays) a ete atteinte en 2009, ce qui constitue un evenement puisqu'il est le premier traite environnemental international a atteindre ce statut.
L'
Union europeenne
a propose en 1989 une interdiction totale de l'utilisation des CFC (
chlorofluorocarbure
) durant les annees 1990, qui fut approuvee par les
Etats-Unis
. L'Union europeenne s'est ensuite dotee d'outils juridiques, dont le reglement europeen (1005/2009) visant a transposer le Protocole de Montreal en droit europeen, tout en fixant des objectifs plus ambitieux de reduction ou d'interdiction de certains gaz detruisant la couche d'ozone.
Les delegues de 190 pays reunis a
Montreal
le
ont pu saluer, vingt ans apres la signature du protocole, la reussite du projet qui se concretise par un arret total de la production des
chlorofluorocarbures
prevu en 2010 et une estimation optimiste de la communaute scientifique : la couche d'ozone retrouvera normalement son etat de 1980 entre 2055 et 2065.
Il etait prevu d'eliminer les
hydrochlorofluorocarbures
, les principaux substituts des chlorofluorocarbures, d'ici a 2020 pour les pays industrialises et 2040 pour les pays en voie de developpement. Des chercheurs ont etabli recemment que l'elimination precoce (dix ans plus tot, soit en 2030) des hydrochlorofluorocarbures reduirait l'effet de serre dans une proportion superieure a ce que doit permettre le
Protocole de Kyoto
sur le changement climatique. Un accord a ete conclu, lors de cette
19
e
reunion des parties qui permet une acceleration de la sortie de l'utilisation des hydrochlorofluorocarbures. En vertu de cette entente, la production de ces substances sera gelee en 2013 a son niveau moyen de 2009-2010. Les pays industrialises arreteront la production et la consommation en 2020, reduisant celles-ci a 75 % en 2010 et 90 % en 2015
[
N 7
]
. Les pays en developpement reduiront de 10 % en 2015, 35 % en 2020, 67,5 % en 2025, gardant 2,5 % en moyenne sur les cinq dernieres annees pour la maintenance.
Si le lien de causalite entre CFC et trou est demontre ou si ce dernier disparait sur une longue periode on pourra etablir que le
Protocole de Montreal
a ete un succes de la communaute internationale, capable de resoudre des problemes environnementaux.
Un rapport scientifique de l'
ONU
, publie en janvier 2023, indique que la couche d'ozone est ≪ en bonne voie ≫ pour se reconstituer en 40 ans. Cependant, certains projets tels que l'injection de particules dans l'atmosphere, ≪ pourrai[en]t avoir pour consequence une grave baisse du niveau de l'ozone ≫, selon le copresident du panel scientifique
[
13
]
.
- ↑
Entre 20 et 50
km
d'altitude.
- ↑
objet de cet article
- ↑
Du sol a environ 20
km
d'altitude.
- ↑
≪ DU ≫ en anglais,
Dobson Unit
en hommage au specialiste anglais G.M.B Dobson, un des premiers scientifiques a etudier la couche d'ozone et inventeur du
spectrometre Dobson
. Une unite DU correspond a 0,01
mm
d'epaisseur a temperature et pression atmospherique standard.
- ↑
Catalytique
signifie que le constituant qui attaque l'ozone est regenere a la fin de la reaction. A travers une succession de ces reactions en chaine, un unique atome d'un constituant peut donc permettre la destruction d'un tres grand nombre de molecules d'ozone (de l'ordre de 10 000 a 100 000). Des lors, des constituants dont l'abondance relative ne se chiffre pourtant qu'en milliardiemes peuvent suffire a controler chimiquement l'equilibre de l'ozone, dont l'abondance relative est pourtant mille fois superieure.
- ↑
L'arrivee des
ultraviolets
provoque non seulement des
cancers de la peau
, mais aussi des
mutations
de l'
ADN
des organismes vivants. Ces modifications consistent en la realisation d'une nouvelle liaison, notamment entre deux
thymines
situees sur le meme brin d'ADN. Ces deux thymines forment alors un
dimere
de
thymine
qui perturbe le fonctionnement des
cellules
de peau et qui peut provoquer leur mort. Toutefois, ces cellules possedent un mecanisme de reparation (
NER
) capable de dissocier les dimeres de thymines eventuellement formes apres une exposition aux UV.
- ↑
0,5 % sont autorises pour la maintenance
- ↑
Haute Atmosphere: Chimie du Chlore
Sur le site
Societe Max-Planck
atmosphere.mpg.de
- ↑
(en)
G. Ryan Ken
et al.
≪ Historical ozone concentrations and flavonoid levels in herbarium specimens of the Antarctic moss Bryum argenteum ≫
Global change biology
. 2009;15:1694-702.
- ↑
≪
Surveillance mondiale de l’ozone atmospherique
≫, sur
Organisation meteorologique mondiale
,
(consulte le
)
.
- ↑
(en)
≪
Ozone layer on the mend, thanks to chemical ban
≫, sur
Science
,
(consulte le
)
.
- ↑
(en)
≪
NASA Leads Study of Unprecedented Arctic Ozone Loss
≫, NASA
.
- ↑
article du journal
Le Monde
du 10 septembre 2014
- ↑
article du journal
Le Monde
du
1
er
juillet 2016
- ↑
≪
La couche d'ozone est en voie de guerison, se felicite l'ONU
≫, sur
ONU Info
,
(consulte le
)
.
- ↑
(en)
James W. Elkins, ≪
An unexpected and persistent increase in global emissions of ozone-depleting CFC-11
≫, sur
Nature
,
(
DOI
10.1038/s41586-018-0106-2
, consulte le
)
.
- ↑
fr, ≪
Un gaz nefaste pour la couche d'ozone, pourtant interdit, repere en Chine - Sciences et Avenir
≫, sur
Sciences et Avenir
,
(consulte le
)
.
- ↑
Tristan Vey, ≪
Couche d’ozone : la Chine emet en toute illegalite un gaz destructeur
≫, sur
lefigaro.fr
,
(
ISSN
0182-5852
, consulte le
)
.
- ↑
(en)
≪
A seasonal ozone layer over the martian south pole
≫, sur
sci.esa.int
,
.
- ↑
≪
Environnement : la couche d'ozone "en bonne voie" pour se reconstituer en quatre decennies, selon un rapport scientifique de l'ONU
≫
 , sur
France Info
,
(consulte le
)
, sur
France Info
,
(consulte le
)
Sur les autres projets Wikimedia :
- M.T. Abdoulwahab,
Etude de la variabilite et la tendance de l'ozone stratospherique au-dessus des tropiques et subtropiques sud
, these de doctorat, universite de la Reunion, 2016
- Gerard Megie
,
L'ozone stratospherique
, Londres/Paris/New York, Tec & Doc Lavoisier,
coll.
≪ Rapport de l'Academie des sciences ≫,
, 271
p.
(
ISBN
2-7430-0256-5
,
presentation en ligne
)
- Patrick Aimedieu
,
L'ozone stratospherique
, Paris,
Presses universitaires de France
,
coll.
≪
Que sais-je ?
≫,
, 127
p.
(
ISBN
2-13-047443-8
)
- (en)
Sophie Godin-Bekkmann, Paul A. Newnan et Irina Petropavlovskikh, ≪
30th Anniversary of the Montreal Protocol : From the safeguard of the ozone layer to the protection of the Earth Climate
≫,
Comptes Rendus Geoscience
,
vol.
350,
n
o
7,
,
p.
331-448
, un numero special consacre a l'apres-Montreal