Als
Salinitat
(von
lateinisch
salinitas
) bezeichnet man (vereinfachend) den
Salzgehalt
eines
Gewassers
,
Wasserkorpers
bzw.
Wassers
. Im einfachsten Fall wird sie als Massenanteil in g/kg (Gramm Salz pro Kilogramm Salzwasser bzw. Losung) oder in Prozent angegeben (1 % entspricht 10 g/kg).
Die Salinitat kann mit Hilfe eines
Salinometers
bestimmt werden. Dabei wird ausgenutzt, dass die
elektrische Leitfahigkeit
des Wassers proportional zum Salzgehalt ist.
[1]
In der
Ozeanographie
ist die Salinitat eine wichtige Kenngroße bei der Bestimmung von Wassermassen und
Meeresstromungen
.
Mit der Salinitatsbestimmung will man herausfinden, wie viel Salz in einer Menge von Wasser gelost ist. Der Salzgehalt ist zusammen mit dem
Druck
und der
Temperatur
fur die
Dichte
beziehungsweise die
potentielle Dichte
des Wassers verantwortlich. Damit haben unterschiedliche Salzgehalte großen Einfluss auf die Meeresstromungen.
Die ursprunglichste Methode ist die Verdunstung von Wasser und die Wagung dessen, was nicht verdunstet ist.
Das Problem ist, dass Wasser dabei in Salzkristallen eingeschlossen werden kann. Um dieses Wasser aus den Salzkristallen zu losen, sind hohe Temperaturen notwendig. Durch die hohe Temperatur zerfallen jedoch einige Salze (z. B. MgCO
3
→ MgO + CO
2
).
Schon
Robert Boyle
stellte im 17. Jahrhundert fest, dass die Trocknung und Wagung von Meerwasser zu wenig reproduzierbaren Ergebnissen fur die Konzentration von gelosten Substanzen fuhrte.
Im 19. Jahrhundert wurde das
Marcet
-Prinzip oder auch das Gesetz der konstanten Proportionen formuliert. Es besagt: Ungeachtet wie stark sich die Salinitat von Ort zu Ort unterscheidet, die Anteile der wichtigsten Ionen (engl. Major Ions) im Wasser des offenen Ozeans sind fast konstant.
Anfang des 20. Jahrhunderts kamen neue Methoden zur Bestimmung des Salzgehaltes auf.
Um reproduzierbare Ergebnisse zu bekommen, wurde eine erste strikte Definition eingefuhrt.
?Salinitat ist definiert als das Gewicht in Gramm der gelosten anorganischen Stoffe in einem Kilogramm Seewassers, nachdem alle
Bromide
und
Iodide
mit der gleichen Menge an
Chloriden
ersetzt wurden und alle Kohlenstoff-Verbindungen oxidiert wurden.“ D. h. alle Kohlenstoffverbindungen gasen als CO
2
aus.
Dazu wurde das Seewasser, HCl und gesattigtes Chlorwasser getrocknet, fur 72 Stunden bei 480 °C erhitzt und schließlich das ruckstandige Chlorid
titriert
.
Diese Methode brachte nun zwar reproduzierbare Ergebnisse, war aber sehr umstandlich und zur Anwendung auf See nur sehr bedingt geeignet.
Durch das Gesetz der konstanten Proportionen ist es moglich, aus dem Gehalt eines Salzes den Gehalt der restlichen Salze recht genau abzuschatzen.
Mit Hilfe der
Mohr-Titration
konnte die Menge der
Halogeniden
in Seewasser bestimmt werden. Bei der Anwendung mit Seewasser fallt neben Silberchlorid noch Silberbromid und Silberiodid aus, welches nun gewogen werden kann. Damit die Ergebnisse
prazise
sind, wird die Silbernitrat-Losung gegen sogenanntes Standard-Seewasser mit bekannter Chlorinitat geeicht.
Um nun aus der ermittelten Chlorinitat die Salinitat zu berechnen, maß Sørensen die Salinitat von neun Seewasserproben direkt und bestimmte außerdem die Chlorinitat. Die daraus abgeleitete Korrelation war:
Salinitat [‰] = 1,805 · Chlorinitat [‰] + 0,030
.
Diese Methode ist sehr genau und auch auf See wesentlich besser anwendbar als die von 1902.
Wie die Addition eines konstanten Wertes in der obigen Korrelation schon vermuten lasst, gab es jedoch ein Problem. Die neun Proben stammten zum Teil aus der Ostsee. Die Ostsee hat jedoch eine andere Ionenkomposition als der offene Ozean. Dieser Fehler wurde durch eine neue Kalibrierung nach nun 60 Jahren korrigiert:
Salinitat [‰] = 1,80655 · Chlorinitat [‰]
Dieser Artikel oder Abschnitt bedarf einer grundsatzlichen Uberarbeitung. Naheres sollte auf der
Diskussionsseite
angegeben sein. Bitte hilf mit, ihn zu
verbessern
, und entferne anschließend diese Markierung.
Die
Practical Salinity Scale
(PSS-78
[2]
[3]
) beruht auf der Proportionalitat von Salzgehalt und
elektrolytischer Leitfahigkeit
und ist dimensionslos. Haufig findet man jedoch zur Angabe der Salinitat nachfolgend ein PSU, welches fur Practical Salinity Unit steht. Dies ist keine physikalische Einheit.
Zur Errechnung des Salzgehaltes aus der Leitfahigkeit wird folgende Formel benutzt:
[2]

Dabei gibt
K
15
das Verhaltnis von der gemessenen Leitfahigkeit zur Leitfahigkeit einer Kalium-Chlorid-Losung von 32.4356 g/kg bei 15 °C und bei einem Druck von einem Bar an. Die Große
S
heißt
praktische Salinitat
. Ist das Verhaltnis
K
15
gleich eins, ist
S
= 35.
Die Messung der Leitfahigkeit erfolgt meist automatisiert mit Hilfe einer
Conductivity Temperature Depth
-Sonde (
CTD
), auf Deutsch einer Leitfahigkeit-Temperatur-Tiefensonde.
Im Jahr 2010 nahm die
Intergovernmental Oceanographic Commission
den Standard
TEOS-10
an (
Thermodynamic Equation Of Seawater - 2010
). Teil des neuen Standards war die Einfuhrung der absoluten Salinitat, d. h. des Masseanteils von Salz im Wasser, als Kenngroße fur Meerwasser. Die absolute Salinitat wird ublicherweise in g/kg angegeben.
[4]
[5]
Durch den Einfluss von
Wetter
und
Gezeiten
unterliegt die Salinitat naturlichen Schwankungen. Zum einen das Ansteigen der Salinitat durch Verdunstung bei
Ebbe
in ufernahen Bereichen (
Wattenmeer
,
Gezeitentumpel
) bis hin zur Ausbildung von
Salzwiesen
, zum Beispiel durch langere Sonnenperioden nach
Sturmfluten
. Bei Vorliegen einer wasserundurchlassigen Bodenschicht kann sich in
Marschgebieten
stark salzhaltiges flaches
Grundwasser
bilden, das auf der Insel
Læsø
im
Kattegat
eine Salinitat von bis zu 15 Prozent erreicht. Eine Herabsetzung der Salinitat kann sich durch
Sußwassereintrag
in Flussmundungen, in
Schmelzwasserzonen
und bei starkem
Regen
ergeben.
Auch wenn Meerwasser gefriert, bleibt Salz zuruck. Zwar befindet sich das Salz nach dem Gefrieren zunachst im Eis, ein Großteil diffundiert aber heraus und gelangt wieder ins Meerwasser, dessen Salzgehalt dadurch steigt.
[Beleg?]
Der Salzgehalt an der Wasseroberflache unterscheidet sich typischerweise von Meer zu Meer. Im Ostseeraum, wo die Niederschlage (mit eingerechnet die Landflache, aus der die
Ostsee
gespeist wird) wesentlich großer sind als die Verdunstung, wird das Oberflachenwasser verdunnt. Je weiter man nach Osten kommt, desto geringer ist die Oberflachensalinitat. Die Verdunnung des Oberflachenwassers fuhrt zu einer stabilen Wasserschichtung, wo salzarmes Ostseewasser uber salzreicherem, aus der Nordsee stammendem Wasser liegt.
Das Gegenteil passiert im
Mittelmeer
? dort ist die Verdunstung großer als die Niederschlagsmenge. Das Salz bleibt im Wasser zuruck, sein Gehalt steigt. Tritt das Mittelmeerwasser bei Gibraltar aus dem Mittelmeer aus, sinkt es trotz seiner hohen Temperatur in mittlere Tiefen ab. Es kann anhand seines hohen Salzgehaltes quasi im ganzen Nordatlantik identifiziert werden.
[6]
Dieser Abschnitt ist nicht hinreichend mit
Belegen
(beispielsweise
Einzelnachweisen
) ausgestattet. Angaben ohne ausreichenden Beleg konnten demnachst entfernt werden. Bitte hilf Wikipedia, indem du die Angaben recherchierst und
gute Belege einfugst.
Hauptbestandteile des Meersalzes (g / 100 g):
| Chlorid
|
55,04
|
| Natrium
|
30,61
|
| Sulfat
|
7,68
|
| Magnesium
|
3,69
|
| Calcium
|
1,16
|
| Kalium
|
1,10
|
| Hydrogencarbonat
|
0,41
|
| Bromid
|
0,19
|
| Borat
|
0,07
|
| Strontium
|
0,04
|
Die wichtigsten gelosten Salz
ionen
des Meerwassers haben in den Weltmeeren den gleichen Anteil an der Salinitat, sie sind konservativ. Das heißt, auch bei unterschiedlicher Salinitat ist der Anteil der Ionen zueinander der gleiche. Dies liegt daran, dass sie nach ihrem Eintrag ins Meer nicht mehr nennenswert von biologischen oder geochemischen Prozessen beeinflusst werden.
Eine einfache begriffliche Einteilung lautet: ?Wasser kann polyhalin sein (uber 10 Promille Salze ? nur Meerestiere), mesohalin (1,0 bis 10 Promille Salze ? spezielle Brackwasserfauna) oder oligohalin (0,1 bis 1,0 Promille Salze ? schon Sußwassertiere)“
- Sußwasser
weist eine Salinitat von unter 0,1 % auf (d. h. unter 1 g/kg.)
- Beim
Brackwasser
liegt die Salinitat zwischen 0,1 % und 1,0 %.
- Ab einer Salinitat uber 1,0 % spricht man von
Salzwasser
.
Zum Vergleich:
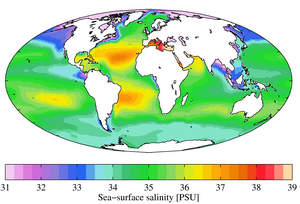 Salzgehalt (in PSU) im Jahresmittel
Salzgehalt (in PSU) im Jahresmittel
- Ostsee
: 0,8 % im Durchschnitt (westliche Ostsee 1,3 %, Finnischer und Bottnischer Meerbusen < 0,5 %)
- Nordsee
: 3,5 %
- Flussmundungen: 1,5 % ? 2,5 %
- Nordliche Nordsee: 3,2 % ? 3,5 %
- Mittelmeer
: 3,74 %
- Schwarzes Meer
1,7 % ? 1,8 %
- Persischer Golf
: 4 %
- Rotes Meer
: 4 %
- Asowsches Meer
: 0,2 % ? 1,1 %
Bei den anderen Nebenmeeren liegt die Salinitat zwischen 3 und 4 %.
- Kaspisches Meer
: 1,3 %
- Mono Lake
: 7,3 %
- Qarunsee
: 11,8 %
- Totes Meer
: 28 % (Durchschnitt)
- Totes Meer: 32,66 % in einer Tiefe von 50 Metern
- Aralsee
: 0,9 % (1960)
- Kleiner Aralsee: 2 % (2003)
- Großer Aralsee: 7,5 % (2003)
- Assalsee
: 34,8 % (Durchschnitt)
- Assalsee: 38,8 % in einer Tiefe von 20 Metern
- Don-Juan-See
: 44,2 % (welthochster Wert fur ein Gewasser)
- ↑
Gunter Dietrich, Kurt Kalle, Wolfgang Krauss, Gerold Siedler:
Allgemeine Meereskunde.
3. Auflage. Borntraeger, Berlin 1975,
ISBN 3-443-01016-4
.
- ↑
a
b
Temperature and Salinity Scales
(
Memento
vom 11. Januar 2006 im
Internet Archive
)
- ↑
T. Dauphinee:
Introduction to the Special Issue on the Practical Salinity Scale 1978
. In:
IEEE Journal of Oceanic Engineering
.
Band
5
,
Nr.
1
, 1980,
S.
1?2
(
PDF
– Einleitung zur Sonderausgabe uber die PSS-78 ? freier Volltext).
- ↑
Thermodynamic Equation Of Seawater - 2010 (TEOS-10: Home).
Joint Committee on the Properties of Seawater,
abgerufen am 9. Marz 2024
.
- ↑
Robert Marsh, Erik van Sebille:
Ocean Currents ? Physical Drivers in a Changing World
. Elsevier, 2021, Chapter 2 ? Frameworks, data, and methods,
doi
:
10.1016/B978-0-12-816059-6.00009-7
.
- ↑
Joseph Moran:
Ocean studies: Introduction to oceanography
. Hrsg.: American Meteorological Society. 3. Auflage. American Meteorological Society, Boston 2011.