Ein
Aggregatzustand
ist die Art der Verbindung und Verschiebbarkeit der kleinsten Teile, aus denen
Materie
zusammengesetzt ist. Anders formuliert sind Aggregatzustande fundamentale Erscheinungsformen von Materie, die sich jeweils sprunghaft in der Mobilitat ihrer
Atome
und
Molekule
sowie in der Starke der Wechselwirkungen zwischen diesen unterscheiden.
[1]
[2]
[3]
Die klassischen Aggregatzustande
fest
,
flussig
und
gasformig
lassen sich daher
sensorisch
anhand ihrer unterschiedlichen
makroskopischen
mechanischen
und
rheologischen
Eigenschaften identifizieren.
[4]
Daneben werden in der
Physik
auch weitere, in der
Biosphare
der
Erde
nicht oder kaum naturlich vorkommende Erscheinungsformen der Materie als Aggregatzustand bezeichnet. So gilt
Plasma
, aus dem beispielsweise die
Sonne
besteht, als vierter Aggregatzustand der Materie.
[5]
Bestimmte
Stoffe
, wie etwa
Flussigkristalle
,
viskoelastische Stoffe
oder Schmelzen besonders langkettiger
Polymere
, konnen Merkmale sowohl des festen als auch des flussigen Aggregatzustandes aufweisen.
Glaser
ataktischer
Polymere mit hohen
Molekulargewichten
werden oft als Festkorper betrachtet, obwohl es sich bei diesen lediglich um Flussigkeiten mit einer ? verglichen mit den Zeitskalen menschlicher Wahrnehmung ? stark verlangsamten
Dynamik
handelt.
[6]
[7]
Der Begriff Aggregatzustand ist vom enger gefassten Begriff
Phase
abzugrenzen. Eine Phase ist innerhalb eines Materials ein raumlich begrenzter Bereich, der chemisch und physikalisch einheitliche Eigenschaften aufweist.
[8]
Ein Aggregatzustand kann mehrere Phasen umfassen. Beispielsweise konnen
homogene
Feststoffe
bei unterschiedlichen
Temperaturen
und
Drucken
in unterschiedlichen
Kristallmodifikationen
vorliegen, die durch
enantiotrope
Umwandlungen ineinander uberfuhrbar sind und die jeweils eine eigene Phase darstellen. Heterogene
Gemische
konnen einheitlich im festen oder flussigen Aggregatzustand vorliegen, aber mehrere Phasen unterschiedlicher stofflicher Zusammensetzungen enthalten. Bei Gasen und Plasmen lassen sich die Begriffe Aggregatzustand und Phase
synonym
verwenden.
Die Uberfuhrung eines Stoffes in einen anderen Aggregatzustand erfolgt durch einen
Phasenubergang
, der sich durch eine
Zustandsanderung
herbeifuhren lasst, etwa durch eine Anderung der Temperatur, des Drucks oder des
Volumens
. Die
Grenzen
zwischen den verschiedenen Aggregatzustanden im
Zustandsraum
eines Stoffes lassen sich graphisch mit Hilfe von
Phasendiagrammen
darstellen.
Die drei klassischen Aggregatzustande
 Temperaturabhangige Haufigkeit der Aggregatzustande der Elemente (blau: fest, rot: flussig, grun: gasformig)
Temperaturabhangige Haufigkeit der Aggregatzustande der Elemente (blau: fest, rot: flussig, grun: gasformig)
Ubersicht
Es gibt drei klassische Aggregatzustande:
- fest
(
f
alternativ
s
[9]
): In diesem Zustand behalt ein Stoff meist sowohl Form als auch Volumen bei.
- flussig
(
fl
alternativ
l
[10]
): Hier wird das Volumen beibehalten, aber die Form ist unbestandig und passt sich dem umgebenden Raum an.
- gasformig
(
g
): Hier entfallt auch die Volumenbestandigkeit, ein Gas fullt den zur Verfugung stehenden Raum vollstandig aus.
Fur feste Stoffe und flussige Stoffe gibt es den zusammenfassenden Begriff
kondensierte Materie
. Flussigkeiten und Gase werden in der Physik unter dem Oberbegriff
Fluide
zusammengefasst.
Bei Feststoffen unterscheidet man auch nach anderen Merkmalen:
Die klassischen Aggregatzustande lassen sich mit einem
Teilchenmodell
erklaren, das die kleinsten Teilchen eines Stoffes (Atome, Molekule,
Ionen
) auf kleine Kugeln reduziert. Die mittlere
kinetische Energie
aller Teilchen ist in allen Zustanden ein Maß fur die Temperatur. Die Art der Bewegung ist in den drei Aggregatzustanden jedoch vollig unterschiedlich. Im Gas bewegen sich die Teilchen geradlinig wie Billardkugeln, bis sie mit einem anderen oder mit der Gefaßwand zusammenstoßen. In der Flussigkeit mussen sich die Teilchen durch Lucken zwischen ihren Nachbarn hindurchzwangen (
Diffusion
,
Brownsche Molekularbewegung
). Im Festkorper schwingen die Teilchen nur um ihre Ruhelage.
Teilchenbewegung in den verschiedenen Aggregatzustanden
Feststoff
Flussigkeit
Gas
Fest
 Teilchenmodell eines kristallinen Feststoffes
Teilchenmodell eines kristallinen Feststoffes
Bewegung
Die kleinsten Teilchen sind bei einem Feststoff nur wenig in Bewegung. Sie schwingen um eine feste Position, ihren Gitterplatz, und rotieren meist um ihre Achsen. Je hoher die Temperatur wird, desto heftiger schwingen bzw. rotieren sie, und der Abstand zwischen den Teilchen nimmt (meist) zu. Ausnahme:
Dichteanomalie
.
- Die Form des Feststoffes bleibt unverandert.
- Stoffe im festen Aggregatzustand lassen sich nur schwer aufteilen.
- Sie lassen sich nur schwer
verformen
(geringe
Verformbarkeit
,
sprode
).
Hinweis: Betrachtet man die Teilchen mit
quantenmechanischen
Grundsatzen, so durfen aufgrund der
Heisenbergschen Unscharferelation
eigentlich Teilchen nie ruhig stehen. Sie haben kleine Schwingungen, die man auch als
Nullpunktsfluktuationen
bezeichnet. Das entspricht dem Grundzustand des
harmonischen Oszillators
.
Anziehung
Zwischen den kleinsten Teilchen wirken verschiedene Krafte, namlich die
Van-der-Waals-Krafte
, die
elektrostatische Kraft
zwischen Ionen,
Wasserstoffbruckenbindungen
oder
kovalente Bindungen
. Die Art der Kraft ist durch den atomaren Aufbau der Teilchen (
Ionen
, Molekule,
Dipole
…) bestimmt. Bei Stoffen, die auch bei hohen Temperaturen fest sind, ist die Anziehung besonders stark.
Anordnung
Durch die schwache Bewegung und den festen Zusammenhalt sind die Teilchen regelmaßig angeordnet.
- Die meisten festen
Reinstoffe
haben deshalb eine regelmaßige Struktur (Kristall), nur wenige sind
amorph
.
- Die Teilchenanordnung in einem amorphen Festkorper ist ahnlich ungeordnet wie in der Flussigkeit, er ist jedoch formstabil, da die Teilchenbewegungen gegeneinander weitgehend eingefroren sind.
Abstand
Durch die starke Anziehung sind die Teilchen eng beieinander (hohe
Packungsdichte
)
Flussig
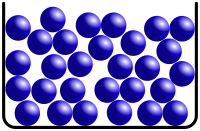 Teilchenmodell einer Flussigkeit bzw. eines amorphen Festkorpers
Teilchenmodell einer Flussigkeit bzw. eines amorphen Festkorpers
Bewegung
Die Teilchen sind nicht wie beim Feststoff ortsfest, sondern konnen sich gegenseitig verschieben. Bei Erhohung der Temperatur werden die Teilchenbewegungen immer schneller.
Anziehung
Durch die Erwarmung ist die Bewegung der Teilchen so stark, dass die Wechselwirkungskrafte nicht mehr ausreichend sind, um die Teilchen an ihrem Platz zu halten. Die Teilchen konnen sich nun frei bewegen.
- Ein flussiger Stoff verteilt sich von allein, wenn er nicht in einem Gefaß festgehalten wird.
- Ein Farbstoff verteilt sich von allein in einer Flussigkeit (
Diffusion
).
Abstand
Obwohl der Abstand der Teilchen durch die schnellere Bewegung ein wenig großer wird (die meisten festen Stoffe nehmen beim Schmelzen einen großeren Raum ein), hangen die Teilchen weiter aneinander. Fur die Verringerung des Volumens einer Flussigkeit durch Kompression gilt ahnliches wie bei einem Festkorper, wobei der entsprechende
Kompressionsmodul
der Flussigkeit zum Tragen kommt. Bei einer Temperaturverringerung wird das Volumen ebenfalls kleiner, bei Wasser jedoch nur bis zu einer Temperatur von 4 °C (
Anomalie des Wassers
), wahrend darunter bis 0 °C das Volumen wieder ansteigt.
Anordnung
Obwohl die Teilchen sich standig neu anordnen und Zitter-/Rotationsbewegungen durchfuhren, kann eine Anordnung festgestellt werden. Diese
Nahordnung
ist ahnlich wie im amorphen Festkorper, die
Viskositat
ist jedoch sehr viel niedriger, d. h., die Teilchen sind beweglicher.
Gasformig
 Teilchenmodell eines Gases
Teilchenmodell eines Gases
Bewegung
Bei Stoffen im gasformigen Zustand sind die Teilchen schnell in Bewegung. Ein Gas oder gasformiger Stoff verteilt sich schnell in einem Raum. In einem geschlossenen Raum fuhrt das Stoßen der kleinsten Teilchen gegen die Wande zum Druck des Gases.
Anziehung
Beim gasformigen Zustand ist die
Bewegungsenergie
der kleinsten Teilchen so hoch, dass sie nicht mehr zusammenhalten. Die kleinsten Teilchen des gasformigen Stoffes verteilen sich gleichmaßig im gesamten zur Verfugung stehenden Raum.
Abstand
Durch die schnelle Bewegung der Teilchen in einem Gas sind sie weit voneinander entfernt. Sie stoßen nur hin und wieder einander an, bleiben aber im Vergleich zur flussigen Phase auf großer Distanz. Ein gasformiger Stoff lasst sich komprimieren, d. h., das Volumen lasst sich verringern.
Anordnung
Wegen der Bewegung sind die Teilchen ungeordnet.
In der
physikalischen Chemie
unterscheidet man zwischen
Dampf
und Gas. Beide sind physikalisch gesehen nichts anderes als der gasformige Aggregatzustand; die Begriffe haben auch nicht direkt mit
realem Gas
und
idealem Gas
zu tun. Was
umgangssprachlich
als ?Dampf“ bezeichnet wird, ist physikalisch gesehen eine Mischung aus flussigen und gasformigen Bestandteilen, welche man im Falle des Wassers als
Nassdampf
bezeichnet.
Bei einem Dampf im engeren Sinn handelt es sich um einen Gleichgewichtszustand zwischen flussiger und gasformiger Phase. Er kann, ohne Arbeit verrichten zu mussen, verflussigt werden, das heißt beim Verflussigen erfolgt kein Druckanstieg. Ein solcher Dampf wird in der Technik als Nassdampf bezeichnet im Gegensatz zum sogenannten
Heißdampf
oder uberhitzten Dampf, der im eigentlichen Sinn ein reales Gas aus Wassermolekulen darstellt und dessen Temperatur oberhalb der Kondensationstemperatur der flussigen Phase beim jeweiligen Druck liegt.
Ausgewahlte Reinstoffe als Beispiele
Reinstoffe werden entsprechend ihrem Aggregatzustand bei einer Temperatur von 20
°C
(siehe
Raumtemperatur
) und einem Druck von 1013,25
hPa
(
Normaldruck
) als Feststoff, Flussigkeit oder
Gas
bezeichnet. Beispiel: Brom ist bei Raumtemperatur und Normaldruck flussig (siehe Tabelle), also gilt Brom als Flussigkeit.
Diese Bezeichnungen (Feststoff, Flussigkeit, Gas) werden zwar auch gebraucht, wenn Stoffe unter veranderten Bedingungen einen anderen Aggregatzustand annehmen. Im engeren Sinne bezieht sich die Einteilung jedoch auf die oben genannten
Standardbedingungen
; jeder Stoff gehort dann zu einer der Kategorien.
| Stoff
|
Schmelztemperatur
1
|
Siedetemperatur
1
|
Aggregatzustand
im Gefrierschrank (?10 °C)
1
|
Aggregatzustand
bei Raumtemperatur (25 °C)
1
|
Aggregatzustand
im Backofen (150 °C)
1
|
| Eisen
|
1535 °C
|
2750 °C
|
fest
|
fest
|
fest
|
| Kupfer
|
1084 °C
|
2567 °C
|
fest
|
fest
|
fest
|
| Caesium
|
28 °C
|
671 °C
|
fest
|
fest
|
flussig
|
| Sauerstoff
|
?219 °C
|
?183 °C
|
gasformig
|
gasformig
|
gasformig
|
| Helium
|
?272 °C
|
?269 °C
|
gasformig
|
gasformig
|
gasformig
|
| Brom
|
?7 °C
|
59 °C
|
fest
|
flussig
|
gasformig
|
| Chlor
|
?101 °C
|
?35 °C
|
gasformig
|
gasformig
|
gasformig
|
| Wasser
|
0 °C
|
100 °C
|
fest
|
flussig
|
gasformig
|
1
bei Normaldruck
Aggregatzustande in Gemischen
Bei der Vermischung von Stoffen ergeben sich abhangig vom Aggregatzustand der Bestandteile und ihrem mengenmaßigen Anteil charakteristische
Gemische
, zum Beispiel
Nebel
oder
Schaum
.
Anderung des Aggregatzustands
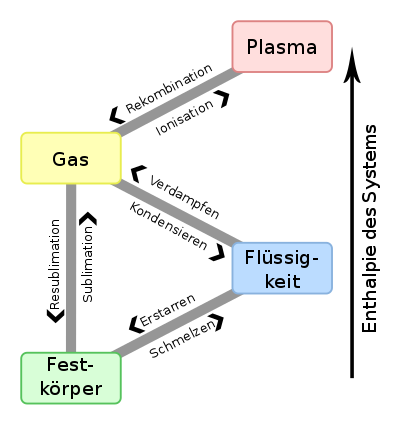 Uberblick uber die Aggregatzustandsanderungen
Uberblick uber die Aggregatzustandsanderungen
Die Ubergange zwischen den verschiedenen Aggregatzustanden haben spezielle Namen (eoc, omc, eon) und spezielle Ubergangsbedingungen, die bei Reinstoffen aus Druck und Temperatur bestehen. Diese Ubergangsbedingungen entsprechen dabei Punkten auf den Phasengrenzlinien von Phasendiagrammen. Hierbei ist fur jeden Phasenubergang eine bestimmte
Warmemenge
notwendig bzw. wird dabei freigesetzt.
Die Sublimation und das Verdampfen kommen auch unterhalb der Sublimations- beziehungsweise Siedepunktes vor. Man spricht hier von einer
Verdunstung
.
 Bezeichnungen fur die Aggregatzustandsanderungen von Wasser
Bezeichnungen fur die Aggregatzustandsanderungen von Wasser
Alle Ubergange konnen am Beispiel
Wasser
im Alltag beobachtet werden (siehe Abbildung):
Schmelzen
Schnee
oder
Eis
fangt im Fruhjahr an flussig zu werden, sobald Temperaturen oberhalb der
Schmelztemperatur
herrschen.
Erstarren
Kuhlt das Wasser in Seen unter den
Gefrierpunkt
ab, bilden sich
Eiskristalle
, die mit der Zeit immer großer werden, bis die Oberflache mit einer Eisschicht uberzogen ist.
Verdampfen
Wird Wasser im Kochtopf uber seine
Siedetemperatur
erhitzt, so wird das Wasser gasformig. Das ?Blubbern“ im Kochtopf kommt zustande, weil das Wasser am heißen Topfboden zuerst die Siedetemperatur erreicht - Die aufsteigenden Blasen sind der
Wasserdampf
, der (wie die meisten gasformigen Stoffe) unsichtbar ist.
Verdunstung
, der Ubergang von flussig in gasformig ohne Erreichen der Siedetemperatur, ist bei Schweiß auf der Haut gut zu beobachten.
Kondensieren
Der deutlich sichtbare
Nebel
oberhalb kochenden Wassers, der meist umgangssprachlich als ?Dampf“ bezeichnet wird, ist zu winzigen Wassertropfchen kondensierter Wasserdampf.
Tau
und
Wolken
entstehen ebenfalls durch kondensierenden Wasserdampf.
Sublimation
Gefrorene Pfutzen konnen im Winter, auch bei Temperaturen weit unterhalb des Gefrierpunktes, durch Sublimation nach und nach ?austrocknen“, bis das Eis vollstandig sublimiert und die Pfutze verschwunden ist.
Resublimation
Raureif
oder
Eisblumen
, die sich im Winter bilden, entstehen durch den aus der Umgebungsluft resublimierenden Wasserdampf.
Teilchenmodell der Phasenubergange
Schmelzen
Durch Erhohen der Temperatur (Zufuhr von thermischer Energie) bewegen sich die kleinsten Teilchen immer heftiger, und ihr Abstand voneinander wird (normalerweise) immer großer. Die
Van-der-Waals-Krafte
halten sie aber noch in ihrer Position, ihrem Gitterplatz. Erst ab der sogenannten
Schmelztemperatur
wird die Schwingungsamplitude der Teilchen so groß, dass die Gitterstruktur teilweise zusammenbricht. Es entstehen Gruppen von Teilchen, die sich frei bewegen konnen. In ihnen herrscht eine
Nahordnung
, im Gegensatz zur
Fernordnung
von Teilchen innerhalb des Kristallgitters fester Stoffe.
Erstarren
Mit Sinken der Temperatur nimmt die Bewegung der Teilchen ab, und ihr Abstand zueinander wird immer geringer. Auch die Rotationsenergie nimmt ab. Bei der sogenannten
Erstarrungstemperatur
wird der Abstand so klein, dass sich die Teilchen gegenseitig blockieren und miteinander verstarkt anziehend wechselwirken ? sie nehmen eine feste Position in einem dreidimensionalen Gitter ein.
Es gibt Flussigkeiten, die sich bei sinkender Temperatur ausdehnen, beispielsweise Wasser. Dieses Verhalten wird als
Dichteanomalie
bezeichnet.
Verdampfen und Sublimation
Die Geschwindigkeit der kleinsten Teilchen ist nicht gleich. Ein Teil ist schneller, ein Teil ist langsamer als der Durchschnitt. Dabei andern die Teilchen durch
Kollisionen
standig ihre aktuelle Geschwindigkeit.
An der Grenze eines Festkorpers oder einer Flussigkeit, dem Ubergang einer
Phase
in eine gasformige, kann es mitunter vorkommen, dass ein Teilchen von seinen Nachbarn zufallig einen so starken Impuls bekommt, dass es aus dem Einflussbereich der
Kohasionskraft
entweicht. Dieses Teilchen tritt dann in den gasformigen Zustand uber und nimmt etwas Warmeenergie in Form der Bewegungsenergie mit, das heißt die feste oder flussige Phase kuhlt ein wenig ab.
Wird thermische Energie einem System zugefuhrt und erreicht die Temperatur die Sublimations- oder Siedetemperatur, geschieht dieser Vorgang kontinuierlich, bis alle kleinsten Teilchen in die gasformige Phase ubergetreten sind. In diesem Fall bleibt die Temperatur in der verdampfenden Phase in der Regel unverandert, bis alle Teilchen mit einer hoheren Temperatur aus dem System verschwunden sind. Die Warmezufuhr wird somit in eine Erhohung der
Entropie
umgesetzt.
Wenn die Kohasionskrafte sehr stark sind, beziehungsweise es sich eigentlich um eine viel starkere
Metall
- oder
Ionenbindung
handelt, dann kommt es nicht zur Verdampfung.
Die durch
Verdampfen
starke Volumenzunahme eines Stoffes kann, wenn sehr viel Hitze schlagartig zugefuhrt wird, zu einer
Physikalischen Explosion
fuhren.
Kondensation und Resublimation
Der umgekehrte Vorgang ist die Kondensation beziehungsweise Resublimation. Ein kleinstes Teilchen trifft zufallig auf einen festen oder flussigen Stoff, ubertragt seinen
Impuls
und wird von den Kohasionskraften festgehalten. Dadurch erwarmt sich der Korper um die Energie, die das kleinste Teilchen mehr trug als der Durchschnitt der kleinsten Teilchen in der festen beziehungsweise flussigen Phase.
Stammt das Teilchen allerdings von einem Stoff, der bei dieser Temperatur gasformig ist, sind die Kohasionskrafte zu schwach, es festzuhalten. Selbst wenn es zufallig so viel Energie verloren hat, dass es gebunden wird, schleudert es die nachste Kollision mit benachbarten kleinsten Teilchen wieder in die Gasphase. Durch Absenken der Temperatur kann man den kleinsten Teilchen ihre Energie entziehen. Dadurch ballen sie sich beim Unterschreiten der Sublimations- oder Erstarrungstemperatur durch die Wechselwirkungskrafte mit anderen Teilchen zusammen und bilden wieder einen Feststoff oder eine Flussigkeit.
Phasendiagramme
 Phasendiagramm eines ?gewohnlichen“ Stoffes und des
Wassers
(
Dichteanomalie
)
Phasendiagramm eines ?gewohnlichen“ Stoffes und des
Wassers
(
Dichteanomalie
)
Das p-T-Phasendiagramm eines Stoffes beschreibt in Abhangigkeit von Druck und Temperatur, in wie vielen Phasen ein Stoff vorliegt und in welchem Aggregatzustand sich diese befinden. Anhand der Linien kann man also erkennen, bei welchem Druck und welcher Temperatur die Stoffe ihren Aggregatzustand verandern. Gewissermaßen findet auf den Linien der Phasenubergang zwischen den Aggregatzustanden statt, weshalb man diese auch als Phasengrenzlinien bezeichnet. Auf ihnen selbst liegen die jeweiligen Aggregatzustande in Form eines
dynamischen Gleichgewichts
nebeneinander in verschiedenen Phasen vor.
- Bei einem bestimmten Druck und einer bestimmten Temperatur, dem so genannten
Tripelpunkt
, konnen alle drei Aggregatzustande gleichzeitig vorliegen. Es handelt sich dabei um den Punkt in der ?Mitte“ des Phasendiagramms, an welchem sich alle drei Phasengrenzlinien treffen. Der Tripelpunkt eignet sich daher als ein Ausgangspunkt dieser Linien und fur die Festlegung vieler
Temperaturskalen
.
- Oberhalb eines bestimmten Druckes und einer bestimmten Temperatur, dem sogenannten
kritischen Punkt
, konnen Gas und Flussigkeit aufgrund ihrer identischen
Dichte
nicht mehr unterschieden werden. In diesem
Zustandsraum
kann daher keine Phasengrenzlinie festgelegt werden.
- Fur Drucke unterhalb des Tripelpunkt-Druckes kann die Substanz bei einer Senkung der Temperatur nur fest oder bei einer Steigerung der Temperatur nur gasformig werden. Die Trennlinie zwischen beiden Bereichen nennt man
Sublimationskurve
. Auf ihr konnen feste und gasformige Phasen gleichzeitig existieren. Die Sublimationskurve beginnt theoretisch am
absoluten Nullpunkt
und endet am Tripelpunkt.
- Fur Drucke oberhalb des Tripelpunkt-Druckes ist die Substanz fur Temperaturen unterhalb des
Schmelzpunktes
fest, zwischen Schmelz- und
Siedepunkt
flussig und oberhalb des Siedepunktes gasformig. Die Trennlinie zwischen fester und flussiger Phase, also die Kurve der Schmelzpunkte, nennt man
Schmelzkurve
, die Trennlinie zwischen Flussigkeit und Gas nennt man
Siedepunktskurve
. Beide Kurven beginnen ebenfalls am Tripelpunkt, wobei sich die Schmelzkurve theoretisch bis in das Unendliche fortsetzt und die Siedepunktskurve am kritischen Punkt endet.
- Die
Freiheitsgrade
innerhalb des Phasendiagramms sind von der betrachteten Ebene abhangig. Am Tripelpunkt und am kritischen Punkt existiert kein Freiheitsgrad, da sowohl Druck als auch Temperatur feste, lediglich stoffabhangige Werte besitzen. An den Phasengrenzlinien sind entweder Druck oder Temperatur frei wahlbar und bedingen einander, es existiert folglich ein Freiheitsgrad. Im reinen Zustandsraum, also in den Flachen des Phasendiagramms, sind Druck und Temperatur frei wahlbar, was zwei Freiheitsgraden entspricht.
Nichtklassische Aggregatzustande
Neben den drei klassischen Aggregatzustanden gibt es weitere Materiezustande, die zum Teil nur unter extremen Bedingungen auftreten (nach Temperatur, tendenziell von hoher zu niedriger, sortiert).
- Der
Plasmazustand
: Bei sehr hohen
Temperaturen
werden die
Atome
in Atomkern und -hulle zerlegt; freie
Elektronen
entstehen. Der Zustand tritt beispielsweise im
Lichtbogen
, in
Sternen
und in
Kernfusionsreaktoren
auf.
- Das
Atomgas
: In ihm existieren keine Molekule mehr, da die standigen Stoße die Bindungen zerstoren, allerdings sind die Elektronen noch fest gebunden.
- Der
uberkritische Zustand
tritt bei Uberschreiten des kritischen Punktes auf und ist ein Mischzustand zwischen flussig und gasformig.
- Der
mesomorphe Zustand
: Er nimmt eine Zwischenposition zwischen den Aggregatzustanden flussig und fest ein und tritt in verschiedener Auspragung beispielsweise bei
Flussigkristallen
oder
plastischen Kristallen
auf.
- Das
Bose-Einstein-Kondensat
: Hierbei handelt es sich um eine Menge extrem kalter Atome, die den gleichen
quantenmechanischen
Zustand einnehmen, dadurch ununterscheidbar werden und sich somit vollkommen
koharent
verhalten.
- Das
Fermionen-Kondensat
: Ein superkalter Zustand von
Fermionen
, welche sich durch ihren halbzahligen Spin von den Bosonen (ganzzahliger Spin) unterscheiden.
- Das
Suprafluid
: Eine Flussigkeit ohne innere Reibung.
- Das
Suprasolid
: Ein Zustand, der bei superkaltem Helium-4 erreicht wird. Die Materie zeigt gleichzeitig sowohl Eigenschaften fester als auch suprafluider Korper.
- Der bosonische Metallzustand
[11]
Literatur
- Peter Kurzweil, Paul Scheipers:
Chemie: Grundlagen, Aufbauwissen, Anwendungen und Experimente
. Springer, 2010,
ISBN 978-3-8348-0341-2
(
eingeschrankte Vorschau
in der Google-Buchsuche).
- Guido Kickelbick:
Chemie fur Ingenieure
. Pearson Deutschland, 2008,
ISBN 978-3-8273-7267-3
(
eingeschrankte Vorschau
in der Google-Buchsuche).
- B. Engels, C. Schmuck, T. Schirmeister, R. Fink:
Chemie fur Mediziner
. Pearson Deutschland, 2008,
ISBN 978-3-8273-7286-4
(
eingeschrankte Vorschau
in der Google-Buchsuche).
- Compact Silver Line:
Physik: Grundwissen Formeln und Gesetze
. Compact Verlag, 2010,
ISBN 978-3-8174-7891-0
(
eingeschrankte Vorschau
in der Google-Buchsuche).
- Dieter Meschede, Christian Gerthsen:
Gerthsen Physik
. Springer, 2003,
ISBN 978-3-540-02622-8
(
eingeschrankte Vorschau
in der Google-Buchsuche – uber Plasma als den ?Vierten Aggregatzustand“).
Weblinks
Einzelnachweise
- ↑
Iwan Gutzow, Jurn Schmelzer:
The Vitreous State
. Springer-Verlag, Berlin/Heidelberg 1995,
ISBN 3-662-03189-2
,
S.
7
,
doi
:
10.1007/978-3-662-03187-2
.
- ↑
Aggregatzustand.
In:
Lexikon der Physik.
Abgerufen am 4. Februar 2021
.
- ↑
Wolfgang Bechmann, Ilko Bald:
Einstieg in die Physikalische Chemie fur Naturwissenschaftler
(=
Studienbucher Chemie
). 7. Auflage. Springer-Verlag, Berlin/Heidelberg 2020,
ISBN 978-3-662-62033-5
, Kapitel
1.1 Begriffe zur Beschreibung stofflicher Zustande
,
doi
:
10.1007/978-3-662-62034-2
.
- ↑
Charles E. Mortimer, Ulrich Muller:
Chemie: Das Basiswissen der Chemie
. 13. Auflage. Georg Thieme Verlag, Stuttgart 2020,
ISBN 978-3-13-242274-2
, Kapitel
1.2 Elemente, Verbindungen, Gemische
,
doi
:
10.1055/b-006-163279
.
- ↑
Ulrich Stroth:
Plasmaphysik ? Phanomene, Grundlagen und Anwendungen
. 2. Auflage. Springer-Verlag, Berlin 2018,
ISBN 978-3-662-55235-3
, Kapitel
1 Einleitung
,
doi
:
10.1007/978-3-662-55236-0
.
- ↑
David I. Bower:
An introduction to polymer physics
. Cambridge University Press, Cambridge 2002,
ISBN 0-511-07757-2
, 7.4 Time?temperature equivalence and superposition.
- ↑
Gert Strobl:
The Physics of Polymers ? Concepts for Understanding Their Structures and Behavior
. 3. Auflage. Springer-Verlag, Berlin/Heidelberg 2007,
ISBN 978-3-540-25278-8
, 6.3 Specific Relaxation Processes and Flow Behavior,
doi
:
10.1007/978-3-540-68411-4
.
- ↑
J. B. Clarke, J. W. Hastie, L. H. E. Kihlborg, R. Metselaar, M. M. Thackeray:
Definitions of terms relating to phase transitions of the solid state (IUPAC Recommendations 1994)
. In:
Pure and Applied Chemistry
.
Band
66
,
Nr.
3
, 1. Januar 1994,
ISSN
1365-3075
,
S.
577?594
,
doi
:
10.1351/pac199466030577
.
- ↑
s
fur
englisch
solid
- ↑
l
fur
englisch
liquid
- ↑
Scinexx
:
Neuer Materialzustand im Supraleiter.
(
scinexx.de
).