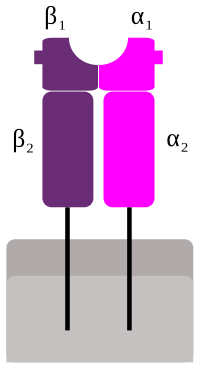
 Schema MHC glykoproteinu II. t?idy
Schema MHC glykoproteinu II. t?idy
MHC glykoproteiny II. t?idy
(MHCII) jsou povrchove
MHC
glykoproteiny
bilych krvinek
, uplat?ujici se p?i zahajeni specificke
imunitni reakce
. Hlavni funkci molekul MHCII je prezentovat
T-lymfocytu
exogenni
peptid
, odvozeny od pohlceneho
antigenu
, tim T-lymfocyt aktivovat, a spustit tedy imunitni odpov?? proti tomuto antigenu.
MHC glykoproteiny II. t?idy jsou
exprimovany
p?edev?im profesionalnimi
antigen prezentujicimi bu?kami
(APC), mezi ktere pat?i
dendriticke bu?ky
,
makrofagy
a
B-lymfocyty
. Inducibiln? mohou MHCII exprimovat neprofesionalni APC, nap?. bu?ky
endotelove
,
epitelove
, nadorove a T-lymfocyty.
Geny kodujici MHC glykoproteiny II. t?idy se nachazi v hlavnim histokompatibilnim komplexu, ktery se u lidi nachazi na VI. a u my?i na XVII.
chromosomu
. Lide exprimuji t?i izotypy MHCII (HLA-DP, HLA-DQ a HLA-DR), zatimco my?i pouze dva (I-A a I-E).
MHCII se sklada ze dvou ?et?zc?, α a β. Na rozdil od podjednotek
MHC I
, oba jsou p?ibli?n? stejn? velke, okolo 30
kDa
. Oba dva jsou take zakotveny v
membran?
a spolu vytva?eji vazebne misto pro peptid, jej? prezentuji. Toto MHC II doka?i vazat peptid obvykle o delce 15-35
aminokyselin
, ale i del?i, co? je podstatn? vice, ne? u MHCI. To je dano tim, ?e ?labek, do n?j? se peptid va?e, neni na koncich uzav?eny, ale otev?eny, tak?e peptid m??e na koncich p?esahovat ven.
[1]
Samotna vazba peptidu se odehrava na srovnatelne delce peptidu.
Na molekulach MHCII jsou prezentovany hlavn? peptidy exogenniho p?vodu. Antigeny, ze kterych tyto peptidy vznikaji, jsou
endocytovany
a na MHCII se va?ou v bu?ce. Mezi mechanizmy endocytozy, vyu?ivane antigen prezentujicimi bu?kami, pat?i
fagocytoza
,
makropinocytoza
,
endocytoza zprost?edkovana receptorem
a endocytoza zavisla na
klathrinu
nebo
kaveolinu
. Endocytovany antigen je transportovan do specializovanych pozdnich
endozom?
, zvanych take MIIC kompartmenty (MHCII rich compartments). Sem take z
Golgiho aparatu
p?ichazi MHCII molekuly v komplexu s dal?im transmembranovym proteinem, zvanym invariantni ?et?zec (Ii), ktery se na n? navazal u? v
endoplasmatickem retikulu
. Funkci Ii je branit navazani endogennich peptid? na MHCII b?hem jeho cesty
sekretorickou drahou
. V MIIC kompartmentu jsou pohlceny antigen a Ii
proteolyticky ?t?peny
a zbytek Ii na MHCII je za pomoci proteinu HLA-DM vym?n?n za peptidovy fragment, pochazejici z antigenu. Komplex peptid-MHCII je nasledn? transportovan na povrch bu?ky, kde je antigen prezentovan na T
H
lymfocytu. Na MHCII mohou byt v?ak krom? exogennich peptid? vystavovany i peptidy endogenniho p?vodu. M??e se jednat o peptidy, pochazejici z protein? rezidentnich v endozomalnim systemu nebo z protein?, transportovanych timto systemem do
lyzozom?
. Na MHCII se take mohou dostat organizmu vlastni peptidy, pochazejici z fagocytovanych
apoptotickych t?lisek
nebo
autofagozom?
.
[2]
Pro aktivaci T-lymfocyt? je zasadni interakce MHCII s
T-bun??nym receptorem
(TCR) a s jeho koreceptorem
CD4
(pro MHCI je to
CD8
). TCR rozeznava MHC v mist? navazaneho peptidu. Pro usp??nou aktivaci T-lymfocytu tak musi specificky rozeznat nejen MHC, ale i peptid exogenniho p?vodu, co? je principem reakce na
patogeny
v organismu. CD4 se na MHCII va?e bez ohledu na navazany peptid a umo??uje, aby na MHCII reagovala jen ta podmno?ina T-lymfocyt?, ktera CD4
exprimuje
, tedy
pomocne T-lymfocyty
(T
H
lymfocyty, CD4
+
T-lymfocyty). Navic je k aktivaci T-lymfocytu pot?eba je?t?
kostimulace
pomoci
CD28
, ktery exprimuji pouze APC aktivovane signalem nebezpe?i, nap?iklad pomoci
Toll-like receptor?
. Bez teto kostimulace T-lymfocyt p?echazi do
anergie
nebo
apoptozy
.
Rozezna-li CD4+ T-lymfocyt pomoci sveho antigenniho receptoru (TCR) komplex MHCII s peptidem na povrchu APC, dojde k jejich vazb? a naslednemu vzniku molekularni struktury mezi APC a T-lymfocytem, ktera se nazyva imunologicka synapse (IS). IS lze rozd?lit centralni a periferni oblast, respektive cSMAC a pSMAC (supramolecullar activation cluster). Ust?ednimi molekulami cSMAC jsou MHCII a TCR s koreceptorem CD4. Dale je zde molekula
CD40
na APC stran? IS a jeji ligand
CD40L
(= CD154) na T-lymfocytarni stran?. V cSMAC na T-lymfocyty se take nachazi kostimula?ni molekula CD28, ktera interaguje s molekulou
CD80
nebo
CD86
na povrchu APC. Periferii IS (pSMAC) tvo?i kruh adhezivnich molekul
ICAM
a
LFA-1
, d?le?itych pro stabilitu IS. Sou?asti IS jsou take
cytoplasmaticke
molekuly lokalizovane pod membranou. Pat?i mezi n? proteiny u?astnici se
signalizace
, vedouci z receptor? v IS (nap?.
protein kinaza C
θ nebo
Lck
), a regulace
cytoskeletu
(v T-lymfocytu je do IS orientovano
mikrotubuly
organizujici centrum
? MTOC).
[3]
[4]
IS m??e byt strukturou r?zn? stabilni (interakce trva n?kolik minut a? hodin), co? je ovlivn?no mirou zralosti T-lymfocytu, druhem APC, mno?stvim antigenu prezentovaneho na MHCII a komplexitou prost?edi, kde se interakce odehrava. IS m??e byt take do r?zne miry uspo?adana. Nejvy??i uspo?adanosti se vyzna?uje stabilni monocentricka synapse s p?esn? vymezenym cSMAC a pSMAC. Od monocentricke IS je pak odvozena sekre?ni synapse, v jejim? st?edu se krom? cSMAC nachazi dal?i domena, kde probiha
exocytoza
aktivnich molekul, jako jsou
cytokiny
nebo
granzymy
a
perforiny
. Sekre?ni synapse je nap?iklad mezi B-lymfocytem a pomocnym T-lymfocytem, ktery sekretuje cytokiny p?ispivajici k vyvoji B-lymfocytu v
plazmatickou bu?ku
produkujici
protilatky
. Mezi T lymfocytem a APC mohou dale vznikat men? uspo?adane synapse, tzv. multicentricke IS, nebo synapse, kde rozd?leni molekul do cSMAC a pSMAC chybi.
[5]
Krom? sve klasicke funkce prezentovat antigen T-lymfocytu slou?i MHCII take jako receptor zprost?edkovavajici signalizaci vedouci do APC, a ovliv?ujici tak jeji dal?i osud. Stimulace MHCII na povrchu dendritickych bun?k je d?le?ita pro jejich zrani, produkci cytokin? a podporuje transport komplex? peptid-MHCII na povrch bu?ky.
[6]
U B-lymfocyt? byla po stimulaci MHCII pozorovana jejich
proliferace
, produkce protilatek a zvy?eni
adhezivity
k T-lymfocytu a exprese kostimula?nich molekul CD80 a CD86. Signalizace zprost?edkovana MHCII m??e tedy vest k proliferaci a
diferenciaci
APC. Po stimulaci MHCII m??e byt ale take spu?t?na apoptoza APC, a signalizace MHCII se tedy m??e podilet jak na zahajeni, tak i na ukon?eni imunitni odpov?di.
[6]
[7]
[8]
[9]
[10]
Mezi signaliza?ni udalosti po stimulaci MHCII pat?i: aktivace proteinovych kinaz z rodiny
Src
a
Syk
,
protein kinazy C
,
MAP kinaz
Erk
a
p38
,
fosfatidylinositol-3 kinazy
,
fosfolipazy C
γ a mobilizace vapniku.
[6]
[5] Signalizace MHCII take vede k aktivaci
transkrip?nich faktor?
NFAT
a
AP-1
.
[11]
MHCII ma jen velmi kratkou intracelularni ?ast bez signaliza?nich motiv?, a pro p?enos signalu z MHCII do bu?ky je tedy nutna asociace s dal?i signaliza?ni molekulou. Mezi molekuly zprost?edkovavajici signalizaci MHCII pat?i
CD19
,
CD20
,
MPYS
a
heterodimer Igα/Igβ
(=CD79a/CD79b), jeho? hlavni funkci je zprost?edkovani signalizace BCR.
[11]
[12]
[13]
[14]
Signalizace MHCII je spou?t?na p?edev?im vazbou TCR p?i prezentaci antigenu. MHCII m??e byt ale take stimulovan vazbou
superantigenu
, molekuly
LAG-3
(=CD223) nebo protilatky proti MHCII, ?eho? se vyu?iva hlavn? experimentaln?.
[6]
Porucha exprese MHCII zp?sobuje zava?nou
imunodeficienci
, ktera se nazyva MHCII deficience nebo take syndrom holych lymfocyt?. Nep?itomnost MHCII v imunitnim systemu vede k poru?e vyvoje CD4+ T-lymfocyt?. V
thymu
toti? nem??e dochazet k jejich
pozitivni selekci
rozeznanim komplexu peptid-MHCII na
thymocytech
prezentujicich antigen a i kdy? se male mno?stvi CD4+ T-lymfocyt? p?esto vyvine, nem??e byt nasledn? aktivovano antigen prezentujicimi bu?kami, proto?e ani ty MHCII neexprimuji. Deficit CD4+ T-lymfocyt? nasledn? vede k poru?e tvorby protilatek, proto?e B-lymfocyty nedostavaji od CD4+ T-lymfocyt? pomocny signal. Deficience MHCII neni zp?sobena mutaci v genu pro MHCII glykoprotein samotny, ale mutacemi v genech pro jeho transkrip?ni faktory, a to CIIT (MHC class II transactivator), RFXANK, RFX5 nebo RFXAP.
MHCII glykoproteiny hraji take d?le?itou roli p?i vzniku
autoimunitnich onemocn?ni
, n?ktere
alely
MHCII toti? zvy?uji sklon k rozvoji t?chto chorob.
[15]
[1]
- ↑
a
b
HO?EJ?I, Vaclav; BART??KOVA, Ji?ina.
Zaklady imunologie
. Praha: Triton, 2009. 320 s.
ISBN
9788073872809
.
- ↑
TROMBETTA, E. Sergio; MELLMAN, Ira. CELL BIOLOGY OF ANTIGEN PROCESSING IN VITRO AND IN VIVO. S. 975?1028.
Annual Review of Immunology
[online]. 2005-04 [cit. 2020-12-10]. Ro?. 23, ?is. 1, s. 975?1028.
DOI
10.1146/annurev.immunol.22.012703.104538
.
PMID
15771591
. (anglicky)
- ↑
BOISVERT, Judie; EDMONDSON, Samuel; KRUMMEL, Matthew F. Immunological Synapse Formation Licenses CD40-CD40L Accumulations at T-APC Contact Sites. S. 3647?3652.
The Journal of Immunology
[online]. 2004-09-15 [cit. 2020-12-10]. Ro?. 173, ?is. 6, s. 3647?3652.
DOI
10.4049/jimmunol.173.6.3647
. (anglicky)
- ↑
THAULAND, Timothy J.; PARKER, David C. Diversity in immunological synapse structure: Immunological synapse diversity. S. 466?472.
Immunology
[online]. 2010-12 [cit. 2020-12-10]. Ro?. 131, ?is. 4, s. 466?472.
Dostupne online
.
DOI
10.1111/j.1365-2567.2010.03366.x
. (anglicky)
- ↑
FRIEDL, Peter; DEN BOER, Annemieke Th.; GUNZER, Matthias. Tuning immune responses: diversity and adaptation of the immunological synapse. S. 532?545.
Nature Reviews Immunology
[online]. 2005-07 [cit. 2020-12-10]. Ro?. 5, ?is. 7, s. 532?545.
Dostupne online
.
DOI
10.1038/nri1647
.
PMID
15999094
. (anglicky)
- ↑
a
b
c
d
AL-DACCAK, Reem; MOONEY, Nuala; CHARRON, Dominique. MHC class II signaling in antigen-presenting cells. S. 108?113.
Current Opinion in Immunology
[online]. 2004-02 [cit. 2020-12-10]. Ro?. 16, ?is. 1, s. 108?113.
DOI
10.1016/j.coi.2003.11.006
.
PMID
14734118
. (anglicky)
- ↑
TABATA, Hiroki; MATSUOKA, Takako; ENDO, Fumio; NISHIMURA, Yasuharu; MATSUSHITA, Sho. Ligation of HLA-DR Molecules on B Cells Induces Enhanced Expression of IgM Heavy Chain Genes in Association with Syk Activation. S. 34998?35005.
Journal of Biological Chemistry
[online]. 2000-11-10 [cit. 2020-12-10]. Ro?. 275, ?is. 45, s. 34998?35005.
Dostupne online
.
DOI
10.1074/jbc.M002089200
. (anglicky)
- ↑
MOURAD, Walid; GEHA, Raif S; CHATILA, Talal. Engagement of major histocompatibility complex class II molecules induces sustained, lymphocyte function-associated molecule 1-dependent cell adhesion.. S. 1513?1516.
Journal of Experimental Medicine
[online]. 1990-11-01 [cit. 2020-12-10]. Ro?. 172, ?is. 5, s. 1513?1516.
Dostupne online
.
DOI
10.1084/jem.172.5.1513
.
PMID
2230655
. (anglicky)
- ↑
NABAVI, N.; FREEMAN, G. J.; GAULT, A.; GODFREY, D.; NADLER, L. M.; GLIMCHER, L. H. Signalling through the MHC class II cytoplasmic domain is required for antigen presentation and induces B7 expression. S. 266?268.
Nature
[online]. 1992-11 [cit. 2020-12-10]. Ro?. 360, ?is. 6401, s. 266?268.
Dostupne online
.
DOI
10.1038/360266a0
.
PMID
1279442
. (anglicky)
- ↑
NASHAR, Toufic O.; DRAKE, James R. Dynamics of MHC Class II-Activating Signals in Murine Resting B Cells. S. 827?838.
The Journal of Immunology
[online]. 2006-01-15 [cit. 2020-12-10]. Ro?. 176, ?is. 2, s. 827?838.
DOI
10.4049/jimmunol.176.2.827
. (anglicky)
- ↑
a
b
BOBBITT, Kevin R.; JUSTEMENT, Louis B. Regulation of MHC Class II Signal Transduction by the B Cell Coreceptors CD19 and CD22. S. 5588?5596.
The Journal of Immunology
[online]. 2000-11-15 [cit. 2020-12-11]. Ro?. 165, ?is. 10, s. 5588?5596.
Dostupne online
.
DOI
10.4049/jimmunol.165.10.5588
.
PMID
11067914
. (anglicky)
- ↑
LEVEILLE, Claire; CASTAIGNE, Jean-Gabriel; CHARRON, Dominique; AL?DACCAK, Reem. MHC class II isotype-specific signaling complex on human B cells. S. 2282?2291.
European Journal of Immunology
[online]. 2002 [cit. 2020-12-11]. Ro?. 32, ?is. 8, s. 2282?2291.
Dostupne online
.
DOI
10.1002/1521-4141(200208)32:8<2282::AID-IMMU2282>3.0.CO;2-M
.
PMID
12209641
. (anglicky)
- ↑
JIN, Lei; WATERMAN, Paul M.; JONSCHER, Karen R.; SHORT, Cindy M.; REISDORPH, Nichole A.; CAMBIER, John C. MPYS, a Novel Membrane Tetraspanner, Is Associated with Major Histocompatibility Complex Class II and Mediates Transduction of Apoptotic Signals. S. 5014?5026.
Molecular and Cellular Biology
[online]. 2008-08-15 [cit. 2020-12-11]. Ro?. 28, ?is. 16, s. 5014?5026.
Dostupne online
.
DOI
10.1128/MCB.00640-08
.
PMID
18559423
. (anglicky)
- ↑
JIN, Lei; STOLPA, John C.; YOUNG, Ryan M.; PUGH-BERNARD, Aimee E.; REFAELI, Yosef; CAMBIER, John C. MHC class II structural requirements for the association with Igα/β, and signaling of calcium mobilization and cell death. S. 184?194.
Immunology Letters
[online]. 2008-03 [cit. 2020-12-11]. Ro?. 116, ?is. 2, s. 184?194.
Dostupne online
.
DOI
10.1016/j.imlet.2007.11.023
.
PMID
18194817
. (anglicky)
- ↑
Murphy, K.M., P. Travers, and M. Walport, Janeway's Immunobiology2011: Garland Science.