 Fosforylovany
serinovy
zbytek
Fosforylovany
serinovy
zbytek
Fosforylace
je
adice
fosfatovych skupin (PO
3?
4
) na proteiny nebo jine organicke
molekuly
. M??e m?nit strukturu
protein?
v
enzymech
a tim i jejich funkci a ?innost. Fosforylace protein? hraje vyznamnou roli v cele ?ad? bun??nych proces?. Z tohoto d?vodu se stava p?edm?tem ?ady biochemickych vyzkum?.
V roce 1906 Phoebus A. Levene v Rockefellerov? ustavu pro leka?sky vyzkum identifikoval
fosfat
v bilkovin? vitellin,
[1]
a v roce 1933 Fritz Lipmann objevil fosfoserin v kaseinu.
[2]
Nicmen? trvalo dal?ich 20 let, ne? Eugene P. Kennedy popsal prvni "enzymatickou fosforylaci protein?".
[3]
Reverzibilni fosforylace protein? je d?le?ity regula?ni mechanismus, ktery se vyskytuje u
prokaryotickych
i
eukaryotickych organism?
.
[4]
[5]
[6]
[7]
Kinazy
fosforyluji bilkoviny a fosfatazy bilkoviny defosforyluji. Mnohe enzymy a
receptory
jsou ve stavu "zapnuty" nebo "vypnuty" prost?ednictvim fosforylace a defosforylace. Reverzibilni fosforylace vede ke konforma?nim zm?nam struktury mnohych
enzym?
a
receptor?
, ktere zp?sobuji aktivaci nebo deaktivaci. Fosforylace se v eukaryotickych proteinech obvykle vyskytuje na
aminokyselinach
serin
,
threonin
,
tyrosin
a
histidinovych zbytcich
. Histidinova fosforylace eukaryotickych protein? je ?ast?j?i ne? fosforylace na
tyrosinu
. V prokaryotickych bilkovinach dochazi k fosforylaci zbytk? aminokyselin serin, threonin, tyrosin, histidin,
arginin
nebo
lysin
.
[4]
[5]
[8]
[8]
[9]
P?idanim
fosfatovych iont?
(HPO
2-
4
) na polarni R skupiny
aminokyselinovych zbytk?
se mohou zm?nit hydrofobni ?asti proteinu na polarni a extremn? hydrofilni ?ast molekuly. Timto zp?sobem je mo?ne zavest konforma?ni zm?nu ve struktu?e proteinu prost?ednictvim interakce s jinymi hydrofobnimi a hydrofilnimi ?astmi
proteinu
.
Jeden takovy p?iklad regulace je fosforylace
p53
tumor supresorovych protein?. Protein
p53
je siln? regulovan
[10]
a obsahuje vice ne? 18 r?znych mist fosforylace. Aktivace p53 m??e vest k zastav?
bun??neho cyklu
, ktery m??e byt obracen a za ur?itych okolnosti m??e vest k
apoptoticke bun??ne smrti
.
[11]
Tato aktivita se vyskytuje pouze v situacich, kdy jsou bu?ky po?kozene, nebo je u zdravych jedinc? naru?ena jejich
fyziologie
. Po deaktiva?nim signalu je protein znovu defosforylovan a p?estane fungovat. Aktivace fosforylaci je mechanismus, ktery se vyskytuje v mnoha formach p?enosu signal?, jako nap?iklad zp?sob, jakym se sv?tlo zpracovava ve sv?tlo?ivnych bu?kach sitnice.
Regula?ni role fosforylace:
- Termodynamika biologickych system? pro reakce vy?adujici energii
- Fosforylace Na
+
/K
+
-ATPazy b?hem p?epravy sodikovych (Na
+
) a draslikovych (K
+
) iont? p?es
bun??nou membranu
v osmoregulaci pro udr?eni
homeostazy
v t?le.
- Zprost?edkovani inhibice enzymu
- Fosforylace enzymu GSK-3 pomoci protein kinazy B jako sou?ast inzulinove signalni drahy.
[12]
- Fosforylace Src tyrozin kinazy p?es C-terminalni Src kinazu (Csk) indukuje konforma?ni zm?nu v enzymu, ktera zakryva jeho kinazove domeny, a tak se vypne kinazova aktivita.
[13]
- Protein-proteinove interakce prost?ednictvim "rozeznavacich domen"
- Fosforylace cytosolickych komponent? NADPH oxidazy, co? je velky membranov? vazany multi-proteinovy enzym p?itomny u
fagocytarnich bun?k
, hraje d?le?itou roli v regulaci protein-proteinovych interakci v tomto enzymu.
[14]
- Degradace protein?
- V roce 1990 bylo zji?t?no, ?e fosforylace n?kterych protein? zp?sobuje jejich degradaci p?es ATP-dependentni ubiquitin / proteazomove drahy. Tyto cilove proteiny se stanou substraty pro jednotlive E3 ubiquitin ligazy pouze tehdy, jsou-li fosforylovany.
Objasn?ni komplexni signalni drahy fosforylace m??e byt obti?ne. V bun??nych signalnich drahach protein A fosforyluje protein B a protein B pak fosforyluje protein C. Nicmen?, v jinych signalnich drahach protein D fosforyluje protein A, nebo fosforyluje protein C. Globalni p?istupy jako je fosfoproteomika (co? je studium fosforylovanych protein? prost?ednictvim proteomiky v kombinaci s hmotnostni spektrometrii), byly vyu?ity k identifikaci a kvantifikaci dynamickych zm?n fosforylovanych protein? v pr?b?hu ?asu. Tyto techniky jsou d?le?ite pro systematickou analyzu komplexnich fosforyla?nich siti.
[15]
Byly usp??n? pou?ity k identifikaci dynamickych zm?n ve stavu fosforylace na vice ne? 6000 mistech po stimulaci epidermalnim r?stovym faktorem.
[16]
Jiny p?istup k pochopeni fosforyla?nich siti je na zaklad? m??eni geneticke interakce mezi vice fosforylovanymi proteiny a jejich cili. To ukazuje zajimave opakujici se vzorce interakci tzv. si?ove motivy.
[17]
Existuje tisice r?znych fosforyla?nich mist v dane bu?ce, proto?e:
- Existuje tisice r?znych druh? bilkovin v konkretni bu?ce (nap?iklad
lymfocyt?
)
- Odhaduje se, ?e 1/10 a? 1/2 protein? je fosforylovana (v ur?item bun??nem stavu)
- Fosforylace se ?asto vyskytuje na n?kolika r?znych mistech na danem proteinu
Fosforylace jakehokoli mista na danem proteinu m??e zm?nit funkci nebo lokalizaci tohoto proteinu. Nap?iklad, pokud je aminokyselina Serin-473 ("S473") v proteinu AKT fosforylovana, protein kinaza B je funk?n? aktivni jako kinaza. Pokud protein kinaza B neni fosforylovana, je to neaktivni
kinaza
.
Uvnit? bilkoviny m??e dojit k fosforylaci na n?kolika aminokyselinach. Fosforylace na
serinu
je nej?ast?j?i, hned za nim nasleduje
threonin
. Tyrosinova fosforylace je pom?rn? vzacna. Vzhledem k tomu, ?e tyrosin-fosforylovane proteiny je pom?rn? snadne purifikovat pomoci
protilatek
, jsou fosforylace prost?ednictvim tyrosinu pom?rn? dob?e prozkoumane. Fosforylace histidinu a
aspartatu
se vyskytuji hlavn? u prokaryot jako sou?ast dvouslo?kove signalizace. V n?kterych specifickych p?ipadech se m??e vyskytovat take v signalnich drahach u eukaryot.
[18]
Protilatky mohou byt pou?ity jako vykonne nastroje pro detekci toho, zda je protein na ur?item mist? fosforylovan. Protilatky va?ou a detekuji konforma?ni zm?ny vyvolane fosforylaci protein?. Tyto protilatky se nazyvaji fosfo-specificke. Nyni jsou k dispozici stovky t?chto protilatek.
[19]
Jsou to d?le?ite biochemicke nastroje a to jak pro zakladni vyzkum, tak pro klinicke diagnozy.
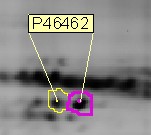 P?iklad posttransla?ni modifikace detekovane na 2D gelu YUI(hranice byly vymezene podle analytickeho softwaru, identifikace byla provedena hmotnostni spektrometrii, P46462 je ID proteinu v Expasy)
P?iklad posttransla?ni modifikace detekovane na 2D gelu YUI(hranice byly vymezene podle analytickeho softwaru, identifikace byla provedena hmotnostni spektrometrii, P46462 je ID proteinu v Expasy)
PTM (Posttransla?ni modifikace) izoformy jsou snadno zjistitelne na 2D gelu. Fosforylace nahrazuje neutralni
hydroxylove skupiny
na serinech a threoninech nebo tyrosinech za negativn? nabite fosfatove skupiny s pKs kolem 1.2 a 6.5. Pod
pH
5,5 fosfaty p?idaji jeden zaporny naboj, u pH 6,5 p?idavaji 1,5 zaporneho naboje, nad pH 7,5 p?idavaji 2 zaporne naboje. Relativni mno?stvi ka?de izoformy m??e byt take snadno a rychle ur?eno z intenzity zbarveni na 2D gelu.
V n?kterych velmi specifickych p?ipadech, je mo?ne detekovat fosforylaci jako posun v proteinu. Tuhle elektroforetickou pohyblivost lze provad?t pomoci jednoduchych 1rozm?rnych SDS-PAGE gel?, jak je to popsano nap?iklad pro transkrip?ni koaktivator v ?lanku Kovacs et al.
[20]
V?t?ina fosforyla?nich mist, pro ktere byly tyto mobilni posuny popsany spadaji do kategorie SP a TP mist. (tj. prolinove zbytky nasledovane fosforylovanymi serinovymi nebo threoninovymi zbytky).
Nedavne rozsahle analyzy
hmotnostni spektrometrie
byly pou?ity k ur?eni mista fosforylace protein?. Za posledni 4 roky, desitky studii zve?ejnily ka?dou identifikaci tisic? mist, z nich? d?ive mnohe nebyly popsany.
[21]
[22]
Hmotnostni spektrometrie je idealni pro takove analyzy, pro ktere p?idavani fosforylace vede ke zvy?eni mno?stvi protein? a fosforylovaneho zbytku. Nicmen?, pokro?ile, vysoce p?esne hmotnostni spektrometry jsou u t?chto studii nezbytne, co? p?edstavuje omezeni pouze na laborato?e s nejmodern?j?imi hmotnostnimi spektrometry.
Podrobna charakterizace lokalit fosforylace je velmi obti?na, a kvantifikaci protein? fosforylaci pomoci hmotnostni spektrometrie vy?aduje vnit?ni standardni p?istupy s pou?itim
izotop?
[23]
Relativni kvantifikaci lze ziskat s r?znymi diferencialnimi technologiemi, nap?iklad ozna?ovani prost?ednictvim izotop?.
[24]
Existuje take n?kolik kvantitativnich metod proteinove fosforylace, v?etn? fluorescen?nich a imunologickych, FRET, TRF,
fluorescen?ni polarizace
,
fluorescen?ni spektroskopie
,
gelova retarda?ni analyza (EMSA)
, bead-based detekce (metoda pozostavajici ze t?ech prvk?: kuli?ka (pr?m?rem 5,6-microm?), oligomerni zachycovaci sondy p?ipojene k povrchu a t?i fluorofory pro multiplexni detekci), cell-based metody (metody zalo?ene na bazi bun??nych test? se vztahuji na n?ktery z ?ady r?znych experiment? zalo?enych na pou?iti ?ivych bun?k. Tyto metody mohou obsahovat r?zne testy, ktere m??i proliferaci bun?k, toxicitu, motilitu, m??itelnou vyrobu produktu, a morfologii bun?k. Cell-based testy nabizeji p?esn?j?i vyjad?eni realneho ?ivota v modelu, proto?e jsou pou?ivany ?ive bu?ky, a take nabizeji mo?nost dynamickeho experimentu prost?ednictvim sledovani mno?stvi nebo chovani ?ivych bun?k).
[25]
[26]
ATP, "vysoce energeticke" vym?nne medium v bu?ce, je syntetizovano v mitochondriich p?idanim t?eti fosfatove skupiny na ADP v procesu nazvanem oxida?ni fosforylace. Dal?i zp?sob tvorby ATP je syntetizace na ukor slune?ni energie v procesu fotofosforylace v
chloroplastech
rostlinnych bun?k.
Fosforylace cukr? je ?asto prvni faze jejich
katabolismu
. To umo??uje bu?kam hromadit cukry, proto?e fosfatova skupina brani molekulam difundovat zpatky p?es jejich transportery. Dale existuje tzv.
substratova fosforylace
, p?i ktere vznikne ATP mimo
dychaci ?et?zec
(nap?.: z
GTP
vznikajici v
Citratovem cyklu
, p?i
glykolyze
, apod...).
V tomto ?lanku byl pou?it
p?eklad
textu z ?lanku
Phosphorylation
na anglicke Wikipedii.
- ↑
Levene PA; ALSBERG CL. The cleavage products of vitellin.
J. Biol. Chem.
. 1906, s. 127?133.
Dostupne v archivu
po?izenem dne 2020-06-09.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Lipmann FA; LEVENE PA. Serinephosphoric acid obtained on hydrolysis of vitellinic acid.
J. Biol. Chem.
. 1932, s. 109?114.
Dostupne v archivu
po?izenem dne 2020-06-09.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Burnett G; KENNEDY EP. The enzymatic phosphorylation of proteins.
J. Biol. Chem.
. 1954, s. 969?80.
Dostupne v archivu
po?izenem dne 2020-06-09.
PMID
13221602
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
a
b
Cozzone AJ. Protein phosphorylation in prokaryotes.
Annu. Rev. Microbiol.
. 1988, s. 97?125.
DOI
10.1146/annurev.mi.42.100188.000525
.
PMID
2849375
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
a
b
Stock JB; NINFA AJ; STOCK AM. Protein phosphorylation and regulation of adaptive responses in bacteria.
Microbiol. Rev.
. 1989, s. 450?90.
PMID
2556636
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Chang C; STEWART RC. The Two-Component System . Regulation of Diverse Signaling Pathways in Prokaryotes and Eukaryotes.
Plant Physiol.
. 1998, s. 723?31.
DOI
10.1104/PPSOE.117.3.723
.
PMID
9662515
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Barford D; DAS AK; EGLOFF MP. The structure and mechanism of protein phosphatases: insights into catalysis and regulation.
Annu Rev Biophys Biomol Struct
. 1998, s. 133?64.
DOI
10.1146/annurev.biophys.27.1.133
.
PMID
9646865
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
a
b
Ciesla J; FRACZYK T; RODE W. Phosphorylation of basic amino acid residues in proteins: important but easily missed.
Acta Biochim Pol
. 2011, s. 137?47.
PMID
21623415
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Deutscher J; SAIER. Ser/Thr/Tyr protein phosphorylation in bacteria - for long time neglected, now well established.
J Mol Microbiol Biotechnol
. 2005, s. 125?31.
DOI
10.1159/000089641
.
PMID
16415586
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Ashcroft M; KUBBUTAT MH; VOUSDEN KH. Regulation of p53 Function and Stability by Phosphorylation.
Mol. Cell. Biol.
. 1999, s. 1751?8.
PMID
10022862
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Bates S; VOUSDEN KH. p53 in signaling checkpoint arrest or apoptosis.
Curr. Opin. Genet. Dev.
. 1996, s. 12?8.
DOI
10.1016/S0959-437X(96)90004-0
.
PMID
8791489
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
van Weeren PC; DE BRUYN KM; DE VRIES-SMITS AM; VAN LINT J; BURGERING BM. Essential role for protein kinase B (PKB) in insulin-induced glycogen synthase kinase 3 inactivation. Characterization of dominant-negative mutant of PKB.
J. Biol. Chem.
. 1998, s. 13150?6.
DOI
10.1074/jbc.273.21.13150
.
PMID
9582355
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Cole PA; SHEN K; QIAO Y; WANG D. Protein tyrosine kinases Src and Csk: a tail's tale.
Curr Opin Chem Biol
. 2003, s. 580?5.
DOI
10.1016/j.cbpa.2003.08.009
.
PMID
14580561
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Babior BM. NADPH oxidase: an update.
Blood
. 1999, s. 1464?76.
PMID
10029572
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Olsen JV; BLAGOEV B; GNAD F; MACEK B; KUMAR C; MORTENSEN P; MANN M. Global, in vivo, and site-specific phosphorylation dynamics in signaling networks.
Cell
. 2006, s. 635?48.
DOI
10.1016/j.cell.2006.09.026
.
PMID
17081983
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Li-Rong Y; ISSAQ HJ; VEENSTRA TD. Phosphoproteomics for the discovery of kinases as cancer biomarkers and drug targets.
Proteomics - Clinical Applications
. 2007, s. 1042?1057.
DOI
10.1002/prca.200700102
.
PMID
21136756
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Fiedler D; BRABERG H; MEHTA M; CHECHIK G; CAGNEY, Gerard; MUKHERJEE, Paromita; SILVA, Andrea C. Functional Organization of the S. cerevisiae Phosphorylation Network.
Cell
. 2009, s. 952?963.
DOI
10.1016/j.cell.2008.12.039
.
PMID
19269370
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Thomason P; KAY R. Eukaryotic signal transduction via histidine-aspartate phosphorelay.
J. Cell. Sci.
. 2000, s. 3141?50.
Dostupne online
.
PMID
10954413
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
phospho antibody
[online]. [cit. 2009-01-22].
Dostupne v archivu
po?izenem dne 2009-01-29.
Je zde pou?ita ?ablona
{{
Cite web
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
KOVACS KA, Steinmann M, Magistretti PJ, Halfon O, Cardinaux JR. CCAAT/enhancer-binding protein family members recruit the coactivator CREB-binding protein and trigger its phosphorylation.
J Biol. Chem.
. UNITED STATES: 2003, s. 36959?65.
ISSN
0021-9258
.
DOI
10.1074/jbc.M303147200
.
PMID
12857754
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Munton RP; TWEEDIE-CULLEN R; LIVINGSTONE-ZATCHEJ M; WEINANDY F; WAIDELICH M; LONGO D; GEHRIG P. Qualitative and quantitative analyses of protein phosphorylation in naive and stimulated mouse synaptosomal preparations.
Mol. Cell Proteomics
. 2007, s. 283?93.
DOI
10.1074/mcp.M600046-MCP200
.
PMID
17114649
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Trinidad JC; THALHAMMER A; SPECHT CG; LYNN AJ; BAKER PR; SCHOEPFER R; BURLINGAME AL. Quantitative analysis of synaptic phosphorylation and protein expression.
Mol. Cell Proteomics
. 2008, s. 684?96.
DOI
10.1074/mcp.M700170-MCP200
.
PMID
18056256
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Gerber SA; RUSH J; STEMMAN O; KIRSCHNER MW; GYGI SP. Absolute quantification of proteins and phosphoproteins from cell lysates by tandem MS.
Proc. Natl. Acad. Sci. U.S.A.
. 2003, s. 6940?5.
DOI
10.1073/pnas.0832254100
.
PMID
12771378
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Gygi SP; RIST B; GRIFFIN TJ; ENG J; AEBERSOLD R. Proteome analysis of low-abundance proteins using multidimensional chromatography and isotope-coded affinity tags.
J. Proteome Res.
. 2002, s. 47?54.
DOI
10.1021/pr015509n
.
PMID
12643526
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Olive DM. Quantitative methods for the analysis of protein phosphorylation in drug development.
Expert Rev Proteomics
. 2004, s. 327?41.
DOI
10.1586/14789450.1.3.327
.
PMID
15966829
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.
- ↑
Chen H; KOVAR J; SISSONS S; COX K; MATTER W; CHADWELL F; LUAN P. A cell-based immunocytockemical assay for monitoring kinase signaling pathways and drug efficacy.
Anal. Biochem.
. 2005, s. 136?42.
DOI
10.1016/j.ab.2004.11.015
.
PMID
15707944
.
Je zde pou?ita ?ablona
{{
Cite journal
}}
ozna?ena jako k ?pouze do?asnemu pou?iti“.