 aparatura na elektroforezu
aparatura na elektroforezu
Elektroforeza
je soubor
separa?nich metod
, ktere vyu?ivaji k d?leni latek jejich odli?nou pohyblivost ve stejnosm?rnem elektrickem poli. Na principu rozdilnych
elektroforetickych mobilit
se p?i ni d?li nabite
molekuly
(
ionty
).
P?i separaci latek v kapila?e se zde vedle elektroforetickeho principu (pohyb nabitych molekul v elektrickem poli) uplat?uje te?
elektroosmoticky tok
(angl. electroosmotic flow, EOF), co? je spontanni tok kapaliny v kapila?e v d?sledku naboje (obvykle zaporneho) na vnit?ni st?n? kapilary.
V roce
1892
bylo publikovano, ?e anorganicke ?astice v
koloidnim roztoku
pod vlivem
elektrickeho pole
nenahodn? putuji. Nedlouho pote byl tento jev popsan i u protein? ve vodnych roztocich.
V roce
1948
byl
Nobelovou cenou
ocen?n
?vedsky
chemik
Arne Tiselius
, ktery ve 30. letech minuleho stoleti postavil aparaturu separujici proteiny krevniho sera na zaklad? jejich elektroforetickych mobilit.
Podle prost?edi, ve kterem k separaci dochazi, se elektroforeticke metody dale d?li na:
 schema kapilarni zonove elektroforezy
schema kapilarni zonove elektroforezy
Kapilarni zonova elektroforeza
(te?
CZE
z angl.
Capillary Zone Electrophoresis
) je druh elektroforezy, p?i ni? jsou nabite molekuly una?eny
elektroosmotickym
tokem separa?niho
pufru
uvnit?
kapilary
a? k
detektoru
. Proto?e tyto ionty migruji v pufru rozdilnymi elektroforetickymi rychlostmi, dochazi k separaci. B?hem jedineho
experimentu
lze d?lit a detekovat jak kladn?, tak zaporn? nabite molekuly (ionty), ale take neutralni ?astice.
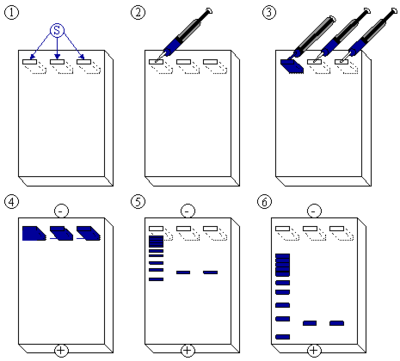 schema elektroforezy
schema elektroforezy
Kapilarni gelova elektroforeza
( te?
CGE
z angl.
Capillary Gel Electrophoresis
) je druh elektroforezy, p?i ni? se latky rozd?luji na zaklad? pohyblivosti v gelu. V kapila?e se nachazi
gel
, jen? maximalizuje diference mezi elektroforetickymi rychlostmi velkych iont? r?znych tvar?, ktere r?zn? usp??n? migruji pory gelu.
Gel zabra?uje vzniku elektroosmotickeho toku, a proto jen jeden druh kladnych ?i zapornych iont? putuje sm?rem k detektoru.
Pohyblivost v gelu zavisi na naboji separovane molekuly a jeji molekulove hmotnosti, intenzit? elektrickeho pole a samoz?ejm? typu a porozit? gelu (k nejb??n?j?im gel?m pat?i polyakrylamidovy a agarosovy gel).
Na rozdil od
CZE
p?i
CGE
m??e byt separovan a detekovan b?hem jednoho experimentu pouze jeden typ iont?. Kapilarni gelova elektroforeza se vyu?iva zejmena pro velke ionty, jakymi jsou sacharidy, peptidy,
bilkoviny
, sest?ihy
DNA
a
RNA
.
Existuji i varianty teto metody (elektroforeza v polyakrylamidovem gelu v p?itomnosti
dodecylsiranu sodneho
, angl. sodium-dodecyl-sulphate-polyacrylamide-gel-electrophoresis,
SDS-PAGE
), kde se molekuly bilkovin d?li tem?? vyhradn? podle sve molekulove hmotnosti.
Gelova elektroforeza je v sou?asnosti nejroz?i?en?j?i elektroforetickou metodou.
Rychlost elektroforezy lze vyjad?it nasledujicim vztahem:
- υ
=
C
.
E
.
ζ
.
ε
r
.
ε
0
/
η
kde
- υ
je linearni rychlost pohybu ?astice,
- C
je parametr zavisejici na tvaru ?astic a tlou??ce elektricke dvojvrstvy
- E
je intenzita elektrickeho pole
- ζ
je elektrokineticky potencial
- ε
r
je relativni permitivita kapaliny
- ε
0
je permitivita vakua
- η
je viskozita prost?edi