| Acetanhydrid
|
|---|
 Vzhled
|
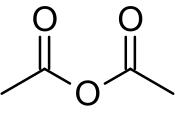
 Struktura
|
| Obecne
|
|---|
| Systematicky nazev
| Anhydrid kyseliny octove
|
|---|
| Ostatni nazvy
| Acetanhydrid
|
|---|
| Sumarni vzorec
| C
4
H
6
O
3
|
|---|
| Vzhled
| Pr?hledna kapalina
|
|---|
| Identifikace
|
|---|
| Registra?ni ?islo CAS
| 108-24-7
|
|---|
| Vlastnosti
|
|---|
| Molarni hmotnost
| 102,09 g/mol
|
|---|
| Teplota tani
| ?73,1 °C (
200,0
K
)
|
|---|
| Teplota varu
| 139,8 °C (
413 K
)
|
|---|
| Hustota
| 1,082 g/cm
3
|
|---|
| Index lomu
| 1,390 1
|
|---|
| Rozpustnost
ve
vod?
| 2,6 g/100 ml
|
|---|
| Bezpe?nost
|
|---|
 GHS02 GHS02
 GHS05 GHS05
 GHS07 GHS07
Nebezpe?i
[1]
|
| R-v?ty
| R10
R20/22
R34
|
|---|
| S-v?ty
| (
S1/2
)
S26
S36/37/39
S45
|
|---|
| NFPA 704
| |
|---|
| Teplota vzplanuti
| 49 °C
|
|---|
| Teplota vzniceni
| 316 °C
|
|---|
| Meze vybu?nosti
| 2,7?10,3 %
|
|---|
Neni-li uvedeno jinak, jsou pou?ity
jednotky
SI
a
STP
(25 °C, 100 kPa).
|
Acetanhydrid
(te?
anhydrid kyseliny octove
, systematicky
anhydrid kyseliny ethanove
) je
organicka slou?enina
se vzorcem (CH
3
CO)
2
O, znama take pod zkratkou Ac
2
O. jedna se o nejjednodu??i izolovatelny
anhydrid karboxylove kyseliny
, s ?irokym vyu?itim v organickych syntezach. Je to ?ira kapalina vyzna?ujici se silnym zapachem po
kyselin? octove
, kterou tvo?i p?i reakci se vzdu?nou vlhkosti.
Acetanhydrid je flexibilni molekulou, jeji? struktura neni planarni.
[2]
Rezonan?ni posun elektron?
pi vazeb
p?es centralni atom kysliku ma jen maly vliv na stabilitu struktury oproti dipolove interakci mezi dv?ma
karbonylovymi
kysliky. Rozdily v energiich mezi nejvyhodn?j?imi mo?nostmi prostoroveho uspo?adani jsou rovn?? nizke.
[3]
Jako u v?t?iny anhydrid? i zde plati, ?e karbonylovy atom uhliku ma
elektrofilni
charakter a odstupujici skupinou je
karboxylat
. Na vysokou elektrofilitu ma vliv asymetricka prostorova struktura.
Acetanhydrid poprve syntetizoval v roce 1852 francouzsky chemik
Charles Frederic Gerhardt
zah?ivanim
octanu draselneho
s
benzoylchloridem
.
[4]
Nukleofilni acylova substituce
chloridu kyseliny karboxylatovym aniontem je typicky zp?sob p?ipravy anhydrid? obecn?.
[5]
Pr?myslov? se vyrabi reakci
oxidu uhelnateho
s
methylesterem kyseliny octove
,
[6]
dle rovnice:
- CO
+
CH
3
CO
2
CH
3
?
LiI
,
RhI
3
→ (CH
3
CO)
2
O
Tato reakce probiha za
katalyzy
jodidem lithnym
a
jodidem rhoditym
.
Lze jej rovn?? vyrobit reakci
ketenu
s
kyselinou octovou
p?i teplot? 45?55 °C a nizkem tlaku (0,05?0,2 bar). Tento zp?sob byl vyvinut v roce 1922 firmou
Wacker Chemie
v reakci na rostouci poptavku acetanhydridu pro vyrobu
acetatu celulozy
.
[7]
Diky nizke cen? neni acetanhydrid b??n? v laborato?ich p?ipravovan.
Acetanhydrid je vhodnym ?inidlem pro
acetylaci
, tedy navazani acetylove skupiny na organicke substraty. V t?chto reakcich figuruje jako zdroj CH3CO
+
.
Alkoholy
lze acetylovat snadno,
[8]
reakce probiha dle obecne rovnice
za vzniku
ester? kyseliny octove
a kyseliny octove. Katalyzatorem je ?asto baze, nap?.
pyridin
, pro specializovane aplikace se vyu?ivaji
skandiove
soli jako?to
Lewisovy kyseliny
.
[9]
Obdobna je reakce s
aminy
.
Acetanhydrid rovn?? acetyluje aromaticka jadra, obvykle za katalyzy kyselinami. Mezi nazorne reakce pat?i acetylace
benzenu
na
acetofenon
[10]
a
ferrocenu
na
acetylferrocen
:
[11]
- (C
5
H
5
)
2
Fe + (CH
3
CO)
2
O → (C
5
H
5
)Fe(C
5
H
4
COCH
3
) + CH
3
CO
2
H
Dikarboxylove kyseliny
tvo?i po reakci s acetanhydridem p?islu?ne
anhydridy
.
[12]
Lze tak p?ipravit i sm?sne anhydridy, nap?.
acetyl-nitrat
reakci s
kyselinou dusi?nou
.
Acetanhydrid se pouze omezen? rozpou?ti ve vod?, proto?e s ni reaguje, a lze tedy dosahnout maximalni
koncentrace
p?ibli?n? 2,6 gram? ve 100 mililitrech vody;
[13]
stabilita vodnych roztoku je omezena, proto?e slou?enina reaguje na produkt voln? misitelny s vodou:
[14]
- (CH
3
CO)
2
O +
H
2
O
→ 2
CH
3
COOH
Aby se p?ede?lo znehodnoceni acetanhydridu vzdu?nou vlhkosti, je nutne jej skladovat ve vzduchot?snych ampulich a po otev?eni se musi rychle spot?ebovat.
 N?mecky popsana lahev acetanhydridu
N?mecky popsana lahev acetanhydridu
Acetanhydrid se vyu?iva zejmena na acetylaci pr?myslov? vyznamnych chemickych surovin. Nejroz?i?en?j?im pou?itim je p?evad?ni
celulozy
na acetat celulozy, ktery je sou?asti
fotografickeho filmu
, jinych pota?enych material? a
cigaretovych filtr?
. Acetylaci
kyseliny salicylove
vznika kyselina
kyselina acetylsalicylova
, znama pod obchodnimi nazvy aspirin ?i acylpyrin. V
autoklavu
lze acetanhydrid vyu?it k napu?t?ni a nasledne acetylaci d?eva za u?elem zvy?eni jeho odolnosti.
[15]
V potravina?stvi je b??nym acetyla?nim ?inidlem p?i vyrob?
modifikovanych ?krob?
(E1414, E1420, E1422).
Rovn?? se pou?iva p?i vyrob?
heroinu
(diacetylmorfinu) z
morfia
.
Acetanhydrid lze vyu?it k acetylaci
morfinu
na
heroin
(diacetylmorfin). Z tohoto d?vodu je na seznamu regulovanych latek americke
DEA
, a v mnoha dal?ich zemich je jeho prodej omezen.
[16]
[17]
Acetanhydrid je dra?divou a ho?lavou kapalinou, zp?sobuje zava?ne
poleptani
k??e a ma slzotvorne u?inky. ?kodlive jsou i pary.
[18]
Kv?li reaktivit? s vodou a alkoholem jsou pro ha?eni po?aru preferovane p?nove nebo sn?hove
hasici p?istroje
.
[19]
V tomto ?lanku byl pou?it
p?eklad
textu z ?lanku
Acetic anhydride
na anglicke Wikipedii.
- ↑
a
b
Acetic anhydride.
pubchem.ncbi.nlm.nih.gov
[online]. PubChem [cit. 2021-05-23].
Dostupne online
. (anglicky)
- ↑
SEIDEL, R. W.; GODDARD, R.; NOTHLING, N. Acetic anhydride at 100 K: the first crystal structure determination.
Acta Crystallographica Section C: Structural Chemistry
. 2016-10-01, ro?. 72, ?is. 10, s. 753?757.
Dostupne online
[cit. 2023-10-28].
ISSN
2053-2296
.
DOI
10.1107/S2053229616015047
. (anglicky)
- ↑
WU, Guang; VAN ALSENOY, C.; GEISE, H. J. Acetic Anhydride in the Gas Phase, Studied by Electron Diffraction and Infrared Spectroscopy, Supplemented With ab Initio Calculations of Geometries and Force Fields.
The Journal of Physical Chemistry A
. 2000-02-01, ro?. 104, ?is. 7, s. 1576?1587.
Dostupne online
[cit. 2023-10-28].
ISSN
1089-5639
.
DOI
10.1021/jp993131z
. (anglicky)
- ↑
GERHARDT, Charles.
Recherches sur les acides organiques anhydres
. [s.l.]: [s.n.] 1074 s.
Dostupne online
. (francouzsky) Google-Books-ID: MXkbAAAAMAAJ.
- ↑
MCMURRY, John.
Organic chemistry
. Ninth edition. vyd. Boston, MA, USA: Cengage Learning 1054 s.
ISBN
978-1-305-08048-5
,
ISBN
978-1-305-63871-6
. S. 701.
- ↑
ZOELLER, Joseph R.; AGREDA, Victor H.; COOK, Steven L. Eastman chemical company acetic anhydride process.
Catalysis Today
. 1992-03-11, ro?. 13, ?is. 1, s. 73?91.
Dostupne online
[cit. 2023-10-27].
ISSN
0920-5861
.
DOI
10.1016/0920-5861(92)80188-S
.
- ↑
History.
www.wacker.com
[online]. [cit. 2023-10-27].
Dostupne online
. (anglicky)
- ↑
Chemical of the Week -- Acetic Acid and Acetic Anhydride.
web.archive.org
[online]. 2006-03-03 [cit. 2023-10-27].
Dostupne v archivu
po?izenem z
originalu
dne 2006-03-03.
- ↑
Organic Syntheses Procedure.
www.orgsyn.org
[online]. [cit. 2023-10-27].
Dostupne online
. (anglicky)
- ↑
Organic Syntheses Procedure.
orgsyn.org
[online]. [cit. 2023-10-27].
Dostupne online
. (anglicky)
- ↑
TABER, Douglas F. Column chromatography: Preparation of Acetyl Ferrocene.
valhalla.chem.udel.edu
[online]. Department of Chemistry and Biochemistry, University of Delaware [cit. 2023-10-27].
Dostupne v archivu
po?izenem z
originalu
dne 2009-05-02.
- ↑
Organic Syntheses Procedure.
orgsyn.org
[online]. [cit. 2023-10-27].
Dostupne online
. (anglicky)
- ↑
Acetic Anhydride: Frequently Asked Questions.
www.bp.com
[online]. British Petroleum [cit. 2023-10-27].
Dostupne v archivu
po?izenem z
originalu
dne 2007-10-11.
- ↑
Acetic Anhydride: Material Safety Data Sheet (PDF).
www.celanese.com
[online]. Celanese [cit. 2023-10-27].
Dostupne v archivu
po?izenem z
originalu
dne 2007-09-27.
- ↑
Making Wood Last Forever With Acetylation.
Chemical & Engineering News
[online]. [cit. 2023-10-27].
Dostupne online
. (anglicky)
- ↑
Federal Register :: Request Access.
unblock.federalregister.gov
[online]. [cit. 2023-10-27].
Dostupne online
.
- ↑
UN Intercepts Taliban's Heroin Chemical in Rare Afghan Victory - Bloomberg.
web.archive.org
[online]. 2012-10-22 [cit. 2023-10-27].
Dostupne v archivu
po?izenem z
originalu
dne 2012-10-22.
- ↑
ICSC 0209 - ACETIC ANHYDRIDE.
www.inchem.org
[online]. [cit. 2023-10-27].
Dostupne online
.
- ↑
CDC - NIOSH Pocket Guide to Chemical Hazards - Acetic anhydride.
www.cdc.gov
[online]. [cit. 2023-10-27].
Dostupne online
.