Оксиди ам?н?в
(N-оксиди) ? пох?дн? третинних (зокрема ? гетероароматичних)
ам?н?в
загально? формули
 . До N-оксид?в також в?дносять аналог?чн? пох?дн? первинних та вторинних ам?н?в
[1]
. N-оксиди
?м?н?в
називають
н?тронами
[2]
.
. До N-оксид?в також в?дносять аналог?чн? пох?дн? первинних та вторинних ам?н?в
[1]
. N-оксиди
?м?н?в
називають
н?тронами
[2]
.
Оксиди третинних ам?н?в ? стаб?льн? речовини, нижч? N-оксиди розчиняються у вод? та обмежено розчинн? в неполярних розчинниках. Оксиди первинних ? вторинних ам?н?в нестаб?льн? ? перегруповуються
in situ
в
г?дроксилам?ни
.
Х?м?ки вивчали оксиди ам?н?в ще до 1900 року, але т?льки п?сля того, як компан?я
IGFarbenindustrie
1939 року отримала патент на речовину диметилдодецил ам?н оксид, оксиди ам?н?в стали загальновизнаними
поверхнево-активними речовинами (ПАР)
. За 22 роки виявлено корисн?сть включення оксид?в ам?ну в рецептури р?дких засоб?в побутово? х?м??, що сприяло широкому ?нтересу виробник?в до цього класу сполук. Зам?на алканолам?д?в жирних кислот, традиц?йно використовуваних, як п?ноутворювач? в рецептурах засоб?в для миття посуду оксидом ам?ну ? це приклад застосування ц??? речовини, що призв?в до ?? популяризац??. Сп?вв?дношення м?ж к?льк?стю оксиду ам?ну, що вводиться в рецептуру, ? одержуваним ефектом компенсувало його вищу варт?сть.
Реакц?я м?ж
перекисом водню
? вторинними або первинними ам?нами не приводить до синтезу речовин, ц?кавих з комерц?йно? точки зору, зате реакц?я з третинними ам?нами да? можлив?сть отримувати речовини, як? можна використовувати не т?льки в р?зних
мийних засобах
, але й у р?дких в?дб?лювачах на основ?
г?похлориту натр?ю
, ? як
антистатик
у
текстильн?й промисловост?
, як стаб?л?затор п?ни при виробництв?
гуми
, як
катал?затори
пол?меризац??
при виготовленн?
пластик?в
, як
антикороз?йн?
склади, як
диспергатор
кальц??вого мила та антибактер?альний агент у твердих
дезодорантах
, що обумовлено доброю сум?сн?стю з ?ншими компонентами складу та
синерг?змом
. Оксиди ам?ну одержують в результат? екзотерм?чно? реакц?? другого порядку м?ж перекисом водню та третинними ам?нами, природа яких може бути
ал?фатичною
,
ароматичною
,
гетероцикл?чною
,
ал?цикл?чною
або ?х комб?нац??ю. У поширених оксидах ам?ну попередня ПАР зазвичай C12-C18 алк?лдиметил ам?н.
Оксиди ам?н?в в?дносять до особливого класу ПАР, класиф?кованих як амфотерн? ПАР. Це пов'язано з тим, що оксид ам?ну ?
цв?тер-?онною
молекулою, яка при зм?н?
pH
в?д низько? до високо? величини зм?ню? свою природу з кат?онно? на не?оногенну.
Оксиди ам?ну мають низький коеф?ц??нт б?олог?чного накопичення, легко видаляються стандартними способами очищення
ст?чних вод
, б?орозкладн? п?д д??ю
аеробних
та
анаеробних бактер?й
. Ус? оксиди ам?ну мають
токсичн?сть
в?д низько? до пом?рно?
[3]
.
Зв'язок
 в N-оксидах диполярний з? сутт?во п?двищеною
електронною густиною
на атом?
кисню
, що ? нуклеоф?льним центром.
в N-оксидах диполярний з? сутт?во п?двищеною
електронною густиною
на атом?
кисню
, що ? нуклеоф?льним центром.
Так, N-оксиди протонуються, утворюючи кристал?чн? сол? з сильними кислотами, однак ? слабшими
основами
, н?ж початков? ам?ни. N-оксиди
алк?люються
з утворенням солей тетразам?щеного
г?дроксиамон?ю
, що розкладаються у водному
лугу
з утворенням
альдег?д?в
та третинних ам?н?в:


Ацилювання
ал?фатичних N-оксид?в приводить до нестаб?льних O-ацилпох?дних, котр?, як ? O-алк?лпох?дн?, розкладаються з утворенням альдег?ду та зам?щеного
ацетам?ду
:


Ця реакц?я з подальшим
г?дрол?зом
ацетам?ду використову?ться як метод
деметилювання
метилам?н?в (
реакц?я Полоновського
):

N-оксиди третинних ам?н?в, в алк?льних зам?сниках яких ? атом
водню
в β-положенн? до N-оксидного азоту, при нагр?ванн? розкладаються з утворенням
алкен?в
та
г?дроксилам?н?в
. Реакц?ю використовують для синтезу алкен?в ?з третинних ам?н?в, N-оксиди яких найчаст?ше синтезують
in situ
?, не очищаючи, п?ддають терм?чному розкладання (
ел?м?нування за Коупом
)
[4]
:

При нагр?ванн? в розчин? лугу або при
фотол?з?
N-оксиди третинних ам?н?в перегруповуються в O-зам?щен? г?дроксилам?ни (
реакц?я Майзенхаймера
), реакц?я зазвичай прот?ка? як 1,2-зсув:

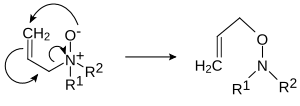
У раз? N-оксид?в ал?лам?н?в можливе 2,3-перегрупування в O-ал?лг?дроксилам?ни:
За катал?тичного
г?дрування
над
н?келем
або
палад??м
, а також п?д д??ю
фосф?н?в
N-оксиди в?дновлюються до початкових ам?н?в.
Загальний метод синтезу N-оксид?в ? окислення третинних ам?н?в
перекисом водню
, реакц?ю в раз? ал?фатичних ам?н?в проводять у нейтральному середовищ?, в раз? ароматичних ? у кислому:

 Кокц?нел?н
Кокц?нел?н
Триметилам?ноксид
[en]
утворю?ться в орган?зм? людини з
триметилам?ну
[en]
, який, у свою чергу, ? результатом переробки
карн?тину
,
хол?ну
,
бета?ну
та
лецитину
кишковим
м?кроб?омом
[5]
.
N-оксиди перг?дроазафенален?в ?
кокцинел?н
[6]
? конверг?н
[7]
входять до складу гемол?мфи
сонечок
, при захисн?й реакц?? гемол?мфа вид?ля?ться з отвор?в б?ля рота ? в суглобах н?жок, надзвичайно г?ркий смак цих сполук в?д?гра? захисну роль.
- ↑
amine oxides // IUPAC Gold Book
.
Арх?в
ориг?налу за 2 листопада 2013
. Процитовано 8 жовтня 2013
.
- ↑
nitrones // IUPAC Gold Book
.
Арх?в
ориг?налу за 21 жовтня 2012
. Процитовано 8 жовтня 2013
.
- ↑
Об оксидах аминов
.
https://nobel-group.by
(русский) . 11 грудня 2017.
Арх?в
ориг?налу за 29 червня 2021
. Процитовано 29 червня 2021
.
- ↑
Arthur C. Cope, Engelbert Ciganek
. Methylenecyclohexane and n, n-dimethylhydroxylamine hydrochloride. Organic Syntheses, Coll. Vol. 4, p.612 (1963); Vol. 39, p.40 (1959)
. Арх?в
ориг?налу
за 22 серпня 2010
. Процитовано 8 жовтня 2013
.
- ↑
Chhibber-Goel J, Singhal V, Parakh N, Bhargava B, Sharma A.
The Metabolite Trimethylamine-N-Oxide is an Emergent Biomarker of Human Health
.
PubMed
.
- ↑
Holloway, Graham J.; de Jong, Peter W.; Brakefield, Paul M.; de Vos, Helene (1 грудня 1991).
Chemical defence in ladybird beetles (Coccinellidae). I. Distribution of coccinelline and individual variation in defence in 7-spot ladybirds (Coccinella septempunctata)
.
CHEMOECOLOGY
.
2
(1): 7?14.
doi
:
10.1007/BF01240660
.
ISSN
1423-0445
. Процитовано 10 вересня 2020
.
- ↑
Tursch, B.; Daloze, D.; Braekman, J. C.; Hootele, C.; Cravador, A.; Losman, D.; Karlsson, R. (1974).
Chemical ecology of arthropods. 9. Structure and absolute configuration of hippodamine and convergine, two novel alkaloids from american ladybug hippodamia convergens (coleoptera- coccinellidae)
.
Tetrahedron Letters
: 409?412.
ISSN
0040-4039
. Арх?в
ориг?налу
за 31 липня 2016
. Процитовано 10 вересня 2020
.