Valens
, vardighet, ar en nagot diffus term som sedan gammalt (1868) anvands inom kemin for att ange antalet bindningar som en atom kan bilda till andra atomer.
Vateatomen
, som endast kan binda en annan atom, sags saledes ha valensen 1,
syreatomen
, som kan binda tva andra atomer (t.ex. i vatten, H
2
O) har valensen 2,
kvaveatomen
3 och
kolatomen
4. Ett och samma amne kan dock ha olika valens i olika foreningar, saledes har jarn i
jarnklorid
(FeCl
2
) valensen 2, i
jarntriklorid
(FeCl
3
) daremot 3. Valensen har numera i stor utstrackning ersatts med det mera valdefinierade begreppet
oxidationstal
.
Vid namngivningen av oorganiska foreningar anges ofta valensen med romerska siffror; i t.ex. jarn(III)klorid (FeCl
3
) har
jarn
saledes valens 3.
Ett amnes valens bestams framst av hur manga
valenselektroner
det har. Kemiska amnen stravar namligen efter att via bindningar dra till sig, avge eller dela
elektroner
sinsemellan, for att pa sa satt komplettera sitt yttersta
elektronskal
och darigenom uppna
adelgasstruktur
.
Begreppet valens anvands forutom om atomer aven om atomgrupperingar eller joner; sulfatjonen (SO
4
2-
) sags saledes ha valensen 2.
| Forening
|
H
2
|
CH
4
|
C
3
H
8
|
C
2
H
2
|
NH
3
|
NaCN
|
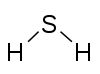
H
2
S
|
H
2
SO
4
|
Cl
2
O
7
|
| Diagram
|

|

|

|

|

|
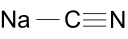
|
|

|

|
| Valenser
|
Vate, 1
|
Kol, 4
Vate, 1
|
Kol, 4
Vate, 1
|
Kol, 4
Vate, 1
|
Kvave, 3
Vate, 1
|
Natrium, 1
Kol, 4
Kvave, 3
|
Svavel, 2
Vate, 1
|
Svavel, 6
Syre, 2
Vate, 1
|
Klor, 7
Syre, 2
|
Etymologin av ordet
"valens"
gar tillbaka till 1425, och betyder
"extrakt, forberedelse"
, fran latinets valentia
"styrka, kapacitet"
, fran tidigare
"vard, varde"
, och den kemiska betydelsen
"ett grundamnes kombinationsstyrka"
noterades fran 1884, fran det tyska
Valenz
.
 William Higgins "kombinationer av ultimata partiklar” (1789).
William Higgins "kombinationer av ultimata partiklar” (1789).
Ar 1789 publicerade
William Higgins
sin syn pa vad han kallade kombinationer av "ultimata" partiklar, som foregick begreppet valensbindningar. Om till exempel, enligt Higgins, kraften mellan en ultimat partikel av syre och ultimat partikel av kvave var sex, sa skulle styrkan av kraften delas i enlighet darmed och likasa for andra kombinationer av slutliga partiklar (se bild).
Den tydliga starten for teorin om kemiska valenser kan emellertid sparas till 1852 i en skrift av
Edward Frank
, dar han kombinerade aldre teorier om fria radikaler och "typteori" med tankar om kemisk affinitet for att visa att vissa partiklar har tendens att kombinera med andra element for att bilda foreningar innehallande 3, det vill saga i de tre-atomgrupper (t.ex. NO
3
, NH
3
, Ni
3
, etc.) eller 5, det vill saga i de fem-atomgrupper (t.ex. NO
5
, NH
5
O, PO
5
, etc.), ekvivalenter av de bifogade elementen. Det ar pa detta satt, enligt Frankland, som deras affiniteter blir bast uppfylld.
De flesta 1800-talskemister definierade valens av ett element som antalet av dess bindningar utan att sarskilja olika typer av valens eller bindningar. Men i det av
Alfred Werner
1893 beskrivna overgangsmetallkoordinationskomplexet som [Co (NH
3
)
6
] Cl
3
, urskiljde han primara och sekundara valenser, motsvarande de moderna begreppen oxidationstillstand respektive koordinationstal.
For huvudgruppelement avsag
Richard Abegg
1904 positiva och negativa valenser (maximal och minimal oxidationstillstand), och foreslog Abegg-regeln om att deras skillnad ofta ar 8.
- Den har artikeln ar helt eller delvis baserad pa material fran
engelsksprakiga Wikipedia
,
Valence (chemistry)
,
tidigare version
.