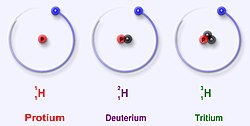
 Forenklade modeller av isotoper av vate, neutronerna ar svarta pa bilden, protonerna roda och elektronerna bla.
Forenklade modeller av isotoper av vate, neutronerna ar svarta pa bilden, protonerna roda och elektronerna bla.
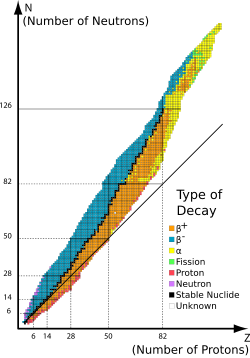 En nuklidkarta.
En nuklidkarta.
En
isotop
av ett
grundamne
ar en variant med ett specifikt antal
neutroner
.
Atomslaget
bestams av antalet
protoner
i karnan,
atomnumret
, och ar avgorande for
elektronkonfigurationen
, och darmed de kemiska egenskaperna hos ett amne. I karnan finns ocksa for de flesta grundamnen neutroner, som paverkar de kemiska egenskaperna i langt mindre grad. Olika isotoper av samma amne har darfor vanligen nastan helt identiska kemiska egenskaper, aven om
masstalet
skiljer.
Skillnaderna i masstal kan dock innebara att vissa fysikaliska egenskaper, som
densitet
, smaltpunkt och
kokpunkt
, ar olika. For
vate
, dar atommassan ar lag fran borjan, paverkar ocksa skillnaden i massa mellan vanligt och
tungt vate
de kemiska egenskaperna nagot. Dessutom varierar atomkarnans stabilitet kraftigt mellan olika isotoper, varfor man vanligen bara kan hitta ett fatal olika isotoper av ett amne i naturen. Andra isotoper kan skapas i laboratorier, men ar da radioaktiva.
For lattare atomslag ar antalet neutroner i karnan ungefar lika med antalet protoner. Tyngre grundamnen har en hogre andel neutroner vilket ses i nuklidkartan.
Ordet isotoper anvands ibland oegentligt i stallet for nuklider.
[
1
]
Begreppet nuklid syftar i forsta hand pa nukleara egenskaper framfor kemiska egenskaper, medan begreppet isotop framst syftar pa kemiska egenskaper framfor nukleara. Nar man fokuserar pa en bestamd typ av atomkarna och dess egenskaper, till exempel i karnreaktioner, valjer man lampligast
nuklid
. Nar det handlar om att gruppera olika slags atomer av ett visst grundamne ar
isotop
det mer adekvata begreppet.
Som exempel visar nuklidkartan att grundamne nummer 50 ?
tenn
- har 7 stabila isotoper (svarta rutor) och ytterligare 31 instabila isotoper (orange och bla rutor). Kartan visar ocksa att det finns 3 stabila nuklider (
88
Sr,
89
Y och
90
Zr) med neutronantalet 50. For de tva sistnamnda finns det dock aven de radioaktiva
karnisomererna
89m
Y och
90m
Zr vilka inte markeras i kartan.
Stabila isotoper ar isotoper som inte genomgar
radioaktivt sonderfall
. Det finns 254 kanda stabila
nuklider
, fordelade pa 80 olika
grundamnen
. De flesta isotoper ar radioaktiva, men eftersom de flesta radioaktiva isotoper har halveringstider som ar betydligt kortare an jordens alder och sonderfallskedjor alltid avslutas med nagon stabil isotop, bestar huvuddelen av materien pa jorden av stabila isotoper. Ett
grundamne
kan sakna stabila isotoper, eller ha en enda stabil isotop (vara
monoisotopt
) eller flera. Den tyngsta kanda stabila isotopen ar
bly
-208.
For de flesta grundamnen med flera isotoper ar en stabil isotop dominerande i naturen. Detta gor att de flesta grundamnen har en
atommassa
som ligger nara ett heltal. Ett undantag ar
klor
med en atommassa pa 35,5 u, eftersom naturligt klor bestar av ¾
35
Cl och ¼
37
Cl.
Kunskapen om huruvida en isotop ar stabil eller inte, grundar sig pa matningar av dess sonderfall. Det innebar att vissa av de isotoper som idag raknas som stabila, kan tankas ha ett mycket langsamt sonderfall, som annu inte kunnat observeras.
Manga isotoper finns men ar instabila, det vill saga att de genomgar
radioaktivt sonderfall
. En isotops
halveringstid
beskriver den tid det tar for halften av atomerna att sonderfalla.
Det ar givet att stabila isotoper och isotoper med lang halveringstid forekommer i naturen i hogre grad an andra. For vissa (tyngre) atomslag saknas helt stabila isotoper.
For naturligt forekommande isotoper sker sonderfallet med antingen
alfasonderfall
eller
betasonderfall
; i alfasonderfallet minskar atomtalet med 2 och masstalet med 4; i betasonderfallet okar atomtalet med 1 och masstalet ar oforandrat, eftersom en neutron blir en proton och sedan skjuts en elektron (betapartikel) ivag. I manga fall uppstar pa sa satt en ny instabil isotop som sonderfaller vidare. Pa sa vis bildas en
sonderfallskedja
. Vissa kortlivade isotoper som skapas i
fission
kan aven sonderfalla genom att skicka ut en neutron.
Instabila isotoper pa jorden kan delas in i fyra grupper beroende pa dess kalla.
- Sadana som finns kvar sedan jorden skapades. Dessa har en halveringstid pa over 100 miljoner ar.
- Sonderfallsprodukter fran langlivade isotoper.
- Isotoper som kontinuerligt nybildas av kosmisk stralning.
- Isotoper som skapats vid manskliga aktiviteter.
Radioaktiva amnen kallas amnen som innehaller instabila isotoper. Vid sonderfallet avges stralning som kan vara skadlig for levande organismer och naturligtvis aven forandra doda material. Det radioaktiva sonderfallet, exempelvis
uran
till
bly
, kan aven anvandas for att datera olika bergarter.
Den upphojda siffran i exemplen anger
masstalet
.
Vate
har atomnummer 1, och forekommer som
- 1
H (
protium
), 99,985 %, stabil
- 2
H (
deuterium
), 0,015 %, stabil
- 3
H (
tritium
), halveringstid 12,2 ar. Nybildas av kosmisk stralning.
Deuterium kallas ocksa tungt vate, och
vattenmolekyler
som innehaller deuterium kallas
tungt vatten
. Tungt vatten har nagot annorlunda kemiska egenskaper an vanligt vatten och har cirka 10 % storre massa per volymenhet. Deuteriums karnsammansattning ar viktig vid anvandning som moderator i vissa karnreaktioner.
Kol
har atomnummer 6 och forekommer naturligt som
- 12
C, 98,9 %, stabil
- 13
C, 1,1 %, stabil
- 14
C, spar, halveringstid 5730 ar. Nybildas av kosmisk stralning.
Det sistnamnda ar kant i den vanliga metoden for
radiometrisk datering
i bland annat
arkeologi
,
kol-14-metoden
.
Uran
har atomnummer 92 och forekommer naturligt som
- 234
U, 0,006 %, halveringstid 0,25 miljon ar. Sonderfallsprodukt i
238
U:s sonderfallskedja.
- 235
U, 0,72 %, halveringstid 0,7 miljard ar.
- 238
U, 99,275 %, halveringstid 4,5 miljard ar.
235
U ar den
klyvbara
isotop som anvands i
karnkraftverk
. Uran behover darfor
isotopanrikas
, en sorteringsprocess dar man sallar bort
238
U och behaller
235
U. Avfallet efter anrikning kallas
utarmat uran
. Urans langa halveringstid utnyttjas vid
radiometriska dateringar
av aldre
bergarter
.
- ^
Hagg, G. 1963, Allman och oorganisk kemi, Almqvist & Wiksell Uppsala, avsnitt 1-3c sid 23