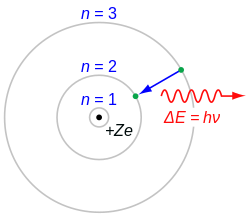
 Rutherford?Bohr-modellen
av
vateatomen
. I denna modell ar det en vasentlig egenskap att fotonens energi (eller frekvens) hos den emitterade elektromagnetiska stralningen nar en elektron hoppar fran en orbital till en annan, ar proportionell mot kvadraten pa atomens laddning, Z.
Rutherford?Bohr-modellen
av
vateatomen
. I denna modell ar det en vasentlig egenskap att fotonens energi (eller frekvens) hos den emitterade elektromagnetiska stralningen nar en elektron hoppar fran en orbital till en annan, ar proportionell mot kvadraten pa atomens laddning, Z.
Atomnummer
ar, inom
kemi
och
fysik
, antalet
protoner
i
karnan
av en
atom
av ett
grundamne
och ar darmed identiskt med karnans
elektriska laddning
. Atomnumret betecknas vanligen med
Z
och identifierar ett grundamne. I en
oladdad
atom ar atomnumret ocksa lika med antalet
elektroner
.
Atomnumret,
Z
, skall inte forvaxlas med
masstalet
A
, som ar antalet
nukleoner
, det totala antalet protoner och
neutroner
i en atoms karna. Antalet neutroner,
N
, kallas atomens
neutrontal
; alltsa,
A
=
Z
+
N
(dessa kvantiteter ar alltid
heltal
). Eftersom protoner och neutroner har ungefar samma massa (och elektronernas massa ar forsumbar for manga andamal) och da
bindningsenergin
for en nukleon alltid ar liten jamfort med nukleonens massa, ar
atommassan
, uttryckt i atommassenheter, ungefar (till inom en procent) lika med heltalet
A
.
Atomer med samma atomnummer
Z
, men olika neutrontal
N
och darmed olika masstal, kallas
isotoper
. Lite mer an tre fjardedelar av naturligt forekommande element existerar som en blandning av isotoper och den genomsnittliga isotopmassan av en isotopblandning for ett element (kallas den relativa atommassan) i en definierad miljo pa jorden bestammer elementets standard
atomvikt
. Historiskt sett var det dessa atomvikter av element (i jamforelse med vate) som var mojliga att mata for 1800-talets kemister.