| Atom helijuma
|
 Osnovno stanje atoma helijuma. Osnovno stanje atoma helijuma.
|
| Ilustracija atoma
helijuma
. Prikazan je
nukleus
(ljubi?asto) i distribucija
elektronskog oblaka
(crno). Nukleus (gore desno) u helijumu-4 je u realnosti sferno simetri?an i blisko je sli?an elektronskom oblaku, mada kod komplikovanijih nukleusa to nije slu?aj. Crna linja predstavlja jedan
angstrom
(
?ablon:FormattingError
ili 100 pm).
|
| Klasifikacija
|
|
|
| Svojstva
|
|
|
Atom
je najmanja gradivna ?estica obi?ne
materije
koja zadr?ava osobine nekog
hemijskog elementa
. Svako ?vrsto tijelo, te?nost, plin i plazma sastavljeni su iz neutralnih ili
ioniziranih
atoma. Atomi su veli?inom ekstremno mali, obi?no se njihova veli?ina kre?e oko 100 pikometara (deset-milijarditi dio metra).
Atomi su dovoljno mali tako da poku?aji da se pretpostavi njihovo pona?anje kori?tenjem postulata klasi?ne
fizike
, naprimjer prikazuju?i ih u obliku
bilijarskih
kugli i sli?no, daju izrazito neta?na predviđanja i rezultate, a uzrok toga su
kvantni efekti
. Tokom razvoja teoretske atomske fizike, u modele atoma uklju?eni su kvantni principi za bolje obja?njavanje i predviđanje pona?anja atoma.
Svaki atom sastavljen je iz atomskog jezgra i jednog ili vi?e
elektrona
vezanih za to jezgro. Atomsko jezgro sastavljeno je iz jednog ili vi?e
protona
i ?esto istog ili pribli?no istog broja
neutrona
. Protoni i neutroni nazivaju se i
nukleoni
. Vi?e od 99,94% mase atoma otpada na njegovo jezgro. Protoni imaju pozitivan elektri?ni naboj, elektroni negativan naboj, dok neutroni nemaju elektri?nog naboja. Ako u atomu postoji jednak broj protona i elektrona, takav atom je elektri?no neutralan. Ako atom ima vi?e ili manje elektrona od protona, tada je on op?enitno negativno ili pozitivno naelektrisan, te se naziva
ion
.
Elektromagnetna sila
privla?i elektrone protonima u atomskoj jezgri. Unutar jezgre, protoni i neutroni se međusobno privla?e
nuklearnim silama
, koja je obi?no mnogo sna?nija od elektromagnetnih sila koji odbija pozitivno naelektrisane protone jedne od drugih. Pod određenim okolnostima, odbijaju?a elektromagnetna sila postane ja?a od nuklearnih sila, te se nukleoni izbacuju iz jezgra, a atom tog elementa pretvara se u atom drugog elementa, ?to predstavlja nuklearni raspad, ?iji je krajnji rezultat nuklearna transmutacija.
Broj protona u jezgru definira kojem hemijskom elementu taj atom pripada; naprimjer, svi atomi
bakra
imaju 29 protona. Broj neutrona u jezgru definira
izotop
tog elementa. Broj elektrona utje?e na elektromagnetske osobine atoma. Atom se mo?e spojiti sa jednim ili vi?e drugih atoma putem
hemijskih veza
grade?i
hemijske spojeve
u vidu
molekula
. Sposobnost atoma da se međusobno spajaju i razdvajaju odgovorna je za ve?inu fizi?kih promjena koje se mogu zapaziti u prirodi i predmet je izu?avanja
hemijskih nauka
.
Glavni ?lanak:
Atomska teorija
Ideja da je sva materija sastavljena iz sitnih ?estica je vrlo stara ideja, koja se pojavljuje u mnogim drevnim kulturama poput gr?ke i indijske. Rije? "atom" (
gr?ki
:
?τομο?
, atomos
), ?to zna?i "nedjeljiv", "koji se ne mo?e rezati", prvi je spomenuo
anti?ki gr?ki filozof
Leukip
i njegov u?enik
Demokrit
.
[1]
[2]
[3]
[4]
Demokrit je smatrao da je broj atoma beskona?an, da ne mogu nastati niti nestati, da su vje?ni te da su osobine nekog predmeta rezultat toga od koje vrste atoma je sastavljen.
[2]
[3]
[4]
Demokritov
atomizam
razradio je i usavr?io kasniji filozof
Epikur
.
[3]
[4]
Tokom ranog
Srednjeg vijeka
, na atomizam se gotovo zaboravilo u zapadnoevropskoj filozofiji, ali je "pre?ivio" u radovima nekih
islamskih filozofa
.
[3]
Tokom 12. vijeka, u zapadnoj Evropi ponovno se javljaju ideje atomizma, koga su tada?nji evropski filozofi spoznali kroz iznova "otkrivene"
Aristotelove
radove.
[3]
U 14. vijeku, ponovna "otkri?a" velikih dijela anti?kih atomista, uklju?uju?i djela
Lukrecija
De rerum natura
i
Diogena Laertija
?ivoti i mi?ljenja eminentnih filozofa
, dovela su do pove?anja interesovanja za ovu temu.
[3]
Ipak, po?to je atomizam bio vezan sa filozofijom
Epikura
, ?to je bilo u suprotnosti sa ortodoksnim kr??anskim u?enjem, vjerovanje u postojanje atoma nije bilo prihvatljivo.
[3]
Francuski katoli?ki sve?tenik Pierre Gassendi (1592?1655) o?ivio je Epikurov atomizam uz određena prilagođavanja, tako da je tvrdio da je atome kreirao
Bog
, pa iako ih ima u nezamislivo ogromnom broju, taj broj nije beskona?an.
[3]
[4]
Gassendijeva izmijenjena atomska teorija bila je ?iroko prihva?ena u Francuskoj, a zagovarao ju je i fizi?ar
Francois Bernier
(1620?1688), kao i u Engleskoj gdje se njome bavio filozof
Walter Charleton
(1619?1707).
[3]
Hemi?ar
Robert Boyle
i fizi?ar
Isaac Newton
(1642?1727) branili su postulate atomizma te je on krajem 17. vijeka postao prihva?ena teorija u nau?nim krugovima.
[3]
Po?etkom 19. vijeka,
John Dalton
je koristio koncept atoma u obja?njavanju teorija za?to
elementi
uvijek
reagiraju
u odnosima malih cijelih brojeva (zakon vi?estrukih proporcija). Naprimjer, postoje dvije vrste oksida
kalaja
: jedan sa 88,1% kalaja i 11,9% kisika a drugi sa 78,7% kalaja i 21,3% kisika (
kalaj(II)-oksid
i
kalaj-dioksid
). To zna?i da se 100 grama kalaja mo?e spojiti sa 13,5 g ili 27 g kisika. Odnos 13,5 i 27 stoji u proporciji 1:2, tj. proporciji malih cijelih brojeva. Ova op?enita ?ema u hemiji dala je ideju Daltonu da elementi reagiraju vi?estrukim kona?nim jednicama, drugim rije?ima, atomima. U navedenom primjeru oksida kalaja, jedan atom kalaja spaja se bilo sa jednim ili sa dva atoma
kisika
.
[5]
Dalton je također vjerovao da atomska teorija mo?e objasniti za?to
voda
apsorbira
razli?ite plinove u razli?itim proporcijama. Naprimjer, on je otkrio da voda apsorbira
ugljik-dioksid
mnogo bolje nego ?to apsorbira
du?ik
.
[6]
Dalton je pretpostavio da je razlog tome razlika između masa i konfiguracija ?estica plina, jer su molekule ugljik-dioksida (CO
2
) te?e i ve?e od molekula du?ika (N
2
).
Godine 1827, botani?ar
Robert Brown
je pomo?u
mikroskopa
posmatrao ?estice pra?ine koje su plutale u vodi i otkrio da su one kretale haoti?no i bez reda, a taj fenomen je kasnije nazvan "
Brownovo kretanje
". U to vrijeme smatralo se da molekule vode udaraju u ?estice pra?ine i tako ih pomjeraju. Godine 1905.
Albert Einstein
je dokazao stvarnost ovih molekula i njihovog kretanja prave?i prvu statisti?ku fizikalnu analizu Brownovog kretanja.
[7]
[8]
[9]
Na osnovu Einsteinovog rada, francuski fizi?ar
Jean Perrin
je eksperimentalno odredio masu i dimenzije atoma, te time nedvosmisleno dokazao Daltonovu atomsku teoriju.
[10]
Fizi?ar
J.J. Thomson
je mjerio masu katodnih zraka, te dokazao da su one sastavljene iz ?estica, ali su one bile oko 1800 puta lak?e od najlak?eg poznatog atoma,
vodika
. Iz toga je zaklju?eno da to nisu bili atomi nego nove ?estice, odnosno prve otkrivene subatomske ?estice koje su najprije nazvane
korpuskule
, da bi kasnije dobile ime
elektroni
, prema nazivu kojeg je predlo?io George Johnstone Stoney u svojim radovima iz 1874. godine. Thomson je također dokazao da su to identi?ne ?estice onima koje emitiraju
fotoelektri?ni
i
radioaktivni
materijali.
[11]
Vrlo brzo do?lo se do shvatanja da su to ?estice koje "prenose"
elektri?nu struju
u metalnim provodnicima, te unutar atoma nose negativni elektri?ni naboj. Thomsonu je 1906. godine za svoj rad dodijeljena
Nobelova nagrada za fiziku
. Time je on oborio vjerovanje su atomi nedjeljive, gradivne ?estice materije.
[12]
Međutim, Thomson je postavio pogre?nu teoriju da su negativno naelektrisani elektroni, vrlo male mase, ravnomjerno raspoređeni po atomu kao jednoli?ni sloj negativnog naelektrisanja. Ovaj model atoma postao je poznat pod nazivom "
model pudinga od ?ljiva
".
Godine 1909.
Hans Geiger
i
Ernest Marsden
, prema savjetima
Ernesta Rutherforda
, izvr?ili su eksperiment bombardiranja metalne folije
alfa ?esticama
i mjerili kako se one pona?aju pri sudaru s njom. Prema njihovim pretpostavkama, sve alfa ?estice trebale su pro?i ravno kroz foliju uz nimalo ili vrlo malo rasipanje ili odbijanje, jer je Thomsonov model atoma pretpostavljao da su naelektrisanja u atomu toliko ra?trkana da njihova
elektri?na polja
ne mogu mnogo utjecati na alfa ?estice. Međutim, Geiger i Mardsen su uo?ili da su se neke alfa ?estice odbijale od atoma pod uglovima ve?im od 90°, za ?ta Thomsonov model nije mogao pru?iti nikakvo obja?njenje. Da bi takvu pojavu objasnio, Rutherford je postavio teoriju da su pozitivna naelektrisanja u atomu koncentrirana u malom jezgru u sredi?tu atoma.
[13]
Dok je eksperimentirao sa proizvodima
radioaktivnog raspada
1913. godine, hemi?ar
Frederick Soddy
otkrio je da se u
periodnom sistemu
javlja vi?e od jedne vrste atoma na svakom mjestu u PSE.
[14]
Pojam
izotop
skovala je Margaret Todd kao pogodno ime za razli?ite vrste atoma koji pripadaju istom hemijskom elementu. J.J. Thomson izumio je tehniku separacije izotopa tokom svog rada na prou?avanju ioniziranih plinova, ?to je u kona?nici dovelo do otkri?a stabilnih izotopa.
[15]
 Bohrov model atoma, danas prevaziđen
Bohrov model atoma, danas prevaziđen
Godine 1913. fizi?ar
Niels Bohr
predlo?io je model atoma u kojem njegovi elektroni orbitiraju oko jezgra, ali po strogo određenom broju orbita, te da mogu prelaziti između orbita samo uz ta?no određenu promjenu energije koja odgovara apsorpciji ili emitiraju fotona.
[16]
Ova kvantizacija se koristila za obja?njavanje za?to su orbite elektrona stabilne (tj. da nema promjena u ubrzanju njihovog kretanja, uklju?uju?i kru?no kretanje i gubitak kineti?ke energije koja se emitira kao elektromagnetno zra?enje) i za?to hemijski elementi apsorbiraju i emitiraju elektromagnetno zra?enje u ta?no određenom spektru.
[17]
Kasnije iste godine
Henry Moseley
dao je dodatne eksperimentalne dokaze koji su podr?ali Bohrovu teoriju. Ove rezultate pobolj?ali su Rutherfordov i Van den Broekov model atoma, koji su predviđali da atom u svom jezgru sadr?i određen broj pozitivnih nuklearnih naboja koji su jednaki atomskom broju tog elementa u periodnom sistemu. U vremenu prije tih eksperimenata, za
atomski broj
se nije smatralo da je fizi?ka ili eksperimentalna koli?ina. ?injenica da nuklearni naboj atoma odgovara atomskom broj, ostala je va?e?a i kod dana?njih teorija modela atoma.
[18]
Godine 1916.
Gilbert Newton Lewis
postavio je teoriju o
hemijskim vezama
između atoma, prema kojoj su one zapravo interakcije između elektrona u tim atomima.
[19]
Po?to su hemijske osobine elemenata ve?inom bile poznate i da su se one prete?no ponavljale u skladu periodi?nih zakona,
[20]
tako je 1919. ameri?ki hemi?ar
Irving Langmuir
postavio teoriju da bi se taj pojava mogla objasniti ako su elektroni u atomu povezani ili na neki na?in grupisani. Takve grupe elektrona koje "zauzimaju" ta?no određeno podru?je oko jezgra nazvane su elektronske ljuske.
[21]
Stern?Gerlachov eksperiment
iz 1922. dao je daljnje dokaze o kvantnoj prirodi atomskih osobina. Tokom tog eksperimenta, snop atoma
srebra
usmjeren je kroz posebno oblikovano
magnetno polje
, te se on razdvojio na na?in koji odgovara smjeru ugaonog momenta atoma odnosno
spinu
. Kako je smjer spina isprva bio nasumi?an, o?ekivalo se da ?e se snop odbiti u nasumi?nom smjeru. Umjesto toga, snop se razdvojio u dvije usmjerene komponente koje odgovaraju stanju da li je atomski spin usmjeren prema dolje ili gore u odnosu na magnetno polje.
[22]
Godine 1925.
Werner Heisenberg
je objavio prvu konzistentnu
matemati?ku formulaciju kvantne mehanike
(
matri?na kvantna mehanika
).
[18]
Godinu ranije, 1924,
Louis de Broglie
je postavio teoriju da se sve ?estice pona?aju i kre?u u obliku talasa, pa je tako 1926.
Erwin Schrodinger
upotrijebio tu ideju za razvoj matemati?kog modela atoma (
talasna mehanika
) kojim je opisao elektrone u obliku trodimenzionalnog talasa umjesto kao do tada u obliku ta?kaste ?estice.
Kao posljedica postojanja talasnog oblika kojim se opisuju ?estice, matemati?ki je nemogu?e dobiti neke ta?ne vrijednosti ni za geometrijsku poziciju ni za moment ?estice u bilo kojem vremenskom trenutku. Taj princip postao je poznat kao
princip neodređenosti
a formulirao ga je
Werner Heisenberg
1927. godine.
[18]
Prema tom konceptu, uz određenu ta?nost pri mjerenju mjesta nekog elektrona mogu?e je dobiti samo raspon mogu?ih vrijednosti momenta i obrnuto.
[23]
Takav model mogao je objasniti mjerenja i posmatranja atomskih osobina ?to prethodni modeli nisu mogli, poput određenih strukturnih i spektralnih osobina atoma te?ih od vodika. Prema tome, planetarni modeli atoma su prevaziđeni modelom koji je opisao mogu?e zone atomskih orbitala oko jezgra gdje postoji najve?a vjerovatno?a da bi se određeni elektron mogao nalaziti u određenom vremenu.
[24]
[25]
Otkri?e
masene spektrometrije
omogu?ilo je mjerenje mase atoma mnogo preciznije nego ?to je to bilo ranije mogu?e. Uređaj je koristio magnet koji je slu?io za skretanje pravca kretanja snopa iona, te se na osnovu koli?ine odbijanja snopa mo?e odrediti odnos u promjeni
masa
atoma prije i nakon toga. Hemi?ar
Francis William Aston
koristio je ovaj instrument kako bi pokazao da izotopi imaju razli?ite mase.
Atomske mase
tih izotopa varirale su i razlikovale međusobno u cijelim iznosima, ?to je nazvano
pravilo cijelih brojeva
.
[26]
Obja?njenje tih razli?itih izotopa ?ekalo je do otkri?a
neutrona
, nenabijene ?estice mase sli?noj
protonu
, ?to je 1932. uspjelo fizi?aru
Jamesu Chadwicku
. Na taj na?in, otkriveno je da su izotopi hemijski elementi sa istim brojem protona, ali razli?itim brojem neutrona u svom jezgru.
[27]
Godine 1938, njema?ki hemi?ar
Otto Hahn
, student Ernesta Rutherforda, vr?io je eksperiment tako ?to je usmjerio snop neutrona u atome
uranija
, o?ekuju?i da ?e dobiti neki transuranijski element. Umjesto toga, rezultati njegovog eksperimenta pokazali su da je dobio
barij
.
[28]
[29]
Godinu kasnije,
Lise Meitner
i njen sestri?
Otto Robert Frisch
potvrdili su Hahnove rezultate kao prvu eksperimentalno izvedenu
nuklearnu fisiju
.
[30]
[31]
Hahn je 1944. za svoje otkri?e fisije dobio
Nobelovu nagradu za hemiju
. Međutim, i pored Hahnovog zalaganja, doprinosi Meitner i Frischa ovom otkri?u nisu priznati.
[32]
Tokom 1950ih, razvoj naprednih uređaja ubrziva?a (akceleratora) ?estica i uređaja za njihovu detekciju omogu?io je nau?nicima izu?avanje procesa sudaranja atoma koji se kre?u s vrlo visokim kineti?kim energijama.
[33]
Za neutrone i protone utvrđeno je da su to zapravo
hadroni
, odnosno sastavljeni iz jo? manjih ?estica nazvanih
kvarkovi
. Time je razvijen standardni model fizike ?estica koji je do danas uspje?no predstavio osobine jezgra atoma u smislu da tih subatomskih ?estica kao i sila koje određuju njihova međudjelovanja.
[34]
Iako je pojam
atom
prvobitno ozna?avao ?esticu koja se ne mo?e razbiti u manje ?estice, u modernom nau?nom ?argonu, smatra se da je atom sastavljen iz vi?e subatomskih ?estica. Gradivne ?estice atoma su
elektroni
,
protoni
i
neutroni
. Sve tri vrste ?estice spadaju u
fermione
. Međutim, atom vodika (izotop H-1) nema neutrona, dok
hidron
-ion (
1
H
+
) nema elektrona.
Elektroni su ubjedljivo najlak?e među ovim ?esticama, mase
?ablon:FormattingError
, sa negativnim elektri?nim nabojem i veli?ine tako male da ga je nemogu?e izmjeriti pomo?u danas dostupnih tehnika.
[35]
On je bio najlak?a ?estica sa pozitivnom masom u mirovanju, sve do otkri?a
neutrina
i određivanja njegove mase. U uobi?ajenim okolnostima, elektroni su vezani sa pozitivno naelektrisanim jezgrom putem sile privla?enja suprotno naelektrisanog naboja. Ukoliko atom ima jedan vi?e ili manje elektrona od svog atomskog broja, tada postaje negativno ili pozitivno naelektrisan, respektivno, a nabijeni (naelektrisani) atom naziva se
ion
. Elektroni su otkriveni krajem 19. vijeka, uglavnom zahvaljuju?i radovima
J.J. Thomsona
.
Protoni imaju pozitivni naboj i masu 1.836 puta ve?u od elektron, oko
?ablon:FormattingError
. Broj protona u atomu naziva se
atomski broj
.
Ernest Rutherford
(1919) prou?avao je
du?ik
i bombardirao ga alfa-?esticama, pri ?emu je zapazio da du?ik pri tom emitira ne?to ?to izgleda kao jezgro vodika. Naredne godine, preformulirao je otkri?e tako da je zaklju?io da je jezgro vodika posebna ?estica unutar atoma koju je nazvao
proton
.
Neutroni nemaju elektri?ni naboj te imaju slobodnu masu 1.839 puta ve?u od mase elektrona ili oko
?ablon:FormattingError
.
[36]
[37]
Neutroni su najte?i od tri osnovne gradivne ?estice atoma, ali se njihova masa mo?e reducirati nuklearnom energijom vezanja. Neutroni i protoni (zajedni?ki nazvani nukleoni) imaju pribli?no iste dimenzije, veli?ine reda
?ablon:FormattingError
, mada "povr?ina" ovih ?estica nije jasno definirana.
[38]
Neutrone je 1932. otkrio engleski fizi?ar
James Chadwick
.
U
standardnom modelu
fizike, elektroni su prave elementarne ?estice bez unutra?nje strukture. Međutim, i protoni i neutroni su slo?ene ?estice sastavljene iz elementarnih ?estica nazvanih
kvarkovi
. Postoji dvije vrste kvarkova u atomu, svaki sa djelimi?nim elektri?nim nabojem. Protoni su sastavljeni iz dva
gornja kvarka
(
up
-kvark) (svaki sa nabojem +
2
3
) i jednog
donjeg kvarka
(sa nabojem -
1
3
). Neutroni su sastavljeni iz jednog gornjeg i dva donja kvarka. Ova razlika "odgovorna" je i za razliku u masama i nabojima između ove dvije ?estice.
[39]
[40]
Kvarkovi se dr?e na okupu djelovanjem jake interakcije (tj. jake sile), koju reguliraju
gluoni
. Protone i neutrone u jezgru međusobno ve?e djelovanje nuklearnih sila, koja je "ostatak" jakih sila koje donekle imaju razli?ite osobine u pogledu udaljenosti na kojoj djeluju. Gluoni su ?lanovi porodice
ba?darnih bozona
, koje su elementarne ?estice preko kojih se ispoljavaju fizi?ke sile.
[39]
[40]
Glavni ?lanak:
Atomsko jezgro
 Energija vezivanja potrebna da bi nukleon "pobjegao" iz jezgra, podaci se odnose na razne izotope
Energija vezivanja potrebna da bi nukleon "pobjegao" iz jezgra, podaci se odnose na razne izotope
Svi vezani protoni i neutroni u atomu sa?injavaju relativno malo
atomsko jezgro
, te se kolektivno nazivaju
nukleoni
. Pre?nik atomskog jezgra pribli?no je jednak 1,07
3
√
A
femtometara, gdje je
A
ukupni broj nukleona u njemu.
[41]
To je znatno manje od pre?nika cijelog atoma, koji je reda veli?ine 10
5
fm. Nukleoni se dr?e zajedno vezani privla?nim potencijalom koji djeluje na kratkoj udaljenosti, a naziva se
rezidualna jaka nuklearna sila
. Na udaljenostima kra?im od 2,5 fm ova sila je znatno sna?nije od elektrostati?ke sile koja uzrokuje da se pozitivno nabijeni protoni odbijaju jedan od drugog.
[42]
Atomi istog
elementa
imaju isti broj protona u jezgru, a taj broj odgovara
atomskom broju
elementa. Za svaki hemijski element, postoje atomi kod kojih broj neutrona varira, a taj broj određuje
izotop
tog elementa. Ukupan broj protona i neutrona određuje o kojem
nuklidu
se radi. Broj neutrona u odnosu na broj protona određuje koliko je to jezgro stabilno, jer se određeni izotopi raspadaju nekim od
radioaktivnih
na?ina raspada.
[43]
Proton, elektron i neutron svrstani su u grupu
fermionskih
?estica. Za fermione va?ni
Paulijev princip isklju?enja
, koji zabranjuje
identi?nim
fermionima, kao ?to je vi?e od jednog protona, da zauzimaju isto kvantno stanje u isto vrijeme. Stoga, svaki proton u jezgru mora zauzimati kvantno stanje razli?ito od svih drugih protona, a isti princip se primjenjuje i na sve neutrone u jezgru i sve elektrone u elektronskom oblaku.
[44]
Atomska jezgra koja imaju razli?it broj protona i neutrona imaju potencijal da pređu u ni?e energetsko stanje putem radioaktivnog raspada ?ije posljedice se ogledaju u tome da se broj neutrona pribli?i broju protona. Rezultat tog procesa je da nastaju atomi koji imaju podjednak broj protona i neutrona i koji su mnogo "otporniji" na raspad. Ipak, pove?anjem atomskog broja, međusobno odbijanje protona zahtijeva pove?anje odnosa broja neutrona u odnosu na broj protona kako bi se odr?avala stabilnost jezgra, ?to neznatno mijenja ovaj trend jednakog broja protona i neutrona kod atoma sa ni?im atomskim brojevima.
[44]
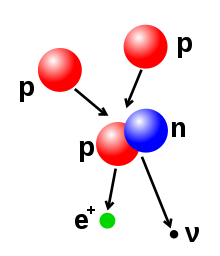 Ilustracija procesa nuklearne fuzije kojom od dva protona nastaje jezgro
deuterija
, a koje se sastoji iz protona i neutrona.
Pozitron
(e
+
), antimaterijski elektron, emitira se zajedno sa elektron-
neutrinoom
.
Ilustracija procesa nuklearne fuzije kojom od dva protona nastaje jezgro
deuterija
, a koje se sastoji iz protona i neutrona.
Pozitron
(e
+
), antimaterijski elektron, emitira se zajedno sa elektron-
neutrinoom
.
 Jama potencijala, prema klasi?noj mehanici, pokazuje minimum energije
V
(
x
) potrebne da se dosegne svaka pozicija
x
. Prema klasi?nom tuma?enju, ?estica energije
E
ograni?ena je na raspon pozicija između
x
1
i
x
2
.
Jama potencijala, prema klasi?noj mehanici, pokazuje minimum energije
V
(
x
) potrebne da se dosegne svaka pozicija
x
. Prema klasi?nom tuma?enju, ?estica energije
E
ograni?ena je na raspon pozicija između
x
1
i
x
2
.
Broj protona i neutrona u atomskom jezgru mo?e se promijeniti, ali je za to potrebna veoma velika energija zbog vrlo sna?nih sila koje djeluju unutar jezgra.
Nuklearna fuzija
se de?ava kada se ve?i broj lak?ih atomskih ?estica međusobno spoje i izgrade te?e atomsko jezgro, poput energetskih sudara dva atomska jezgra. Naprimjer, u sredi?tu
Sunca
protonima je potrebno pribli?no 3?10 keV energije da bi svladali sile njihovog međusobnog odbijanja, te spojili se u jednu atomsko jezgru. Ta energetska granica nazvana je
Coulombova barijera
.
[45]
Nuklearna fisija
je proces suprotan fuziji, pri kojoj se atomsko jezgro raspada na dva manja jezgra, obi?no pra?eno radioaktivnim raspadom. Jegra se mogu izmijeniti i bombardiranjem subatomskim ?esticama ili
fotonima
visoke energije. Ako se u tom procesu promijeni broj protona u jezgru, atom prelazi u drugi hemijski element.
[46]
[47]
Ako je masa jezgra nastalog nakon reakcije fuzije manja od masa polaznih ?estica koje su u?estvovale u reakciji, tada se razlika između ove dvije vrijednosti mo?e emitirati u vidu neke korisne energije (poput gama zraka) ili
kineti?ke energije
u vidu beta ?estica, kako je opisano poznatom
Einsteinovom
formulom ekvivalencije mase i energije,
 , gdje je
, gdje je
 razlika u gubitku mase a
razlika u gubitku mase a
 brzina svjetlosti
. Ovaj deficit mase je dio energije vezivanja novonastalog jezgra, i to je nepovratni gubitak energije koji uzrokuje da spojene ?estice ostanu zajedno u stanju koje zahtijeva ovu energije da bi se razdvojile.
[48]
brzina svjetlosti
. Ovaj deficit mase je dio energije vezivanja novonastalog jezgra, i to je nepovratni gubitak energije koji uzrokuje da spojene ?estice ostanu zajedno u stanju koje zahtijeva ovu energije da bi se razdvojile.
[48]
Fuzija dva jezgra kojom nastaje ve?e i te?e jegro sa atomskim masama manjim od
Fe
i
Ni
, gdje je ukupni broj nukleona oko 60, obi?no je
egzotermi?ka reakcija
, kojom se otpu?ta vi?e enegije nego ?to je potrebno da bi se ona spojila.
[49]
Ovaj proces kojim se otpu?ta energija omogu?ava da se nuklearna fuzija u
zvijezdama
neprekidno odvija. Kod te?ih jezgara, energija vezivanja po jednom nukleonu u jezgru po?inje opadati. To zna?i da su procesi fuzije, kojima nastaju atomi atomskih brojeva vi?ih od 26 i atomskim masama vi?im od 60, endotermi?ke rekacije. Zbog toga masivnije jezge ne mogu odr?avati reakcije fuzije kojima nastaje "vi?ak" energije niti mogu odr?avati hidrostati?ku ravnote?u zvijezde.
[44]
Elektrone u atomu privla?e protoni iz njegovog jezgra
elektromagnetnim silama
. Ove sile ve?u elektrone unutar elektrostati?ke
jame potencijala
okru?uju?i malo atomsko jezgro, ?to zna?i da je elektronu za "bijeg" iz atoma potreban vanjski izvor energije. ?to god je elektron bli?i jezgru, ve?a je njegova privla?na sila. Prema tome, elektroni vezani bli?e centru jame potencijala zahtijevaju vi?e energije kako bi bili izbijeni iz atoma, od onih elektrona koji se nalaze dalje od jezgra.
Kao i druge ?estice, elektroni imaju i ?esti?ne i talasne osobine. Elektronski oblak je podru?je unutar jame potencijala gdje svaki elektron gradi neku vrstu trodimenzionalnog stacionarnog talasa, tj. oblika talasa koji se ne kre?e u odnosu na jezgro. Ovo pona?anje definira atomsku orbitalu u obliku
matemati?ke
funkcije koju karakterizira
vjerovatno?a
da ?e se elektron nalaziti na određenom polo?aju u trenutku kada se njegov polo?aj mjeri.
[50]
Postoji samo diskretno kvantizirani set takvih orbitala oko atomskog jezgra, jer se druge mogu?e talasne pozicije vrlo brzo raspadnu na neku od stabilnijih formi.
[51]
Orbitale mogu imati jednu ili vi?e prstenastih ili ta?kastih struktura te se jedna od druge razlikuju u veli?ini, obliku i usmjerenju (orjentaciji).
[52]
Svaka atomska orbitala odgovara određenom nivou energije elektrona. Elektroni mogu promijeniti svoje stanje na vi?i energetski nivo putem apsorpcije
fotona
koji nosi dovoljnu koli?inu energije kojom je mogu?e pobuditi elektron do novog vi?eg kvantnog stanja. Na sli?an na?in, putem spontane emisije, elektron na vi?em energetskom nivou mo?e pre?i na ni?i energetski nivo istovremeno emitiraju?i vi?ak energije u vidu fotona. Takve karakteristi?ne vrijednosti energije, definirane kao razlike između energija određenih kvantnih stanja, odgovorne su za pojavu
atomskih spektralnih linija
.
[51]
Iznos energije potrebne da se doda ili ukloni elektron, tj. energije vezivanja elektrona, daleko je manji od energije vezivanja nukleona. Naprimjer, potrebno je "samo" 13,6 eV da se ukloni elektron u osnovnom stanju iz atoma
vodika
,
[53]
u odnosu na 2,23
miliona
eV potrebnih da bi se razbilo jezgro
deuterija
.
[54]
Atomi su u elektri?no neutralnom stanju ako imaju isti broj protona i neutrona. Atomi koji imaju vi?ak ili manjak elektrona nazivaju se
ioni
. Elektroni koji se nalaze najdalje od jezgra mogu pre?i na druge susjedne atome ili ih dva atoma mogu dijeliti kao zajedni?ke. Tim mehanizmom, atomi mogu graditi
hemijske veze
te se međusobno vezati u
molekule
i druge vrste
hemijskih spojeva
poput ionskog i
kovalentnog
sistema
kristala
.
[55]
Po definiciji, bilo koja dva atoma sa identi?nim brojem
protona
u njihovim jezgrima, pripadaju istom
hemijskom elementu
. Atomi sa istim brojem protona, ali razli?itim brojem
neutrona
predstavljaju razli?ite
izotope
istog elementa. Naprimjer, svi atomi vodika imaju po jedan proton u jezgru, ali postoji razni izotopi među kojim je izotop bez
neutrona
u jezgru (vodik-1, kojeg ima ubjedljivo najvi?e,
[56]
zvani protij), sa jednim (
deuterij
), dva (
tricij
) ili vi?e neutrona. Svi poznati elementi ?ine set atomskih brojeva, po?ev od elementa sa jednim (
vodik
) do elementa sa 118 protona (
oganeson
).
[57]
Svi poznati izotopi elemenata koji imaju atomske brojeve ve?e od 82 su
radioaktivni
, mada je radioaktivnost elementa 83 (
bizmut
) tako slaba da se prakti?no mo?e smatrati da je nema.
[58]
[59]
Na
Zemlji
je otkriveno pribli?no 339 nuklida,
[60]
a kod 254 od njih (oko 75%) nije opa?en raspad, te se oni definiraju kao "stabilni izotopi". Ipak, samo 90 tih nuklida su stabilni u odnosu na sve vrste radioaktivnog raspada, ?ak i u teoriji. Za ostalih 164 (?to ?ini ukupno 254 nuklida) nisu opa?eni raspadi, mada je prema njihovoj strukturi u teoriji mogu? njihov raspad. Ovi nuklidi se formalno smatraju "stabilnim". Dodatna 34 radioaktivna nuklida imaju vremena poluraspada du?a od 80 miliona godina, te su dovoljno dugo?ivu?i da bi se na Zemlji mogli nalaziti jo? iz perioda nastanka Sun?evog sistema. Ova "kolekcija" od 288 nuklida poznati su i kao
primordijalni nuklidi
. Najzad, poznat je jo? i 51 kratko?ivu?i nuklid za koje se zna da se prirodno javljaju na Zemlji, kao proizvodi raspada primordijalnih nuklida (poput
radija
iz
uranija
) ili neki drugi na?in u vidu proizvoda prirodnih energetskih procesa na Zemlji, naprimjer bombardiranjem kosmi?kih zraka (poput nastanka ugljika-14).
[61]
[note 1]
Od svih hemijskih elemenata, njih 80 ima barem jedan stabilni izotop. Mnogi hemijski elementi imaju nekoliko stabilnih izotopa, prosje?no postoji 3,2 stabilna izotopa po svakom hemijskom elementu. Dvadeset ?est elemenata ima samo jedan stabilni izotop, dok najve?i broj stabilnih izotopa od svih elemenata ima
kalaj
sa deset stabilnih izotopa. Elementi
43
,
61
, i svi elementi sa atomskim brojevima
83
i ve?im nemaju niti jedan stabilan izotop.
[62]
Na stabilnost izotopa primarno uti?e odnos broja protona i neutrona, ali također i prisustvo određenih "magi?nih brojeva" neutrona i protona koji predstavljaju zatvorene i u potpunosti popunjene kvantne ljuske. Te kvantne ljuske odgovaraju i ta?no definisanim setovima nivoa energije unutar modela ljusaka jezgra; popunjene ljuske, kao ?to je naprimjer popunjena ljuska sa 50 protona kod kalaja, daje neuobi?ajenu stabilnost tom nuklidu. Od 254 poznata stabilna nuklida, samo njih ?etiri imaju i neparan broj protona
i
neparan broj neutrona: izotop vodika-2 (
deuterij
),
litij
-6, bor-10 i
du?ik
-14. Osim toga, samo ?etiri nuklida koji se javljaju u prirodi, a koji su radioaktivni, imaju neparne brojeve protona i neutrona u jezgru:
kalij
-40,
vanadij
-50,
lantan
-138 i
tantal
-180m. Ovi nuklidi imaju vrijeme poluraspada du?e od milijardu godina. Ve?ina jezgara sa neparnim brojem i protona i neutrona su veoma nestabilna u odnosu na beta raspad, jer proizvodi raspada imaju parne brojeve i protona i neutrona, pa su stoga mnogo sna?nije vezani zbog nuklearnih efekata sparivanja.
[62]
Velika ve?ina mase atoma sadr?ana je u protonima i neutronima u njegovom jezgru. Ukupan broj ovih ?estica (nazvanih "nukleoni") u nekom atomu naziva se
maseni broj
. To je pozitivan, cijeli broj, bez jedinice mjere (iako ima masenu dimenziju) jer ozna?ava broj ?estica. Primjer kori?tenja masenog broja je
ugljik
-12, ?to zna?i da u jezgru ovog izotopa ima 12 nukleona (?est protona i ?est neutrona).
Stvarna masa atoma u mirovanju ?esto se izra?ava pomo?u unificirane
jedinice atomske mase
(
u
), također zvane i
dalton
(Da). Ova jedinica definirana je kao dvanaestina mase slobodnog neutralnog atoma izotopa ugljika-12, a pribli?no izra?eno u
kilogramima
ona iznosi
?ablon:FormattingError
.
[63]
Vodik-1 (
protij
) (najlak?i izotop vodika, a također i nuklid sa najni?om masom) ima atomsku te?inu 1,007825
u
.
[64]
Vrijednost ovog broja naziva se
atomska masa
. Određeni atom ima atomsku masu koja je pribli?no jednaka (uz razliku do 1%) njegovom masenom broju pomno?enom sa jedinicom atomske mase (naprimjer masa atoma du?ika-14 je pribli?no 14
u
). Međutim, ovaj broj ne?e uvijek biti cijeli broj osim kod ugljika-12.
[65]
Najte?i stabilni atom,
olovo
-208,
[58]
ima masu
?ablon:FormattingError
.
[66]
Po?to su i najte?i atomi isuvi?e lahki da bi se s njima moglo direktno raditi i mjeriti, hemi?ari dogovorno upotrebljavaju jedinicu
mol
. Jedan atoma (ili bilo kojih drugih ?estica) bilo kojeg elementa uvijek ima isti broj atoma (?estica), oko
?ablon:FormattingError
. Taj broj naziva se
Avogadrova konstanta
. On je odabran tako da ako element ima atomsku masu 1
u
, jedan mol tog elementa imat ?e masu pribli?no jedan gram. Zbog definicije unificirane jedinice atomske mase, svaki atom ugljika-12 ima atomsku masu ta?no 12
u
, pa jedan mol atoma ugljika-12 ima masu ta?no 0,012 kg.
[63]
Glavni ?lanak:
Atomski radijus
Atomima nedostaje strogo definirana vanjska granica, pa se njihove dimenzije obi?no opisivaju pojmom
atomskog radijusa
. On mjeri razdaljinu koliko se elektronski oblak udaljava od jezgra.
[67]
Međutim, time se eksplicitno pretpostavlja da atom ima
loptast
oblik, ?to je mogu?e ako se atomi posmatraju u
vakuumu
ili slobodnom prostoru. Atomski radijusi se mogu izra?unati iz udaljenosti između dva jezgra u slu?aju kada se dva atoma spoje pomo?u neke od
hemijskih veza
. Radijusi su dosta varijabilni u zavisnosti od polo?aja atoma u periodnom sistemu, vrste hemijske veze koju grade sa drugim atomima, broja susjednih atoma (
koordinacijski broj
) i kvantno-mehani?kih osobina poput spina.
[68]
Na
periodnom sistemu elemenata
, atomi te?e pove?anju atomskog radijusa idu?i kroz periode prema dolje, te smanjivanju idu?i s lijeva na desno kroz grupe hemijskih elemenata.
[69]
Kao posljedica toga, najmanji atom po atomskim radijusima jeste
helij
sa radijusom od 32 pikometra, dok je jedan od najve?ih
cezij
sa 225 pikometara.
[70]
Kada na njega djeluju vanjske sile poput elektri?nog polja, oblika atoma mo?e zna?ajno odstupiti od loptaste simetrije. Deformacija zavisi od snage elektri?nog polja i vrste orbite krajnje vanjske elektronske ljuske, kako to predviđaju
teorije grupa
. Asferi?ne (neloptaste) devijacije mogu biti izazvane naprimjer u
kristalima
, gdje se velika kristalno-elektri?na polja mogu javiti na mjestima re?etke s
niskom simetrijom
.
[71]
[72]
Zna?ajne
elipsoidne
deformacije mogu se javiti kod iona
sumpora
[73]
i
halkogenih
iona
[74]
u spojevima sli?nih
piritu
. Veli?ina atoma je reda veli?ine oko hiljadu puta manja talasne du?ine vidljive svjetlosti (400?700
nm
) tako da se oni ne mogu vidjeti pod
opti?kim mikroskopom
. Međutim, pomo?u
skeniraju?eg tunelskog mikroskopa
mogu?e je vidjeti pojedina?ne atome. Da bi se lak?e predstavila veli?ina atoma, smatra se da je debljina obi?ne ljudske dlake u pre?niku reda oko milion atoma ugljika.
[75]
Jedna kap
vode
sadr?i pribli?no 2 x 10
21
atoma kisika i dvostruko ve?i broj atoma vodika.
[76]
Dijamant
od jednog karata, mase
?ablon:FormattingError
, sadr?i oko 10
22
atoma ugljika.
[note 2]
Kada bi se
jabuka
pove?ala do veli?ine planete Zemlje, tada bi atomi te jabuke bili pribli?no veli?ine prvobitne jabuke.
[77]
Glavni ?lanak:
Radioaktivnost
 Dijagram prikazuje
vrijeme poluraspada
(T
½
) nekih izotopa sa Z protona i N neutrona.
Dijagram prikazuje
vrijeme poluraspada
(T
½
) nekih izotopa sa Z protona i N neutrona.
Svaki element ima jedan ili vi?e izotopa koji imaju nestabilno jezgro i koje se raspada nekim od radioaktivnih na?ina raspada, pri ?emu jezgro emitira ?estice ili elektromagnetsku radijaciju.
Radioaktivnost
se mo?e javiti kada je radijus atomskog jezgra dosta ve?i u odnosu na radijus jake sile, koja mo?e djelovati samo na udaljenostima reda veli?ine 1 fm.
[78]
Neki od naj?e??ih na?ina radioaktivnog raspada su:
[79]
[80]
- Alfa raspad
: ovaj proces de?ava se kada jezgro emitira alfa-?esticu, koja je zapravo jezgro atoma helija sa dva protona i dva neutrona. Rezultat ove emisije je novi element sa ni?im
atomskim brojem
.
- Beta raspad
(i
elektronski zahvat
): ove procese regulira slaba sila a njihov rezultat je transformacija jednog neutrona u proton ili obrnuto. Prijelaz iz neutrona u proton de?ava se istovremeno sa emisijom elektrona i
antineutrina
, dok prijelaz iz protona u neutron (osim kod elektronskog zahvata) uzrokuje emisiju
pozitrona
i
neutrina
. Emisije elektrona ili pozitrona nazivaju se beta ?estice. Pri beta raspadu de?ava se ili pove?anje ili smanjenje atomskog broja jezgra za jedan. Elektronski zahvat je mnogo ?e??i od emisije pozitrona jer je za njega potrebno mnogo manje energije. Kod ove vrste raspada, jezgro apsorbira jedan elektron umjesto da se iz njega emitira pozitron. U tom procesu se i dalje emitira neutrino a proton prelazi u neutron.
- Gama raspad
: u ovom procesu dolazi do promjene energetskih nivoa jezgra u ni?e stanje, ?to dovodi do emisije elektromagnetskog zra?enja. Pobuđeno stanje jezgra rezultira gama zra?enjem nakon ?ega dolazi do emisije alfa ili beta ?estice. Prema tome, nakon gama raspada naj?e??e slijedi alfa ili beta raspad.
Postoje i neki rijetki tipovi radioaktivnog raspada koji, između ostalog, uklju?uju izbacivanje neutrona ili protona ili grupe nukleona iz jezgra, ili vi?e od jedne beta ?estice. Analogno gama zra?enju koje omogu?ava pobuđenom jezgru da izgubi energiju na jedan od na?ina, postoji i proces
interne konverzije
kojim nastaju izuzetno brzi elektroni a koji ne spadaju u beta zrake, dok istovremeno nastaju visokoenergetski
fotoni
koji nisu gama zraci. Također, mogu?e je da nekoliko velikih atomskih jezgara eksplodira daju?i dva ili vi?e nabijenih fragmenata raznih masa te nekoliko neutrona u procesu koji se naziva spontana
nuklearna fisija
.
Svaki radioaktivni izotop ima karakteristi?no vrijeme raspada koje se naziva
vrijeme poluraspada
. Ono je definirano kao vremenski period potreban da se raspadne polovina uzorka tog izotopa. To je proces eksponencijalnog raspada kojim se stalno smanjuje preostali udio nekog izotopa za 50% za svaki period vremena poluraspada. Prema tome, nakon dva perioda vremena poluraspada preostaje samo 25% prvobitne koli?ine izotopa i tako dalje.
[78]
Elementarne ?estice imaju vlastitu kvantno-mehani?ku osobinu poznatu kao
spin
. On je analogan
ugaonom momentu
nekog predmeta koji se okre?e oko svog centra mase, mada ako se uzme prema definiciji, ove ?estice se smatraju ta?kama i pa se ne mo?e re?i da rotiraju. Spin se mjeri u jedinicama reducirane
Planckove konstante
(ħ), pri ?emu elektroni, protoni i neutroni imaju spin ½ ħ, ili "spin-½". U atomu, elektroni koji se kre?u oko jezgra, pored spina, imaju i orbitalni ugaoni moment, dok samo jezgro ima vlastiti ugaoni moment zbog svog nuklearnog spina.
[81]
Atom proizvodi
magnetno polje
, odnosno magnetni moment, koji se određuje prema tim raznim oblicima ugaonog momenta, sli?no kao svaki rotiraju?i naelektrisani objekat koji proizvodi magnetno polje. Ipak, najzna?ajniji doprinos nastanku ovog polja dolazi od spina elektrona. Zbog prirode elektrona da se pona?aju prema
Paulijevom principu isklju?enja
, prema kojem se dva elektrona ne mogu nalaziti u istom kvantnom stanju, vezani elektroni se uparuju međusobno, pri ?emu jedan ?lan svakog elektronskog para ima stanje spina
up
dok drugi ?lan ima suprotno stanje spina,
down
. Prema tome, ova dva stanja spina se međusobno poni?tavaju, smanjuju?i ukupni magnetni dipol moment na nulu kod nekih atoma koji imaju paran broj elektrona.
[82]
Kod feromagnetnih elemenata poput
?eljeza
,
kobalta
i
nikla
, neparan broj elektrona dovodi do postojanja nesparenog elektrona i pojavu određenog ukupnog magnetnog momenta. Orbitale susjednih atoma se preklapaju te se dosti?e stanje ni?e energije kada se spinovi nesparenih elektrona spontano "poravnaju" jedan s drugim, ?to se naziva interakcija izmjene. Kada se poravnaju magnetni momenti feromagnetnih atoma, tada predmet ili materijal mo?e proizvesti mjerljivo makroskopsko magnetno polje. Paramagnetni materijali imaju atome sa magnetnim momentima koji se poravnavaju u nasumi?nim pravcima kada nije prisutno magnetno polje, ali se u prisustvu takvog polja poravnaju (usmjere u istom pravcu).
[82]
[83]
Jezgro atoma ne?e imati nikakav spin kada u sebi sadr?i paran broj i neutrona i protona, međutim u slu?ajevima kada su neparni brojevi nukleona, onda i jezgro mo?e imati spin. Obi?no su jezgra sa spinom poravnati u nasumi?nim pravcima zbog termalne ravnote?e. Međutim, kod određenih elemenata (poput
ksenona
-129) mogu?e je da se polariziraju zna?ajni udjeli stanja nuklearnog spina tako da su onda jezgra poravnata u istom pravu. Takvo stanje u fizici naziva se
hiperpolarizacija
. Ona ima vrlo va?ne oblasti primjene naprimjer pri snimanju
magnetnom rezonancom
.
[84]
[85]
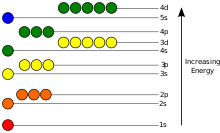 Prikazani su energetski nivoi elektrona (nisu u skali) koji su dovoljni za stabilna stanja atoma do
kadmija
(5s
2
4d
10
) (uklju?uju?i). Treba zapaziti da je ?ak i vrh dijagrama znatno ni?i od energetskih stanja nevezanih elektrona.
Prikazani su energetski nivoi elektrona (nisu u skali) koji su dovoljni za stabilna stanja atoma do
kadmija
(5s
2
4d
10
) (uklju?uju?i). Treba zapaziti da je ?ak i vrh dijagrama znatno ni?i od energetskih stanja nevezanih elektrona.
Potencijalna energija
elektrona u atomu je
negativna
, a zavisnost njegove pozicije dose?e minimum (najvi?u
apsolutnu vrijednost
) unutar jezgra, te potpuno nestaje kada udaljenost od jezgra dosegne beskona?nost, ugrubo ra?unaju?i obrnutno proporcionalno udaljenosti. Prema kvantno-mehani?kom modelu, vezani elektron mo?e zauzeti samo jedan set kvantnih stanja sa centrom u jezgru, a svako stanje odgovara određenom energetskom nivou. Teoretsko razmatranje tog modela obrađuje
vremenski nezavisna Schrodingerova jedna?ina
. Energetski nivo mo?e biti izmjeren pomo?u koli?ine energije potrebne da se elektron izdvoji iz atoma, te se naj?e??e izra?ava
elektronvoltima
(eV). Najni?e stanje energije vezanog elektrona naziva se osnovno stanje, odnosno stacionarno stanje, dok se tranzicija elektrona na neke vi?e nivoe ozna?ava kao pobuđeno stanje.
[86]
Energija elektrona pove?ava se pri pove?anju
n
(osnovnog kvantnog broja) jer se pove?ava (prosje?na) udaljenost od jezgra. Zavisnost energije od
ℓ
nije uzrokovana elektrostati?kim potencijalom jezgra ve? interakcijom između elektrona.
Elektron koji prelazi između dva razli?ita stanja, naprimjer između osnovnog i prvog pobuđenog, on mora apsorbirati ili emitirati
foton
energije koja odgovara razlici između potencijalnih energija ta dva nivoa, u skladu sa Bohrovim modelom, ?to se vrlo precizno mo?e izra?unati
Schrodingerovom jedna?inom
. Elektroni "ska?u" između orbitala na na?in kako bi to ?inili da su ?estice. Naprimjer, ako jedan foton udari u vi?e elektrona, samo jedan elektron promijeni svoje stanje kao odgovor na udar fotona. Energija emitiranog fotona proporcionalna je njegovoj
frekvenciji
pa se određeni specifi?ni energetski nivoi javljaju u vidu određenih talasnih du?ina elektromagnetskog spektra.
[87]
Svaki hemijski element ima karakteristi?an spektar koji zavisi od njegovog nuklearnog naboja, podljusaka napunjenih elektronima i elektromagnetnih međudjelovanja između elektrona te drugih faktora.
[88]
Kada kontinuirani elektromagnetni spektar energije prođe kroz
plin
ili
plazmu
, neke fotone apsorbiraju pojedini atomi uzrokuju?i da elektroni promijene svoje energetske nivoe. Tako pobuđeni elektroni koji ostanu vezani na svojim atomima spontano emitiraju primljenu energiju u vidu fotona u nasumi?nom pravcu te se nakon toga vra?aju na ni?e energetske nivoe. Na taj na?in atomi se pona?aju kao filteri koji formiraju seriju tamnih apsorpcijskih vrpci u izlaznom snopu energije. Posmatra? koji posmatra atome tamo gdje nema kontinuiranog spektra u pozadini, umjesto apsorpcijskih vrpci vidi serije emisijskih linija od emitiranih fotona iz atoma.
Spektroskopska
mjerenja snage i ?irine atomskih spektralnih linija omogu?ava određivanje sadr?aja i fizi?kih osobina ispitivane supstance.
[89]
Detaljnijim istra?ivanjem spektralnih linija otkrivena je pojava izdvajanja finih spektralnih struktura. To se de?ava zbog kuplovanja spina i orbitale, ?to predstavlja međudjelovanje između spina i kretanja najudaljenijih vanjskih elektrona.
[90]
Kada se atom nalazi u vanjskom magnetnom polju, spektralne linije se ras?lanjuju u tri ili vi?e komponenti. Takav fenomen nazvan je
Zeemanov efekt
. On se de?ava zbog međudjelovanja magnetnog polja i magnetnog momenta atoma i njegovih elektrona. Neki atomi mogu imati vi?e elektronskih konfiguracija sa istim nivoom energije, pa oni izgledaju kao jedinstvena spektralna linija. Interakcija magnetnog polja sa atomom neznatno pomijera ove
elektronske konfiguracije
do druga?ijih energetskih nivoa, ?to dovodi do pojave vi?estrukih spektralnih linija.
[91]
Prisustvo vanjskog
elektri?nog polja
mo?e također uzrokovati sli?na razdvajanja i pomijeranja spektralnih linija tako ?to se mijenjaju energetski nivoi elektrona, a taj fenomen naziva se
Starkov efekt
.
[92]
Ako se vezani elektron nalazi u pobuđenom stanju, foton koji djeluje na njega određenom energijom mo?e prouzrokovati stimuliranu emisiju fotona istog energetskog nivoa. Da bi se to desilo, elektron prvo mora pre?i na ni?i energetski nivo koji ima razliku u energijama koja odgovara energiji fotona koji djeluje na elektron. Emitirani foton i foton koji je međudjelovao sa elektronom odlaze u paralelnim pravcima i u istim su faznim stanjima. Drugim rije?ima, talasni obrazac dva fotona je sinhroniziran. Ova fizi?ka osobina iskori?tena je u raznim vrstama
lasera
, koji emitiraju koherentni snop svjetlosne energije u uskom frekvencijskom opsegu.
[93]
 Grafi?ka ilustracija nastanka
Bose?Einsteinovog kondenzata
.
Grafi?ka ilustracija nastanka
Bose?Einsteinovog kondenzata
.
Valencija je potencijalna snaga spajanja nekog elementa. Ona je jednaka broju atoma vodika s kojima se neki atom mo?e spojiti ili istisnuti grade?i neki
hemijski spoj
. Krajnja vanjska elektronska ljuska nekog atoma u svom slobodnom, nespojenom stanju se naziva valentna ljuska, dok se elektroni u toj ljusci nazivaju valentni elektroni. Broj valentnih elektrona određuje i
hemijsko vezivanje
atoma s drugim atomima. Oni te?e da
reagiraju
jedni sa drugim na na?in da popune (ili isprazne) svoje vanjske valentne ljuske.
[94]
Naprimjer, prijelaz jednog elektrona između atoma korisna je aproksimacija za veze koje nastaju između atoma sa jednim elektronom vi?ka od potpuno popunjene orbitale, dok drugom nedostaje jedan elektron za popunu orbitale, ?to je proces koji se de?ava u spoju
natrij-hlorid
i drugim
ionskim
solima. Međutim, kod mnogih elemenata javljaju se dva ili vi?e valentnih stanja odnosno tendencija da dijele razli?it broj elektrona u razli?itim spojevima. Prema tome, hemijsko vezivanje između tih elemenata javlja se u raznim oblicima dijeljenja elektrona ?to je sasvim druga?iji oblik vezanja od jednostavnog prijelaza elektrona. Takvi primjeri su kod
ugljika
i
organskih spojeva
.
[95]
U
periodnom sistemu
, hemijski elementi ?esto se prikazuju tako da su grupisani prema ponavljaju?im hemijskim osobinama, pa tako elementi sa istim valentnim brojem elektrona grade grupe elemenata koji su svrstani u istu kolonu tabele PSE. Horizontalne kolone odgovaraju redoslijedu popunjavanja kvantnih ljusaka elektronima. Elementi koji su svrstani u krajnju desnu kolonu tabele imaju svoju krajnju vanjsku ljusku u potpunosti popunjenu elektronima, ?to za posljedicu ima da su oni hemijski inertni elementi, poznati i kao
plemeniti plinovi
.
[96]
[97]
Koli?ine atoma koje se mogu na?i u razli?itim agregatnim stanjima materije zavise od fizi?kih uslova kao ?to su
temperatura
i
pritisak
. Mijenjanjem ovih uslova, materijali mogu prelaziti između raznih agregatnih stanja:
?vrstog
,
te?nog
, plinovitog i plazme.
[98]
U određenom agregatnom stanju, neka supstanca mo?e također postojati u razli?itim
alotropnim oblicima
. Primjer alotropa je ?vrsti ugljik, koji se u prirodi javlja kao
grafit
ili
dijamant
.
[99]
Također postoje i plinoviti alotropi kao ?to je to slu?aj kod
molekulskog kisika
i
ozona
. Na temperaturama bliskim
apsolutnoj nuli
, atomi mogu formirati i
Bose-Einsteinov kondenzat
, u kojem efekti kvantne mehanike mogu biti posmatrani i na makroskopskoj skali.
[100]
[101]
Ova super ohlađena kolekcija atoma pona?a se kao jedan ogromni atom, na kojem se mogu vr?iti fundamentalni eksperimenti o kvantno-mehani?kom pona?anju atoma.
[102]
 Slika na?injena skeniraju?im tunelskim mikroskopom prikazuje pojedina?ne atome na povr?ini
zlata
. Povr?inski atomi odstupaju od op?enite kristalne strukture te su poredani u kolone ?iroke nekoliko atoma sa prazninama između njih.
Slika na?injena skeniraju?im tunelskim mikroskopom prikazuje pojedina?ne atome na povr?ini
zlata
. Povr?inski atomi odstupaju od op?enite kristalne strukture te su poredani u kolone ?iroke nekoliko atoma sa prazninama između njih.
Skeniraju?i tunelski mikroskop
je uređaj pomo?u kojeg je mogu?e posmatrati povr?inu uzroka na atomskom nivou. On iskori?tava fenomen
kvantnog
tuneliranja
, koji omogu?ava da ?estice prođu kroz barijeru, kroz koju ina?e ne bi mogle pro?i. Elektroni ulaze u "tunel" kroz
vakuum
između dvije planarne
metalne
elektrode, a na svakoj od njih je adsorbiran atom, daju?i gusto?u tunelske struje dovoljnu da se mo?e izmjeriti. Skeniranje jednog atoma dok se kre?e pored drugih omogu?ava iscrtavanje vrha odmaka u odnosu uporednu separaciju uz neku konstantnu struju. Izra?uni pokazuju u kojoj mjeri se na slikama na?injenim skeniraju?im tunelskim mikroskopom mogu vidjeti pojedina?ni atomi. S tim se uz vrlo mali postotak gre?ke potvrđuje da mikroskopske slike prikazuju prostorno prosje?ne dimenzije elektronskih orbitala du? gusto zbijenih energetskih nivoa, tj. Fermijev nivo lokalnih gusto?a stanja.
[103]
[104]
Atom se mo?e
ionizirati
uklanjanjem jednog ili vi?e elektrona iz njega.
Elektri?ni naboj
uzrokuje da se putanja atoma iskrivljuje kada on putuje kroz
magnetno polje
. Radijus u kojem se putanja iona koji se kre?e iskrivljuje u magnetnom polju zavisi od mase atoma.
Maseni spektrometar
radi na ovom principu ?ime se mjeri odnos mase i naboja iona. Ako uzorak sadr?i vi?e izotopa, masenim spektrometrom se mo?e odrediti proporcija svakog izotopa u uzorku, mjerenjem intenziteta razli?itih snopova iona. Tehnike isparavanja atoma uklju?uju, između ostalih, induktivno spregnutu plazmu atomsku emisionu spektroskopiju i induktivno spregnutu plazmu masenu spektroskopiju. Obje tehnike koriste plazmu da bi uzroke pretvorili u plin za analizu.
[105]
Metoda kojom se mo?e preciznije odabrati određeno podru?je je
spektroskopija gubitka energije elektrona
, kojom se mjeri gubitak energije snopa elektrona unutar transmisijskog elektronskog mikroskopa kada oni međudjeluju sa dijelom ispitivanog uzorka. Tomografija atomskom sondom ima rezoluciju manju od nanometra u trodimenzionalnom okru?enju te se pomo?u nje pojedini atomi mogu hemijski identificirati masenom spektrometrijom koriste?i se TOF analizatorom.
[106]
Spektar pobuđenih stanja se mo?e koristiti za analizu atomskog sastava udaljenih
zvijezda
. Određene talasne du?ine svjetlosti sadr?ane u posmatranoj svjetlosti koja dolazi sa neke zvijezde mogu se razdvojiti i po njima odrediti kvanizirani prijelazi u slobodnim atomima plina. Te boje se mogu replicirati koriste?i sijalicu sa metalnim parama koja sadr?i ispitivani element.
[107]
Na ovaj na?in otkriven je plin
helij
u spektru Sun?eve svjetlosti, 23 godine prije nego ?to je isti plin otkriven na Zemlji.
[108]
Barionska
materija sa?injava oko 4% sveukupne gusto?e energije u
vidljivom svemiru
, pri ?emu prosje?na gusto?a iznosi oko 0,25 ?estica/m
3
(uglavnom u obliku
protona
i
elektrona
).
[109]
Unutar
galaksija
, kao ?to je na?
Mlije?ni put
, ?estice se ponegdje nalaze u mnogo ve?im koncentracijama, gdje se gusto?a materije u međuzvjezdanom prostoru kre?e od 10
5
do 10
9
atoms/m
3
.
[110]
Smatra se da se
Sunce
nalazi unutar Lokalne grupe zvijezda, tako da je gusto?a materije u Sun?evom kom?iluku pribli?no 10
3
atoma/m
3
.
[111]
Zvijezde se formiraju od gustih oblaka u međuzvjezdanom prostoru, a evolucijski procesi zvijezda rezultirali su konstantnim oboga?ivanjem međuzvjezdanog prostora elementima te?im od vodika i helija.
Oko 95% barionske materije Mlije?nog puta koncentrirana je unutar zvijezda gdje vladaju uslovi koji ne pogoduju atomskoj materiji. Ukupna barionska masa zauzima oko 10% mase galaksije;
[112]
dok ostatak otpada na pretpostavljenu
tamnu materiju
.
[113]
Ekstremno visoke
temperature
koje vladaju unutar zvijezda mijenjaju atome tako da postaju u potpunosti ionizirani, to jest
svi
elektroni se odvajaju od jezgra. U
kompaktnim zvijezdama
, uz izuzetak njihovih povr?inskih slojeva, izuzetan pritisak ?ini nemogu?im postojanje elektronskih orbitala.
Smatra da su elektroni u Svemiru postojali jo? od prvih trenutaka nakon
Velikog praska
. Atomska jezgra formirala su se tokom
nukleosintetskih
reakcija. Tokom tri minute nukleosinteze nakon Velikog praska nastala je ve?ina atoma
helija
,
litija
i
deuterija
u Svemiru, a mo?da i ne?to atoma
berilija
i
bora
.
[114]
[115]
[116]
Sveprisutnost i stabilnost atoma po?iva na njihovoj energiji vezivanja, ?to zna?i da atom ima ni?u energiju nego sistem nepovezanih atomskih jezgara i elektrona. Na mjestima gdje je
temperatura
znatno vi?a od ionizacijskog potencijala, materija postoji u obliku
plazme
, plina sastavljenog iz pozitivno nabijenih iona (mogu?e i ogoljenih jezgara) i elektrona. Kada temperatura spadne ispod ionizacijskog potencijala, atomi postaju statisti?ki povoljni. Atomi (cijeli sa vezanim elektronima) postali su dominantni u odnosu na nabijene ?estice tek 380 hiljada godina nakon Velikog praska. Ta epoha nazvana je rekombinacija, kada se
Svemir
pri ?irenju ohladio u dovoljnoj mjeri da su se elektroni po?eli vezivati za atomska jezgra.
[117]
Po?ev od Velikog praska, tokom kojeg nisu nastali atomi
ugljika
niti elementi te?i od njega, jezgra atoma su se spajala unutar
zvijezda
procesom
nuklearne fuzije
?ime su nastajale nove koli?ine elementa
helija
, te (trostrukim alfa procesom) atomi elemenata po?ev od ugljika do
?eljeza
.
[118]
Taj proces naziva se zvjezdana nukleosinteza. Izotopi kao ?to je
litij
-6, kao i određena koli?ina berilija i bora, nastali su svemiru putem procesa spalacije kosmi?kim zrakama.
[119]
Ona se javlja kada visokoenergetski protoni udare u atomska jezgra izbijaju?i ve?i broj nukleona iz njega.
Elementi te?i od ?eljeza nastali su
r-procesom
tokom
supernove
kao i
s-procesom
u
zvijezdama asimptotskog divovskog ogranka
. Oba ova procesa uklju?uju zahvatanje neutrona unutar atomskog jezgra.
[120]
Elementi kao ?to je
olovo
uglavnom nastaju radioaktivnim raspadom te?ih elemenata.
[121]
Ve?ina atoma, koji sa?injavaju planetu
Zemlju
i njene stanovnike, bila je prisutna u dana?njem obliku u
maglini
koja se uru?ila iz
molekularnog oblaka
i iz koje je nastao dana?nji
Sun?ev sistem
. Mali dio atoma na Zemlji rezultat je procesa radioaktivnog raspada te se relativni odnos tih atoma mo?e koristiti za određivanje starosti Zemlje putem radiometrijskog datiranja.
[122]
Ve?ina helija u Zemljinoj kori (oko 99% helija iz plinovitih izvora, ?to pokazuje i mala rasprostranjenost izotopa helija-3) proizvod je alfa raspada.
[124]
Postoji vrlo malo atoma u tragovima na Zemlji koji nisu bili prisutni u vrijeme njenog nastanka (tj. nisu
primordijalni
atomi), a nisu ni rezultat radioaktivnog raspada. Izotop ugljika-14 stalno nastaje u atmosferi djelovanjem kosmi?kih zraka.
[125]
Neki atomi na Zemlji napravljeni su vje?ta?ki bilo kao rezultat rada nau?nika ili kao nusproizvod u nuklearnim reaktorima ili pri nuklearnim eksplozijama.
[126]
[127]
Od svih tranuranijskih elemenata, odnosno elemenata sa atomskim brojevima ve?im od 92, samo se
plutonij
i
neptunij
mogu prona?i na Zemlji u prirodnom stanju.
[128]
[129]
Transuranijski elementi imaju radioaktivni "?ivotni vijek" znatno kra?i od starosti Zemlje
[130]
pa su se njihove mjerljive koli?ine ve? odavno raspale na lak?e elemente. Jedan od rijetkih izuzetaka je izotop
plutonija
-244, ?ije tragove je mogu?e detektirati u si?u?nim uzorcima kosmi?ke pra?ine.
Prirodni depoziti plutonija i neptunija nastaju zahvatom neutrona u rudama
uranija
.
[131]
Prema određenim procjenama, na Zemlji se nalazi
?ablon:FormattingError
atoma.
[132]
Iako postoji vrlo mali broj atoma koji nisu vezani u molekulu, kao ?to su atomi plemenitih plinova:
argon
,
neon
i
helij
, 99% atoma u Zemljinoj atmosferi vezano je u obliku molekula poput
ugljik-dioksida
ili dvoatomskih molekula
kisika
i
du?ika
. Na povr?ini Zemlje, ogromna ve?ina atoma spojena je u obliku raznih spojeva, uklju?uju?i
vodu
, soli, silikate i okside. Atomi su također spojeni u obliku materijala koji se ne sastoje iz molekula, kao ?to su kristali ili te?ni i ?vrsti metali.
[133]
[134]
Takva atomska materija gradi umre?ene sisteme koji ne posjeduju određenu vrstu kona?nog, razdijeljenog rasporeda u vrlo malom obimu, ?to je karakteristika molekularne materije.
[135]
Iako je poznato da su izotopi sa atomskim brojem vi?im od 82 (
olovo
) radioaktivni, neki nau?nici ?pekuli?u o postojanju "
ostrva stabilnosti
" za neke elemente sa atomskim brojevima iznad 103. Takvi superte?ki elementi bi mogli imati atomska jezgra koja su relativno stabilna u odnosu na radioaktivni raspad.
[136]
Jedan od mogu?ih kandidata za stabilni superte?ki atom jeste
unbiheksij
, koji bi trebao imati 126 protona i 184 neutrona.
[137]
Svaka ?estica materija ima odgovaraju?u ?esticu
antimaterije
sa suprotnim elektri?nim nabojem. Prema tome,
pozitron
je pozitivni naelektrisani antielektron dok je
antiproton
negativno nabijeni ekvivalent protonu. Prema pretpostavkama, kada se ?estice obi?ne materije i antimaterije dodirnu, one poni?tavaju jedna drugu. Iz tog razloga, zajedno sa neravnote?om između broja ?estice materije i antimaterije, antimaterija je vrlo rijetka u svemiru. Konkretni razlozi za ovu neravnote?u jo? uvijek nisu u potpunosti shva?eni, mada teorije
bariogeneze
nude određena obja?njenja. Kao rezultat te pojave, u prirodi jo? nisu otkriveni atomi antimaterije.
[138]
[139]
Međutim, u laboratoriji
CERN
u
?enevi
1996. godine sintetiziran je antimaterijski ekvivalent atomu vodika (antivodik, antihidrogen).
[140]
[141]
Druge egzoti?ne vrste atoma napravljene su zamjenom jednog od protona, neutrona ili elektrona sa drugim ?esticama iste vrste naelektrisanja. Naprimjer, elektron se mo?e zamijeniti mnogo masivnijom ?esticom,
mionom
, pri ?emu nastaje
mionski atom
. Takve vrste atoma se mogu koristiti za istra?ivanje osnovnih pretpostavki fizike.
[142]
[143]
[144]
- ↑
Za najnovija a?uriranja pogledajte
interaktivnu kartu nuklida (Nacionalna laboratorija Brookhaven)
Arhivirano
2020-07-25 na
Wayback Machine-u
.
- ↑
Karat ima 200 miligrama.
Po definiciji
, izotop ugljik-12 ima masu 0,012 kg po molu.
Avogadrova konstanta
definira da u jednom molu ima
?ablon:FormattingError
atoma.
- ↑
Pullman Bernard (1998).
The Atom in the History of Human Thought
. Oxford, Engleska: Oxford University Press. str. 31?33.
ISBN
978-0-19-515040-7
.
- ↑
2,0
2,1
Kenny Anthony (2004).
Ancient Philosophy
. A New History of Western Philosophy.
1
. Oxford, Engleska: Oxford University Press. str. 26?28.
ISBN
978-0-19-875273-8
.
- ↑
3,00
3,01
3,02
3,03
3,04
3,05
3,06
3,07
3,08
3,09
Pyle Andrew (2010).
?Atoms and Atomism”
. u: Grafton Anthony; Most Glenn W.; Settis Salvatore.
The Classical Tradition
. Cambridge, Massachusetts and London: The Belknap Press of Harvard University Press. str. 103?104.
ISBN
978-0-674-03572-0
.
- ↑
4,0
4,1
4,2
4,3
Cohen Henri; Lefebvre Claire, ur. (2017).
Handbook of Categorization in Cognitive Science
(2 izd.). Amsterdam, Holandija: Elsevier. str. 427.
ISBN
978-0-08-101107-2
.
- ↑
Andrew G. van Melsen (1952).
From Atomos to Atom
. Mineola, NY: Dover Publications.
ISBN
978-0-486-49584-2
.
- ↑
Dalton, John. "
On the Absorption of Gases by Water and Other Liquids
", u
Memoirs of the Literary and Philosophical Society of Manchester
. 1803. Pristupljeno 29. augusta 2007.
- ↑
Einstein Albert (1905).
?Uber die von der molekularkinetischen Theorie der Warme geforderte Bewegung von in ruhenden Flussigkeiten suspendierten Teilchen”
(de).
Annalen der Physik
322
(8): 549?560.
Bibcode
1905AnP...322..549E
.
DOI
:
10.1002/andp.19053220806
. Arhivirano iz
originala
na datum 2007-07-18
. Pristupljeno 2020-08-22
.
- ↑
Mazo Robert M. (2002).
Brownian Motion: Fluctuations, Dynamics, and Applications
. Oxford University Press. str. 1?7.
ISBN
978-0-19-851567-8
.
OCLC
48753074
.
- ↑
Lee Y.K.; Hoon, K. (1995).
?Brownian Motion”
. Imperial College. Arhivirano iz
originala
na datum 18. 12. 2007
. Pristupljeno 20. 5. 2019
.
- ↑
Patterson G. (2007).
?Jean Perrin and the triumph of the atomic doctrine”
.
Endeavour
31
(2): 50?53.
DOI
:
10.1016/j.endeavour.2007.05.003
.
PMID
17602746
.
- ↑
Thomson J.J..
?On bodies smaller than atoms”
.
The Popular Science Monthly
: 323?335.
- ↑
?J.J. Thomson”
. Nobelova fondacija. 1906
. Pristupljeno 20. 12. 2007
.
- ↑
Rutherford E. (1911).
?The Scattering of α and β Particles by Matter and the Structure of the Atom”
.
Philosophical Magazine
21
(125): 669?688.
DOI
:
10.1080/14786440508637080
.
- ↑
?Frederick Soddy, The Nobel Prize in Chemistry 1921”
. Nobelova fondacija
. Pristupljeno 18. 1. 2008
.
- ↑
Thomson Joseph John (1913).
?Rays of positive electricity”
.
Proceedings of the Royal Society
. A
89
(607): 1?20.
Bibcode
1913RSPSA..89....1T
.
DOI
:
10.1098/rspa.1913.0057
.
- ↑
Stern David P..
?The Atomic Nucleus and Bohr's Early Model of the Atom”
. NASA/Svemirski centar Goddard. Arhivirano iz
originala
na datum 2007-08-20
. Pristupljeno 2020-08-22
.
- ↑
Bohr Niels.
?Niels Bohr, The Nobel Prize in Physics 1922, Nobel Lecture”
. Nobelova fondacija
. Pristupljeno 16. 2. 2008
.
- ↑
18,0
18,1
18,2
Pais Abraham (1986).
Inward Bound: Of Matter and Forces in the Physical World
. New York: Oxford University Press. str.
228?230
.
ISBN
978-0-19-851971-3
.
- ↑
Lewis Gilbert N. (1916). ?The Atom and the Molecule”.
Journal of the American Chemical Society
38
(4): 762?786.
DOI
:
10.1021/ja02261a002
.
- ↑
Scerri Eric R. (2007).
The periodic table: its story and its significance
. Oxford University Press US. str.
205?226
.
ISBN
978-0-19-530573-9
.
- ↑
Langmuir Irving (1919).
?The Arrangement of Electrons in Atoms and Molecules”
.
Journal of the American Chemical Society
41
(6): 868?934.
DOI
:
10.1021/ja02227a002
.
- ↑
Scully Marlan O.; Lamb, Willis E.; Barut, Asim (1987). ?On the theory of the Stern-Gerlach apparatus”.
Foundations of Physics
17
(6): 575?583.
Bibcode
1987FoPh...17..575S
.
DOI
:
10.1007/BF01882788
.
- ↑
Chad Orzel.
?What is the Heisenberg Uncertainty Principle?”
. TED-Ed.
- ↑
Brown Kevin (2007).
?The Hydrogen Atom”
. MathPages
. Pristupljeno 21. 12. 2007
.
- ↑
Harrison David M. (2000).
?The Development of Quantum Mechanics”
. Univerzitet u Torontu. Arhivirano iz
originala
na datum 25. 12. 2007
. Pristupljeno 21. 12. 2007
.
- ↑
Aston Francis W. (1920). ?The constitution of atmospheric neon”.
Philosophical Magazine
39
(6): 449?455.
DOI
:
10.1080/14786440408636058
.
- ↑
Chadwick James.
?Nobel Lecture: The Neutron and Its Properties”
. Nobelova fondacija
. Pristupljeno 21. 12. 2007
.
- ↑
Bowden Mary Ellen (1997).
?Otto Hahn, Lise Meitner, and Fritz Strassmann”
.
Chemical achievers : the human face of the chemical sciences
. Philadelphia, PA: Chemical Heritage Foundation. str.
76?80, 125
.
ISBN
978-0-941901-12-3
.
- ↑
?Otto Hahn, Lise Meitner, and Fritz Strassmann”
. Science History Institute
. Pristupljeno 20. 3. 2018
.
- ↑
Meitner Lise; Frisch Otto Robert (1939). ?Disintegration of uranium by neutrons: a new type of nuclear reaction”.
Nature
143
(3615): 239?240.
Bibcode
1939Natur.143..239M
.
DOI
:
10.1038/143239a0
.
- ↑
Schroeder M..
?Lise Meitner ? Zur 125. Wiederkehr Ihres Geburtstages”
(de). Arhivirano iz
originala
na datum 19. 7. 2011
. Pristupljeno 4. 6. 2009
.
- ↑
Crawford E.; Sime Ruth Lewin; Walker Mark (1997).
?A Nobel tale of postwar injustice”
.
Physics Today
50
(9): 26?32.
Bibcode
1997PhT....50i..26C
.
DOI
:
10.1063/1.881933
.
- ↑
Kullander Sven.
?Accelerators and Nobel Laureates”
. Nobelova fondacija
. Pristupljeno 31. 1. 2008
.
- ↑
?The Nobel Prize in Physics 1990”
. Nobelova fondacija
. Pristupljeno 31. 1. 2008
.
- ↑
Demtroder Wolfgang (2002).
Atoms, Molecules and Photons: An Introduction to Atomic- Molecular- and Quantum Physics
(1 izd.). Springer. str. 39?42.
ISBN
978-3-540-20631-6
.
OCLC
181435713
.
- ↑
Woan Graham (2000).
The Cambridge Handbook of Physics
. Cambridge University Press. str.
8
.
ISBN
978-0-521-57507-2
.
OCLC
224032426
.
- ↑
Mohr, P.J.; Taylor, B.N.; Newell, D.B. (2014),
"The 2014 CODATA Recommended Values of the Fundamental Physical Constants"
(Web verzija 7.0). Bazu podataka razvili su J. Baker, M. Douma i S. Kotochigova. (2014). Nacionalni institut za standarde i tehnologiju SAD, Gaithersburg, Maryland 20899.
- ↑
MacGregor Malcolm H. (1992).
The Enigmatic Electron
. Oxford University Press. str.
33?37
.
ISBN
978-0-19-521833-6
.
OCLC
223372888
.
- ↑
39,0
39,1
Particle Data Group (2002).
?The Particle Adventure”
. Lawrence Berkeley Laboratory. Arhivirano iz
originala
na datum 4. 1. 2007
. Pristupljeno 3. 1. 2007
.
- ↑
40,0
40,1
James Schombert.
?Elementary Particles”
. University of Oregon. Arhivirano iz
originala
na datum 2011-08-30
. Pristupljeno 2015-04-25
.
- ↑
Jevremovic Tatjana (2005) (en).
Nuclear Principles in Engineering
. Springer. str.
63
.
ISBN
978-0-387-23284-3
.
OCLC
228384008
.
- ↑
Pfeffer Jeremy I.; Nir Shlomo (2000).
Modern Physics: An Introductory Text
. Imperial College Press. str. 330?336.
ISBN
978-1-86094-250-1
.
OCLC
45900880
.
- ↑
Wenner Jennifer M..
?How Does Radioactive Decay Work?”
. Carleton College
. Pristupljeno 9. 1. 2008
.
- ↑
44,0
44,1
44,2
Raymond David.
?Nuclear Binding Energies”
. New Mexico Tech. Arhivirano iz
originala
na datum 2002-12-01
. Pristupljeno 2015-04-25
.
- ↑
Mihos Chris.
?Overcoming the Coulomb Barrier”
. Case Western Reserve University
. Pristupljeno 13. 2. 2008
.
- ↑
uredni?tvo.
?ABC's of Nuclear Science”
. Lawrence Berkeley National Laboratory. Arhivirano iz
originala
na datum 5. 12. 2006
. Pristupljeno 3. 1. 2007
.
- ↑
Arjun Makhijani; Saleska, Scott.
?Basics of Nuclear Physics and Fission”
. Institute for Energy and Environmental Research. Arhivirano iz
originala
na datum 16. 1. 2007
. Pristupljeno 3. 1. 2007
.
- ↑
Shultis J. Kenneth; Faw Richard E. (2002).
Fundamentals of Nuclear Science and Engineering
. CRC Press. str. 10?17.
ISBN
978-0-8247-0834-4
.
OCLC
123346507
.
- ↑
Fewell M.P. (1995). ?The atomic nuclide with the highest mean binding energy”.
American Journal of Physics
63
(7): 653?658.
Bibcode
1995AmJPh..63..653F
.
DOI
:
10.1119/1.17828
.
- ↑
Mulliken Robert S. (1967). ?Spectroscopy, Molecular Orbitals, and Chemical Bonding”.
Science
157
(3784): 13?24.
Bibcode
1967Sci...157...13M
.
DOI
:
10.1126/science.157.3784.13
.
PMID
5338306
.
- ↑
51,0
51,1
Brucat Philip J. (2008).
?The Quantum Atom”
. Univerzitet Floride. Arhivirano iz
originala
na datum 7. 12. 2006
. Pristupljeno 4. 1. 2007
.
- ↑
Manthey David (2001).
?Atomic Orbitals”
. Orbital Central. Arhivirano iz
originala
na datum 10. 1. 2008
. Pristupljeno 21. 1. 2008
.
- ↑
Herter Terry (2006).
?Lecture 8: The Hydrogen Atom”
. Univerzitet Cornell. Arhivirano iz
originala
na datum 22. 2. 2012
. Pristupljeno 14. 2. 2008
.
- ↑
Bell R.E.; Elliott L.G. (1950). ?Gamma-Rays from the Reaction H
1
(n,γ)D
2
and the Binding Energy of the Deuteron”.
Physical Review
79
(2): 282?285.
Bibcode
1950PhRv...79..282B
.
DOI
:
10.1103/PhysRev.79.282
.
- ↑
Smirnov Boris M. (2003).
Physics of Atoms and Ions
. Springer. str. 249?272.
ISBN
978-0-387-95550-6
.
- ↑
Matis Howard S..
?The Isotopes of Hydrogen”
. Nacionalna laboratorija Lawrence Berkeley. Arhivirano iz
originala
na datum 18. 12. 2007
. Pristupljeno 21. 12. 2007
.
- ↑
Weiss Rick.
?Scientists Announce Creation of Atomic Element, the Heaviest Yet”
.
Washington Post
.
- ↑
58,0
58,1
Sills Alan D. (2003).
Earth Science the Easy Way
. Barron's Educational Series. str.
131?134
.
ISBN
978-0-7641-2146-3
.
OCLC
51543743
.
- ↑
Dume Belle.
?Bismuth breaks half-life record for alpha decay”
. Physics World. Arhivirano iz
originala
na datum 14. 12. 2007.
- ↑
Lindsay Don.
?Radioactives Missing From The Earth”
. Don Lindsay Archive. Arhivirano iz
originala
na datum 28. 4. 2007
. Pristupljeno 23. 5. 2007
.
- ↑
Jagdish K. Tuli.
?Nuclear Wallet Cards”
. Nacionalni centar za nuklearne podatke, Nacionalna laboratorija Brookhaven
. Pristupljeno 16. 4. 2011
.
- ↑
62,0
62,1
David R. Lide (ur.):
CRC Handbook
, 83. izd, CRC Press, 2002.
ISBN
978-0849304835
- ↑
63,0
63,1
Mills Ian; Cvita?, Tomislav; Homann, Klaus; Kallay, Nikola; Kuchitsu, Kozo (1993).
Quantities, Units and Symbols in Physical Chemistry
(2 izd.). Oxford: IUPAC. str.
70
.
ISBN
978-0-632-03583-0
.
OCLC
27011505
.
- ↑
Chieh Chung.
?Nuclide Stability”
. University of Waterloo. Arhivirano iz
originala
na datum 2007-08-30
. Pristupljeno 2020-08-22
.
- ↑
?Atomic Weights and Isotopic Compositions for All Elements”
. NIST. Arhivirano iz
originala
na datum 31. 12. 2006
. Pristupljeno 4. 1. 2007
.
- ↑
?The Ame2003 atomic mass evaluation (II)”
.
Nuclear Physics A
729
(1): 337?676. 2003.
Bibcode
2003NuPhA.729..337A
.
DOI
:
10.1016/j.nuclphysa.2003.11.003
. Arhivirano iz
originala
na datum 2005-10-16
. Pristupljeno 2020-08-22
.
- ↑
Ghosh, D.C.; Biswas, R. (2002). ?Theoretical calculation of Absolute Radii of Atoms and Ions. Part 1. The Atomic Radii”.
Int. J. Mol. Sci.
3
(11): 87?113.
DOI
:
10.3390/i3020087
.
- ↑
?Revised effective ionic radii and systematic studies of interatomic distances in halides and chalcogenides”.
Acta Crystallographica A
32
(5): 751?767. 1976.
Bibcode
1976AcCrA..32..751S
.
DOI
:
10.1107/S0567739476001551
.
- ↑
?Diameter of an Atom”
. The Physics Factbook. 1998. Arhivirano iz
originala
na datum 4. 11. 2007
. Pristupljeno 19. 11. 2007
.
- ↑
Zumdahl Steven S. (2002).
Introductory Chemistry: A Foundation
(5 izd.). Houghton Mifflin.
ISBN
978-0-618-34342-3
.
OCLC
173081482
. Arhivirano iz
originala
na datum 4. 3. 2008
. Pristupljeno 5. 2. 2008
.
- ↑
Bethe, Hans (1929). ?Termaufspaltung in Kristallen”.
Annalen der Physik
3
(2): 133?208.
Bibcode
1929AnP...395..133B
.
DOI
:
10.1002/andp.19293950202
.
- ↑
Birkholz, Mario (1995).
?Crystal-field induced dipoles in heteropolar crystals ? I. concept”
.
Z. Phys. B
96
(3): 325?332.
Bibcode
1995ZPhyB..96..325B
.
DOI
:
10.1007/BF01313054
.
- ↑
Birkholz, M.; Rudert, R. (2008).
?Interatomic distances in pyrite-structure disulfides ? a case for ellipsoidal modeling of sulfur ions”
.
Physica Status Solidi B
245
(9): 1858?1864.
Bibcode
2008PSSBR.245.1858B
.
DOI
:
10.1002/pssb.200879532
.
- ↑
Birkholz, M. (2014). ?Modeling the Shape of Ions in Pyrite-Type Crystals”.
Crystals
4
(3): 390?403.
DOI
:
10.3390/cryst4030390
.
- ↑
urednici (2007).
?Small Miracles: Harnessing nanotechnology”
. Oregon State University
. Pristupljeno 7. 1. 2007
.
- ↑
Padilla Michael J.; Miaoulis, Ioannis; Cyr, Martha (2002).
Prentice Hall Science Explorer: Chemical Building Blocks
. Upper Saddle River, New Jersey: Prentice-Hall, Inc.. str. 32.
ISBN
978-0-13-054091-1
.
OCLC
47925884
.
- ↑
Feynman Richard (1995).
Six Easy Pieces
. The Penguin Group. str. 5.
ISBN
978-0-14-027666-4
.
OCLC
40499574
.
- ↑
78,0
78,1
?Radioactivity”
. Splung.com. Arhivirano iz
originala
na datum 4. 12. 2007
. Pristupljeno 19. 12. 2007
.
- ↑
L'Annunziata Michael F. (2003).
Handbook of Radioactivity Analysis
. Academic Press. str.
3
?56.
ISBN
978-0-12-436603-9
.
OCLC
16212955
.
- ↑
Firestone Richard B..
?Radioactive Decay Modes”
. Berkeley Laboratory. Arhivirano iz
originala
na datum 29. 9. 2006
. Pristupljeno 7. 1. 2007
.
- ↑
Hornak J.P. (2006).
?Chapter 3: Spin Physics”
. Rochester Institute of Technology. Arhivirano iz
originala
na datum 3. 2. 2007
. Pristupljeno 7. 1. 2007
.
- ↑
82,0
82,1
Schroeder Paul A..
?Magnetic Properties”
. Univerzitet Georgije. Arhivirano iz
originala
na datum 29. 4. 2007
. Pristupljeno 7. 1. 2007
.
- ↑
Goebel Greg.
?[4.3] Magnetic Properties of the Atom”
. In The Public Domain website. Arhivirano iz
originala
na datum 21. 8. 2011
. Pristupljeno 7. 1. 2007
.
- ↑
Yarris Lynn.
?Talking Pictures”
.
Berkeley Lab Research Review
. Arhivirano iz
originala
na datum 13. 1. 2008.
- ↑
Liang Z.-P.; Haacke E.M. (1999). Webster, J.G.. ur.
Encyclopedia of Electrical and Electronics Engineering: Magnetic Resonance Imaging
.
2
. John Wiley & Sons. str. 412?426.
ISBN
978-0-471-13946-1
.
- ↑
Zeghbroeck Bart J. Van (1998).
?Energy levels”
. Shippensburg University. Arhivirano iz
originala
na datum 15. 1. 2005
. Pristupljeno 23. 12. 2007
.
- ↑
Fowles Grant R. (1989).
Introduction to Modern Optics
. Courier Dover Publications. str. 227?233.
ISBN
978-0-486-65957-2
.
OCLC
18834711
.
- ↑
Martin W.C.; Wiese, W.L..
?Atomic Spectroscopy: A Compendium of Basic Ideas, Notation, Data, and Formulas”
. National Institute of Standards and Technology. Arhivirano iz
originala
na datum 8. 2. 2007
. Pristupljeno 8. 1. 2007
.
- ↑
?Atomic Emission Spectra ? Origin of Spectral Lines”
. Avogadro Web Site. Arhivirano iz
originala
na datum 28. 2. 2006
. Pristupljeno 10. 8. 2006
.
- ↑
Fitzpatrick Richard.
?Fine structure”
. University of Texas at Austin
. Pristupljeno 14. 2. 2008
.
- ↑
Weiss Michael (2001).
?The Zeeman Effect”
. University of California-Riverside. Arhivirano iz
originala
na datum 2. 2. 2008
. Pristupljeno 6. 2. 2008
.
- ↑
Beyer H.F.; Shevelko V.P. (2003).
Introduction to the Physics of Highly Charged Ions
. CRC Press. str. 232?236.
ISBN
978-0-7503-0481-8
.
OCLC
47150433
.
- ↑
Watkins Thayer.
?Coherence in Stimulated Emission”
. San Jose State University. Arhivirano iz
originala
na datum 12. 1. 2008
. Pristupljeno 23. 12. 2007
.
- ↑
Reusch William.
?Virtual Textbook of Organic Chemistry”
. Michigan State University. Arhivirano iz
originala
na datum 29. 10. 2007
. Pristupljeno 11. 1. 2008
.
- ↑
?Covalent bonding ? Single bonds”
. chemguide. 2000.
- ↑
Husted Robert.
?Periodic Table of the Elements”
. Nacionalna laboratorija Los Alamos. Arhivirano iz
originala
na datum 10. 1. 2008
. Pristupljeno 11. 1. 2008
.
- ↑
Rudy Baum (2003).
?It's Elemental: The Periodic Table”
.
Chemical & Engineering News
.
- ↑
Goodstein David L. (2002).
States of Matter
. Courier Dover Publications. str. 436?438.
ISBN
978-0-13-843557-8
.
- ↑
Brazhkin Vadim V. (2006). ?Metastable phases, phase transformations, and phase diagrams in physics and chemistry”.
Physics-Uspekhi
49
(7): 719?724.
Bibcode
2006PhyU...49..719B
.
DOI
:
10.1070/PU2006v049n07ABEH006013
.
- ↑
Myers Richard (2003).
The Basics of Chemistry
. Greenwood Press. str.
85
.
ISBN
978-0-313-31664-7
.
OCLC
50164580
.
- ↑
urednici.
?Bose-Einstein Condensate: A New Form of Matter”
. National Institute of Standards and Technology. Arhivirano iz
originala
na datum 3. 1. 2008.
- ↑
Colton Imogen; Fyffe, Jeanette.
?Super Atoms from Bose-Einstein Condensation”
. Univerzitet Melbournea. Arhivirano iz
originala
na datum 29. 8. 2007
. Pristupljeno 6. 2. 2008
.
- ↑
Jacox Marilyn; Gadzuk, J. William.
?Scanning Tunneling Microscope”
. Nacionalni institut za standarde i tehnologiju SAD. Arhivirano iz
originala
na datum 7. 1. 2008
. Pristupljeno 11. 1. 2008
.
- ↑
?The Nobel Prize in Physics 1986”
. Nobelova fondacija
. Pristupljeno 11. 1. 2008
.
- ↑
N. Jakubowski; Moens Luc; Vanhaecke Frank (1998). ?Sector field mass spectrometers in ICP-MS”.
Spectrochimica Acta Part B: Atomic Spectroscopy
53
(13): 1739?1763.
Bibcode
1998AcSpe..53.1739J
.
DOI
:
10.1016/S0584-8547(98)00222-5
.
- ↑
Muller Erwin W.; Panitz John A.; McLane S. Brooks (1968). ?The Atom-Probe Field Ion Microscope”.
Review of Scientific Instruments
39
(1): 83?86.
Bibcode
1968RScI...39...83M
.
DOI
:
10.1063/1.1683116
.
- ↑
Lochner Jim; Gibb, Meredith; Newman, Phil.
?What Do Spectra Tell Us?”
. NASA/Goddard svemirski centar. Arhivirano iz
originala
na datum 16. 1. 2008
. Pristupljeno 3. 1. 2008
.
- ↑
Winter Mark (2007).
?Helium”
. WebElements. Arhivirano iz
originala
na datum 30. 12. 2007
. Pristupljeno 3. 1. 2008
.
- ↑
Hinshaw Gary.
?What is the Universe Made Of?”
. NASA/WMAP. Arhivirano iz
originala
na datum 31. 12. 2007
. Pristupljeno 7. 1. 2008
.
- ↑
Choppin Gregory R.; Liljenzin Jan-Olov; Rydberg Jan (2001).
Radiochemistry and Nuclear Chemistry
. Elsevier. str. 441.
ISBN
978-0-7506-7463-8
.
OCLC
162592180
.
- ↑
Davidsen Arthur F. (1993). ?Far-Ultraviolet Astronomy on the Astro-1 Space Shuttle Mission”.
Science
259
(5093): 327?334.
Bibcode
1993Sci...259..327D
.
DOI
:
10.1126/science.259.5093.327
.
PMID
17832344
.
- ↑
Lequeux James (2005).
The Interstellar Medium
. Springer. str.
4
.
ISBN
978-3-540-21326-0
.
OCLC
133157789
.
- ↑
Nigel Smith.
?The search for dark matter”
. Physics World. Arhivirano iz
originala
na datum 16. 2. 2008
. Pristupljeno 14. 2. 2008
.
- ↑
Croswell Ken (1991).
?Boron, bumps and the Big Bang: Was matter spread evenly when the Universe began? Perhaps not; the clues lie in the creation of the lighter elements such as boron and beryllium”
.
New Scientist
(1794): 42. Arhivirano iz
originala
na datum 7. 2. 2008.
- ↑
Copi Craig J.; Schramm DN; Turner MS (1995).
?Big-Bang Nucleosynthesis and the Baryon Density of the Universe”
.
Science
267
(5195): 192?199.
arXiv
:
astro-ph/9407006
.
Bibcode
1995Sci...267..192C
.
DOI
:
10.1126/science.7809624
.
PMID
7809624
.
- ↑
Hinshaw Gary.
?Tests of the Big Bang: The Light Elements”
. NASA/WMAP. Arhivirano iz
originala
na datum 17. 1. 2008
. Pristupljeno 13. 1. 2008
.
- ↑
Abbott Brian.
?Microwave (WMAP) All-Sky Survey”
. Hayden Planetarium. Arhivirano iz
originala
na datum 13. 2. 2013
. Pristupljeno 13. 1. 2008
.
- ↑
F. Hoyle (1946). ?The synthesis of the elements from hydrogen”.
Monthly Notices of the Royal Astronomical Society
106
(5): 343?383.
Bibcode
1946MNRAS.106..343H
.
DOI
:
10.1093/mnras/106.5.343
.
- ↑
Knauth D.C.; Lambert David L.; Crane P. (2000). ?Newly synthesized lithium in the interstellar medium”.
Nature
405
(6787): 656?658.
Bibcode
2000Natur.405..656K
.
DOI
:
10.1038/35015028
.
PMID
10864316
.
- ↑
Mashnik Stepan G. (2000). ?On Solar System and Cosmic Rays Nucleosynthesis and Spallation Processes”.
MISSING LINK.
.
- ↑
Geolo?ki zavod Kansasa.
?Age of the Earth”
. Univerzitet Kansasa. Arhivirano iz
originala
na datum 2008-07-05
. Pristupljeno 2020-08-22
.
- ↑
Dalrymple G. Brent (2001).
?The age of the Earth in the twentieth century: a problem (mostly) solved”
.
Geological Society, London, Special Publications
190
(1): 205?221.
Bibcode
2001GSLSP.190..205D
.
DOI
:
10.1144/GSL.SP.2001.190.01.14
.
- ↑
Anderson Don L.; Foulger, G.R.; Meibom, Anders.
?Helium: Fundamental models”
. MantlePlumes.org. Arhivirano iz
originala
na datum 8. 2. 2007
. Pristupljeno 14. 1. 2007
.
- ↑
Pennicott Katie.
?Carbon clock could show the wrong time”
. PhysicsWeb. Arhivirano iz
originala
na datum 15. 12. 2007.
- ↑
Yarris Lynn.
?New Superheavy Elements 118 and 116 Discovered at Berkeley Lab”
. Berkeley Lab. Arhivirano iz
originala
na datum 9. 1. 2008.
- ↑
Diamond, H (1960). ?Heavy Isotope Abundances in Mike Thermonuclear Device”.
Physical Review
119
(6): 2000?2004.
Bibcode
1960PhRv..119.2000D
.
DOI
:
10.1103/PhysRev.119.2000
.
- ↑
Poston Sr.; John W..
?Do transuranic elements such as plutonium ever occur naturally?”
.
Scientific American
.
- ↑
Keller C (1973). ?Natural occurrence of lanthanides, actinides, and superheavy elements”.
Chemiker Zeitung
97
(10): 522?530.
OSTI
4353086
.
- ↑
Zaider Marco; Rossi Harald H. (2001).
Radiation Science for Physicians and Public Health Workers
. Springer. str.
17
.
ISBN
978-0-306-46403-4
.
OCLC
44110319
.
- ↑
?Oklo Fossil Reactors”
. Curtin University of Technology. Arhivirano iz
originala
na datum 18. 12. 2007
. Pristupljeno 15. 1. 2008
.
- ↑
Weisenberger Drew.
?How many atoms are there in the world?”
. Jefferson Lab
. Pristupljeno 16. 1. 2008
.
- ↑
Pidwirny Michael.
?Fundamentals of Physical Geography”
. University of British Columbia Okanagan. Arhivirano iz
originala
na datum 21. 1. 2008
. Pristupljeno 16. 1. 2008
.
- ↑
Anderson Don L. (2002).
?The inner inner core of Earth”
.
Proceedings of the National Academy of Sciences
99
(22): 13966?13968.
Bibcode
2002PNAS...9913966A
.
DOI
:
10.1073/pnas.232565899
.
PMC
137819
.
PMID
12391308
.
- ↑
Pauling Linus (1960).
The Nature of the Chemical Bond
. Cornell University Press. str.
5
?10.
ISBN
978-0-8014-0333-0
.
OCLC
17518275
.
- ↑
anonimni autor.
?Second postcard from the island of stability”
.
CERN Courier
. Arhivirano iz
originala
na datum 3. 2. 2008.
- ↑
Jacoby Mitch (2006). ?As-yet-unsynthesized superheavy atom should form a stable diatomic molecule with fluorine”.
Chemical & Engineering News
84
(10): 19.
DOI
:
10.1021/cen-v084n010.p019a
.
- ↑
Koppes Steve.
?Fermilab Physicists Find New Matter-Antimatter Asymmetry”
. Univerzitet u Chicagu.
- ↑
Cromie William J..
?A lifetime of trillionths of a second: Scientists explore antimatter”
. Glasilo Univerziteta Harvard
. Pristupljeno 14. 1. 2008
.
- ↑
Hijmans Tom W. (2002). ?Particle physics: Cold antihydrogen”.
Nature
419
(6906): 439?440.
Bibcode
2002Natur.419..439H
.
DOI
:
10.1038/419439a
.
PMID
12368837
.
- ↑
urednici.
?Researchers 'look inside' antimatter”
.
BBC News
.
- ↑
Barrett Roger (1990).
?The Strange World of the Exotic Atom”
.
New Scientist
(1728): 77?115. Arhivirano iz
originala
na datum 21. 12. 2007.
- ↑
Indelicato Paul (2004).
?Exotic Atoms”
.
Physica Scripta
T112
(1): 20?26.
arXiv
:
physics/0409058
.
Bibcode
2004PhST..112...20I
.
DOI
:
10.1238/Physica.Topical.112a00020
.
- ↑
Ripin Barrett H..
?Recent Experiments on Exotic Atoms”
. Ameri?ko fizi?ko dru?tvo. Arhivirano iz
originala
na datum 23. 7. 2012
. Pristupljeno 15. 2. 2008
.