 Молекула метана CH
4
Молекула метана CH
4
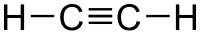 Молекула ацетилена C
2
H
2
Молекула ацетилена C
2
H
2
Валентность
(од лат. ?аlепt?а ? сила) ? способность
атомох
творити хемичны вязбы. Понятя валентность е днесь застар?ле и не може быти хосноване про каждый припад хемичных вязб. Валентность атома
гидрогена
ровна 1. Валентность иншого атома може быти означена, як число атомох
гидрогена
, котры може тот атом звязати. Наприм?р зо штруктуры молекул
метана
и
ацетилена
видиме, же валентность атома
карбона
ровна 4.
Валентность мож дефиновати як способность атома оддавати або привязовати даяке число
електронох
. Валентность позитивна, кедь
атом
оддавать
електроны
, або негативна, кедь
атом
их приимать.
[1]
Повный образ штруктуры
молекул
розличных класох и хемичных вязб е крайн? компликованый и вецефайтовый, зато единой и всеобсяжной дефиниции валентности н?т. Авшак во векшин? припадох мож ся ограничити на розбор двох типох валентности:
ковалентность
и
йонова валентность
(посл?дна еще бывать называна таксамо електровалентностьов або гетеровалентностьов).
Ковалентность
ровна числу ковалентных вязб, утвореных даным
атомом
, циже вязб, взниклых зосполочн?ньом пар
електронох
(при простой вязб? то една пара, при двоитой вязб? ? дв? пары и т.п.). Чисто
ковалентна вязба
реализуе ся лем в гомеополарных молекулах (з еднакыма
атомами
), такых як H
2
, O
2
, N
2
и т.п.
[2]
Ковалентна вязба
все реализуе ся межи
атомами
неметалох
.
Йонова валентность дефинуе ся числом
електронох
, котре даный
атом
оддав або достав при утвор?ню
йоновой вязбы
.
Йонова вязба
реализуе ся межи
атомами
металох
и
атомами
неметалох
В гетерополарных молекулах (з нееднакыма
атомами
) хемична вязба реализуе ся комбинациов йоновой и ковалентной вязбы.
[2]
- Прохоров А.М. (гл. ред.). Физическая энциклопедия. Научное издательство "Большая Российская энциклопедия". М. 1998.
- ↑
Прохоров А.М. (гл. ред.). Физическая энциклопедия, т. 1, с. 238.
- ↑
2,0
2,1
Прохоров А.М. (гл. ред.). Физическая энциклопедия, т. 2, с. 389.