 Метан
, CH
4
Метан
, CH
4
Органи?ческая хи?мия
? раздел
химии
, изучающий структуру, свойства и методы
синтеза
соединений
углерода
с другими химическими элементами, относящихся к
органическим соединениям
[1]
[2]
. Первоначальное значение термина органическая химия подразумевало изучение только соединений
углерода
растительного и животного происхождения. По этой причине ряд углеродсодержащих соединений традиционно не относят к
органическим
(например,
монооксид углерода
,
диоксид углерода
,
циановодород
,
сероуглерод
,
карбонилы металлов
), а рассматривают как
неорганические соединения
. Условно можно считать, что структурным прототипом
органических соединений
являются
углеводороды
[2]
.
Наибольшее количество соединений углерод образует с так называемыми
элементами-
органогенами
:
H
,
N
,
O
,
S
,
P
[3]
. Способность углерода соединяться с большинством элементов и образовывать молекулы различного состава и строения обусловливает многообразие органических соединений. Органические соединения (например,
нуклеотиды
,
природные аминокислоты
,
углеводы
) играют ключевую роль в существовании живых организмов.
Предмет органической химии включает следующие цели, экспериментальные методы и теоретические представления:
- Выделение индивидуальных веществ из растительного, животного или ископаемого сырья
- Синтез и очистка соединений
- Определение структуры веществ
- Изучение механизмов химических реакций
- Выявление зависимостей между структурой органических веществ и их свойствами
Количество известных органических соединений
[
править
|
править код
]
24 мая 1999 года число известных химических соединений превышало 25 млн, из них 12 млн были органическими
[4]
, ко 2 мая 2014 года общее число известных неорганических и органических соединений превысило 87 млн
[5]
. На 8 апреля 2018 года в реестре
Химической реферативной службы США (CAS)
зарегистрирован 141 млн химических веществ
[6]
.

 Полный синтез
витамина B
12
являлся крупным достижением органической химии.
Полный синтез
витамина B
12
являлся крупным достижением органической химии.
 Пример металлоорганической молекулы, катализатора, называемого
катализатором Граббса
. Его формула часто приводится как RuCl
2
(PCy
3
)
2
(=CHPh), где шарообразная модель основана на
рентгеновской кристаллографии
.
[7]
Пример металлоорганической молекулы, катализатора, называемого
катализатором Граббса
. Его формула часто приводится как RuCl
2
(PCy
3
)
2
(=CHPh), где шарообразная модель основана на
рентгеновской кристаллографии
.
[7]
Способы получения различных
органических веществ
были известны ещё в древности.
Египтяне
и
римляне
использовали красители
индиго
и
ализарин
, содержащиеся в растительных веществах. Многие народы знали секреты производства спиртных напитков и
уксуса
из сахара и крахмалсодержащего сырья.
Во времена
Средневековья
к этим знаниям ничего не прибавилось, некоторый прогресс начался только в XVI?XVII веках: были получены некоторые вещества, в основном путём перегонки определённых растительных продуктов. Большое экономическое значение имело обнаружение
Андреасом Маргграфом
сахара
в
свёкле
[8]
:6
(в дополнение к известному в то время его источнику ?
сахарному тростнику
), о чём он сообщил в статье ≪Химические попытки извлекать настоящий сахар из растений нашей страны≫ в
1747 году
[9]
. В 1769?1785 годах
Шееле
выделил несколько органических
кислот
, среди них
яблочная
,
винная
,
лимонная
,
галловая
,
молочная
и
щавелевая
. В
1773
году
Руэль
выделил из человеческой мочи
мочевину
.
Выделенные из животного или растительного сырья продукты имели между собой много общего, но отличались от
неорганических соединений
. При этом полагали, что эти вещества могут быть получены только в живых организмах благодаря ≪жизненной силе≫. Так, в 1753 году известный шведский естествоиспытатель
Юхан Валлериус
в предисловии к сборнику работ другого видного шведского учёного,
Урабана Йерне
, утверждал
[10]
: ≪…ни животные, ни растительные тела, ни их части не могут быть воспроизведены поэтому химическим искусством≫
[8]
:7
. В первом томе своей книги ≪Лекции по животной химии≫ (≪Forelasningar i Djurkemien≫), вышедшем в
1806 году
,
Якоб Берцелиус
впервые вводит понятие ≪органическая химия≫ (
швед.
organisk Kemi
), определяя её как ≪часть физиологии, которая описывает состав живых тел вместе с химическими процессами, происходящими в них≫
[11]
.
Представление о ≪жизненной силе≫ было поколеблено синтезом образующихся в живых организмах веществ из неорганических, проведённым в первой половине XIX века
[8]
:15-16
, так, в
1824 году
Фридрих Вёлер
впервые получил органическое вещество ?
щавелевую кислоту
, а в
1824 году
он провел синтез ещё одного органического соединения
мочевины
в результате упаривания водного
раствора
цианата аммония
(NH
4
OCN).
Важными этапами развития теоретической органической химии стали теория
валентности
, разработанная
Арчибальдом Купером
и
Фридрихом Кекуле
в
1857
году, а также
теории химического строения
, предложенная в
1861
году
Александром Бутлеровым
. В основу этих теорий были положены четырёхвалентность углерода и его способность к образованию цепей. В первом томе своего труда по органической химии, вышедшем в
1859 году
,
Кекуле
впервые вводит близкое к современному определение понятия ≪органическая химия≫ ? это ≪химия соединений углерода≫
[12]
, что отражено уже в самом названии этого труда, которое переводится как ≪Учебник органической химии, или химии углеродистых соединений≫. В 1850-х годах профессор Московского университета
Николай Лясковский
выразил мнение, что ≪органическая химия не есть химия веществ, встречаемых в организмах, а химия соединений углерода≫, которое впоследствии сделалось господствующим в науке воззрением
[13]
. В
1865 году
Кекуле предложил
структурную формулу
бензола
, что стало одним из важнейших открытий в органической химии. В
1875
г.
Вант-Гофф
и
Ле Бель
предложили
тетраэдрическую
модель
атома
углерода
, по которой связи атомов углерода направлены к вершинам
тетраэдра
, если атом углерода поместить в центр этого тетраэдра. В
1917 году
Льюис
предложил рассматривать
химическую связь
с помощью
электронных пар
.
В
1931
г.
Хюккель
применил
квантовую теорию
для объяснения свойств альтернативных
ароматических углеродов
, чем основал новое направление в органической химии ? квантовую химию. В
1933
г.
Ингольд
провёл изучение кинетики реакции замещения у насыщенного атома углерода, что привело к масштабному изучению кинетики большинства типов органических реакций.
На заре органической химии предметом изучения были преимущественно субстанции
биологического
происхождения, которым органическая химия обязана своим названием. Научно-технический прогресс не стоял на месте, и в конце XIX века основной материальной базой органической химии стала
каменноугольная смола
, выделяемая при получении
кокса
прокаливанием
каменного угля
. Именно на основе переработки каменноугольной смолы возник
основной органический синтез
и связанная с ним
химическая технология
. В 50?60 годах XX века произошёл переход основного органического синтеза на новую материальную базу ?
нефть
. Таким образом, появилась новая область химии ?
нефтехимия
, которая вызвала бум в органической химии и определила интенсивное развитие новой области ? химии полимеров.
Классификация органических соединений
[
править
|
править код
]
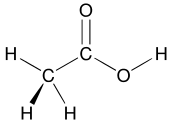 Уксусная кислота
. Семейство
карбоновых кислот
содержит карбоксильную (-COOH)
функциональную группу
.
Уксусная кислота
. Семейство
карбоновых кислот
содержит карбоксильную (-COOH)
функциональную группу
.
Правила и особенности классификации
[
править
|
править код
]
В основе классификации лежит структура органических соединений. Основа описания структуры ?
структурная формула
. Атомы элементов обозначаются латинскими символами, как они обозначены в
периодической таблице химических элементов
(
таблице Менделеева
).
Водородные
и
электронодефицитные связи
обозначаются пунктирной линией,
ионные связи
обозначаются указанием
зарядов
частиц, входящих в состав молекулы. Поскольку в подавляющее большинство органических молекул входит
водород
, его обычно не обозначают при изображении структуры. Таким образом, если в структуре у одного из атомов изображена недостаточная
валентность
, значит, возле этого атома расположен один или несколько атомов водорода.
Атомы могут образовывать циклические и ароматические системы.
Основные классы органических соединений
[
править
|
править код
]
 Бензол
? одно из самых простых и стабильных ароматических соединений.
Бензол
? одно из самых простых и стабильных ароматических соединений.
- Соединения с
гетероатомами
в функциональных группах ? соединения, в которых
углеводородный радикал
R связан с функциональной группой. По характеру функциональных групп делятся на:
- Галогенсодержащие.
- Спирты
,
фенолы
.
Спирты?
(устар.
алкого?ли
,
англ.
alcohols
; от
лат.
spiritus
? дух) ?
органические соединения
, содержащие одну или более
гидроксильных групп
(гидроксил,
?
O
H
), непосредственно связанных с насыщенным (находящемся в состоянии
sp³ гибридизации
) атомом
углерода
[14]
. Спирты можно рассматривать как производные
воды (
H?O?H
)
, в которых один
атом
водорода
замещён на органическую
функциональную группу
:
R?O?H
. В номенклатуре IUPAC для соединений, в которых гидроксильная группа связана с ненасыщенным (находящемся в состоянии
sp
2
гибридизации
атомом углерода, рекомендуются названия ≪
енолы
≫ (гидроксил связан с винильной C=C связью)
[15]
и ≪
фенолы
≫ (гидроксил связан с
бензольным
или другим ароматическим циклом)
[16]
.
- Соединения, содержащие карбоксильную группу (
карбоновые кислоты
,
сложные эфиры
):
- Сложные эфиры
(
эстеры
)
? производные оксокислот (как
карбоновых
так и минеральных) R
k
E(=O)
l
(OH)
m
, (l ≠ 0), формально являющиеся продуктами замещения атомов водорода
гидроксилов
?OH кислотной функции на углеводородный радикал (алифатический, ароматический или гетероароматический); также могут рассматриваться как ацилпроизводные
спиртов
. В номенклатуре IUPAC к сложным эфирам относят также ацилпроизводные
халькогенидных
аналогов спиртов (
тиолов
, селенолов и теллуролов)
[17]
.
- Соединения, содержащие карбонильную группу
- Альдегиды
(от
лат.
al
cohol
dehyd
rogenatum
?
спирт
,
лишённый водорода
) ? класс
органических соединений
, содержащих альдегидную группу (?СН=О), связанную с углеводородным радикалом. Общая формула альдегидов: R?СН=О
- Кетоны
? это органические вещества, в молекулах которых
карбонильная группа
(С=О) связана с двумя углеводородными радикалами. Общая формула кетонов: R
1
?CO?R
2
. Наличие в кетонах именно двух атомов углерода, непосредственно связанных с карбонильной группой, отличает их от
карбоновых кислот
и их производных, а также
альдегидов
.
- Хиноны
? полностью сопряжённые циклогексадиеноны и их аннулированные аналоги. Существуют два класса хинонов: пара-хиноны с пара-расположением карбонильных групп (1,4-хиноны) и орто-хиноны с орто-расположением карбонильных групп (1,2-хиноны).
- Серосодержащие соединения
- Азотсодержащие соединения
- Металлоорганические соединения
- Гетероциклические
? содержат гетероатомы в составе кольца. Различаются по числу атомов в цикле, по виду гетероатома, по количеству гетероатомов в цикле.
 Доска для плавания изготовлена ??из
полистирола
? одного из полимеров.
Доска для плавания изготовлена ??из
полистирола
? одного из полимеров.
- Полимеры
? вещества, которые состоят из периодически повторяющихся фрагментов ? мономерных звеньев, зачастую имеют большую молекулярную массу.
Строение органических молекул
[
править
|
править код
]
 Различные названия и изображения одного органического соединения.
Различные названия и изображения одного органического соединения.
Органические молекулы, в основном, образованы
ковалентными
неполярными связями C?C, или ковалентными полярными типа C?O, C?N, C?Hal. Согласно
октетной теории
Льюиса
и
Косселя
молекула является устойчивой, если внешние
орбитали
всех атомов полностью заполнены. Для таких элементов как
C
,
N
,
O
,
галогены
необходимо 8 электронов, чтобы заполнить внешние
валентные орбитали
, для
водорода
необходимо только 2 электрона.
Полярность
объясняется смещением электронной плотности в сторону более
электроотрицательного
атома.
Классическая
теория валентных связей
не в состоянии объяснить все типы связей, существующие в органических соединениях, поэтому современная теория использует
методы молекулярных орбиталей
и квантово-химические методы.
Строение органического вещества
[
править
|
править код
]
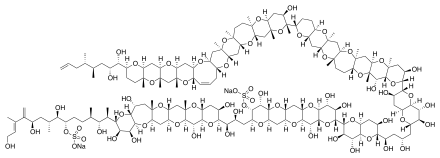
Майтотоксин
, сложный органический биологический токсин.
 Молекулярные модели
кофеина
.
Молекулярные модели
кофеина
.
 Синтез
осельтамивира
(Тамифлю), разработанного
Э. Дж. Кори
. Этот синтез включает 11 различных реакций.
Синтез
осельтамивира
(Тамифлю), разработанного
Э. Дж. Кори
. Этот синтез включает 11 различных реакций.
Свойства органических веществ определяются не только строением их молекул, но и числом и характером их взаимодействий с соседними молекулами, а также взаимным пространственным расположением. Наиболее ярко эти факторы проявляются в различии свойств веществ, находящихся в разных агрегатных состояниях. Так, вещества, легко взаимодействующие в виде газа, могут совершенно не реагировать в твёрдом состоянии, или их реакция может приводить к другим продуктам.
В твёрдых органических веществах, в которых наиболее ярко проявляются эти факторы, различают органические кристаллы и аморфные тела. Их описанием занимается наука ≪
химия органического твёрдого тела
≫, основание которой связывают с именем советского физика-кристаллографа
А. И. Китайгородского
. Примеры полезных органических твёрдых тел ? органические люминофоры, разнообразные полимеры, сенсоры, катализаторы, электропроводки, магниты и другие.
Особенности органических реакций
[
править
|
править код
]
В
неорганических реакциях
обычно участвуют
ионы
, они проходят быстро и до конца при комнатной температуре. В
органических реакциях
часто происходят разрывы
ковалентных связей
с образованием новых. Как правило, эти процессы требуют особых условий: определённой температуры, времени реакции и часто наличия
катализатора
. Обычно протекает не одна, а сразу несколько реакций, поэтому
выход
целевого вещества зачастую не превышает 50 %. Поэтому, зачастую, при изображении органических реакций используют не уравнения, а схемы без расчёта
стехиометрии
.
Реакции могут протекать очень сложным образом и в несколько стадий. В качестве промежуточных соединений могут возникать
карбкатионы
R
+
,
карбанионы
R
?
,
радикалы
R·,
карбены
:CX
2
,
катион-радикалы
,
анион-радикалы
и другие активные или нестабильные короткоживущие частицы. Подробное описание всех превращений, происходящих на молекулярном уровне во время реакции, называется
механизмом реакции
.
Реакции классифицируются в зависимости от способов разрыва и образования связей и их
молекулярности
.
Определение состава и строения органических соединений
[
править
|
править код
]
Важнейшей задачей органической химии является установление состава и строения (порядка связывания атомов между собой и их расположения в пространстве) органических соединений.
Существует несколько методов решения этих задач:
- Элементный анализ
. Заключается в том, что вещество разлагается на более простые молекулы, по количеству которых можно определить количество атомов, входящее в состав соединения. Используют для установления элементного состава соединений.
- Инфракрасная спектроскопия
и
спектроскопия комбинационного рассеяния
(ИК-спектроскопия и КР-спектроскопия). Вещество взаимодействует с электромагнитным излучением (
светом
) инфракрасного диапазона (в ИК-спектроскопии наблюдают поглощение, в КР-спектроскопии ? рассеяние излучения). Это излучение при поглощении возбуждает колебательные и вращательные электронные уровни молекул. Опорными данными являются число, частота и интенсивность колебаний молекулы, связанные с изменением дипольного момента (ИК-спектроскопия) или поляризуемости (КР-спектроскопия). Методы позволяют установить наличие определённых функциональных групп в молекуле. Часто используются для того чтобы подтвердить идентичность исследуемого вещества, путем сравнения спектра исследуемого вещества со спектром уже известного вещества.
- Масс-спектроскопия
. Вещество при определённых условиях (электронный удар, химическая ионизация и др.) превращают в
ионы
без потери атомов (молекулярные ионы) и с их потерей (осколочные). Позволяет определить
молекулярную массу
молекул и иногда позволяет установить наличие различных
функциональных групп
.
- Метод ядерного магнитного резонанса
(
ЯМР
). Основан на взаимодействии ядер, обладающих собственным магнитным моментом (спином) и помещённых во внешнее постоянное магнитное поле, с электромагнитным излучением радиочастотного диапазона. Один из главных методов, который может быть использован для определения химической структуры. Метод используют также для изучения пространственного строения молекул, динамики молекул, механизмов реакций. В зависимости от ядер, взаимодействующих с излучением, различают, например:
- Использование комбинации этих методов ЯМР позволяет комплексно решать задачу установления структуры органических соединений
- ↑
Органическая химия
Архивная копия
от 28 сентября 2015 на
Wayback Machine
.
БСЭ
.
- ↑
1
2
Органическая химия //
Химическая энциклопедия
:
[
рус.
]
: [
арх.
6 октября 2021
] :
в 5 т.
/ под ред. И. Л. Кнунянца. ?
М.
: Большая Российская энциклопедия, 1992. ? Т. 3. ? С. 396?399. ? 639 с. ?
ISBN 5-85270-039-8
.
- ↑
Предмет органической химии. Исторический обзор
// Начала органической химии. ?
М.
: Химия, 1970. ? Т. 1. ? С. 11?26. ? 664 с. ?
19 000 экз.
- ↑
Greenberg A.
From Alchemy to Chemistry in Picture and Story
(англ.)
. ?
John Wiley & Sons
, 2006. ? P. 422.
- ↑
American Chemical Society.
CAS REGISTRY and CAS Registry Number FAQs
(англ.)
. Дата обращения: 2 мая 2014.
Архивировано
12 апреля 2016 года.
- ↑
CAS REGISTRY
(англ.)
.
CAS
. Дата обращения: 24 мая 2023.
Архивировано
30 июля 2023 года.
- ↑
Torker, Sebastian; MuLler, Andre; Sigrist, Raphael; Chen, Peter (2010). "Tuning the Steric Properties of a Metathesis Catalyst for Copolymerization of Norbornene and Cyclooctene toward Complete Alternation".
Organometallics
.
29
(12): 2735?2751.
doi
:
10.1021/om100185g
.
- ↑
1
2
3
Быков Г.В.
Возникновение органической химии как науки // Книга для чтения по органической химии. Пособие для учащихся. ?
М.
:
Просвещение
, 1975. ?
С. 5?19
.
- ↑
Marggraf A.
Experiences chimiques faites dans le dessein de tirer un veritable sucre de diverses plantes, qui croissent dans nos contrees
(фр.)
// Histoire de l'academie royale des sciences et belles-lettres de Berlin. Annee MDCCXLVII : magazine. ? 1749. ?
P. 79?90
.
- ↑
Urbani Hierne.
Tentaminum Chemicorum in Reg. Laboratorio Holmiensi peractorum, tomus secundus, nunc primum in lucem editorum cum annotationibus Joh. Gotschalk Wallerii. Praefatio
(неопр.)
. ? Stockholmiae, 1753. ? С. VIII.
- ↑
Berzelius J.J.
Forelasningar i Djurkemien
(неопр.)
. ? Stockholm, 1806. ? Т. 1. ? С. 6.
- ↑
Издание 1861 года доступно в интернете, см. в нём:
Kekule A.
Lehrbuch der organischen Chemie oder der Chemie der Kohlenstoffverbindungen
(нем.)
. ? 1861. ? Bd. 1. ? S. 11.
- ↑
В. Н. Лясковский.
Николай Эрастович Лясковский
(неопр.)
. ? М.: Университетская типография (М. Катков), 1884. ? С. 40.
Архивировано
21 января 2022 года.
- ↑
Alcohols
(англ.)
. IUPAC. Compendium of Chemical Terminology, 2nd ed. (the "Gold Book").
doi
:
10.1351/goldbook.A00204
. Дата обращения: 2 сентября 2010.
Архивировано
21 августа 2011 года.
- ↑
Enols
(англ.)
. IUPAC. Compendium of Chemical Terminology, 2nd ed. (the ≪Gold Book≫).
doi
:
10.1351/goldbook.E02124
. Дата обращения: 2 сентября 2010.
Архивировано
21 августа 2011 года.
- ↑
Phenols
(англ.)
. IUPAC. Compendium of Chemical Terminology, 2nd ed. (the ≪Gold Book≫).
doi
:
10.1351/goldbook.P04539
. Дата обращения: 2 сентября 2010.
Архивировано
21 августа 2011 года.
- ↑
esters // IUPAG Gold Book
(неопр.)
. Дата обращения: 11 апреля 2012.
Архивировано
19 апреля 2012 года.
- Быков Г. В. История органической химии. М.: Химия, 1976. 360 с.
- Гауптман З., Грефе Ю., Ремане Х., ≪Органическая химия≫. Москва, ≪Химия≫, 1979.
- Марч Дж., ≪Органическая химия: реакции, механизмы и структура≫, в 4-х томах. Москва, ≪Мир≫, 1987.
- Кери Ф., Сандберг Р., ≪Углубленный курс органической химии≫, в 2-х томах. Москва, ≪Химия≫, 1981.
- Реутов О. А., Курц А. Л., Бутин К. П. ≪Органическая химия≫, в 4-х частях. Москва, Изд-во МГУ, ≪БИНОМ. Лаборатория знаний≫, 1999?2004.
http://edu.prometey.org/library/autor/7883.html
Архивная копия
от 14 декабря 2017 на
Wayback Machine
- Травень В. Ф. ≪Органическая химия≫, в 2-х томах. Москва, ИКЦ ≪Академкнига≫, 2004.
- Химическая энциклопедия
, п. ред. Кнунянц, т. 3. Москва, ≪Большая Российская Энциклопедия≫, 1992.
- Робертс Дж., Касерио М. , ≪Основы органической химии≫. Изд. 2, в 2-х томах. Москва, ≪Мир≫, 1978.
- Моррисон Р., Бойд Р., ≪Органическая химия≫. Москва, ≪Мир≫, 1974.
- Clayden J., Greeves N., Warren S., Wothers P. Organic Chemistry. ? Oxford University Press, 2012.
 Ссылки на внешние ресурсы
|
|---|
| |
|---|
В библиографических каталогах
|
|---|
|
|