Моло?чная кислота?
(
химическая формула
?
C
3
H
6
O
3
) ?
cлабая
химическая
органическая кислота
, относящаяся к классу предельных
карбоновых кислот
.
При
стандартных условиях
молочная кислота
? это одноосновная
карбоновая
оксикислота
белого цвета с характерным запахом. Соли и эфиры молочной кислоты называются
лактатами
.
Малотоннажная химия производит молочную кислоту 4 сортов: химически чистую, ≪фармакопейную≫, ≪техническую≫ и ≪пищевую≫.
Молочную кислоту открыл
шведский
химик
Карл Шееле
. В
1780 году
он выделил её из прокисшего молока в виде коричневого сиропа. Французский химик
Анри Браконно
обнаружил, что она образуется при
молочнокислом брожении
[1]
.
В 1807 году
Йенс Якоб Берцелиус
выделил из мышц цинковую соль молочной кислоты.
Производство молочной кислоты в Советском Союзе было организовано в 1930 году на основе работ
Сергея Павловича Костычева
и
Владимира Степановича Буткевича
[2]
.
Молочная кислота является простейшей
хиральной
карбоновой кислотой и может существовать в виде двух
энантиомеров
: L-(+)-молочной кислоты, D-(?)-молочной кислоты или их
рацемической смеси
? DL-молочной кислоты. Если в смеси энантиомеров один находится в избытке, его можно выделить дробными
перекристаллизациями
из смеси
диэтилового эфира
и
диизопропилового эфира
[1]
. Чистые энантиомеры имеют температуру плавления 52,7?52,8 °С
[1]
.
 Энантиомеры молочной кислоты: L-(-)-молочная кислота (слева) и D-(+)-молочная кислота (справа)
Энантиомеры молочной кислоты: L-(-)-молочная кислота (слева) и D-(+)-молочная кислота (справа)
Молочная кислота очень
гигроскопична
и обычно существует в виде водного раствора с концентрацией до 90 мас. %. В связи с этим очень сложно установить её температуру плавления; литература приводит значения от 18 до 33 °С. Кроме того, в таких растворах присутствует значительное количество
лактоилмолочной кислоты
и других
олигомеров
молочной кислоты
[1]
.
Молочная кислота растворима в
воде
,
этаноле
и других органических растворителях, смешивающихся с водой, а также в диэтиловом эфире. Она практически нерастворима в
бензоле
и
хлороформе
[3]
.
При взаимодействии с окислителями молочная кислота разлагается. При окислении кислородом
воздуха
или
азотной кислотой
в присутствии
железа
или
меди
она превращается в
муравьиную кислоту
,
уксусную кислоту
,
щавелевую кислоту
,
уксусный альдегид
,
углекислый газ
и
пировиноградную кислоту
. Молочную кислоту можно восстановить до
пропионовой кислоты
действием
иодоводорода
[4]
Промышленный интерес представляет
дегидратация
молочной кислоты до
акриловой кислоты
и её восстановление до
пропиленгликоля
[5]
.
Поскольку молочная кислота является одновременно карбоновой кислотой и
спиртом
, она вступает в межмолекулярную
этерификацию
, давая лактоилмолочную кислоту. При дальнейшей конденсации образуется
лактид
? циклический
сложный эфир
. Также при конденсации могут образовываться линейные
полилактиды
. Эти соединения являются примесями в молочной кислоте. Так, в 6,5%-й молочной кислоте содержится около 0,2 % лактоилмолочной кислоты, 88%-я молочная кислота содержит меньше 60 % свободной молочной кислоты, а 100%-я ? только 32 %
[3]
.
В промышленности молочную кислоту получают либо ферментативным способом, либо синтетическим. Первый из них имеет преимущество, поскольку приводит к молочной кислоте с более высокой стереохимической чистотой, поэтому новые производства, открывавшиеся с 1995 года, пользуются этим способом
[5]
.
Для ферментативного производства молочной кислоты необходимо иметь
углеводное
сырьё, питательные вещества и соответствующие микроорганизмы. В качестве сырья используют
глюкозу
,
кукурузные
сиропы,
мелассу
, сок
сахарной свёклы
,
сыворотку
и
крахмал
. Питательными веществами являются
пептиды
и
аминокислоты
,
фосфаты
, соли
аммония
и
витамины
. Здесь находят применение
дрожжевой экстракт
,
кукурузный ликёр
[англ.]
,
кукурузная глютеновая мука
[англ.]
, солодовые ростки, соевый или мясной
пептон
. Молочную кислоту из углеводов вырабатывают культуры
Lactobacillus
,
Bacillus
и
Rhizopus
. Последняя из них является грибной и не требует сложных источников азота, хотя и даёт более низкий выход, чем бактериальные культуры
[5]
.
Во время процесса вырабатывается кислота, поэтому необходимо поддерживать
pH
в области 5,0?6,5: для этого используют
гидроксид кальция
,
карбонат кальция
,
аммиак
и
гидроксид натрия
. Из-за этого в процессе ферментации образуются соответствующие соли молочной кислоты. Разработка новых подходов к ферментации связана с выведением бактерий, способных работать в области низких pH: это позволило бы получать саму молочную кислоту, а не её соли, снизило бы затраты на подщелачивающие реагенты и на серную кислоту, используемую для выделения молочной кислоты из солей
[5]
.
После ферментации молочную кислоту подвергают очистке. Микроорганизмы отделяют
флокуляцией
в щелочной среде либо
ультрафильтрацией
. Образовавшиеся соли молочной кислоты переводят в саму кислоту под действием
серной кислоты
. При этом образуется также малополезный
сульфат кальция
. Ведётся поиск других методов очистки, при которых образование этой побочной соли не происходило бы. Для некоторых пищевых целей смесь пропускают через
активированный уголь
и
ионообменную
колонну
[6]
.
Для фармацевтической промышленности и получения полимеров необходима более глубокая очистка. Интерес представляет
экстракция
молочной кислоты в органическую фазу длинноцепными
третичными аминами
, а затем обратная экстракция в воду. Этот метод позволяет эффективно очистить продукт от остаточных углеводов и белков. Также возможна
перегонка
молочной кислоты, если предпринимаются меры против её
олигомеризации
[6]
.
Выход молочной кислоты в процессе ферментации составляет 85?95 %. Побочными продуктами являются
муравьиная
и
уксусная кислота
.
[5]
.
С 1960-х гг.
рацемическую
молочную кислоту производят в промышленности также синтетически. Подход основан на реакции
ацетальдегида
с
циановодородом
и последующем гидролизе образовавшегося
лактонитрила
. Недостатком синтетического подхода является то, что получаемая молочная кислота является рацемической, а подходящий и дешёвый
хиральный
катализатор пока не найден. Важнейшим крупным производителем синтетической молочной кислоты является фирма ≪Musashino≫
[6]
.

Годовая потребность в молочной кислоте составляет примерно 450 тыс. тонн. Крупнейшим производителем молочной кислоты является компания NatureWorks LLC: её завод, размещённый в штате
Небраска
(
США
), имеет приблизительную мощность 180 тыс. тонн в год. Это в 3?4 раза больше, чем у следующего завода по порядку. Рынок молочной кислоты очень чувствителен к потребности в
полилактиде
, поскольку его производство является либо вскоре станет крупнейшим направлением использования молочной кислоты
[7]
.
Молочная кислота формируется при анаэробном распаде
глюкозы
. Иногда называемая ≪кровяным сахаром≫ глюкоза является главным углеводом в нашем организме. Глюкоза ? это основной источник энергии для мозга и нервной системы, так же как и для мышц во время физической нагрузки. Когда расщепляется глюкоза, клетки производят
АТФ (аденозинтрифосфат)
, который обеспечивает энергией большинство химических реакций в организме. Уровень АТФ определяет, как быстро и как долго мышцы смогут сокращаться при физической нагрузке.
Производство молочной кислоты не требует присутствия кислорода, поэтому этот процесс её синтеза часто называют ≪анаэробным метаболизмом≫ (см.
Аэробная тренировка
). Ранее считалось, что мышцы производят молочную кислоту при нехватке кислорода в крови. Однако современные исследования показывают, что молочная кислота образуется и в мышцах, получающих достаточно кислорода. Увеличение количества молочной кислоты в кровотоке свидетельствует лишь о том, что уровень её поступления превышает уровень удаления
[8]
[9]
. Резкое увеличение (в 2?3 раза) уровня лактата в сыворотке крови наблюдается при тяжёлых расстройствах кровообращения, таких как геморрагический шок, острая левожелудочковая недостаточность и др., когда одновременно страдает и поступление кислорода в ткани, и печёночный кровоток.
Зависимое от лактата производство АТФ очень незначительно, но имеет большую скорость. Это обстоятельство делает идеальным его использование в качестве источника энергии, когда нагрузка превышает 50 % от максимальной. При отдыхе и умеренной нагрузке организм предпочитает расщеплять жиры для получения энергии. При нагрузках в 50 % от максимума (порог интенсивности для большинства тренировочных программ) организм перестраивается на преимущественное потребление углеводов. Чем больше углеводов человек использует в качестве топлива, тем больше производство молочной кислоты.
Исследования показали, что у престарелых людей в
головном мозге
количество солей кислоты (лактатов) повышено
[10]
.
Чтобы
глюкоза
могла проходить через
клеточные мембраны
, ей необходим
инсулин
. Молекула же молочной кислоты в два раза меньше молекулы глюкозы, и гормональная поддержка ей не нужна ? она с лёгкостью сама проходит через клеточные мембраны.
Количественный анализ молочной кислоты обычно проводят
титрованием
гидроксидом натрия
в присутствии
фенолфталеина
. Этот способ не подходит для концентрированных растворов, потому что в них молочная кислота частично находится в виде лактоилмолочной кислоты. Если такой раствор нужно оттитровать, используют приём
обратного титрования
: молочную кислоту обрабатывают избытком
щёлочи
(лактоилмолочная кислота при этом
гидролизуется
), а затем остаток щёлочи оттитровывают соляной кислотой
[7]
.
В промышленности и исследовательских лабораториях молочную кислоту анализируют методом
ВЭЖХ
. Содержание
энантиомерных
форм в молочной кислоте можно определить ферментативным методом либо ВЭЖХ на хиральной колонке. Такие колонки, как и образцы высокочистых энантиомеров молочной кислоты коммерчески доступны
[7]
.
Молочную кислоту можно обнаружить по следующим
качественным реакциям
:
- Взаимодействие с
n
-оксидифенилом и серной кислотой:
При осторожном нагревании молочной кислоты с концентрированной серной кислотой она вначале образует уксусный альдегид и муравьиную кислоту; последняя немедленно разлагается:
CH
3
CH(OH)COOH → CH
3
CHO + HCOOH (→ H
2
O + CO)
Уксусный альдегид взаимодействует с
n
-оксидифенилом, причём, по-видимому, происходит
конденсация
в
o
-положении к OH-группе с образованием 1,1-ди(оксидифенил)этана:

В растворе серной кислоты медленно окисляется в фиолетовый продукт неизвестного состава. Поэтому, как и при обнаружении гликолевой кислоты с помощью 2,7-диоксинафталина, в данном случае происходит взаимодействие альдегида с фенолом, при котором концентрированная серная кислота действует как конденсирующий агент и окислитель. Такую же цветную реакцию дают α-оксимасляная и
пировиноградная
кислоты.
Выполнение реакции:
В сухой пробирке нагревают в течение 2 минут на водяной бане при 85 °C каплю исследуемого раствора с 1 мл концентрированной серной кислоты. После этого охлаждают под краном до 28 °C, добавляют небольшое количество твёрдого
n
-оксидифенила и, перемешав несколько раз, дают постоять 10-30 минут. Фиолетовое окрашивание появляется постепенно и через некоторое время становится более глубоким. Открываемый минимум: 1,5?10
?6
г молочной кислоты.
- Взаимодействие с подкисленным серной кислотой раствором перманганата калия
Выполнение реакции:
В пробирку прилить 1 мл молочной кислоты, а затем немного подкисленного серной кислотой раствора перманганата калия. Нагревать в течение 2 минут на слабом огне. Ощущается запах уксусной кислоты.
С
3
Н
6
О
3
+ [O] = C
3
Н
4
O
3
+ H
2
O↑
Продуктом данной реакции может быть пировиноградная кислота С
3
Н
4
О
3
, которая тоже имеет запах уксусной кислоты. Однако пировиноградная кислота при обычных условиях неустойчива и быстро окисляется до уксусной кислоты, поэтому реакция протекает согласно суммарному уравнению:
С
3
Н
6
О
3
+ 2[O] = CH
3
COOH + CO
2
↑ + H
2
O
- Взаимодействие с фенолятом железа
Описание реакции:
Эта реакция называется реакцией Уффельмана и используется, например, в клинической медицине для определения присутствия молочной кислоты в желудочном соке, открыта
Юлиусом Уффельманом
[нем.]
в 1880-х гг. Для проведения реакции нужно растворить одну каплю
хлорида железа
и 0,4 грамма
фенола
в 50 см
3
воды. Затем добавить тестируемую жидкость, если в ней есть молочная кислота, то синий цвет раствора сменится жёлтым
[11]
[12]
, поскольку образуется
лактат железа
.
Молочная кислота используется преимущественно в двух сферах:
пищевой промышленности
и производстве
полимеров
, а также в других промышленных целях
[13]
.
В пищевой промышленности молочная кислота используется как
консервант
и
подкислитель
. Благодаря тому, что её соли хорошо растворимы в воде, их также можно использовать в тех продуктах, где важно значение
pH
. Молочная кислота и её соли используются в напитках, конфетах, мясных изделиях и соусах.
Лактат кальция
добавляется в продукты как источник кальция.
[13]
В полимерной промышленности из молочной кислоты получают
полилактид
. Производится он из
лактида
полимеризацией с раскрытием цикла
. Сам же лактид получают конденсацией молочной кислоты
[13]
.
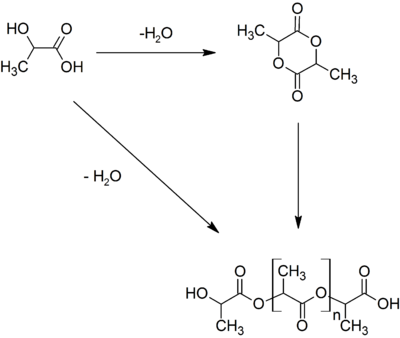
Также молочная кислота используется в покрытии металлов, косметике, текстильной и кожевенной промышленности. Её эфиры находят применение в производстве красок и чернил, электроники и чистке металлов
[13]
.
Молочная кислота ? это органическая карбоновая кислота, которая присутствует во многих организмах и является безопасной для окружающей среды. Увеличение производства молочной кислоты и, соответственно,
полилактида
оказывает положительное влияние тем, что вытесняет использование полимеров, производимых из нефти, снижает выбросы
углекислого газа
и предоставляет более широкие возможности по
утилизации
отходов
[14]
.
Молочная кислота также используется в пищевой промышленности и не является
токсичной
. Тем не менее при попадании в глаза или на повреждённую кожу она вызывает раздражение.
Полулетальная доза
для крыс при оральном приёме составляет 3,73 г/кг
[14]
.
- ↑
1
2
3
4
Ullmann, 2014
, p. 1.
- ↑
rsl.ru
(неопр.)
. Дата обращения: 5 февраля 2020.
Архивировано
5 февраля 2020 года.
- ↑
1
2
Ullmann, 2014
, p. 2.
- ↑
Трегер Ю. А.
Молочная кислота
//
Химическая энциклопедия
: в 5 т. / Гл. ред.
И. Л. Кнунянц
. ?
М.
:
Большая Российская энциклопедия
, 1992. ? Т. 3: Меди ? Полимерные. ? С. 130?131. ? 639 с. ?
48 000 экз.
?
ISBN 5-85270-039-8
.
- ↑
1
2
3
4
5
Ullmann, 2014
, p. 3.
- ↑
1
2
3
Ullmann, 2014
, p. 4.
- ↑
1
2
3
Ullmann, 2014
, p. 6.
- ↑
Dr. George A. Brooks
Архивная копия
от 5 сентября 2008 на
Wayback Machine
(англ.)
- ↑
George A. Brooks.
What does glycolysis make and why is it important?
// Journal of Applied Physiology. ? 2010. ?
Вып. 108
,
№ 6
. ?
С. 1450-1451
. ?
doi
:
10.1152/japplphysiol.00308.2010
.
- ↑
Надежда Маркина.
Старость заполняет мозг солями молочной кислоты
(рус.)
. Infox.ru (7 ноября 2010). Дата обращения: 7 ноября 2010.
Архивировано
23 августа 2011 года.
- ↑
Handbuch der Lebensmittelchemie
. ? Springer, 1935. ? Vol. 2. Allgemeine Untersuchungsmethoden. Zweiter Teil: Chemische und Biologische Methoden. ? С. 1099. ?
ISBN 9783662019481
.
- ↑
Uffelmann: Pharmazeutische Zentralhalle fur Deutschland. 1887,
28
, 582.
- ↑
1
2
3
4
Ullmann, 2014
, p. 5.
- ↑
1
2
Ullmann, 2014
, p. 7.