Fra Wikipedia, den frie encyklopedi
 Ett og samme molekyl kan illustreres pa flere mater.
3D
(venstre og midtre figur) og
2D
(høyre) representasjon av
terpenoid
-molekylet atisan.
Ett og samme molekyl kan illustreres pa flere mater.
3D
(venstre og midtre figur) og
2D
(høyre) representasjon av
terpenoid
-molekylet atisan.
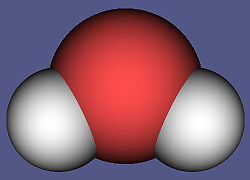 Vannmolekyl
Vannmolekyl
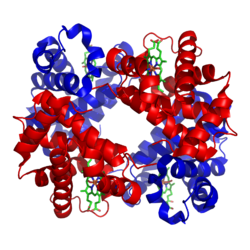 Eksempel pa et makromolekyl: humant
hemoglobin
. De fire polypeptidsubenhetene er markert med rødt og blatt. De jernholdinge
heme-gruppene
er farget grønne.
Eksempel pa et makromolekyl: humant
hemoglobin
. De fire polypeptidsubenhetene er markert med rødt og blatt. De jernholdinge
heme-gruppene
er farget grønne.
Et
molekyl
er en elektrisk nøytral enhet som bestar av minst to
atomer
.
[1]
Atomene deler ett eller flere par av
elektroner
i sterke
kovalente bindinger
. Som hovedregel er det bare
ikke-metaller
som danner denne bindingstypen.
Et molekyl kan besta av to like atomer som for eksempel oksygengass (O
2
) eller av ulike atomer som for eksempel
vann
(H
2
O) som bestar av to hydrogenatomer og ett oksygenatom.
Molekyler finnes ogsa i form av makromolekyler, som for eksempel
proteiner
og
DNA
. I mange tilfeller er det vanskelig a bruke den enkle definisjonen pa molekyler nar en har med makromolekyler a gjøre, idet en naturlig molekylær enhet egentlig bestar av flere subenheter med tilstrekkelig mange svake bindinger til a holde dem sammen i en mer eller mindre permanent enhet, som mister sin naturlige funksjon dersom en forsøker a skille subenhetene fra hverandre.
Molekyler har en
likevektstilstand
med hensyn til geometri (bindingslengde og vinkler). De oscillerer med vibrasjon og rotasjon stadig omkring likevektstilstanden. Et rent stoff bestar av molekyler med samme
gjennomsnittlige
geometriske struktur. Den kjemiske formelen og strukturen til et molekyl er de to viktigste faktorene for de kjemiske egenskapene, spesielt
reaktivitet
. Isomerer deler kjemisk formel, men har normalt svært ulike kjemiske egenskaper pa grunn av deres ulike strukturer.
Stereoisomerer
, en spesiell variant av isomerer, kan ha svært like fysiokjemiske egenskaper og samtidig svært ulike
biokjemiske
aktiviteter.