| Klor
|
|---|
 |
| Basisdata
|
| Navn
| Klor
|
|---|
| Symbol
| Cl
|
|---|
| Atomnummer
| 17
|
|---|
| Utseende
| Gulaktig grønn
|
|---|
| Plass i
periodesystemet
|
| Gruppe
| 17
|
|---|
| Periode
| 3
|
|---|
| Blokk
| p
|
|---|
| Kjemisk serie
| halogen
|
|---|
| Atomegenskaper
|
| Atomvekt
| 35,453
u
|
|---|
| Empirisk
atomradius
| 100
pm
|
|---|
| Kalkulert
atomradius
| 79 pm
|
|---|
| Kovalent atomradius
| 99 pm
|
|---|
| Elektronkonfigurasjon
| [
Ne
] 3s
2
3p
5
|
|---|
| Elektroner
per energiniva
| 2, 8, 7
|
|---|
| Oksidasjonstilstander
| ±1, 3, 5, 7
|
|---|
| Krystallstruktur
| ortorombisk
|
|---|
| Fysiske egenskaper
|
| Stofftilstand
| gass
|
|---|
| Smeltepunkt
| ?101,5 °
C
|
|---|
| Kokepunkt
| ?34,04 °C
|
|---|
| Molart volum
| 22,1 · 10
-3
m³
/
mol
|
|---|
| Tetthet
| 3,214
kg
/m³
|
|---|
| Kritisk temperatur
| 416,9
K
|
|---|
| Kritisk trykk
| 7,991 M
Pa
|
|---|
| Kritisk tetthet
| 567 kg/m³
|
|---|
| Fordampningsvarme
| 10,2 kJ/mol
|
|---|
| Smeltevarme
| 3,203 kJ/mol
|
|---|
| Damptrykk
| 3,67 · 10
6
Pa
|
|---|
| Lydfart
| 206
m/s
|
|---|
| Diverse
|
| Elektronegativitet
etter Pauling-skalaen
| 3,16
|
|---|
| Spesifikk varmekapasitet
| 480
J
/(kg · K)
|
|---|
| Elektrisk ledningsevne
| 0
S
/m
|
|---|
| Termisk konduktivitet
| 0,0089
W
/(m · K)
|
|---|
SI
-enheter &
STP
er brukt, hvis ikke annet er nevnt. MV = Manglende verdi.
|
Klor
er et
grunnstoff
med
kjemisk symbol
Cl
(av
gresk
chloros
) og
atomnummer
17.
Klor ble første gang isolert i 1774 av den svenske kjemikeren
Carl Wilhelm Scheele
ved a la mangandioksid (
MnO
2
)
reagere
med
saltsyre
(
HCl
). Han var overbevist om at han hadde funnet en oksygen-forbindelse, men i 1810 slo den engelske kjemikeren
Humphry Davy
fast at det dreide seg om et grunnstoff.
Davy døpte det nye grunnstoffet
chlorine
fra
gresk
χλωρ??
chloros
som betyr gulgrønn.
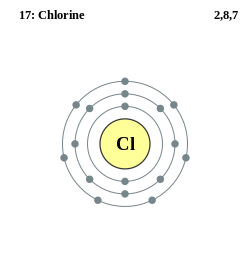 Kloratomets
elektronskall
Kloratomets
elektronskall
Klor er et
halogen
som vi finner i gruppe 17 i
det periodiske systemet
. Ved romtemperatur er rent klor en diatomisk (
Cl
2
) gul-grønn
gass
. Den er to og en halv ganger sa tung som luft, har en intens ubehagelig
kvelende
lukt
og er
giftig
. Klor inngar lett
kjemiske forbindelser
med alle andre grunnstoff bortsett fra
O
2
,
N
2
og
edelgassene
, men
brenner
ikke i luft. Det er imidlertid ikke like reaktivt som
fluor
. Klor løses lett opp i
vann
. Sammen med
hydrogen
? i det som kalles klorknallgass ? reagerer det kraftig ved oppvarming. Ren klorgass er giftig.
Naturlig forekommende klor bestar av to stabile
isotoper
:
35
Cl
(75,77 %) og
37
Cl
(24,23 %). I tillegg finnes 22 kunstig fremstilte ustabile (og dermed
radioaktive
) isotoper hvorav de mest stabile er
36
Cl
med
halveringstid
3,01 · 10
5
ar,
39
Cl
med halveringstid 55,6 minutter,
38
Cl
med halveringstid 37,24 minutter,
34m
Cl
med halveringstid 32 minutter og
40
Cl
med halveringstid 1,35 minutter. Alle de resterende isotopene har halveringstider kortere enn 1 minutt, og de fleste kortere enn 10 sekunder.
[1]
CAS
-nummer: 7782-50-5
 Glassampulle med klorgass
Glassampulle med klorgass
Klor forekommer ikke i ren form naturlig, men finnes særlig i
klorid
-forbindelser, siden det er et svært reaktivt (reaksjonsvillig) grunnstoff. Som bestanddel i
salter
(som for eksempel
natriumklorid
,
kaliumklorid
og
sinkklorid
) finnes det i store mengder over hele jorden. Andelen av klor i jordskorpen er omtrent 0,05 %. Det finnes over 2 400 kjente naturlige klorforbindelser.
[2]
Fremstilling av klor foregar ved
elektrolyse
av natriumklorid eller kaliumklorid.
Klor brukes i en rekke produkter, og brukes i tillegg til desinfisering av svømmebasseng og drikkevann. Klorgass har ogsa vært brukt som
stridsgass
i krig.