| Chemische binding
|
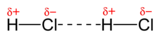
|
Dipool-dipoolinteracties
|
| Moleculen (intramoleculair)
Moleculen (intermoleculair)
Zouten
Metalen
Covalente netwerken
Theorieen
Eigenschappen
|
Portaal
 Scheikunde
Scheikunde
|
Een
ion(aire)-
of
ionenbinding
(ook wel
elektrovalente
of
heteropolaire binding
) is een
chemische binding
die ontstaat door de
elektrostatische
aantrekking tussen
ionen
: respectievelijk positief en negatief geladen
atomen
(of
moleculen
in het geval van
polyatomische ionen
). Een ionaire binding is alleen mogelijk tussen atomen met een groot verschil in
elektronegativiteit
: atomen met respectievelijk een
metaalkarakter
en een
niet-metaalkarakter
. De elektrostatische aantrekkingskracht is, bij
stoffen
die worden gekenmerkt door een ionbinding (
zouten
), de belangrijkste bindende kracht tussen de atomen. De sterkste ionbinding komt voor in
cesiumfluoride
, doordat de elektronegativiteit van de
elementen
cesium
en
fluor
maximaal verschilt, met een waarde van respectievelijk 0,79 en 3,98.
Een ionbinding is een
intermoleculaire
noch een
intramoleculaire kracht
.
De ionbinding werd rond 1916 door
Albrecht Kossel
beschreven. Atomen van de verschillende chemische elementen streven in hun buitenste
elektronenschil
naar een
edelgasconfiguratie
s
2
p
6
, bij chemische elementen hogerop in het
periodiek systeem
, vanaf
gallium
, ook naar een gesloten s
2
p
6
d
10
elektronenconfiguratie. Dit kan door ofwel elektronenafgifte worden bereikt, waarbij enkelvoudig of meervoudig positief geladen
kationen
worden gevormd, ofwel door elektronenopname, waarbij eenvoudig of meervoudig negatief geladen
anionen
ontstaan.
Er worden bij deze
chemische binding
geen
stoffen
bestaande uit losse moleculen gevormd, maar stoffen bestaande uit een star
kristalrooster
met een dichte stapeling van ionen, die overigens wel (mede) uit reeds gevormde, geladen moleculen (poly-atomische ionen) kunnen bestaan. In
waterige oplossing
komen ionen in
gehydrateerde
toestand voor. De sterkte van de binding is
omgekeerd evenredig
met de onderlinge afstand van de ionen in de kristalstructuur.


Ionaire stoffen zijn elektrisch neutraal: ze hebben geen netto
lading
. Door de sterke ionaire bindingen binnen hun kristalrooster zijn deze stoffen bros, en niet kneed- of
vervormbaar
. Ze geleiden
stroom
niet in
vaste aggregatietoestand
, maar hun
elektrische geleidbaarheid
neemt sterk toe als ze in
gesmolten
of in
opgeloste toestand
verkeren. De kristalstructuur wordt dan verbroken en de ladingdragers, de kationen en de anionen, kunnen vrij bewegen.
Super-ionaire geleiders, bijvoorbeeld
AgI
, geleiden wel goed in vaste toestand. Ze hebben een hoog
smeltpunt
en een hoog
kookpunt
. Deze laatste is zo hoog, dat de
damp
uit ionaire moleculen in plaats van aparte
ionen
bestaat.
 Lithiumfluoride
Lithiumfluoride
De eigenschappen van enkele ionaire verbindingen: