Een
aromatische verbinding
of
aromaat
is in de
scheikunde
een
organische verbinding
die voldoet aan de
regel van Huckel
. Die zegt dat een verbinding aromatisch is als die boven en onder het molecuul een cyclische wolk van
gedelokaliseerde
π-elektronen (elektronen in een p-
orbitaal
) heeft en het aantal gedelokaliseerde π-elektronen 4
n
+ 2 is. (
n
= 0, 1, 2, ... ). Een belangrijk kenmerk van aromatische verbindingen is het feit dat alle atomen in een plat vlak liggen.
Wanneer tussen twee
atomen
niet twee, maar vier elektronen worden gedeeld en zo zorgen voor de
chemische binding
(een zogenaamde
dubbele binding
of pi-binding), bevinden zich twee van die elektronen tussen de atomen, en twee andere in een vlak naast de binding. Deze laatste twee worden π-elektronen genoemd. Deze π-elektronen bevinden zich niet alleen tussen de atomen die ze binden, maar ook een beetje ernaast. Wanneer twee dubbele bindingen in een structuur gescheiden zijn door een enkele binding liggen de π-elektronen van de twee dubbele bindingen in hetzelfde vlak, en kunnen de π-elektronen van de ene dubbele binding naar de andere komen. Zulke systemen worden
geconjugeerd
genoemd, en de elektronen die door het molecuul kunnen bewegen noemt men
gedelokaliseerd
. Wanneer in een geconjugeerd systeem 4n+2 elektronen zitten (2, 6, 10, 14 of ...)
en
deze elektronen in ringen gedelokaliseerd zijn, dan levert dit een heel grote extra stabiliteit aan het
molecuul
. Een molecuul met zo'n systeem wordt
aromatisch
genoemd.
De eenvoudigste aromatische verbinding is
benzeen
.
Naftaleen
bestaat uit twee zesringen met 10 elektronen, daarop volgen met drie zesringen
antraceen
en
fenantreen
.
Pyreen
is een voorbeeld van een aromatisch molecuul met vier zesringen en 18 π-elektronen.
Aromatische verbindingen met een groot aantal ringen worden
polycyclische aromatische koolwaterstoffen
of PAK's genoemd. Deze verbindingen zijn veelal
carcinogeen
, omdat ze kunnen
intercaleren
in het
DNA
.
In een aromatisch systeem zijn veel van de atomen
koolstofatomen
, maar dat is niet noodzakelijk. Ook andere atoomtypen als bijvoorbeeld
zuurstof
of
stikstof
kunnen aan een aromatisch systeem bijdragen. Vaak is het zo dat zulke
heteroatomen
meer dan een elektron of juist geen enkel elektron aan het aromatische systeem bijdragen. Zo kunnen aromatische systemen waar nog steeds 6 elektronen in zitten uit meer of minder dan 6 atomen bestaan. Een aantal eenvoudige voorbeelden zijn
pyridine
,
chinoline
,
isochinoline
en
1,10-fenantroline
met stikstofatomen in het aromatische systeem. De stikstofatomen dragen 1 elektron bij aan het aromatische systeem. Voorbeelden met een zuurstof- en zwavelatoom zijn
furaan
en
thiofeen
. Bij deze laatste twee verbindingen dragen de heteroatomen twee elektronen bij aan het π-systeem.
Bij heteroatomen uit de tweede en hogere periode wordt de aromatische stabiliteit minder door de naast koolstof minder gunstige
elektronenbanen
in deze atomen.
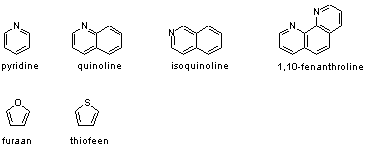
Ook is het mogelijk dat door de extra stabiliteit die wordt gewonnen als er 2, 6 of 10 elektronen in een aromatisch systeem zitten, er uit een geconjugeerd systeem van 3, 7 of 11 elektronen een elektron wordt uitgestoten of in een systeem van 5 of 9 elektronen een extra elektron wordt ingevangen. Een voorbeeld hiervan met 2 elektronen is het cyclopropenyl-kation. Voorbeelden met 6 elektronen zijn het
cyclopentadienylanion
(extra elektron naast 5 'eigen'): C
5
H
5
?
, en
tropylium-kation
(een elektron minder): C
7
H
7
+
.
Azuleen
is een isomeer van
naftaleen
. In plaats van twee zesringen beschikt het molecuul over een vijfring en een ring van 7 koolstofatomen. De vijfring heeft een negatieve lading, de andere ring een positieve.
Veel aromaten zijn
carcinogeen
, dit komt omdat het polaire stoffen zijn die vrijuit door onze celmembranen bewegen en schade kunnen aanrichten aan
DNA
.
Benzeen
kent een
MAC-waarde
van 0,2 [ppm].