 Algemene
structuurformule
van een ether.
Algemene
structuurformule
van een ether.
Een
ether
is een
organische verbinding
van de algemene vorm R-O-R', waarbij de centrale
zuurstof
een directe
binding
heeft met twee
koolstofatomen
die deel zijn van een
alkyl-
of
arylgroep
. De benaming ether is de triviale naam van
di-ethylether
/
kroonether
.
 Structuurformule van tetrahydrofuraan, een cyclisch ether.
Structuurformule van tetrahydrofuraan, een cyclisch ether.
De eenvoudigste alkylether is
dimethylether
(CH
3
-O-CH
3
).
Di-ethylether
is de meest voorkomende en wordt algemeen gebruikt als
oplosmiddel
. Voorbeelden van arylethers zijn
anisol
en
ethylfenylether
. Alkylethers kunnen ook cyclisch zijn, zoals
tetrahydrofuraan
of
etheenoxide
.
Acetalen
zijn organische verbindingen waarbij twee etherfuncties op hetzelfde koolstofatoom staan.
 Zie
Kroonether
voor het hoofdartikel over dit onderwerp.
Zie
Kroonether
voor het hoofdartikel over dit onderwerp.
Kroonethers zijn verbindingen met een aantal zuurstofatomen in een cyclische structuur. Hierbij ontstaat door de moleculaire structuur een kooi van zuurstofatomen. Kroonethers worden vaak gebruikt om kationen, zoals
kalium
, te complexeren.
 Zie
Polyether
voor het hoofdartikel over dit onderwerp.
Zie
Polyether
voor het hoofdartikel over dit onderwerp.
Polyethers zijn
polymeren
waarin de functionele groep van een ether (R-O-R') periodiek voorkomt.
Deze benamingen worden om aan te geven welk type
koolstofatoom
gebonden is aan het zuurstofatoom. In een primaire ether is die koolstof slechts met een andere koolstof gebonden (bijvoorbeeld
di-ethylether
), bij een secundaire twee (zoals in
di-isopropylether
), en bij een tertiaire drie (zoals in
methyl-
tert
-butylether
).
Er zijn diverse methoden beschikbaar om ethers te bereiden. De meest intuitieve reactie is de
dehydratie
van twee
alcoholen
onder invloed van een katalytische hoeveelheid
sterk zuur
(zoals
zwavelzuur
) en bij verhoogde temperatuur (125°C):
[1]
 Synthese van ethers
Synthese van ethers
Logischerwijs is deze directe substitutie enkel mogelijk om symmetrische ethers te vormen. Bij mengsels van alcoholen kunnen namelijk verschillende symmetrische en asymmetrische ethers gevormd worden. De scheiding daarvan zou omslachtig zijn. De dehydratiemethode wordt hoofdzakelijk gebruikt om cyclische ethers te bereiden, zoals
tetrahydrofuraan
(THF).
De
Williamson-ethersynthese
is geschikt om zowel symmetrische als asymmetrische ethers te bereiden. Hierbij wordt een alcohol in contact gebracht met een
sterke base
, zodat een
alkoxide
ontstaat. Daarna vindt een
S
N
2-reactie
plaats:
 Verloop van de Williamson-ethersynthese
Verloop van de Williamson-ethersynthese
De groepen R
1
en R
2
stellen hierbij
alkyl-
of
arylgroepen
voor. Deze kunnen beiden gelijk zijn (dan wordt een symmetrisch ether gevormd) of zij kunnen verschillen (dan wordt een asymmetrisch ether gevormd). Het element X is het halogenide (de
leaving group
), doorgaans
chloor
,
broom
of
jood
. De
Ullmann-condensatie
is een gelijkaardige methode, maar wordt specifiek gebruikt om diarylethers te synthetiseren. Een voorbeeld is de reactie van
broombenzeen
met
4-nitrofenol
tot een
difenyletherderivaat
:
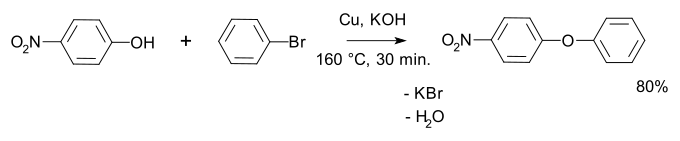 Ullmann-condensatie
Ullmann-condensatie
Een laatste methode is de zuur-gekatalyseerde additie van een alcohol aan een
alkeen
:
 Synthese van een ether
Synthese van een ether
Ethers zijn zeer
stabiel
en het zijn zwak
polaire
oplosmiddelen
die in de
organische chemie
veel worden toegepast. De
laagmoleculaire
ethers die hiervoor worden gebruikt zijn vaak erg vluchtig en brandbaar. Bovendien kunnen ethers blootgesteld aan de
zuurstof
van de
lucht
geleidelijk organische
peroxiden
vormen. Deze verbindingen zijn zeer
reactief
(soms zelfs
explosief
). Doordat de moleculen wat zwaarder zijn hebben de peroxiden een hoger kookpunt dan de overeenkomstige ethers. De hoeveelheid peroxiden wordt relatief steeds groter: er wordt steeds meer gevormd en doordat de ether sneller verdampt wordt de concentratie peroxide in de achterblijvende vloeistof steeds hoger. Dit kan tot zeer gevaarlijke situaties leiden, met name bij
destillaties
of
indampingen
. De vorming van peroxiden wordt verder ook versneld door aanwezigheid van
metalen
en
aldehyden
.
Als over ether gesproken wordt, zonder verdere kwalificatie, wordt meestal
di-ethylether
bedoeld. Dit is een kleurloze, zeer
vluchtige
en brandbare vloeistof die bij 34,6°C kookt. Het gas dat vrijkomt bij het vervliegen, is zo brandbaar dat de vlam van bijvoorbeeld een waxinelichtje over de tafel naar de ether kan 'overstappen'.
Aan
benzine
wordt vaak
methyl-
tert
-butylether
(MTBE) toegevoegd om de
klopvastheid
te verhogen.
Niet alle moleculen waarin de structuur R-O-R' in voorkomt worden ethers genoemd. De volgende stoffen zijn geen ethers:
Bronnen, noten en/of referenties
- ↑
(
en
)
J. Clayden, N. Greeves & S. Warren
(2012) -
Organic chemistry
, second edition, Oxford University Press, pp. 173-174 -
ISBN 978-0-19-927029-3
|