Калиум ци?анид
|

|
|
|
| Назнаки
|
|
|
151-50-8
 Ок Ок
|
| ChEBI
|
CHEBI:33191
 Н Н
|
| ChemSpider
|
8681
 Ок Ок
|
| EC-бро?
|
205-792-3
|
InChI=1S/CN.K/c1-2;/q-1;+1
 Ок Ок
Key: NNFCIKHAZHQZJG-UHFFFAOYSA-N
 Ок Ок
InChI=1/CN.K/c1-2;/q-1;+1
Key: NNFCIKHAZHQZJG-UHFFFAOYAH
|
| 3Д-модел (
Jmol
)
|
Слика
|
| PubChem
|
9032
|
| RTECS-бр.
|
TS8750000
|
|
|
| UNII
|
MQD255M2ZO
 Ок Ок
|
| ОН-бр.
|
1680
|
| Сво?ства
|
| Хемиска формула
|
|
| Моларна маса
|
0 g mol
?1
|
| Изглед
|
Бела кристална цврста супстанца
deliquescent
|
| Мирис
|
слаб, арома на бадем
|
| Густина
|
1,52 g/cm
3
Solubility = 71.6 g/100 ml (25 °C)
100 g/100 mL (100 °C)
|
| Точка на топе?е
|
|
| Точка на врие?е
|
|
| Растворливост
во
метанол
|
4,91 g/100 mL (20 °C)
|
| Растворливост
во
глицерол
|
soluble
|
| Растворливост
во
формамид
|
14,6 g/100 mL
|
| Растворливост
во
етанол
|
0,57 g/100mL
|
| Растворливост
во
хироксиламин
|
41 g/100 mL
|
| Киселост
(p
K
a
)
|
11,0
|
|
|
−37,0·10
?6
cm
3
/mol
|
| Показател на прекршува?е
(
n
D
)
|
1,410
|
| Термохеми?а
|
Ст. енталпи?а на
формира?е
Δ
f
H
o
298
|
−131,5 kJ/mol
|
Стандардна моларна
ентропи?а
S
o
298
|
127,8 J K
−1
mol
−1
|
| Опасност
|
| GHS
-ознаки
:
|
Пиктограми
|
   
|
Сигнални зборови
|
Опасност
|
Из?ави за опасност
|
H290
,
H300
,
H310
,
H330
,
H370
,
H372
,
H410
|
Из?ави за претпазливост
|
P260
,
P264
,
P273
,
P280
,
P284
,
P301+P310
|
| NFPA 704
|
|
| Температура на запалува?е
|
{{{value}}}
|
| Смртоносна доза
или концентраци?а:
|
|
|
5 mg/kg (орално, за?ак)
10 mg/kg (орално, стаорец)
5 mg/kg (орално, стаоред)
8.5 mg/kg (орално, глушец)
[2]
|
| NIOSH
(здравствени граници во САД):
|
PEL (дозволива)
|
TWA 5 mg/m
3
[1]
|
REL (препорачана)
|
C 5 mg/m
3
(4.7 ppm) [10-минути]
[1]
|
IDLH (непосредна опасност)
|
25 mg/m
3
[1]
|
| Безбедносен лист
|
ICSC 0671
|
| Слични супстанци
|
| Други
ан?они
|
Калиум ци?анит
Калиум тиоци?анат
|
| Други
кат?они
|
Натриум ци?анид
Рубидиум ци?анид
Литиум ци?анид
Цeзиум ци?анид
|
| Дополнителни податоци
|
|
|
 Ок
(што е ова?)
(провери) Ок
(што е ова?)
(провери)
Освен ако не е поинаку укажано, податоците се однесуваат на матери?алите во нивната
стандардна состо?ба (25 °C, 100 kPa)
|
| Наводи
|
Калиум ци?анид
е соединение со формулата
KCN
. Оваа безбо?на кристална сол, по изглед слична на ше?ерот, е многу растворлива во вода. Пове?ето KCN се користи во ископува?ето на злато, во органски синтези и за галванизаци?а. Помалите употреби вклучуваат при хемиско обложува?е и пече?е на накит.
[4]
Калиум ци?анидот е многу токсичен. Влажната цврста сол од KCN испушта мали количини на водород ци?анид поради хидролиза, што може да мириса на горчлив бадем.
[5]
Сепак, не секо? може да намириса ци?анид; способноста да се направи тоа е генетска одлика.
Вкусот на калиум ци?анид е опишан како остар и горчлив, со чувство на пече?е
[6]
слично на лугата.
[7]
KCN се произведува со третира?е на водород ци?анид со воден раствор на калиум хидроксид, проследено со испарува?е на растворот во вакуум:
[8]
HCN + KOH → KCN + H
2
O
Годишно се произведуваат околу 50.000 тони калиум ци?анид.
[4]
Пред 1900 година и пронао?а?ето на Кастнеровиот процес, калиум ци?анидот бил на?важниот извор на ци?аниди од алкални метали.
[4]
Во ово? историски процес, калиум ци?анидот бил произведен со распа?а?е на калиум фероци?анид:
[9]
K
4
[Fe(CN)
6
] → 4 KCN + FeC
2
+ N
2
Во воден раствор, KCN дисоцира на хидрирани ?они на калиум(K
+
) и ци?анидни ?они (CN
?
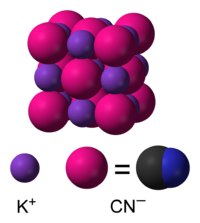
). Вообичаената форма на цврст KCN, стабилна на амбиентален притисок и температура, ?а има истата кубна кристална структура како и натриум хлоридот, при што секо? ?он на калиум е опкружен со шест ?они на ци?анид, и обратно. И покра? тоа што ?оните на ци?анид се двоатомски, а со тоа и помалку симетрични од хлоридот, тие ротираат толку брзо што нивната форма во просек за време е сферична. При ниска температура и висок притисок, оваа слободна ротаци?а е попречена, што резултира со помалку симетрична кристална структура со ци?анидни ?они распоредени во листови
[10]
[11]
KCN и натриум ци?анид (NaCN) широко користени во органската синтеза за подготовка на нитрили и карбоксилни киселини, особено во реакци?ата на von Richter. Исто така, нао?а употреба за синтеза на хидантоини, кои можат да бидат корисни синтетички посредници, кога реагираат со карбонилно соединение како што е алдехид или кетон во присуство на амониум карбонат.
KCN се користи како фотографски фиксатор во процесот на колодиум на влажна плоча.
[12]
KCN го раствора среброто онаму каде што не станало нерастворливо од развивачот. Ова ?а открива и стабилизира сликата, што ?а прави пове?е нечувствителна на светлина. Модерните фотографи со влажна плоча можеби претпочитаат помалку токсични фиксатори, често избира??и натриум тиосулфат, но KCN сe уште се користи
Во ископува?ето злато, KCN формира сол растворлива во вода калиум злато ци?анид (или злато калиум ци?анид) и калиум хидроксид од метално злато во присуство на кислород (обично од околниот воздух) и вода:
- 4 Au + 8 KCN + O
2
+ 2 H
2
O → 4 K[Au(CN)
2
] + 4 KOH
Сличен процес користи NaCN за производство на натриум злато ци?анид (NaAu(CN
2
)).
Калиум ци?анидот е мо?ен инхибитор на клеточното дише?е, делува??и на митохондри?алната цитохром c оксидаза, па оттука ?а блокира оксидативната фосфорилаци?а. Потоа се ?авува млечна ацидоза како последица на анаеробен метаболизам. Првично, акутното труе?е со ци?анид предизвикува црвен или румен тен ка? жртвата биде??и ткивата не се во можност да го користат кислородот во крвта. Ефектите на калиум ци?анид и натриум ци?анид се идентични, а симптомите на труе?е обично се ?авуваат во рок од неколку минути по внесува?ето на супстанци?ата: лицето ?а губи свеста и на кра?от следи мозочна смрт. Во ово? период жртвата може да претрпи конвулзии. Смртта е предизвикана од церебрална хипокси?а. Очекуваната доза на LD100 (човечка) за калиум ци?анид е 200?300 mg додека средната смртоносна доза LD50 се проценува на 140 mg.
[13]
Лу?ето кои умреле со самоубиство или биле убиени користе??и калиум ци?анид се:
- Виктор Ма?ер
, германски хемичар од 19 век, умрел со самоубиство во 1897 година откако земал ци?анид
[14]
- Густав Вид
, дански романсиер, поет и драматург, во 1914 година
- Притилата Вадедар
, индиски револуционерен националист, земал ци?анид во 1932 година за да избегне фа?а?е од британската полици?а
- Бадал Гупта
, револуционер од Бенгал, ко? започнал напад врз Зградата на писателите во Калкута, конзумирал ци?анид во 1930 година веднаш по нападот
- Волас Каротерс
, полимерен хемичар ко? умрел со самоубиство во 1937 година, откако со години се борел со депреси?а
Високи личности во нацистичка Германи?а, како Ервин Ромел, долгогодишната придружничка на Хитлер, Ева Браун, ?озеф Гебелс, Ха?нрих Химлер и Херман Геринг
- Алан Т?уринг
, комп?утерски научник ко? починал од труе?е со ци?анид во 1954 г
- Рамон Сампедро
, шпански тетраплегичар и активист чие потпомогнато самоубиство во 1998 година предизвика национална дебата за евтанази?ата, и беше тема на филмот награден со Оскар ?The Sea Inside“
- Роналд Кларк О'Бра?ан
, оптичар од Тексас ко? го уби сво?от син со врзува?е на пикси стап со калиум ци?анид во 1974 година
- Храмот на народот, секташкото самоубиство од 1978 година во (?онстаун), Гва?ана
- MЧленови на
LTTE
вклучени во атентатот на индискиот премиер Ра?ив Ганди во 1991 година
- ?е?сон Алтом
, перспективен дипломиран студент во лаборатори?ата на нобеловецот Е.?. Кори на Харвард, почина откако испил калиум ци?анид во 1998 година.
- Слободан Пра?ак
, воен генерал во Република Хрватска, почина со самоубиство пие??и од шишенце со калиум ци?анид за време на чита?ето на неговата жалбена пресуда во Хаг за Ме?ународниот кривичен трибунал за поранешна ?угослави?а (МКТ?) на 29 ноември 2017 година.
[15]
Професионалните ентомолози го користат како средство за убива?е при собира?е во тегли, биде??и инсектите за неколку секунди подлегнуваат на испарува?ата од HCN што ги испушта, со што се минимизира штетата дури и на многу кревките примероци.
KCN може на?ефикасно да се детоксицира со водород пероксид или со раствор од натриум хипохлорит. Таквите раствори треба да се чуваат алкални секогаш кога е можно за да се елиминира можноста за создава?е на водород ци?анид:
[4]
- KCN + H
2
O
2
→ K
OCN
+ H
2
O
- ↑
1,0
1,1
1,2
??ебен водич за опасните хемиски материи #0522“
. Национален институт за безбедност и здрав?е при работа (NIOSH).
(англиски)
- ↑
?Cyanides (as CN)“
.
Immediately Dangerous to Life and Health
.
National Institute for Occupational Safety and Health
(NIOSH).
- ↑
?POTASSIUM CYANIDE | CAMEO Chemicals | NOAA“
.
- ↑
4,0
4,1
4,2
4,3
Andreas Rubo, Raf Kellens, Jay Reddy, Joshua Wooten, Wolfgang Hasenpusch "Alkali Metal Cyanides" in Ullmann's Encyclopedia of Industrial Chemistry 2006 Wiley-VCH, Weinheim, Germany.
doi
:
10.1002/14356007.i01_i01
- ↑
?Suicide note reveals taste of cyanide“
. 2006-07-08.
- ↑
?????, ??????? (2021-12-19).
?
'
?????? ?????????... ???????????...'; ? '???? ??????' ???????????? ?????? ????? ????????? | Madhyamam“
.
www.madhyamam.com
(мала?алски)
. Посетено на
2021-12-21
.
- ↑
?The only taste: Cyanide is acrid“
.
hindustantimes.com
. Hindustan Times. 2006-07-08.
- ↑
Pradyot Patnaik.
Handbook of Inorganic Chemicals
. McGraw-Hill, 2002,
ISBN
0-07-049439-8
- ↑
Von Wagner, Rudolf (1897).
Manual of chemical technology
. New York: D. Appleton & Co. стр. 474 & 477.
- ↑
Crystallography Open Database, Structure of KCN
- ↑
H. T. Stokes; D. L. Decker; H. M. Nelson; J. D. Jorgensen (1993).
?Structure of potassium cyanide at low temperature and high pressure determined by neutron diffraction“
.
Physical Review B
(Submitted manuscript).
47
(17): 11082?11092.
Bibcode
:
1993PhRvB..4711082S
.
doi
:
10.1103/PhysRevB.47.11082
.
PMID
10005242
.
.
- ↑
J. Towler, MD. "The Silver Sunbeam (Facsimile 1864 edition, 1969)" pg 119
- ↑
John Harris Trestrail III.
Criminal Poisoning - Investigational Guide for Law Enforcement, Toxicologists, Forensic Scientists, and Attorneys (2nd edition)
. p. 119
- ↑
?Top 10 Scientists who Committed Suicide“
. 2007-10-07.
- ↑
?War criminal 'took cyanide' in Hague court“
(англиски).
BBC News
. 2017-12-01
. Посетено на
2017-12-01
.
|
|---|
|
| HCN
|
|
|
|
He
|
| LiCN
|
Be(CN)
2
|
B(CN)
3
|
C(CN)
4
C
2
(CN)
2
|
NH
4
CN
,
N
3
CN
|
OCN
?
,
-NCO
|
FCN
|
Ne
|
| NaCN
|
Mg(CN)
2
|
Al(CN)
3
|
Si(CN)
4
,
(CH
3
)
3
SiCN
|
P(CN)
3
|
SCN
?
,
-NCS
,
(SCN)
2
,
S(CN)
2
|
ClCN
|
Ar
|
| KCN
|
Ca(CN)
2
|
|
Sc(CN)
3
|
Ti
|
V
|
Cr(CN)
6
3?
|
Mn
|
Fe(CN)
2
,
Fe(CN)
6
4?
,
Fe(CN)
6
3?
|
Co(CN)
2
|
Ni(CN)
2
Ni(CN)
4
2?
Ni(CN)
4
4?
|
CuCN
|
Zn(CN)
2
|
Ga(CN)
3
|
Ge
|
As(CN)
3
,
(CH
3
)
2
AsCN
|
SeCN
?
(SeCN)
2
Se(CN)
2
|
BrCN
|
Kr
|
| RbCN
|
Sr(CN)
2
|
|
Y(CN)
3
|
Zr
|
Nb
|
Mo(CN)
8
4?
|
Tc
|
Ru
|
Rh
|
Pd(CN)
2
|
AgCN
|
Cd(CN)
2
|
In(CN)
3
|
Sn
|
Sb(CN)
3
|
Te
|
ICN
|
Xe
|
| CsCN
|
Ba(CN)
2
|
*
|
Lu(CN)
3
|
Hf
|
Ta
|
W(CN)
8
4?
|
Re
|
Os
|
Ir
|
Pt(CN)
4
2-
,
Pt(CN)
6
4-
|
AuCN
,
K[Au(CN)
2
]
|
Hg
2
(CN)
2
,
Hg(CN)
2
|
TlCN
|
Pb(CN)
2
|
Bi(CN)
3
|
Po
|
At
|
Rn
|
| Fr
|
Ra
|
**
|
Lr
|
Rf
|
Db
|
Sg
|
Bh
|
Hs
|
Mt
|
Ds
|
Rg
|
Cn
|
Nh
|
Fl
|
Mc
|
Lv
|
Ts
|
Og
|
|
|
|
| *
|
La(CN)
3
|
Ce(CN)
3
,
Ce(CN)
4
|
Pr
|
Nd
|
Pm
|
Sm(CN)
3
|
Eu(CN)
3
|
Gd(CN)
3
|
Tb
|
Dy(CN)
3
|
Ho(CN)
3
|
Er
|
Tm
|
Yb(CN)
3
|
| **
|
Ac(CN)
3
|
Th(CN)
4
|
Pa
|
UO
2
(CN)
2
|
Np
|
Pu
|
Am
|
Cm
|
Bk
|
Cf
|
Es
|
Fm
|
Md
|
No
|
|
|