Во
неорганската хеми?а
,
бикарбонатот
(номенклатура препорачана од
МСЧПХ
:
хидрогенкарбонат
[2]
) ? средна форма во депротонаци?ата на
?аглеродната киселина
. Тоа е полиатомски
ан?он
со хемиска формула
H
C
O
?
3
.
Бикарбонатот има клучна биохемиска улога во физиолошкиот
pH
пуферски
систем.
[3]
Терминот ?бикарбонат“ бил измислен во 1814 година од англискиот хемичар Вили?ам Ха?д Воластон.
[4]
[5]
Името живее како триви?ално.
Бикарбонатниот ?он (хидрогенкарбонат ?он) е
ан?он
со
емпириска формула
HCO
?
3
и молекуларна маса од 61,01
далтони
; се состои од еден централен ?аглероден
атом
опкружен со три атоми на кислород во тригонален планарен распоред, со атом на водород прикачен на еден од кислородите. То? е изоелектронски со
азотна киселина
HNO
3
. Бикарбонатниот ?он носи негативен еден формален полнеж и е
амфипротски
вид ко? има и кисели и базни сво?ства. Тоа е и кон?угирана база на
?аглеродна киселина
H
2
CO
3
; и кон?угирана киселина на
CO
2?
3
,
карбонатниот
?он, како што е прикажано со овие реакции на
рамнотежа
:
- CO
2?
3
+ 2 H
2
O ?
HCO
?
3
+ H
2
O + OH
?
? H
2
CO
3
+ 2 OH
?
- H
2
CO
3
+ 2 H
2
O ?
HCO
?
3
</br>
HCO
?
3
+ H
3
O
+
+ H
2
O ?
CO
2?
3
+ 2 H
3
O
+
.
Бикарбонатна сол се формира кога
позитивно наелектризираниот ?он
се прицврстува на негативно наелектризираните атоми на кислородот на ?онот, формира??и ?онско соединение. Многу бикарбонати се
растворливи
во
вода
при
стандардна температура и притисок
; особено, натриум бикарбонат придонесува за вкупните растворени цврсти материи, заеднички параметар за проценка на
квалитетот на водата
.
[6]
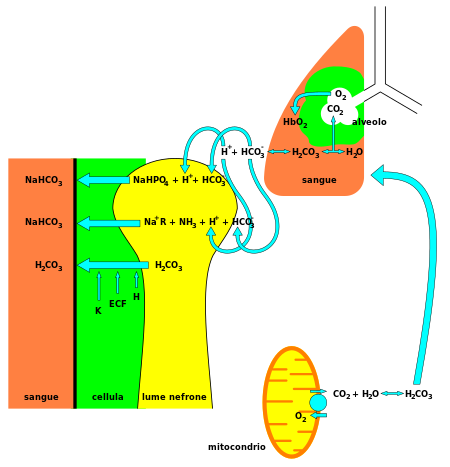 CO
2
произведен како отпаден производ од оксидаци?ата на ше?ерите во митохондриите реагира со вода во реакци?а катализирана од ?аглеродна анхидраза за да формира H
2
CO
3
, ко? е во рамнотежа со кат?онот H
+
и ан?онот HCO
3
?
. Потоа се носи во белите дробови, каде што се ?авува обратна реакци?а и се ослободува гас CO
2
. Во бубрегот (лево), клетките (зелени) што ?а обложуваат проксималната тубула го зачувуваат бикарбонатот транспортира??и го од гломеруларниот филтрат во луменот (жолт) на нефронот назад во крвта (црвено). Точната стехиометри?а во бубрегот е испуштена заради едноставност.
CO
2
произведен како отпаден производ од оксидаци?ата на ше?ерите во митохондриите реагира со вода во реакци?а катализирана од ?аглеродна анхидраза за да формира H
2
CO
3
, ко? е во рамнотежа со кат?онот H
+
и ан?онот HCO
3
?
. Потоа се носи во белите дробови, каде што се ?авува обратна реакци?а и се ослободува гас CO
2
. Во бубрегот (лево), клетките (зелени) што ?а обложуваат проксималната тубула го зачувуваат бикарбонатот транспортира??и го од гломеруларниот филтрат во луменот (жолт) на нефронот назад во крвта (црвено). Точната стехиометри?а во бубрегот е испуштена заради едноставност.
Бикарбонат (
HCO
?
3
) е витална компонента на
системот за пуферира?е
на
pH
[3]
на човечкото тело (одржува?е на киселинско-базната хомеостаза). 70%-75% од CO
2
во телото се претвора во
?аглеродна киселина
(H
2
CO
3
), ко?а е кон?угирана киселина на
HCO
?
3
и брзо може да се претвори во него.
Со ?аглеродна киселина како централен среден вид, бикарбонат - во врска со вода,
водородни ?они
и
?аглерод диоксид
- го формира ово? пуферски систем, ко? се одржува на испарлива рамнотежа
[3]
потребна за да обезбеди брза отпорност на промените на pH и во киселиот и
основни
насоки. Ова е особено важно за заштита на
ткивата
на
централниот нервен систем
, каде pH се менува премногу надвор од нормалниот опсег во ко?а било насока може да се покаже катастрофално (види ацидоза или алкалоза). Неодамна, исто така, било докажано дека клеточниот метаболизам на бикарбона може да се регулира со сигнализаци?а mTORC1.
[7]
Дополнително, бикарбонатот игра клучна улога во дигестивниот систем. ?а зголемува внатрешната pH вредност на желудникот, откако дигестивните сокови со висока киселост ?е завршат со нивното варе?е на храната. Бикарбонатот, исто така, делува за регулира?е на pH вредноста во тенкото црево. Се ослободува од
панкреасот
како одговор на хормонот секретин за да го неутрализира киселиот хим ко? влегува во
дуоденумот
од желудникот.
[8]
Бикарбонатот е доминантна форма на растворен неоргански ?аглерод во морската вода,
[9]
и во пове?ето свежи води. Како таков, то? е важен ми?алник во
?аглеродниот циклус
.
Во слатководната екологи?а, силната
фотосинтетичка
активност на слатководните растени?а на дневна светлина ослободува гасовит
кислород
во водата и во исто време произведува бикарбонатни ?они. Тие ?а поместуваат pH вредноста нагоре додека во одредени околности степенот на алкалност не стане токсичен за некои организми или може да направи други хемиски состо?ки како што е
амони?акот
токсичен. Во темнина, кога не се случува фотосинтеза, процесите на дише?е ослободуваат ?аглерод диоксид и не се создаваат нови бикарбонатни ?они, што резултира со брз пад на pH вредноста.
Протокот на бикарбонатни ?они од карпите кои се избришани од ?аглеродната киселина во дождовницата е важен дел од
?аглеродниот циклус
.
На?честата сол на бикарбонатниот ?он е
натриум бикарбонат
, NaHCO
3
, ко?а е попозната како
сода бикарбона
. Кога се загрева или изложува на
киселина
како што е
оцетна киселина
(оцет), натриум бикарбонат ослободува
?аглерод диоксид
. Ова се користи како квасец при пече?е.
Амониум бикарбонат
се користи во производството на бисквити за варе?е.
Во ди?агностичката медицина, вредноста на бикарбонатот во крвта е еден од неколкуте показатели за состо?бата на киселинско-базната физиологи?а во телото. Се мери, заедно со
?аглерод диоксид
,
хлорид
,
калиум
и
натриум
, за да се проценат нивоата на
електролити
во тест
со електролитен панел
(ко? има Тековна процедурална терминологи?а, CPT, код 80051).
Параметарот
стандардна концентраци?а на бикарбонати
(SBC
e
) е концентраци?ата на бикарбонат во крвта при
P
a
CO
2
од 40ммHg, целосна сатураци?а со кислород и 36 °C.
 Референтни опсези за тестови на крвта, споредува??и ?а содржината на бикарбонат во крвта (прикажано со сино десно) со други состо?ки.
Референтни опсези за тестови на крвта, споредува??и ?а содржината на бикарбонат во крвта (прикажано со сино десно) со други состо?ки.
- ↑
1,0
1,1
?hydrogencarbonate (CHEBI:17544)“
.
Chemical Entities of Biological Interest (ChEBI)
. UK: European Institute of Bioinformatics. IUPAC Names.
Архивирано
од изворникот 2015-06-07.
- ↑
Nomenclature of Inorganic Chemistry IUPAC Recommendations 2005
(PDF)
, IUPAC, стр. 137
- ↑
3,0
3,1
3,2
?Clinical correlates of pH levels: bicarbonate as a buffer“
. Biology.arizona.edu. October 2006. Архивирано од
изворникот
на 2015-05-31.
- ↑
William Hyde Wollaston (1814) "A synoptic scale of chemical equivalents,"
Philosophical Transactions of the Royal Society
,
104
: 1-22.
- ↑
?Baking Soda“
.
Newton ? Ask a Scientist
.
Argonne National Laboratory
. Архивирано од
изворникот
на 26 February 2015
. Посетено на
2 May
2018
.
- ↑
Geor, Raymond J.; Coenen, Manfred; Harris, Pat (31 January 2013).
Equine Applied and Clinical Nutrition: Health, Welfare and Performance
(англиски). Elsevier Health Sciences. стр. 90.
ISBN
978-0-7020-5418-1
.
The most common indicator of water quality is the concentration of total dissolved solids (TDS)
- ↑
?The mTORC1-SLC4A7 axis stimulates bicarbonate import to enhance de novo nucleotide synthesis“
.
Molecular Cell
.
82
(1): 3284?3298.e7. June 2022.
doi
:
10.1016/j.molcel.2022.06.008
.
PMC
9444906
.
PMID
35772404
.
- ↑
Berne & Levy,
Principles of Physiology
- ↑
?The chemistry of ocean acidification : OCB-OA“
.
www.whoi.edu
(англиски). Woods Hole Oceanographic Institution. 24 September 2012. Архивирано од
изворникот
на 19 May 2017
. Посетено на
17 May
2017
.
|
|---|
| | Обични оксиди
| |
|---|
| | Егзотични оксиди
| |
|---|
| | Полимери
| |
|---|
| | Соединени?а изведени од оксиди
| |
|---|
|
|
|---|
| | Соединени?а
| |
|---|
| | ?аглеродни ?они
| |
|---|
| | Наноструктури
| |
|---|
| | Оксиди и поврзано
| |
|---|
|