 Una
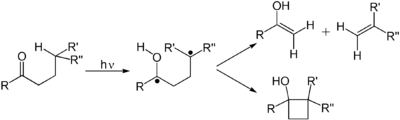
reazioni di Norrish
di tipo II
Una
reazioni di Norrish
di tipo II
La
fotochimica
e una branca della
chimica
che si occupa delle reazioni chimiche indotte dall'interazione della
luce
(in particolare
ultravioletto
,
luce visibile
e il vicino
infrarosso
) con la materia.
Le reazioni fotochimiche sono preziose nella
chimica organica
e in quella
inorganica
perche procedono in modo diverso rispetto alle reazioni termiche. In esse
l'energia necessaria per lo svolgersi della reazione chimica e fornita quindi dai
fotoni
assorbiti dai reagenti, che portano dei particolari gruppi chimici detti
cromofori
, in grado di assorbire la luce. I
fotocatalizzatori
sono opportuni
catalizzatori
che vengono attivati con la luce.
Molti processi importanti coinvolgono la fotochimica. Molte
reazioni redox
sono catalizzate dalla luce, mentre un esempio notevole delle possibilita della fotochimica e quello della
fotosintesi clorofilliana
, in cui le piante formano
amido
e
ossigeno
partendo dall'
acqua
e dall'
anidride carbonica
grazie ai processi della luce sulla
clorofilla
.
Due leggi fondamentali della fotochimica sono le seguenti:
La luce e un tipo di
radiazione elettromagnetica
, una fonte di energia. La legge di Grotthus-Draper (dai chimici
Theodor Grotthuss
e
John W. Draper
), afferma che la luce deve essere assorbita da una sostanza chimica perche abbia luogo una
reazione fotochimica
. Per ogni fotone di luce assorbito da un sistema chimico, non piu di una molecola e attivata per una reazione fotochimica, come definito dalla
resa quantica
.
Le reazioni chimiche si verificano solo quando a una molecola viene fornita la necessaria "
energia di attivazione
". Un semplice esempio puo essere la
combustione
di
benzina
(un
idrocarburo
) in anidride carbonica e acqua. In questa reazione, l'energia di attivazione viene fornita sotto forma di calore o di una scintilla. In caso di reazioni fotochimiche la luce fornisce l'energia di attivazione. Semplificando, la luce e un meccanismo che fornisce l'energia di attivazione necessaria per molte reazioni. Se viene impiegato un
laser
, e possibile eccitare selettivamente una molecola in modo da produrre lo stato elettronico e vibrazionale desiderato. Allo stesso modo, l'emissione da uno stato particolare, puo essere selettivamente monitorato, fornendo una misura di quello stato. Se il sistema chimico e a bassa pressione, questo consente agli scienziati di osservare la distribuzione di energia dei prodotti di una reazione chimica prima che le differenze di energia vengano spalmate ed entrino nella media a causa delle ripetute collisioni.
L'assorbimento di un fotone di luce da una molecola reagente puo anche consentire che una reazione avvenga non solo portando la molecola alla necessaria energia di attivazione, ma anche cambiando la simmetria della configurazione elettronica della molecola, che consente un percorso di reazione altrimenti inaccessibile, come descritto dalle
regole di Woodward-Hoffmann
. Una reazione di
cicloaddizione [2+2]
e un esempio di
reazione periciclica
che puo essere analizzata utilizzando queste regole o la
teoria degli orbitali molecolari
.
Le reazioni fotochimiche implicano la riorganizzazione elettronica iniziata dalla radiazione elettromagnetia. Le reazioni sono diversi ordini di grandezza piu veloce delle reazioni termiche; spesso sono osservate reazioni con una velocita di 10
?9
secondi e processi associati con una velocita di 10
?15
secondi.
I fotochimici in genere utilizzano solo alcune sezioni dello
spettro elettromagnetico
. Alcune delle sezioni piu utilizzate, e le loro lunghezze d'onda, sono le seguenti:
L'esempio principale e la
fotosintesi
, in cui la maggior parte delle piante usa l'energia solare per convertire il
diossido di carbonio
e l'acqua in
glucosio
, producendo l'
ossigeno
come un prodotto collaterale.
Gli esseri umani si basano sulla fotochimica per la
biosintesi
della
vitamina D
.
La
visione
avviene grazie ad una reazione fotochimica della
rodopsina
.
[1]
Nelle
lucciole
, un
enzima
nell'addome catalizza una reazione che si traduce in
bioluminescenza
.
[2]
Processi fotochimici sono utilizzati nella produzione delle
pellicole fotografiche
che e ricoperta da una gelatina contenente piccoli granuli di
bromuro di argento
che avvia la reazione quando la luce colpisce la pellicola. In questo caso il bromuro si dice "sensibilizzato". La reazione porta alla conversione del bromuro d'argento in argento metallico. Per eliminare le particelle di bromuro non sensibilizzato si utilizzano poi i cosiddetti "fissatori" o "fissaggi", delle sostanze chimiche.
Anche nella carta per
cianografie
, ricoperta di citrato di ferroammonio e ferricianuro, avviene una reazione fotochimica simile a quella delle pellicole fotografiche. I citrati, una volta colpiti dalla luce si trasformano in un ferricianuro di colore azzurro intenso.
Le reazioni fotochimiche sono non solo molto utili ma possono essere anche molto fastidiose o dannose, come nei casi di fotodegradazione di molti materiali. I tessuti scuri vengono ad esempio sbiaditi dalla luce del sole. I contenitori in vetro di farmaci sono spesso realizzati con vetro oscurato per evitare che la fotodegradazione dei farmaci.
Molte polimerizzazioni vengono avviate da
fotoiniziatori
che si decompongono assorbendo la luce per produrre i radicali liberi per la
polimerizzazione radicalica
.
Una reazione pervasiva e la generazione di
ossigeno singoletto
da reazioni fotosensibilizzate di ossigeno tripletto. Fotosensibilizzatori tipici includono il
tetrafenilporfirina
e
blu di metilene
. L'ossigeno singoletto che ne risulta e un ossidante aggressivo, capace di convertire legami CH in gruppi C-OH.
Nella
terapia fotodinamica
, la luce viene utilizzata per distruggere i tumori attraverso l'azione dell'ossigeno singoletto.
Una applicazione su larga scala della fotochimica e la tecnologia del
photoresist
, utilizzata nella produzione di componenti microelettronici.
 Vetreria Schlenk
Vetreria Schlenk
Le reazioni fotochimiche richiedono una sorgente di luce che emette lunghezze d'onda corrispondenti ad una transizione elettronica nel reagente. Nei primi esperimenti sulle reazioni fotochimiche, cosi come nella vita quotidiana, la fonte di luce era la luce solare, sebbene questa sia policromatica. In laboratorio sono comuni le
lampade a vapori di mercurio
. Le lampade a vapori di mercurio a bassa pressione emettono principalmente a 254 nm. Per le fonti policromatiche, le variazioni di lunghezza d'onda possono essere selezionate usando i filtri. In alternativa, le lampade a
LED
e i Rayonet producono emissioni monocromatiche.
La luce emessa deve ovviamente raggiungere il
gruppo funzionale
senza essere bloccata dal reattore o da altri gruppi funzionali presenti. Per molte applicazioni, il
quarzo
viene usato per i reattori e per contenere la lampada. Il
Pyrex
assorbe a lunghezze d'onda inferiori ai 275 nm. Il solvente e un importante parametro sperimentale. I solventi sono reagenti potenziali e per questo motivo i solventi clorurati vengono evitati perche il legame C-Cl puo portare alla
clorazione
del substrato. I solventi molto assorbenti possono prevenire il raggiungimento del substrato da parte dei fotoni. I solventi di idrocarburi assorbono solo a lunghezze d'onda corte e sono pertanto preferiti per gli esperimenti fotochimici che richiedono fotoni ad alta energia. I solventi contenenti
soluzioni sature
assorbono a lunghezze d'onda lunghe e possono filtrare le lunghezze d'onda corte.
- P. Atkins, J. De Paula,
"Physical Chemistry"
, Oxford University Press, 2006 (ottava ed.),
ISBN 978-0-19-870072-2
- V. Balzani, P. Ceroni, A. Juris,
"Photochemistry and Photophysics: concepts, research, applications",
Wiley, 2014,
ISBN 978-3-527-33479-7
- fotochimica
, su
Treccani.it ? Enciclopedie on line
,
Istituto dell'Enciclopedia Italiana
.

- (
EN
)
photochemistry
, su
Enciclopedia Britannica
, Encyclopædia Britannica, Inc.

- (
EN
)
IUPAC Gold Book, "photochemistry"
, su
goldbook.iupac.org
.
- Fotochimica
, in
Treccani.it ? Enciclopedie on line
, Roma, Istituto dell'Enciclopedia Italiana.