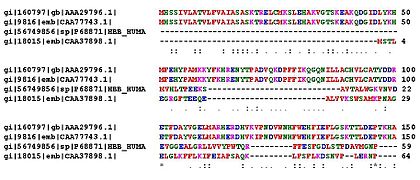
 Penyejajaran sekuens
(
Sequence alignment
), salah satu aplikasi dasar bioinformatika.
Sekuens
yang dianalisis dalam contoh ini adalah
asam amino
dari empat
protein
hemoglobin
.
Penyejajaran sekuens
(
Sequence alignment
), salah satu aplikasi dasar bioinformatika.
Sekuens
yang dianalisis dalam contoh ini adalah
asam amino
dari empat
protein
hemoglobin
.
Bioinformatika
(
bahasa Inggris
:
bioinformatics
) adalah
ilmu
yang mempelajari penerapan teknik
komputasional
untuk mengelola dan menganalisis informasi
biologis
.
[1]
Bidang ini mencakup penerapan metode-metode
matematika
,
statistika
, dan
informatika
untuk memecahkan masalah-masalah biologis, terutama dengan menggunakan sekuens
DNA
dan
asam amino
serta informasi yang berkaitan dengannya. Contoh topik utama bidang ini meliputi
basis data
untuk mengelola informasi biologis, penyejajaran sekuens (
sequence alignment
), prediksi struktur untuk meramalkan bentuk struktur
protein
maupun struktur sekunder
RNA
, analisis
filogenetik
, dan analisis ekspresi
gen
.
[2]
Istilah
bioinformatics
mulai dikemukakan pada pertengahan era
1980-an
untuk mengacu pada penerapan
komputer
dalam biologi. Namun, penerapan bidang-bidang dalam bioinformatika (seperti pembuatan basis data dan pengembangan
algoritme
untuk analisis
sekuens biologis
) sudah dilakukan sejak tahun
1960-an
.
Kemajuan teknik
biologi molekular
dalam mengungkap sekuens biologis dari protein (sejak awal
1950-an
) dan
asam nukleat
(sejak 1960-an) mengawali perkembangan basis data dan teknik analisis sekuens biologis. Basis data sekuens protein mulai dikembangkan pada tahun 1960-an di
Amerika Serikat
, sementara basis data sekuens DNA dikembangkan pada akhir 1970-an di Amerika Serikat dan
Jerman
(pada
European Molecular Biology Laboratory
, Laboratorium Biologi Molekular
Eropa
). Penemuan teknik
sekuensing
DNA yang lebih cepat pada pertengahan 1970-an menjadi landasan terjadinya ledakan jumlah sekuens DNA yang berhasil diungkapkan pada 1980-an dan
1990-an
, menjadi salah satu pembuka jalan bagi proyek-proyek pengungkapan
genom
, meningkatkan kebutuhan akan pengelolaan dan analisis sekuens, dan pada akhirnya menyebabkan lahirnya bioinformatika.
Perkembangan
Internet
juga mendukung berkembangnya bioinformatika. Basis data bioinformatika yang terhubung melalui Internet memudahkan ilmuwan mengumpulkan hasil sekuensing ke dalam basis data tersebut maupun memperoleh sekuens biologis sebagai bahan analisis. Selain itu, penyebaran
program
-program aplikasi bioinformatika melalui Internet memudahkan ilmuwan mengakses program-program tersebut dan kemudian memudahkan pengembangannya.
[3]
Sesuai dengan jenis informasi biologis yang disimpannya,
basis data
sekuens biologis dapat berupa basis data primer untuk menyimpan sekuens primer
asam nukleat
maupun
protein
, basis data sekunder untuk menyimpan motif sekuens protein, dan basis data struktur untuk menyimpan data struktur protein maupun asam nukleat.
Basis data utama untuk sekuens asam nukleat saat ini adalah
GenBank
(Amerika Serikat),
EMBL
(Eropa), dan
DDBJ
(Inggris)
(
DNA Data Bank of Japan
,
Jepang
). Ketiga basis data tersebut bekerja sama dan bertukar data secara harian untuk menjaga keluasan cakupan masing-masing basis data. Sumber utama data sekuens asam nukleat adalah submisi langsung dari periset individual, proyek sekuensing
genom
, dan pendaftaran
paten
. Selain berisi sekuens asam nukleat, entri dalam basis data sekuens asam nukleat umumnya mengandung informasi tentang jenis asam nukleat (
DNA
atau
RNA
), nama
organisme
sumber asam nukleat tersebut, dan pustaka yang berkaitan dengan sekuens asam nukleat tersebut.
Sementara itu, contoh beberapa basis data penting yang menyimpan sekuens primer protein adalah
PIR
[
pranala nonaktif permanen
]
(
Protein Information Resource
, Amerika Serikat),
Swiss-Prot
(Eropa), dan
TrEMBL
(Eropa). Ketiga basis data tersebut telah digabungkan dalam
UniProt
(yang didanai terutama oleh Amerika Serikat). Entri dalam UniProt mengandung informasi tentang sekuens protein, nama organisme sumber protein, pustaka yang berkaitan, dan komentar yang umumnya berisi penjelasan mengenai fungsi protein tersebut.
[4]
BLAST
(
Basic Local Alignment Search Tool
) merupakan perkakas bioinformatika yang berkaitan erat dengan penggunaan basis data sekuens biologis. Penelusuran BLAST (
BLAST search
) pada basis data sekuens memungkinkan ilmuwan untuk mencari sekuens asam nukleat maupun protein yang mirip dengan sekuens tertentu yang dimilikinya. Hal ini berguna misalnya untuk menemukan
gen
sejenis pada beberapa
organisme
atau untuk memeriksa keabsahan hasil
sekuensing
maupun untuk memeriksa fungsi gen hasil sekuensing.
Algoritme
yang mendasari kerja BLAST adalah penyejajaran sekuens.
[2]
PDB
Diarsipkan
2008-08-28 di
Wayback Machine
. (
Protein Data Bank
, Bank Data Protein) adalah basis data tunggal yang menyimpan model struktural tiga dimensi
protein
[4]
dan
asam nukleat
hasil penentuan eksperimental (dengan
kristalografi sinar-X
,
spektroskopi NMR
dan
mikroskopi elektron
). PDB menyimpan data struktur sebagai
koordinat tiga dimensi
yang menggambarkan posisi
atom
-atom dalam protein ataupun asam nukleat.
Penyejajaran sekuens
(
sequence alignment
) adalah proses penyusunan/pengaturan dua atau lebih
sekuens
sehingga persamaan sekuens-sekuens tersebut tampak nyata. Hasil dari proses tersebut juga disebut sebagai
sequence alignment
atau
alignment
saja. Baris sekuens dalam suatu
alignment
diberi sisipan (umumnya dengan tanda "?") sedemikian rupa sehingga kolom-kolomnya memuat karakter yang identik atau sama di antara sekuens-sekuens tersebut. Berikut adalah contoh
alignment
DNA dari dua sekuens pendek DNA yang berbeda, "ccatcaac" dan "caatgggcaac" (tanda "|" menunjukkan kecocokan atau
match
di antara kedua sekuens).
ccat---caac
| || ||||
caatgggcaac
Sequence alignment
merupakan metode dasar dalam analisis sekuens. Metode ini digunakan untuk mempelajari
evolusi
sekuens-sekuens dari leluhur yang sama (
common ancestor
). Ketidakcocokan (
mismatch
) dalam
alignment
diasosiasikan dengan proses
mutasi
, sedangkan kesenjangan (
gap
, tanda "?") diasosiasikan dengan proses insersi atau delesi.
Sequence alignment
memberikan
hipotesis
atas proses
evolusi
yang terjadi dalam sekuens-sekuens tersebut. Misalnya, kedua sekuens dalam contoh
alignment
di atas bisa jadi berevolusi dari sekuens yang sama "ccatgggcaac". Dalam kaitannya dengan hal ini,
alignment
juga dapat menunjukkan posisi-posisi yang dipertahankan (
conserved
) selama evolusi dalam sekuens-sekuens
protein
, yang menunjukkan bahwa posisi-posisi tersebut bisa jadi penting bagi struktur atau fungsi protein tersebut.
Selain itu,
sequence alignment
juga digunakan untuk mencari sekuens yang mirip atau sama dalam
basis data
sekuens. BLAST adalah salah satu metode
alignment
yang sering digunakan dalam penelusuran basis data sekuens. BLAST menggunakan algoritme
heuristik
dalam penyusunan
alignment
.
Beberapa metode
alignment
lain yang merupakan pendahulu BLAST adalah metode "Needleman-Wunsch" dan "Smith-Waterman". Metode Needleman-Wunsch digunakan untuk menyusun
alignment
global
di antara dua atau lebih sekuens, yaitu
alignment
atas keseluruhan panjang sekuens tersebut. Metode Smith-Waterman menghasilkan
alignment
lokal
, yaitu alignment atas bagian-bagian dalam sekuens. Kedua metode tersebut menerapkan
pemrograman dinamik
(
dynamic programming
) dan hanya efektif untuk
alignment
dua sekuens (
pairwise alignment
)
Clustal adalah program bioinformatika untuk
alignment
multipel (
multiple alignment
), yaitu
alignment
beberapa sekuens sekaligus. Dua varian utama Clustal adalah
ClustalW
dan
ClustalX
[
pranala nonaktif permanen
]
.
Metode lain yang dapat diterapkan untuk
alignment
sekuens adalah metode yang berhubungan dengan
Hidden Markov Model
("Model Markov Tersembunyi",
HMM
). HMM merupakan model statistika yang mulanya digunakan dalam
ilmu komputer
untuk mengenali pembicaraan manusia (
speech recognition
). Selain digunakan untuk alignment, HMM juga digunakan dalam metode-metode analisis sekuens lainnya, seperti prediksi daerah pengkode protein dalam
genom
dan prediksi struktur sekunder protein.
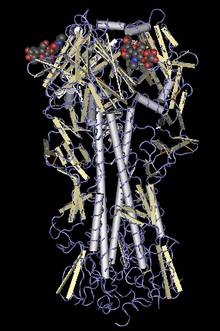 Model protein
hemaglutinin
dari
virus
influensa
Model protein
hemaglutinin
dari
virus
influensa
Secara kimia/fisika, bentuk struktur
protein
diungkap dengan
kristalografi sinar-X
ataupun
spektroskopi NMR
, namun kedua metode tersebut sangat memakan waktu dan relatif mahal. Sementara itu, metode
sekuensing
protein relatif lebih mudah mengungkapkan
sekuens
asam amino
protein.
[4]
Prediksi struktur protein berusaha meramalkan struktur tiga dimensi protein berdasarkan sekuens asam aminonya (dengan kata lain, meramalkan struktur tersier dan struktur sekunder berdasarkan struktur primer protein). Secara umum, metode prediksi struktur protein yang ada saat ini dapat dikategorikan ke dalam dua kelompok, yaitu metode pemodelan protein komparatif dan metode pemodelan
de novo
.
Pemodelan protein komparatif
(
comparative protein modelling
) meramalkan struktur suatu protein berdasarkan struktur protein lain yang sudah diketahui. Salah satu penerapan metode ini adalah
pemodelan homologi
(
homology modelling
), yaitu prediksi struktur tersier protein berdasarkan kesamaan struktur primer protein. Pemodelan homologi didasarkan pada
teori
bahwa dua protein yang
homolog
memiliki struktur yang sangat mirip satu sama lain. Pada metode ini, struktur suatu protein (disebut protein target) ditentukan berdasarkan struktur protein lain (protein templat) yang sudah diketahui dan memiliki kemiripan sekuens dengan protein target tersebut. Selain itu, penerapan lain pemodelan komparatif adalah
protein threading
yang didasarkan pada kemiripan struktur tanpa kemiripan sekuens primer. Latar belakang
protein threading
adalah bahwa struktur protein lebih dikonservasi daripada sekuens protein selama evolusi; daerah-daerah yang penting bagi fungsi protein dipertahankan strukturnya. Pada pendekatan ini, struktur yang paling kompatibel untuk suatu sekuens asam amino dipilih dari semua jenis struktur tiga dimensi protein yang ada. Metode-metode yang tergolong dalam
protein threading
berusaha menentukan tingkat kompatibilitas tersebut.
Dalam pendekatan
de novo
atau
ab initio
, struktur protein ditentukan dari sekuens primernya tanpa membandingkan dengan struktur protein lain. Terdapat banyak kemungkinan dalam pendekatan ini, misalnya dengan menirukan proses pelipatan (
folding
) protein dari sekuens primernya menjadi struktur tersiernya (misalnya dengan simulasi
dinamika molekular
), atau dengan optimisasi global fungsi energi protein. Prosedur-prosedur ini cenderung membutuhkan proses komputasi yang intens, sehingga saat ini hanya digunakan dalam menentukan struktur protein-protein kecil. Beberapa usaha telah dilakukan untuk mengatasi kekurangan sumber daya komputasi tersebut, misalnya dengan
superkomputer
(misalnya superkomputer
Blue Gene
[1]
dari
IBM
) atau
komputasi terdistribusi
(
distributed computing
, misalnya proyek
Folding@home
Diarsipkan
2012-09-08 di
Wayback Machine
.) maupun
komputasi grid
.
 Analisis klastering ekspresi gen pada
kanker payudara
Analisis klastering ekspresi gen pada
kanker payudara
Ekspresi gen
dapat ditentukan dengan mengukur kadar
mRNA
dengan berbagai macam teknik (misalnya dengan
microarray
ataupun
Serial Analysis of Gene Expression
["Analisis Serial Ekspresi Gen", SAGE]). Teknik-teknik tersebut umumnya diterapkan pada analisis ekspresi gen skala besar yang mengukur ekspresi banyak
gen
(bahkan
genom
) dan menghasilkan data skala besar. Metode-metode penggalian data (
data mining
) diterapkan pada data tersebut untuk memperoleh pola-pola informatif. Sebagai contoh, metode-metode komparasi digunakan untuk membandingkan ekspresi di antara gen-gen, sementara metode-metode klastering (
clustering
) digunakan untuk mempartisi data tersebut berdasarkan kesamaan ekspresi gen.
Terdapat sejumlah perangkat lunak gratis dan sumber terbuka yang telah ada dan terus berkembang sejak 1980-an.
[5]
Beberapa paket perangkat lunak sumber terbuka yang tersedia, antara lain
Bioconductor
,
BioPerl
,
Biopython
,
BioJava
,
BioJS
,
BioRuby
,
Bioclipse
,
EMBOSS
,
.NET Bio
,
Orange
,
Apache Taverna
,
UGENE
, dan
GenoCAD
.
Saat ini mata ajaran bioinformatika maupun mata ajaran dengan muatan bioinformatika sudah diajarkan di beberapa
perguruan tinggi
di
Indonesia
.
Sekolah Ilmu dan Teknologi Hayati
ITB
menawarkan mata kuliah "Pengantar Bioinformatika" untuk program Sarjana dan mata kuliah "Bioinformatika" untuk program Pascasarjana.
Fakultas Matematika dan Ilmu Pengetahuan Alam, IPB
menyelenggarakan mata kuliah interdept "Pengantar Bioinformatika" yang wajib diambil oleh mahasiswa program sarjana Ilmu Komputer, Biologi, dan Biokimia. Selain itu pada program
pascasarjana Ilmu Komputer, FMIPA, IPB
tersedia mata kuliah pilihan "Topik dalam Bioinformatika". Fakultas Teknobiologi
Universitas Atma Jaya
,
Jakarta
menawarkan mata kuliah "Pengantar Bioinformatika" sebagai mata kuliah wajib dan "Pemodelan Struktur Protein" sebagai mata kuliah pilihan untuk tingkat program Sarjana. Fakultas Teknobiologi
Universitas Atma Jaya Yogyakarta
(UAJY) menyertakan Mata Kuliah "Bioinformatika" dalam mata kuliah wajib tingkat program Sarjana. Mata kuliah "Bioinformatika" diajarkan pada Program Pascasarjana Kimia Fakultas MIPA
Universitas Indonesia
(UI), Jakarta. Mata kuliah "Proteomik dan Bioinformatika" termasuk dalam kurikulum program S3 bioteknologi
Universitas Gadjah Mada
(UGM),
Yogyakarta
. Materi bioinformatika termasuk di dalam silabus beberapa mata kuliah untuk program
sarjana
maupun
pascasarjana
biokimia,biologi, dan bioteknologi pada
Institut Pertanian Bogor
(IPB). Selain itu, riset-riset yang mengarah pada bioinformatika juga telah dilaksanakan oleh mahasiswa program S1 dan pascasarjana Ilmu Komputer maupun program pascasarjana biologi serta bioteknologi IPB.
Riset bioinformatika protein dilaksanakan sebagai bagian dari aktivitas riset rekayasa protein pada Laboratorium Rekayasa Protein, Pusat Penelitian Bioteknologi
Lembaga Ilmu Pengetahuan Indonesia
(LIPI),
Cibinong
,
Bogor
.
Lembaga Biologi Molekul Eijkman
, Jakarta, secara khusus memiliki laboratorium bioinformatika sebagai fasilitas penunjang kegiatan risetnya. Selain itu, basis data sekuens DNA
mikroorganisme
asli Indonesia sedang dikembangkan di UI. Adapun di
Pusat Studi Biofarmaka Tropika (TropBRC), LPPM, IPB
riset bioinformatika digunakan untuk mendukung riset pengembangan obat dari bahan alam (biofarmaka).
- ^
Susilawati dan Bachtiar, N. (2018).
Biologi Dasar Terintegrasi
(PDF)
. Pekanbaru: Kreasi Edukasi. hlm. 4.
ISBN
978-602-6879-99-8
.
Diarsipkan
(PDF)
dari versi asli tanggal 2021-04-15
. Diakses tanggal
2021-01-30
.
- ^
a
b
Apsari, Gadis Retno; Adawiyah, Robiah; Linatari, Mey Ayu; Rahmayadi, Dessy; Pradana, Mohammad Syaiful (2023).
Bioinformatika: Analisis Pensejajaran Sequence
(PDF)
. Pustaka Ilalang.
ISBN
978-602-6715-37-1
.
- ^
Subekti, Hasan; Handriyan, Aris; Purnomo, Aris Rudi; Wulandari, Fitria Eka; Widiansyah, Arindra Trisn (2019).
BIOTEKNOLOGI: SEBUAH PEMBELAJARAN TERINTEGRASI STEM PADA MATA KULIAH BIOTEKNOLOGI BAGI MAHASISWA CALON GURU IPA
. Gresik: Graniti.
ISBN
978-602-5811-26-5
.
- ^
a
b
c
Pathak, Rajesh Kumar; Singh, Dev Bukhsh; Singh, Rahul (2022).
Introduction to basics of bioinformatics
. Elsevier. hlm. 1?15.
- ^
"Open Bioinformatics Foundation: About us"
.
Official website
.
Open Bioinformatics Foundation
.
Diarsipkan
dari versi asli tanggal 2011-05-12
. Diakses tanggal
10 May
2011
.
- (Inggris)
Attwood, T.K.; Parry-Smith, D.J. (1999),
Introduction to Bioinformatics
, Harlow: Pearson Education,
ISBN
0-582-32788-1
- (Inggris)
Krane, D.E.; Raymer, M.L. (2003),
Fundamental Concepts of Bioinformatics
, San Francisco: Benjamin Cummings,
ISBN
0-8053-4633-3
- (Inggris)
Mount, D.W. (2001),
Bioinformatics: Sequence and Genome Analysis
, Cold Spring Harbor: Cold Spring Harbor Laboratory Press,
ISBN
0-87969-608-7