| Artikel ini perlu
diterjemahkan
dari
bahasa Inggris
ke bahasa Indonesia.
Artikel ini ditulis atau diterjemahkan secara
buruk
dari Wikipedia
bahasa Inggris
. Jika halaman ini ditujukan untuk komunitas
bahasa Inggris
, halaman itu harus dikontribusikan ke
Wikipedia bahasa Inggris
. Lihat
daftar bahasa Wikipedia
.
Artikel yang tidak diterjemahkan dapat dihapus secara cepat
sesuai kriteria A2
.
Jika Anda ingin memeriksa artikel ini, Anda boleh menggunakan mesin penerjemah. Namun ingat,
mohon tidak menyalin hasil terjemahan tersebut ke artikel, karena umumnya merupakan terjemahan berkualitas rendah
.
|
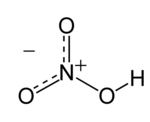
Asam nitrat
|
|
|
| Nama
|
| Nama IUPAC
Asam nitrat
|
| Nama lain
Hidrogen Nitrat
|
| Penanda
|
|
|
|
|
|
|
| 3DMet
|
{{{3DMet}}}
|
| Nomor EC
|
|
|
|
|
| Nomor RTECS
|
{{{value}}}
|
|
|
|
InChI=1S/HNO3/c2-1(3)4/h(H,2,3,4)
|
|
|
| Sifat
|
|
|
H
NO
3
|
| Massa molar
|
63,012 g/mol
|
| Penampilan
|
Cairan bening tidak berwarna
|
| Densitas
|
1,51 g/cm³ (20 °C)
|
| Titik lebur
|
?42 °C (231 K)
|
| Titik didih
|
83 °C (356 K)
|
|
|
tercampurkan
|
| Viskositas
|
1,092 mPa.s (0 °C); 0,746 mPa.s (25 °C); 0,617 mPa.s (40 °C)
|
|
|
2,17 ± 0,02
D
|
| Bahaya
|
|
|
Oksidan (
O
)
Korosif (
C
)
|
| Frasa-R
|
R8
,
R35
|
| Frasa-S
|
(S1/2)
,
S23
,
S26
,
S36
,
S45
|
| Titik nyala
|
tidak tersedia
|
| Senyawa terkait
|
|
|
| Referensi
|
|
|
|
Senyawa kimia
asam nitrat
(
H
N
O
3
) adalah sejenis
cairan
korosif
yang tak berwarna, dan merupakan
asam
beracun
yang dapat menyebabkan luka bakar.
Larutan
asam nitrat dengan kandungan asam nitrat lebih dari 86% disebut sebagai
asam nitrat berasap
, dan dapat dibagi menjadi dua jenis asam, yaitu
asam nitrat berasap putih
dan
asam nitrat berasap merah
.
Asam nitrat pertama kali disintesis sekitar
800
M
oleh
alkimiawan
Jabir ibnu Hayyan
, yang juga menemukan
distilasi
modern dan proses kimiawi dasar lainnya yang masih digunakan sekarang ini.
Asam nitrat adalah larutan
asam kuat
yang mempunyai nilai
pKa
sebesar -2. Di dalam air, asam ini
terdisosiasi
menjadi ion-ionnya, yaitu
ion
nitrat
NO
3
?
dan ion
hidronium
(H
3
O
+
). Garam dari asam nitrat disebut sebagai garam nitrat (contohnya seperti kalsium nitrat atau barium nitrat).
Dalam temperatur ruangan, asam nitrat berbentuk uap berwarna merah atau kuning.
Asam nitrat dan garam nitrat adalah sesuatu yang berbeda dengan
asam nitrit
dan garamnya,
garam nitrit
.
Asam nitrat murni (100%) merupakan cairan tak berwarna dengan berat jenis 1.522 kg/m³. Ia membeku pada suhu -42 °C, membentuk kristal-kristal putih, dan mendidih pada 83 °C. Ketika mendidih pada suhu kamar, terdapat dekomposisi (penguraian) sebagian dengan pembentukan nitrogen dioksida sesudah reaksi:
- 4HNO
3
→ 2H
2
O + 4NO
2
+ O
2
(72 °C)
yang berarti bahwa asam nitrat anhidrat sebaiknya disimpan di bawah 0 °C untuk menghindari penguraian. Nitrogen dioksida (NO
2
) tetap larut dalam asam nitrat yang membuatnya berwarna kuning, atau merah pada suhu yang lebih tinggi. Manakala asam murni cenderung mengeluarkan asap putih ketika terpapar ke udara, asam dengan nitrogen dioksida terlarut mengeluarkan uap berwarna coklat kemerah-merahan, yang membuatnya dijuluki "asam berasap merah" atau "asam nitrat berasap". Asam nitrat berasap juga dirujuk sebagai asam nitrat 16
molar
(bentuk paling pekat asam nitrat pada
temperatur dan tekanan standar
).
Asam nitrat bercampur dengan air dalam berbagai proporsi dan
distilasi
menghasilkan azeotrop dengan konsentrasi 68% HNO
3
dan titik didih 120,5 °C pada 1
atm
. Terdapat dua hidrat padat yang diketahui, yaitu monohidrat (HNO
3
·H
2
O) dan trihidrat (HNO
3
·3H
2
O).
Nitrogen oksida (NO
x
) larut dalam asam nitrat dan sifat ini memengaruhi semua sifat fisik asam nitrat yang bergantung pada konsentrasi oksida (seperti tekanan uap di atas cair, suhu didih, dan warna yang dijelaskan di atas).
Peningkatan konsentrasi asam nitrat dipengaruhi oleh penguraian termal maupun cahaya, dan hal ini dapat menimbulkan sejumlah variasi yang tak dapat diabaikan pada tekanan uap di atas cairan karena nitrogen oksida yang dihasilkan akan terlarut sebagian atau sepenuhnya di dalam asam.
Sebagai mana asam pada umumnya, asam nitrat bereaksi dengan alkali, oksida basa, dan karbonat untuk membentuk
garam
, seperti amonium nitrat. Karena memiliki sifat mengoksidasi, asam nitrat pada umumnya tidak menyumbangkan protonnya (yakni, ia tidak membebaskan hidrogen) pada reaksi dengan logam dan garam yang dihasilkan biasanya berada dalam keadaan teroksidasi yang lebih tinggi.Karenanya, perkaratan (
korosi
) tingkat berat bisa terjadi. Perkaratan bisa dicegah dengan penggunaan logam ataupun aloi anti karat yang tepat.
Asam nitrat memiliki
tetapan disosiasi asam
(pK
a
) 1,4: dalam
larutan
akuatik, asam nitrat hampir sepenuhnya (93% pada 0.1 mol/L) terionisasi menjadi
ion
nitrat NO
3
dan
proton
terhidrasi yang dikenal sebagai ion hidronium, H
3
O
+
.
HNO
3
+ H
2
O → H
3
O
+
+ NO
3
-
Sebagai sebuah oksidator yang kuat, asam nitrat bereaksi dengan hebat dengan sebagian besar bahan-bahan organik dan reaksinya dapat bersifat eksplosif. Produk akhirnya bisa bervariasi tergantung pada konsentrasi asam, suhu, serta reduktor. Reaksi dapat terjadi dengan semua logam kecuali deret logam mulia dan aloi tertentu. Karakteristik ini membuat asam nitrat menjadi agen yang umumnya digunakan dalam uji asam. Sebagai kaidah yang umum, reaksi oksidasi utamanya terjadi dengan asam pekat, memfavoritkan pembentukan nitrogen dioksida (NO
2
).
Cu + 4H
+
+ 2NO
3
-
→ Cu
+2
+ 2NO
2
+ 2H
2
O
Sifat-sifat asam cenderung mendominasi pada asam nitrat encer, diikuti dengan pembentukan nitrogen oksida (NO) yang lebih diutamakan.
3Cu + 8HNO
3
→ 3Cu(NO
3
)
2
+ 2NO + 4H
2
O
Karena asam nitrat merupakan oksidator,
hidrogen
(H
2
) jarang terbentuk. Hanya
magnesium
(Mg),
mangan
(Mn), dan
kalsium
(Ca) yang bereaksi dengan asam nitrat
dingin
dan
encer
yang dapat menghasilkan hidrogen:
Mg
(s)
+ 2HNO
3
(aq)
→ Mg(NO
3
)
2
(aq)
+ H
2
(g)
Asam nitrat mampu menyerang dan melarutkan semua logam yang ada pada tabel periodik, kecuali
emas
dan
platina
.
Kendati
kromium
(Cr),
besi
(Fe), dan
aluminium
(Al) akan terlarut dalam asam nitrat yang encer, asam pekat akan membentuk sebuah lapisan logam oksida yang melindungi logam dari oksidasi lebih lanjut. Hal ini disebut dengan pemasifan. Konsentrasi pemasifan yang umum berkisar dari 18% sampai 22% berat.
Ketika asam nitrat bereaksi dengan berbagai unsur non-logam, terkecuali silikon serta halogen, biasanya ia akan mengoksidasi non-logam tersebut ke keadaan oksidasi tertinggi dengan asam nitrat menjadi nitrogen dioksida untuk asam pekat dan nitrogen monoksida untuk asam encer.
C + 4HNO
3
→ CO
2
+ 4NO
2
+ 2H
2
O
ataupun
3C + 4HNO
3
→ 3CO
2
+ 4NO + 2H
2
O
Asam nitrat dibuat dengan mencampur
nitrogen dioksida
(
N
O
2
) dengan
air
. Menghasilkan asam nitrat yang sangat murni biasanya melibatkan distilasi dengan
asam sulfat
, karena asam nitrat membentuk sebuah
azeotrop
dengan air dengan komposisi 68% asam nitrat dan 32% air. Asam nitrat kualitas komersial biasanya memiliki konsentrasi antara 52% dan 68% asam nitrat. Produksi komersial dari asam nitrat melalui
proses Ostwald
yang ditemukan oleh
Wilhelm Ostwald
.
Asam nitrat dapat dibuat dengan mereaksikan 200 gram
potasium nitrat
(KNO
3
) ke dalam larutan
asam sulfat
(H
2
SO
4
) 96% 106 ml, kemudian mendistilasi campuran ini di titik didih asam nitrat (83 °C) sampai hanya tersisa kristal putih
potasium hidrogen sulfat
(KHSO
4
), di tabung reaksinya.
Asam nitrat biasanya digunakan di laboratorium sebagai
reagen
. Larutan ini juga dipakai untuk memproduksi bahan-bahan yang meledak seperti
nitrogliserin
,
trinitrotoluena
(TNT) dan
Siklotrimetilenatrinitramin
(RDX), dan juga untuk pembuatan
amonium nitrat
.
Asam nitrat juga digunakan di bagian
metalurgi
dan
pengilangan
karena dapat bereaksi dengan
metal
. Ketika dicampurkan dengan
asam klorida
, maka campuran ini akan membentuk
aqua regia
, satu dari sedikit reagen yang dapat melarutkan
emas
dan
platinum
.
Asam nitrat juga merupakan komponen dari
hujan asam
.
|
|---|
| Umum
| |
|---|
| Perpustakaan nasional
| |
|---|
| Lain-lain
| |
|---|