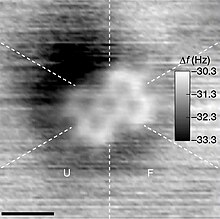
 Citra
mikroskop gaya atom
(AFM) molekul
perilenatetrakarboksilat dianhidrida
(PTCDA), yang mengandung gugus karbon cincin lima.
[1]
Citra
mikroskop gaya atom
(AFM) molekul
perilenatetrakarboksilat dianhidrida
(PTCDA), yang mengandung gugus karbon cincin lima.
[1]
 Citra
mikroskop penerowongan payaran
molekul
pentasena
, yang mengandung rantai lurus dari karbon cincin lima.
[2]
Citra
mikroskop penerowongan payaran
molekul
pentasena
, yang mengandung rantai lurus dari karbon cincin lima.
[2]
 Citra AFM 1,5,9-triokso-13-azatriangulena beserta struktur kimianya.
[3]
Citra AFM 1,5,9-triokso-13-azatriangulena beserta struktur kimianya.
[3]
Molekul
sederhananya adalah dua atau lebih
atom
yang saling terikat bersama dan diikat oleh
ikatan kimia
. Mereka merupakan
gugusan
yang secara
elektris
netral.
[4]
[5]
[6]
[7]
[8]
Molekul dibedakan dari ion berdasarkan ketiadaan
muatan listrik
. Namun, dalam
fisika kuantum
,
kimia organik
, dan
biokimia
, istilah
molekul
sering digunakan dengan agak longgar, juga digunakan untuk
ion poliatomik
.
Dalam
teori kinetika gas
, istilah
molekul
sering digunakan untuk
partikel
gas apapun tanpa memperdulikan komposisinya. Menurut definisi ini, atom
gas mulia
dianggap sebagai molekul sebagai molekul monoatomik.
[9]
Suatu molekul dapat
homonuklir
, yaitu, mengandung atom-atom dari satu
unsur kimia
, misalnya
oksigen
(O
2
); atau dapat pula berupa
heteronuklir
, suatu
senyawa kimia
yang tersusun dari lebih dari satu unsur, misalnya
air
(H
2
O). Atom dan kompleks yang terhubung melalui
ikatan non kovalen
, seperti
ikatan hidrogen
atau
ikatan ionik
, umumnya dianggap sebagai molekul tunggal.
[10]
Molekul sebagai komponen materi jamak terdapat dalam zat organik (dan biokimia tentunya). Mereka menyusun sebagian besar samudera dan atmosfer. Namun, mayoritas zat padat yang kita kenal di Bumi, termasuk sebagian besar mineral yang membentuk
kerak
,
mantel
, dan
inti bumi
, mengandung banyak ikatan kimia, tetapi
tidak
tersusun dari molekul yang dapat diidentifikasi. Selain itu, tidak ada molekul yang khas yang dapat didefinisikan sebagai
kristal ionik
(
garam
) dan kristal kovalen (
padatan jaringan kovalen
,
network solid
), meskipun ini sering tersusun dari
sel unit
yang berulang sehingga membentuk
bidang
(seperti dalam
grafena
) atau tiga dimensi (seperti
intan
,
kuarsa
, atau
natrium klorida
). Tema struktur sel unit yang berulang juga berlaku untuk sebagian besar fase paling padat dengan
ikatan logam
, yang artinya bahwa logam padat juga tidak terbuat dari molekul. Dalam
kaca
(zat padat yang berada dalam keadaan vitreous tak teratur), atom-atom juga dapat disatukan oleh ikatan kimia tanpa adanya molekul definitif apapun, maupun tanpa adanya keterulangan unit yang teratur seperti pada kristal.
Sains molekul disebut
kimia molekular
atau
fisika molekular
, tergantung fokusnya apakah fokus pada kimia atau fisika. Kimia molekular berurusan dengan hukum-hukum yang mengatur interaksi antara molekul yang menghasilkan pembentukan dan pemecahan
ikatan kimia
, sementara fisika molekular berurusan dengan hukum-hukum yang mengatur struktur dan sifat-sifatnya. Namun pada prakteknya, perbedaan ini tidak tegas. Dalam sains molekular, suatu molekul terdiri dari suatu sistem stabil (
keadaan ikatan
[
en
]
yang tersusun dari dua atau lebih
atom
.
Ion poliatomik
kadang-kadang dapat dianggap sebagai molekul bermuatan listrik. Istilah
molekul tak stabil
digunakan untuk molekul yang sangat
reaktif
, yaitu pemasangan jangka pendek (
resonansi
) elektron dan
inti atom
, seperti
radikal
,
ion-ion
molekul,
molekul Rydberg
,
keadaan transisi
,
kompleks van der Waals
, atau sistem dari tumbukan atom seperti
kondensat Bose?Einstein
.
Menurut
Merriam-Webster
dan
Online Etymology Dictionary
, istilah "
molecule
" diturunkan dari the
bahasa Latin
"
moles
" atau unit kecil massa.
- Molecule
(1794) ? "partikel yang teramat halus", dari bahasa Prancis
molecule
(1678), dari bahasa
Neo-Latin
molecula
, kecil dari bahasa Latin
moles
"massa, penghalang". Awal maknanya samar-samar; mode kata (digunakan sampai akhir abad 18 hanya dalam bentuk Latin) dapat ditelusuri ke filsafat
Descartes
.
[11]
[12]
Definisi molekul telah berkembang seiring peningkatan pengetahuan tentang struktur molekul. Definisi sebelumnya kurang tepat, mendefinisikan molekul sebagai "
partikel
terkecil dari
zat kimia
murni yang masih mempertahankan
komposisi
dan sifat kimianya".
[13]
Definisi ini sering terpatahkan karena banyak zat dalam kehidupan sehari-hari, seperti
batuan
,
garam
, dan
logam
, terdiri dari jaringan kristal besar dari atom atau ion yang
berikatan secara kimia
, tetapi tidak terbuat dari molekul diskrit.
Molekul disatukan oleh
ikatan kovalen
atau
ikatan ion
. Beberapa jenis unsur nonlogam hanya ada sebagai molekul di lingkungan. Sebagai contoh, hidrogen hanya ada sebagai molekul hidrogen. Sebuah molekul senyawa terbuat dari dua unsur atau lebih.
[14]
 Pembentukan ikatan kovalen H
2
(kanan) di mana dua
atom hidrogen
berbagi dua elektron.
Pembentukan ikatan kovalen H
2
(kanan) di mana dua
atom hidrogen
berbagi dua elektron.
Ikatan kovalen adalah
ikatan kimia
yang melibatkan pembagian
pasangan elektron
di antara
atom
. Pasangan elektron ini disebut
pasangan bersama
atau
pasangan ikatan
, dan keseimbangan stabil dari gaya tarik dan tolak antar atom, ketika mereka berbagi elektron hal itu disebut
ikatan kovalen
.
[15]
 Natrium
dan
fluor
yang sedang mengalami reaksi redoks membentuk
natrium fluorida
. Natrium kehilangan
elektron
terluarnya untuk memperoleh
konfigurasi elektron
stabilnya, dan elektron ini memasuki atom fluor secara
eksotermal
.
Natrium
dan
fluor
yang sedang mengalami reaksi redoks membentuk
natrium fluorida
. Natrium kehilangan
elektron
terluarnya untuk memperoleh
konfigurasi elektron
stabilnya, dan elektron ini memasuki atom fluor secara
eksotermal
.
Ikatan ionik adalah sejenis
ikatan kimia
yang melibatkan daya tarik
elektrostatik
antara ion dengan muatan berlawanan, dan merupakan interaksi utama yang terjadi pada
senyawa ionik
. Ion adalah atom yang telah kehilangan satu atau lebih
elektron
(disebut
kation
) dan atom yang telah mendapatkan satu atau lebih elektron (disebut
anion
).
[16]
Transfer elektron ini disebut
elektrovalensi
yang merupakan lawan dari
kovalensi
. Dalam kasus yang paling sederhana, kation adalah atom
logam
dan anion adalah atom
nonlogam
, tetapi ion ini bisa menjadi lebih rumit, misalnya, ion molekuler seperti
NH
+
4
atau
SO
2?
4
. Sederhananya, ikatan ionik adalah transfer elektron dari logam ke nonlogam agar kedua atom mendapatkan kelopak valensi yang terisi penuh.
Kebanyakan molekul terlalu kecil untuk dilihat dengan mata telanjang, tapi terdapat pengecualian.
DNA
, sebuah
makromolekul
, dapat mencapai ukuran
makroskopis
, seperti kebanyakan molekul
polimer
. Molekul yang biasa digunakan sebagai blok pembangun untuk sintesis organik memiliki dimensi beberapa
angstrom
(A) sampai beberapa ratus A, atau sekitar seper satu miliar meter. Molekul tunggal biasanya tidak dapat diamati oleh
cahaya
(seperti disebutkan di atas), tetapi molekul kecil dan bahkan kerangka atom dapat ditelusuri dalam beberapa keadaan dengan menggunakan
mikroskop gaya atom
. Beberapa molekul terbesar adalah
makromolekul
atau
supermolekul
.
Molekul terkecil adalah hidrogen
diatomik
(H
2
), dengan panjang ikatan 0,74 A.
[17]
Jari-jari molekul yang efektif adalah ukuran yang ditunjukkan molekul dalam larutan.
[18]
[19]
Tabel permselektivitas berbagai zat
[
en
]
berisi contoh-contoh ini.
Rumus kimia
untuk molekul menggunakan satu baris simbol
unsur kimia
, angka, dan terkadang juga simbol lainnya, seperti tanda kurung, tanda hubung (
dash
), tanda kurung siku, dan tanda
plus
(+) dan
minus
(?). Ini terbatas pada satu baris tipografi simbol, yang mungkin mencakup subskrip dan superskrip.
Rumus empiris
senyawa adalah jenis rumus kimia yang sangat sederhana.
[20]
Ini adalah
rasio
bilangan bulat
paling sederhana dari
unsur kimia
pembentuknya.
[21]
Sebagai contoh, air selalu terdiri dari rasio 2:1 atom
hidrogen
terhadap atom
oksigen
, dan etil
alkohol
atau
etanol
selalu terdiri dari
karbon
,
hidrogen
, dan
oksigen
dalam rasio 2:6:1. Namun, ini tidak menentukan jenis molekul secara unik?
dimetil eter
memiliki rasio yang sama seperti etanol, misalnya. Molekul dengan atom yang sama dalam susunan yang berbeda disebut
isomer
. Juga karbohidrat, misalnya, memiliki rasio yang sama (karbon:hidrogen:oksigen = 1:2:1) (dan dengan demikian rumus empiris yang sama) namun jumlah atom dalam molekulnya berbeda.
Rumus molekul
mencerminkan jumlah atom yang tepat yang membentuk molekul dan mengkarakterisasi molekul yang berbeda. Namun isomer yang berbeda dapat memiliki komposisi atom yang sama saat menjadi molekul yang berbeda.
Rumus empiris sering kali sama dengan rumus molekul tapi tidak selalu. Sebagai contoh, molekul
asetilena
memiliki rumus molekul C
2
H
2
, tetapi rasio unsur yang paling sederhana adalah CH.
Massa molekul
dapat dihitung dari
rumus kimia
dan dinyatakan dalam
satuan massa atom
konvensional sama dengan 1/12 massa atom karbon-12 (
isotop
12
C
) netral. Untuk
padatan jaringan
, istilah
unit rumus
digunakan dalam perhitungan
stoikiometri
.
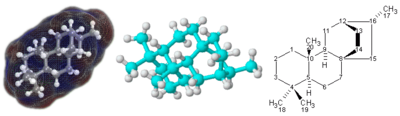 Representasi
3D
(kiri dan tengah) dan
2D
(kanan) dari molekul
terpenoid
atisana.
Representasi
3D
(kiri dan tengah) dan
2D
(kanan) dari molekul
terpenoid
atisana.
Untuk molekul dengan struktur 3 dimensi yang rumit, terutama yang melibatkan atom yang terikat pada empat substituen yang berbeda, formula molekul sederhana atau bahkan
rumus kimia
semi-struktural mungkin tidak cukup untuk menentukan molekul secara lengkap. Dalam kasus ini, mungkin diperlukan jenis formula grafis yang disebut
rumus struktur
. Rumus struktur pada gilirannya dapat diwakili dengan nama kimia satu dimensi, tetapi
tata nama kimia
semacam itu membutuhkan banyak kata dan istilah yang bukan merupakan bagian dari rumus kimia.
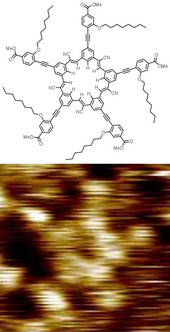 Struktur dan citra
STM
molekul
dendrimer
"sianostar".
[22]
Struktur dan citra
STM
molekul
dendrimer
"sianostar".
[22]
Molekul memiliki
kesetimbangan
geometri?panjang dan sudut ikatan?tetap yang dengannya mereka terus berosilasi melalui gerak vibrasi dan rotasi. Bahan murni terdiri dari molekul dengan struktur geometris rata-rata yang sama. Rumus kimia dan struktur molekul adalah dua faktor penting yang menentukan sifat-sifatnya, terutama
reaktivitasnya
.
Isomer
berbagi rumus kimia tapi biasanya memiliki sifat yang sangat berbeda karena strukturnya yang berbeda.
Stereoisomer
, jenis isomer tertentu, memiliki sifat fisiko-kimia yang sangat mirip dan pada saat bersamaan berbeda aktivitas
biokimianya
.
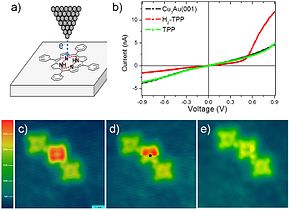 Hidrogen dapat dibebaskan dari molekul
H
2
TPP
dengan menerapkan tegangan berlebih ke ujung
mikroskop penerowongan payaran
(STM, a); penghilangan ini mengubah kurva arus-voltase (I-V) dari molekul TPP, yang diukur dengan menggunakan ujung STM yang sama, dari seperti
dioda
(kurva merah di b) menjadi seperti
resistor
(kurva hijau). Gambar (c) menunjukkan deretan molekul TPP, H
2
TPP dan TPP. Saat memindai gambar (d), kelebihan voltase diterapkan pada H
2
TPP pada titik hitam, yang secara langsung menghilangkan hidrogen, seperti yang ditunjukkan pada bagian bawah (d) dan gambar hasil pemindaian ulang (e). Manipulasi semacam itu bisa digunakan dalam
elektronika molekul tunggal
.
[23]
Hidrogen dapat dibebaskan dari molekul
H
2
TPP
dengan menerapkan tegangan berlebih ke ujung
mikroskop penerowongan payaran
(STM, a); penghilangan ini mengubah kurva arus-voltase (I-V) dari molekul TPP, yang diukur dengan menggunakan ujung STM yang sama, dari seperti
dioda
(kurva merah di b) menjadi seperti
resistor
(kurva hijau). Gambar (c) menunjukkan deretan molekul TPP, H
2
TPP dan TPP. Saat memindai gambar (d), kelebihan voltase diterapkan pada H
2
TPP pada titik hitam, yang secara langsung menghilangkan hidrogen, seperti yang ditunjukkan pada bagian bawah (d) dan gambar hasil pemindaian ulang (e). Manipulasi semacam itu bisa digunakan dalam
elektronika molekul tunggal
.
[23]
Spektroskopi molekuler
berhubungan dengan respon (
spektrum
) molekul yang berinteraksi dengan sinyal probing
energi
yang diketahui (atau
frekuensi
, sesuai dengan
rumus Planck
). Molekul memiliki tingkat energi terkuantisasi yang dapat dianalisis dengan mendeteksi pertukaran energi molekul melalui
absorbansi
atau
emisi
.
[24]
Spektroskopi umumnya tidak mengacu pada studi
difraksi
di mana partikel seperti
neutron
,
elektron
, atau
sinar-X
energi tinggi yang berinteraksi dengan susunan molekul reguler (seperti dalam kristal).
Spektroskopi gelombang mikro
biasanya mengukur perubahan rotasi molekul, dan dapat digunakan untuk mengidentifikasi molekul di luar angkasa.
Spektroskopi inframerah
mengukur perubahan vibrasi molekul, termasuk
stretching
,
bending
atau
twisting
. Ini biasanya digunakan untuk mengidentifikasi jenis ikatan atau
gugus fungsi
dalam molekul. Perubahan pengaturan elektron menghasilkan jalur penyerapan atau emisi pada sinar ultraviolet, sinar tampak atau
inframerah dekat
, dan menghasilkan warna. Spektroskopi resonansi inti sebenarnya mengukur lingkungan inti tertentu dalam molekul, dan dapat digunakan untuk mengkarakterisasi jumlah atom dalam posisi yang berbeda dalam molekul.
Studi tentang molekul melalui
fisika molekuler
dan
kimia teoretis
sebagian besar didasarkan pada
mekanika kuantum
dan sangat penting untuk memahami
ikatan kimia
. Molekul yang paling sederhana adalah
ion-molekul hidrogen
,
H
+
2
, dan yang paling sederhana dari semua ikatan kimia adalah
ikatan satu elektron
.
H
+
2
terdiri dari dua
proton
bermuatan positif dan satu
elektron
bermuatan negatif, yang berarti bahwa
persamaan Schrodinger
untuk sistem tersebut dapat dipecahkan lebih mudah karena kurangnya tolakan elektron?elektron. Seiring dengan kepesatan perkembangan komputer digital, solusi pendekatan untuk molekul yang lebih rumit menjadi mungkin dan merupakan salah satu aspek utama dari
kimia komputasi
.
Ketika mencoba untuk menentukan secara ketat apakah susunan atom
cukup stabil
untuk dianggap sebagai molekul, IUPAC menyarankan agar "sesuai dengan depresi pada
permukaan energi potensial
yang cukup dalam untuk membatasi setidaknya satu keadaan vibrasi".
[4]
Definisi ini tidak bergantung pada sifat interaksi antara atom, tetapi hanya pada kekuatan interaksi. Sebenarnya, ini termasuk spesies yang terikat lemah yang secara tradisional tidak dianggap sebagai molekul, seperti
helium
dimer
,
He
2
, yang memiliki satu
keadaan ikatan
vibrasi
[25]
dan terikat secara longgar sehingga hanya dapat diamati pada suhu yang sangat rendah.
Stabil-tidaknya
susunan atom untuk dianggap sebagai molekul secara inheren merupakan definisi operasional. Secara filosofis, oleh karena itu, sebuah molekul bukanlah entitas fundamental (sebaliknya, misalnya, terhadap
partikel dasar
); sebaliknya, konsep molekul adalah cara kimiawan untuk membuat pernyataan yang berguna tentang kekuatan interaksi skala atom di dunia yang kita amati.
- ^
Iwata, Kota; Yamazaki, Shiro; Mutombo, Pingo; Hapala, Prokop; Ondra?ek, Martin; Jelinek, Pavel; Sugimoto, Yoshiaki (2015).
"Chemical structure imaging of a single molecule by atomic force microscopy at room temperature"
.
Nature Communications
.
6
: 7766.
Bibcode
:
2015NatCo...6E7766I
.
doi
:
10.1038/ncomms8766
.
PMC
4518281
 .
PMID
26178193
.
.
PMID
26178193
.
- ^
Dinca, L. E.; De Marchi, F.; MacLeod, J. M.; Lipton-Duffin, J.; Gatti, R.; Ma, D.; Perepichka, D. F.; Rosei, F. (2015). "Pentacene on Ni(111): Room-temperature molecular packing and temperature-activated conversion to graphene".
Nanoscale
.
7
(7): 3263?9.
Bibcode
:
2015Nanos...7.3263D
.
doi
:
10.1039/C4NR07057G
.
PMID
25619890
.
- ^
Hapala, Prokop; ?vec, Martin; Stetsovych, Oleksandr; Van Der Heijden, Nadine J.; Ondra?ek, Martin; Van Der Lit, Joost; Mutombo, Pingo; Swart, Ingmar; Jelinek, Pavel (2016).
"Mapping the electrostatic force field of single molecules from high-resolution scanning probe images"
.
Nature Communications
.
7
: 11560.
Bibcode
:
2016NatCo...711560H
.
doi
:
10.1038/ncomms11560
.
PMC
4894979
 .
PMID
27230940
.
.
PMID
27230940
.
- ^
a
b
IUPAC
,
Compendium of Chemical Terminology
, edisi ke-2 ("Buku Emas") (1997). Versi koreksi daring: (2006–) "
Molecule
".
- ^
Ebbin, Darrell D. (1990).
General Chemistry
(edisi ke-3rd). Boston: Houghton Mifflin Co.
ISBN
0-395-43302-9
.
- ^
Brown, T.L.; Kenneth C. Kemp; Theodore L. Brown; Harold Eugene LeMay; Bruce Edward Bursten (2003).
Chemistry?the Central Science
(edisi ke-9th). New Jersey: Prentice Hall.
ISBN
0-13-066997-0
.
- ^
Chang, Raymond (1998).
Chemistry
(edisi ke-6th). New York: McGraw Hill.
ISBN
0-07-115221-0
.
- ^
Zumdahl, Steven S. (1997).
Chemistry
(edisi ke-4th). Boston: Houghton Mifflin.
ISBN
0-669-41794-7
.
- ^
Chandra, Sulekh (2005).
Comprehensive Inorganic Chemistry
. New Age Publishers.
ISBN
81-224-1512-1
.
- ^
"Molecule"
.
Encyclopædia Britannica
. 22 January 2016
. Diakses tanggal
23 February
2016
.
- ^
Harper, Douglas.
"molecule"
.
Online Etymology Dictionary
. Diakses tanggal
2016-02-22
.
- ^
"molecule"
. Merriam-Webster.
Diarsipkan
dari versi asli tanggal 2021-02-24
. Diakses tanggal
22 February
2016
.
- ^
Molecule Definition
Diarsipkan
2014-10-13 di
Wayback Machine
. (
Frostburg State University
)
- ^
"The Hutchinson unabridged encyclopedia with atlas and weather guide"
.
worldcat.org
. Oxford, England.
Diarsipkan
dari versi asli tanggal 2020-01-26
. Diakses tanggal
28 February
2016
.
- ^
Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006).
Biology: Exploring Life
. Boston, Massachusetts: Pearson Prentice Hall.
ISBN
0-13-250882-6
.
Diarsipkan
dari versi asli tanggal 2014-11-02
. Diakses tanggal
2012-02-05
.
- ^
Campbell, Flake C. (2008-01-01).
Elements of Metallurgy and Engineering Alloys
(dalam bahasa Inggris). ASM International.
ISBN
9781615030583
.
- ^
Roger L. DeKock; Harry B. Gray; Harry B. Gray (1989).
Chemical structure and bonding
. University Science Books. hlm. 199.
ISBN
0-935702-61-X
.
- ^
Chang RL; Deen WM; Robertson CR; Brenner BM. (1975). "Permselectivity of the glomerular capillary wall: III. Restricted transport of polyanions".
Kidney Int
.
8
(4): 212?218.
doi
:
10.1038/ki.1975.104
.
PMID
1202253
.
- ^
Chang RL; Ueki IF; Troy JL; Deen WM; Robertson CR; Brenner BM. (1975).
"Permselectivity of the glomerular capillary wall to macromolecules. II. Experimental studies in rats using neutral dextran"
.
Biophys J
.
15
(9): 887?906.
Bibcode
:
1975BpJ....15..887C
.
doi
:
10.1016/S0006-3495(75)85863-2
.
PMC
1334749
 .
PMID
1182263
.
.
PMID
1182263
.
- ^
Wink, Donald J.; Fetzer-Gislason, Sharon; McNicholas, Sheila (2003-03-01).
The Practice of Chemistry
(dalam bahasa Inggris). Macmillan.
ISBN
9780716748717
.
- ^
"ChemTeam: Empirical Formula"
.
www.chemteam.info
.
Diarsipkan
dari versi asli tanggal 2021-01-19
. Diakses tanggal
2017-04-16
.
- ^
Hirsch, Brandon E.; Lee, Semin; Qiao, Bo; Chen, Chun-Hsing; McDonald, Kevin P.; Tait, Steven L.; Flood, Amar H. (2014). "Anion-induced dimerization of 5-fold symmetric cyanostars in 3D crystalline solids and 2D self-assembled crystals".
Chemical Communications
.
50
(69): 9827?30.
doi
:
10.1039/C4CC03725A
.
PMID
25080328
.
- ^
Zoldan, V. C.; Faccio, R; Pasa, A. A. (2015).
"N and p type character of single molecule diodes"
.
Scientific Reports
.
5
: 8350.
Bibcode
:
2015NatSR...5E8350Z
.
doi
:
10.1038/srep08350
.
PMC
4322354
 .
PMID
25666850
.
.
PMID
25666850
.
- ^
IUPAC
,
Compendium of Chemical Terminology
, edisi ke-2 ("Buku Emas") (1997). Versi koreksi daring: (2006–) "
Spectroscopy
".
- ^
Anderson JB (May 2004). "Comment on "An exact quantum Monte Carlo calculation of the helium-helium intermolecular potential" [J. Chem. Phys. 115, 4546 (2001)]".
J Chem Phys
.
120
(20): 9886?7.
Bibcode
:
2004JChPh.120.9886A
.
doi
:
10.1063/1.1704638
.
PMID
15268005
.
|
|---|
| Umum
| |
|---|
| Perpustakaan nasional
| |
|---|
| Lain-lain
| |
|---|