|
|
| Altalanos
|
| Nev,
vegyjel
,
rendszam
|
technecium, Tc, 43
|
| Latin megnevezes
|
technetium
|
| Elemi sorozat
|
atmenetifemek
|
| Csoport
,
periodus
,
mez?
|
7
,
5
,
d
|
| Megjelenes
|
ezustszurke

|
| Atomtomeg
|
(98)
g/mol
|
| Elektronszerkezet
|
[
Kr
] 4d
5
5s
2
|
| Elektronok
hejankent
|
2, 8, 18, 13, 2
|
| Fizikai tulajdonsagok
|
| Halmazallapot
|
szilard
|
| S?r?seg
(szobah?m.)
|
11 g/cm³
|
| Olvadaspont
|
2430
K
(2157 °
C
, 3915 °
F
)
|
| Forraspont
|
4538
K
(4265 °
C
, 7709 °
F
)
|
Olvadash?
 |
33,29
kJ/mol
|
Parolgash?
 |
585,2
kJ/mol
|
| Molaris
h?kapacitas
|
(25 °C) 24,27 J/(mol·K)
|
G?znyomas
(extrapolalt)
| P
/Pa
|
1
|
10
|
100
|
1 k
|
10 k
|
100 k
|
| T
/K
|
2727
|
2998
|
3324
|
3726
|
4234
|
4894
|
|
| Atomi tulajdonsagok
|
| Kristalyszerkezet
|
hexagonalis
|
| Oxidacios szam
|
7
(er?sen savas oxid)
|
| Elektronegativitas
|
1,9 (
Pauling-skala
)
|
| Elektronaffinitas
|
-53 kJ/mol
|
| Ionizacios energia
|
1.: 702
kJ/mol
|
| 2.: 1470 kJ/mol
|
| 3.: 2850 kJ/mol
|
| Atomsugar
|
135
pm
|
| Atomsugar
(szamitott)
|
183
pm
|
| Kovalens sugar
|
156
pm
|
| Egyebek
|
| Magnesseg
|
nincs adat
|
| H?merseklet-vezetesi tenyez?
|
(300 K) 50,6
W/(m·K)
|
| CAS-szam
|
7440-26-8
|
| Fontosabb izotopok
|
F? cikk:
A technecium izotopjai
| izotop
|
termeszetes el?fordulas
|
felezesi id?
|
bomlas
|
| mod
|
energia
(
MeV
)
|
termek
|
| 95
m
Tc
|
mesterseges
|
61
d
|
ε
|
-
|
95
Mo
|
| γ
|
0,204, 0,582,
0,835
|
-
|
| IT
|
0,0389,
e
|
95
Tc
|
| 96
Tc
|
mesterseges
|
4,3
d
|
ε
|
-
|
96
Mo
|
| γ
|
0,778, 0,849,
0,812
|
-
|
| 97
m
Tc
|
mesterseges
|
90
d
|
IT
|
0,965, e
|
97
Tc
|
| 97
Tc
|
mesterseges
|
2,6×10
6
y
|
ε
|
-
|
97
Mo
|
| 98
Tc
|
mesterseges
|
4,2×10
6
y
|
β
-
|
0,4
|
98
Ru
|
| γ
|
0,745, 0,652
|
-
|
| 99
m
Tc
|
nyomokban
|
6,01
h
|
IT
|
0,142, 0,002
|
99
Tc
|
| γ
|
0,140
|
-
|
| 99
Tc
|
nyomokban
|
2,111×10
5
y
|
β
-
|
0,294
|
99
Ru
|
|
| Hivatkozasok
|
A
technecium
a legkisebb rendszamu
kemiai elem
, amelynek nincs stabil
izotopja
. Rendszama 43, vegyjele
Tc
. Ezustszurke
atmenetifem
. Kemiai tulajdonsagait tekintve a
mangan
es a
renium
kozott all. A technecium nagy resze szintetikusan el?allitott, es csak nagyon kis mennyisegben talalhato meg a termeszetben, amely az
uran
spontan
maghasadasabol
, vagy molibdenercek neutronbefogassal torten? atalakulasabol szarmazik.
A technecium sok tulajdonsagat mar
Dmitrij Ivanovics Mengyelejev
megjosolta, miel?tt azt felfedeztek volna. Mengyelejev ekamangankent hivatkozott ra periodusos rendszereben. 1937-ben gyartottak el?szor techneciumot (technecium-97-et), a nev a gorog τεχνητ?? (tekhnetosz), ?mesterseges” szobol szarmazik).
A metastabil gammasugarzo technecium-99-et orvosdiagnosztikai tesztek keszitesere hasznaljak. A hosszu elettartamu technecium izotopok az uran-235 maghasadasanak mellektermekei az atomreaktorokban, es a f?t?anyagrudakbol nyerik ?ket.
Felfedezesenek tortenete
[
szerkesztes
]
A 43-as rendszamu elem nyomaban
[
szerkesztes
]
1861
-t?l egeszen
1871
-ig a
Mengyelejev
altal javasolt korai
periodusos rendszer
egy rest tartalmazott a
molibden
(Z=42) es a
rutenium
kozott (Z=44).
1871
-ben Mengyelejev megjosolta, hogy ez a hianyzo elem foglalhatja el a
mangan
alatti ures helyet, igy annak hasonlo kemiai tulajdonsagokkal kell rendelkeznie. Mengyelejev az ekamangan (Em) nevet adta neki a
szanszkrit
?eka” el?tag utan, mely itt arra utal, hogy a mangan alatt eggyel helyezkedik el a keresett elem.
Sok kutato versengett megtalalasaert a periodusos rendszer megalkotasa el?tt es utan egyarant, mivel periodusos rendszerbeli elhelyezkedese alapjan felteteleztek, hogy konnyebben detektalhato, mint mas meg felfedezesre varo elemek. El?szor veltek
1828
-ban, hogy a
platina
ercben talaltak meg, es a polinium nevet adtak neki, de err?l kiderult, hogy nem mas, mint szennyezett
iridium
.
1846
-ban ismet bejelentettek a felfedezeset ilmenium neven, de ez valojaban szennyezett
niobium
volt. Ugyanezt a hibat kovettek el
1847
-ben, akkor pelopium neven hivatkoztak az uj elemre.
1877
-ben Szergej Kern orosz vegyesz bejelentette, hogy a hianyzo elemet megtalalta a platinaercben. Kern az elemre davyum neven hivatkozott (Sir
Humphry Davy
angol kemikus utan), de kiderult, hogy ez
iridium
,
rodium
es
vas
kevereke. Egy ujabb lehetseges jeloltr?l, a luciumrol bebizonyosodott, hogy
ittrium
.
1908
-ban a
japan
tudos, Masataka Ogawa ugy velte, bizonyitekot talalt arra nezve, hogy a hianyzo 43-as rendszamu elem a thorianit nev? asvanyban van jelen. Ogawa az elemet Japan utan (mely japanul Nippon) nipponiumnak nevezte el. 2004-ben Yoshihara rontgenspektroszkopiaval nem tudta kimutatni az Ogawa hagyatekaban talalt fotolemezen ?rzott mintaban a keresett elemet, helyette reniumot talalt.
Walter Noddack, Otto Berg es Ida Noddack publikaltak a 75-os es a 43-as rendszamu elem felfedezeset 1925-ben, utobbit mazurium nevre kereszteltek, mivel Noddack csaladja a Mazuri-tovidekr?l szarmazott.
[1]
A kutatocsoport columbitot (niobit) bombazott elektronsugarral, es arra kovetkeztetett, hogy a 43-as rendszamu elem gyenge jele megtalalhato a kiertekeleskor kapott
rontgendiffrakcios
spektrogramon. A
hullamhosszak
es a rendszam kapcsolatat
Henry Moseley
1913-as osszefuggese szolgaltatta. Kes?bbi kutatasok nem tudtak reprodukalni kiserletuket, igy ma is vitak targyat kepezi, hogy valoban megtalalta-e a csoport a kes?bb techneciumnak nevezett elemet.
Hivatalos felfedezese, el?fordulasa
[
szerkesztes
]
 Emilio Segre (1905-1989)
Emilio Segre (1905-1989)
A 43-as rendszamu elem letezeset hivatalosan 1936 decembereben er?sitette meg a Palermoi Egyetem ket kutatoja, Carlo Perrier es
Emilio Segre
. Segre az 1930-as evek kozepen a Columbia Egyetemen es a Lawrence Berkeley National Laboratory-ban tett latogatasa soran ravette
Ernest Lawrence
amerikai Nobel-dijas
fizikust
, hogy az altala felfedezett
ciklotronbol
szarmazo
radioaktiv
hulladekbol kaphasson mintat. Lawrence molibdenfoliat bocsatott rendelkezesere a keszulek deflektorarol.
Segre rabeszelte palermoi kollegajat, Perrier-t, hogy osszehasonlito kemiai elemzes segitsegevel bizonyitsak be, hogy a
molibdennek
tulajdonitott
aktivitas
valojaban a 43-as rendszamu elemt?l szarmazik. A mintabol sikerult izolalniuk a technecium-95 es technecium-97 izotopokat. A technecium elnevezest 1947-ben kapta az elem. Segre visszaterve Berkeley-be, talalkozott
Glenn T. Seaborg
(kemiai) Nobel-dijas tudossal, akivel sikerult izolalnia a technecium-99m-et (az ?m” az elem fizikai kemiai metastabilitasara utal).
Segre-t 1959-ben
fizikai Nobel-dijjal
jutalmaztak az antiproton felfedezeseert, a technecium mellett meg az
asztacium
(At) felfedezese is a nevehez f?z?dik.
1959-ben Paul W. Merrill Kaliforniaban vizsgalodva eszlelte a techneciumra jellemz? emisszios spektrumot az S tipusu
voros oriasokbol
. Ezek a csillagok eletuk vege fele nagy mennyiseg? techneciumot halmoznak fel, amelyek magreakciok jelenletet bizonyitjak. Ez a bizonyitek tamasztotta ala a korabban feltetelezett elmeletet, miszerint a csillagokban nehez elemek nukleoszintezise is vegbemehet. Ujabban bizonyitottak, hogy ez
neutron
befogasaval valosul meg.
Hivatalos felfedezese utan sok kutatast folytattak arra nezve, vajon megtalalhato-e a Foldon termeszetes forrasu technecium. 1962-ben,
Belga Kongoban
sikerult izolalni rendkivul kis mennyisegben uranszurokercb?l (kb. 0,2 ng/kg), ahol valoszin?leg uran-238
spontan hasadasaval
keletkezik. Arra vonatkozoan is talaltak bizonyitekot, hogy az
okloi
termeszetes
atomreaktor
jelent?s mennyiseg? technecium-99-et termelt, amely azonban azota rutenium-99-ce bomlott. Adott pillanatban a foldkeregben az uranercben es toriumercben vegbemen? spontan hasadas, valamint a molibden neutronbefogasa kovetkezteben ? figyelembe veve, hogy egy kilogramm uran kb. 1 nanogramm (10
?9
g) techneciumot tartalmaz ? mintegy 18 ezer tonna technecium talalhato.
[2]
[3]
[4]
Fizikai tulajdonsagai
[
szerkesztes
]
 Uranerc nyomnyi mennyiseg? techneciummal
Uranerc nyomnyi mennyiseg? techneciummal
A technecium ezustszurkes,
radioaktiv
, megjeleneseben a
platinahoz
hasonlatos fem. Rendszerint szurke por formajaban nyerhet? ki. Az atomos technecium emisszios vonalai az alabbi
hullamhosszakon
talalhato: 363,3 nm, 403,1 nm, 426,2 nm, 429,7 nm es 485,3 nm.
[5]
A fem enyhen
paramagneses
tulajdonsagu, mely azt jelenti, hogy kuls? magneses ter hatasara megfelel? iranyba rendez?dnek a magneses dipolusok, de a mez? megsz?nese utan veletlenszer?en allnak be. A tiszta egykristaly technecium 2-es tipusu
szupravezet?kent
m?kodik 7,46 K alatti h?mersekleteken.
[6]
E h?merseklet alatt a fem London-fele magneses behatolasi melysege rendkivuli mertekben megn?, az elemek kozott a
niobium
utan a masodik legnagyobb erteket adja.
[7]
Kemiai tulajdonsagok
[
szerkesztes
]
A technecium a periodusos rendszer VII. B mellekcsoportjaban talalhato a
renium
es a
mangan
kozott. A technecium a reniumhoz hasonloan kemiailag inert (kevesse reakciokepes), es kotesei
kovalens
jelleg?ek.
[8]
A mangantol elter?en nem alkot keszsegesen
kationokat
(pozitiv toltes? ionok). Jellemz?
oxidacios allapotok
: +4, +5, +7.
[9]
A technecium oldodik
kiralyvizben
,
saletromsavban
es tomeny
kensavban
, de
sosavban
egyaltalan nem.
[10]
Hidridjei es oxidjai
[
szerkesztes
]
A technecium
hidrogennel
valo reakcioja soran
TcH
2?
9
[techneciumhidrid (II)-anion], melynek szerkezete ugyanaz, mint a
ReH
2?
9
-e. Bar a szerkezetet ado hidrogenatomok geometriai elrendez?dese nem ekvivalens, az
elektronszerkezet
majdnem ugyanaz. A
komplex ion
ket hidrogenatomja kicserelhet?
Na
+
es
K
+
-ionokra.
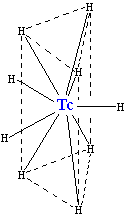 Technecium-hidrid
Technecium-hidrid
A femtechnecium paradus leveg?ben konnyen
korrodalodik
,
[9]
por alakban
oxigennel
egyesul. Ketfele
oxidjat
sikerult el?allitani eddig:
TcO
2
es
Tc
2
O
7
. Oxidativ korulmenyek kozott technecium (VII)-kation keletkezhet, amely
pertechnetationkent
letezik (
TcO
?
4
).
[9]
[11]
400-450 °C kozott halvanysarga technecium-heptoxidda alakul:
- 4 Tc + 7
O
2
→ 2
Tc
2
O
7
A technecium-heptoxid a
natrium-pertechnetat
gyartasanak kiindulasi anyaga (prekurzora):
- Tc
2
O
7
+ 2 NaOH → 2
NaTcO
4
+
H
2
O
A fekete szin? technecium-dioxid (
TcO
2
) a heptoxid formabol nyerhet? femtechneciummal vagy hidrogennel torten? redukcioval.
A
pertechneciumsav
(
HTcO
4
) gyartasa technecium-heptoxidbol vizzel vagy mas oxidalo savval, pl. saletromsavval, tomeny kensavval, kiralyvizzel vagy sosavas-saletromsavas eleggyel tortenik. A keletkez? sotetvoros, higroszkopos (vizmegkot? tulajdonsagu) anyag er?s sav, igy konnyen adja le protonjat.
A pertechnetat (tetroxidotechnetat) anion (
TcO
?
4
) tetraederes szerkezet?, a csucsokban az oxigenatomok, a centrumban a Tc-atom helyezkedik el. A
permanganationnal
ellentetben a pertechnetation csak gyenge
oxidalo reagens
. A pertechnetatot gyakran hasznaljak
katalizatorkent
, valamint a techneciumizotopok kenyelmes vizoldhato forrasakent.
Szulfidjai, szelenidjei, telluridjai
[
szerkesztes
]
A technecium tobbfele
szulfidot
kepez.
TcS
2
el?allithato femtechnecium (Tc) es elemi ken (
S
8
) direkt szintezisevel (kozvetlen reakciojaval), mig a
Tc
2
S
7
az alabbi reakcio alapjan allithato el?:
- 2
HTcO
4
+ 7
H
2
S
→
Tc
2
S
7
+ 8
H
2
O
Melegites hatasara a technecium-heptaszulfid diszulfidra es elemi kenre bomlik:
- Tc
2
S
7
→ 2
TcS
2
+ 3 S
Szelennel
es
tellurral
a fentiek analogiajara jatszodnak le reakciok.
Klaszterek es szerves komplexek
[
szerkesztes
]
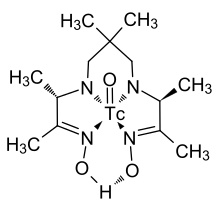 Szerves techneciumkomplex.
[12]
Szerves techneciumkomplex.
[12]
Szamos
techneciumklaszter
ismert, peldaul a
Tc
4
,
Tc
6
,
Tc
8
es
Tc
13
.
[13]
[14]
Stabilabbak a
Tc
6
,
Tc
8
. Szamos szerves techneciumkomplexet sikerult el?allitani, amelyek szerkezete viszonylag jol ismert es behatoan tanulmanyozott az orvostudomanyban valo gyakorlati jelent?sege miatt.
A ditechnecium-dekakarbonil (
Tc
2
(CO)
10
) feher szilard anyag. Ebben a molekulaban ket techneciumatom kapcsolodik ossze joval gyengebben, mint az kovalens kotes eseteben jellemz?, amit a 303 pm-es viszonylag nagy
kotestavolsag
is igazol. A ket techneciumatomot oktaederes alakzatban veszi korul a 10 karbonilligandum, ily modon telit?dnek a megfelel? s, p es d alhejak (ehhez tehat osszesen 18 elektron szukseges). A techneciumatom 7 db d-palyan tartozkodo elektront tartalmaz, ehhez hozzaadodik a karbonilligandumok 2*5 db elektronja. Mivel ebb?l osszesen 17 elektron szarmazik, ez pedig kedvez?tlen, ezert ket techneciumatom osszekapcsolodasaval erhet? el a hej telitettsege, igy a komplex energiaminimuma.
Az abran lathato szerves techneciumkomplexet szinten az orvostudomanyban hasznositjak.
Alkalmazasok, elettani hatasok
[
szerkesztes
]
Az orvostudomanyban a technecium-99m izotopot
radioaktiv nyomjelz?kent
hasznaljak. E celra jol megfelel, mivel 140 keV-os
gamma-sugarzasa
az orvosdiagnosztikai eszkozokkel konnyen eszlelhet?, es
felezesi ideje
6,01 ora, ami azt jelenti, hogy 24 oran belul 94%-a lebomlik az emberi testben. Legalabb 31-fele szeles korben hasznalt technecium-99m alapu
radiofarmakont
hasznalnak az
agy
,
szivizom
,
pajzsmirigy
,
maj
,
tud?
,
vese
,
epeholyag
, a
csontrendszer
, a
ver
es
tumorok
funkcionalis es kepalkoto vizsgalataban.
[15]
Az orvostudomanyon kivul felhasznaljak meg a vegyiparban katalizatorkent. Nehany esetben, pl.
izopropanol
dehidrogenezese soran hatekonyabb, mint a
renium
vagy a
palladium
.
[16]
A kalium-pertechnetat 55 ppm-nyi koncentracioban megakadalyozza az
acel
korroziojat vizbe merites eseten akar 250 °C-ig is.
[17]
A hosszabb (61 nap) felezesi idej? technecium-95m izotop segitsegevel az allat- es novenyvilagban a technecium mozgasat tanulmanyozzak, kovetik nyomon.
[18]
A techneciumnak nincs termeszetes biologiai szerepe, es nem talalhato meg az emberi testben.
[10]
Kemiai toxicitasa csekely. Egy vizsgalatban, melynek soran patkanyokat tobb heten at akar 15 μg/g technecium-99 tartalmu taplalekkal etettek, nem tapasztaltak jelent?s elvaltozast a verosszetetelben, a test vagy szervek tomegeben, valamint az etkezesi szokasokban sem.
[19]
A radiologiai toxicitas fugg a szoban forgo vegyulett?l, a felezesi id?t?l es a sugarzas tipusatol.
[20]
Mindegyik izotopjaval ovatosan kell banni. A technecium-99 gyenge
beta-sugarzo
anyag, amelyet mar a laboratoriumi uvegfal is elnyel. Az els?dleges kockazatot a technecium poranak belelegzese okozza, amely jelent?s mertekben jarulhat hozza
rak
kialakulasahoz. A biztonsagos munkahoz tobbnyire elegend? az elszivofulke, keszty?sbox hasznalata nem szukseges.
[21]
- ↑
Termeszet Vilaga 2012 (143. evf.), 12. sz. 568. o. Makra Zsigmond: Az "atomkor" kezdete
- ↑
Emsley, J..
Nature's Building Blocks: An A-Z Guide to the Elements
. New York: Oxford University Press, 422?425. o. (2001. majus 25.).
ISBN 978-0-19-850340-8
- ↑
(1997. majus 25.) ?Analysis of Naturally Produced Technetium and Plutonium in Geologic Materials”.
Analytical Chemistry
69
(9), 1692?9. o.
DOI
:
10.1021/ac961159q
.
PMID 21639292
.
- ↑
(1999. majus 25.) ?
Nature's uncommon elements: plutonium and technetium
”.
Geochimica et Cosmochimica Acta
63
(2), 275. o.
DOI
:
10.1016/S0016-7037(98)00282-8
.
- ↑
Lide, David R.. Line Spectra of the Elements,
The CRC Handbook
. CRC press, 10?70 (1672). o. (2004?2005).
ISBN 978-0-8493-0595-5
- ↑
Schwochau 2000
, p. 96
- ↑
Autler, S. H.. ?
Technetium as a Material for AC Superconductivity Applications
”,
Proceedings of the 1968 Summer Study on Superconducting Devices and Accelerators
(Hozzaferes: 2009. majus 5.)
- ↑
Greenwood 1997
, p. 1044
- ↑
a
b
c
Husted, R.:
Technetium
.
Periodic Table of the Elements
. Los Alamos National Laboratory, 2003. december 15. (Hozzaferes: 2009. oktober 11.)
- ↑
a
b
Hammond, C. R.. The Elements,
Handbook of Chemistry and Physics
, 81st, CRC press (2004).
ISBN 0-8493-0485-7
- ↑
Rimshaw, S. J..szerk.: Hampel, C. A.:
The Encyclopedia of the Chemical Elements
. New York: Reinhold Book Corporation,
689
?693. o. (1968)
- ↑
3,3,9,9-Tetramethyl-4,8-diazaundecane-2,10-dione dioximato-oxotechnetium(V) [TcO(pnao)];
Schwochau 2000
, p. 176
- ↑
Cotton 1999
, p. 985
- ↑
Fundamental world of quantum chemistry: a tribute to the memory of Per-Olov Lowdin
. Springer, 479. o. (2003).
ISBN 1-4020-1286-1
- ↑
Schwochau 2000
, p. 414
- ↑
Schwochau 2000
, pp. 87?90
- ↑
Emsley 2001
, p. 425
- ↑
Schwochau 2000
, pp. 12?27
- ↑
Desmet, G.; Myttenaere, C.; Commission of the European Communities. Radiation Protection Programme, France. Service d'etudes et de recherches sur l'environnement, United States. Dept. of Energy. Office of Health and Environmental Research.
Technetium in the environment
. Springer, 1986, 392?395. o. (1986. majus 31.).
ISBN 0-85334-421-3
- ↑
Schwochau 2000
, pp. 371?381
- ↑
Schwochau 2000
, p. 40
- Ez a szocikk reszben vagy egeszben a
Technetium
cim? angol Wikipedia-szocikk forditasan alapul. Az eredeti cikk szerkeszt?it annak laptortenete sorolja fel. Ez a jelzes csupan a megfogalmazas eredetet es a szerz?i jogokat jelzi, nem szolgal a cikkben szerepl? informaciok forrasmegjelolesekent.
Tovabbi informaciok
[
szerkesztes
]
- a magyar Wikipedia techneciumot tartalmazo vegyuleteinek listaja
kuls? keres?vel
Kapcsolodo szocikkek
[
szerkesztes
]