 Prikaz atoma
helija
s oblakom
elektrona
u nijansama sive. U jezgri su dva
protona
i dva
neutrona
prikazana crveno i plavo.
Prikaz atoma
helija
s oblakom
elektrona
u nijansama sive. U jezgri su dva
protona
i dva
neutrona
prikazana crveno i plavo.
 1/12 mase
atoma
ugljika
12
C je danas
atomska jedinica mase
.
1/12 mase
atoma
ugljika
12
C je danas
atomska jedinica mase
.
 Jedna od mogu?ih
nuklearnih fisijskih lan?anih reakcija
: 1.) atom
uranija
-235 hvata spori
neutron
i raspada se na dva nova atoma (fisioni fragmenti ?
barij
-141 i
kripton
-92), oslobađaju?i 3 nova neutrona i ogromnu koli?inu energije vezanja (200 MeV), ?to predstavlja u ovom slu?aju
defekt mase
. 2.) jedan od tih neutrona bude uhva?en od atoma uranija-238 i ne nastavlja reakciju. Drugi neutron napu?ta sustav bez da bude uhva?en. Ipak, jedan od neutrona se sudara s novim atomom uranija-235, koji se raspada na dva nova atoma (fisioni fragmenti), oslobađaju?i 3 nova neutrona i ogromnu koli?inu energije vezanja (200 MeV), ?to je opet
defekt mase
. 3.) dva se neutrona sudaraju s dva atoma uranija-235 i svaki se raspada i nastavlja reakciju.
Jedna od mogu?ih
nuklearnih fisijskih lan?anih reakcija
: 1.) atom
uranija
-235 hvata spori
neutron
i raspada se na dva nova atoma (fisioni fragmenti ?
barij
-141 i
kripton
-92), oslobađaju?i 3 nova neutrona i ogromnu koli?inu energije vezanja (200 MeV), ?to predstavlja u ovom slu?aju
defekt mase
. 2.) jedan od tih neutrona bude uhva?en od atoma uranija-238 i ne nastavlja reakciju. Drugi neutron napu?ta sustav bez da bude uhva?en. Ipak, jedan od neutrona se sudara s novim atomom uranija-235, koji se raspada na dva nova atoma (fisioni fragmenti), oslobađaju?i 3 nova neutrona i ogromnu koli?inu energije vezanja (200 MeV), ?to je opet
defekt mase
. 3.) dva se neutrona sudaraju s dva atoma uranija-235 i svaki se raspada i nastavlja reakciju.
 Nuklearna energija vezanja
po
nukleonu
za neke
izotope
.
Nuklearna energija vezanja
po
nukleonu
za neke
izotope
.
 Radioaktivnost
u funkciji
vremena
; vrijeme poluraspada
T
½
= ln(2) ? τ
, gdje je
τ
srednje vrijeme ?ivota
radionuklida
.
Radioaktivnost
u funkciji
vremena
; vrijeme poluraspada
T
½
= ln(2) ? τ
, gdje je
τ
srednje vrijeme ?ivota
radionuklida
.
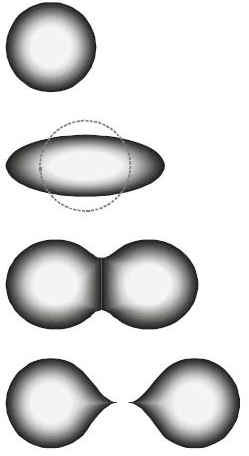 Model teku?e kapljice atomske jezgre.
Model teku?e kapljice atomske jezgre.
 Tri prirodna
izotopa
vodika
, koji se razlikuj po broju
neutrona
u atomskoj jezgri. S lijeva na desno: procijum
1
H je bez neutrona,
deuterij
2
H s jednim neutronom i tricij
3
H s dva neutrona.
Tri prirodna
izotopa
vodika
, koji se razlikuj po broju
neutrona
u atomskoj jezgri. S lijeva na desno: procijum
1
H je bez neutrona,
deuterij
2
H s jednim neutronom i tricij
3
H s dva neutrona.
 Rutherfordov model atoma
ili planetarni model atoma:
elektroni
(zeleno) i atomska jezgra (crveno).
Rutherfordov model atoma
ili planetarni model atoma:
elektroni
(zeleno) i atomska jezgra (crveno).
 U
maglenoj komori
,
alfa-?estica
energije 5,3 M
eV
iz izvora olova-210 u blizini to?ke 1 prolazi kroz
Rutherfordovo raspr?enje
u blizini to?ke 2, odstupaju?i pod kutom od oko 30°. Jo? jednom se raspr?uje blizu to?ke 3 i kona?no se odmara u plinu. Ciljana atomska jezgra u plinu mogla je biti jezgra
du?ika
,
kisika
,
ugljika
ili
vodika
. Pri elasti?nom sudaranju dobio je dovoljno kineti?ke energije da uzrokuje kratki vidljivi tragu blizini to?ke 2 (ljestvica je u centimetrima).
U
maglenoj komori
,
alfa-?estica
energije 5,3 M
eV
iz izvora olova-210 u blizini to?ke 1 prolazi kroz
Rutherfordovo raspr?enje
u blizini to?ke 2, odstupaju?i pod kutom od oko 30°. Jo? jednom se raspr?uje blizu to?ke 3 i kona?no se odmara u plinu. Ciljana atomska jezgra u plinu mogla je biti jezgra
du?ika
,
kisika
,
ugljika
ili
vodika
. Pri elasti?nom sudaranju dobio je dovoljno kineti?ke energije da uzrokuje kratki vidljivi tragu blizini to?ke 2 (ljestvica je u centimetrima).
 Wilsonova komora
: 1.
bljeskalica
, 2.
le?a
, 3.
stakleno
ku?i?te, 4.
fotoaparat
, 5. prostor komore, 6.
kondenzacijska jezgra
, 7. pokretna
membrana
, 8.
klip
.
Wilsonova komora
: 1.
bljeskalica
, 2.
le?a
, 3.
stakleno
ku?i?te, 4.
fotoaparat
, 5. prostor komore, 6.
kondenzacijska jezgra
, 7. pokretna
membrana
, 8.
klip
.
 Nuklearna reakcija
u kojoj
deuterij
bombardira
litij
-6, a nastaju dvije
alfa-?estice
(
protoni
su prestavljeni crvenim kuglicama, a
neutroni
plavim kuglicama).
Nuklearna reakcija
u kojoj
deuterij
bombardira
litij
-6, a nastaju dvije
alfa-?estice
(
protoni
su prestavljeni crvenim kuglicama, a
neutroni
plavim kuglicama).
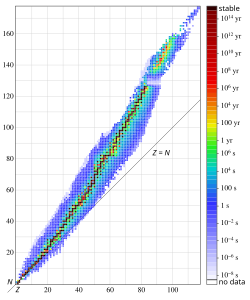 Vrijeme poluraspada
radioaktivnih
izotopa ili
radionuklida
. Treba zapaziti da se teoretska linija za stabilne isotope
Z
=
N
(
Z
?
atomski broj
i
N
-
neutronski broj
), razdvaja od stvarnog odnosa atomskog broja i neutrona, ?to zna?i da se s pove?anjem atomskog broja, pove?ava i nestabilnost atomskih jezgri.
Vrijeme poluraspada
radioaktivnih
izotopa ili
radionuklida
. Treba zapaziti da se teoretska linija za stabilne isotope
Z
=
N
(
Z
?
atomski broj
i
N
-
neutronski broj
), razdvaja od stvarnog odnosa atomskog broja i neutrona, ?to zna?i da se s pove?anjem atomskog broja, pove?ava i nestabilnost atomskih jezgri.
 Budu?i da
polumjer
atomske jezgre iznosi oko 10
-15
m
, a brzina alfa-?estice koja se u njemu kre?e iznosi oko 10
6
m/
s
, izlazi da alfa-?estica dolazi do vanjske povr?ine pribli?no 10
6
/10
-15
= 10
21
puta u sekundi, odnosno da ona pobjegne iz jezgre nakon 10
21
poku?aja. To je u stvari bit
tuneliranja
ili tunelskog u?inka.
Budu?i da
polumjer
atomske jezgre iznosi oko 10
-15
m
, a brzina alfa-?estice koja se u njemu kre?e iznosi oko 10
6
m/
s
, izlazi da alfa-?estica dolazi do vanjske povr?ine pribli?no 10
6
/10
-15
= 10
21
puta u sekundi, odnosno da ona pobjegne iz jezgre nakon 10
21
poku?aja. To je u stvari bit
tuneliranja
ili tunelskog u?inka.
Atomska jezgra
ili
jezgra atoma
nalazi se u sredi?tu
atoma
i ?ini 99,9% njegove
mase
, a zauzima samo oko 10
?14
volumena
(obujma) atoma. Na primjer kada bi atom bio
kugla
promjera
6
kilometara
, atomska jezgra bi bila veli?ine
teniske
loptice
. Svi sastavni dijelovi u atomu u neprestanu su
gibanju
. Jezgra se sastoji od
elektri?ki pozitivno nabijenih
protona
i neutralnih
neutrona
. Promjer atomske jezgre je od 1,75 · 10
?15
metara
(
vodikova
jezgra) do 15 · 10
?15
metara (
uranijeva
jezgra). Protoni i neutroni su u jezgri stopljeni zajedno djelovanjem privla?ne
nuklearne, odnosno jake sile
. Protoni i neutroni sastavljeni su od triju jo? manjih ?estica,
kvarkova
.
[1]
Ukupni naboj same jezgre je pozitivan i ovisi o broju
protona
. U
periodnom sustavu elemenata
atomi su poredani upravo po broju
protona
u jezgri, odnosno
atomskom broju
koji je nazna?en u lijevom donjem indeksu (na primjer
1
H). Zbroj masa
protona
i
neutrona
naziva se
relativna atomska masa
, izra?en je u jedinici unificirane atomske mase
u
i nazna?en je u lijevom gornjem indeksu (na primjer
1,008
H), dok se zbroj protona i neutrona naziva
maseni (nukleonski) broj
, a ozna?ava se s
A
.
Atomski broj
(oznaka
Z
) je broj protona u atomskoj jezgri, određuje svojstva atoma.
Neutronski broj
(oznaka
N
) je broj neutrona u atomskoj jezgri. Mo?e biti razli?it u jezgrama istoga
kemijskog elementa
(takve se jezgre nazivaju
izotopnima
).
Maseni broj
(oznaka
A
) je ukupan broj protona i neutrona (
nukleona
) u atomskoj jezgri.

Defekt mase
je razlika između zbroja masa slobodnih nukleona od kojih se jezgra sastoji i mase jezgre, odgovara ekvivalentnoj energiji vezanja nukleona.
Energija vezanja po nukleonu
[
uredi
|
uredi kod
]
Energija vezanja
po
nukleonu
razlikuje se od jezgre do jezgre i određuje krivulju stabilnosti ovisno o masenome broju elementa (prema energiji vezanja po nukleonu mogu se predvidjeti
fuzijski
procesi na malim vrijednostima i
fisijski
na velikim vrijednostima masenoga broja).
Energija
Sun?eva zra?enja
oslobađa se u efektivnoj pretvorbi ?etiriju protona u jezgru
helija
(fuzijom
kilograma
vodika
u ne?to manje od kilograma helija oslobađa se energija od 6 · 10
14
J
).
Konstanta raspada
opisuje brzinu raspadanja atomskih jezgara ili
subatomskih ?estica
u nekom uzorku
radioaktivne tvari
.
Vrijeme poluraspada
je
vrijeme
potrebno da se raspadne polovica nestabilnih atomskih jezgara ili subatomskih ?estica u nekom uzorku radioaktivne tvari.
Modeli atomske jezgre
[
uredi
|
uredi kod
]
Model kapljice
opisuje atomsku jezgru kao kap nestla?ivoga nuklearnoga
fluida
velike
gusto?e
. Predlo?io ga je
G. Gamow
(1931.), a razvio
N. Bohr
. Analogan je modelu kapljice
teku?ine
koju ?ine
molekule
. Stabilnost atomske jezgre ovisi o obliku kapi, a energija proizlazi od
povr?inske napetosti
i elektri?nog odbijanja među protonima. Model obja?njava kuglasti oblik ve?ine jezgri i poma?e predvidjeti energiju nuklearnog vezivanja. Tako su
H. A. Bethe
i
C. F. von Weizsacker
na temelju modela kapljice teku?ine (1935) izra?unali energiju vezanja nukleona i objasnili
nuklearnu fuziju
atomskih jezgri u
zvijezdama
.
Model ljusaka
opisuje jezgru atoma kao da je izgrađena od međusobno neovisnih ljusaka protona i neutrona djelomi?no analognih ljuskama koje opisuju raspored
elektrona
u atomu. Razvila ga je
M. Goeppert-Mayer
(1949.). Stabilnost jezgre ovisi o broju
nukleona
, a najstabilnije su jezgre punih ljusaka koje imaju
magi?ni broj
protona i neutrona. One su i sferno simetri?ne. Nuklearna deformacija u modelu ljusaka je odstupanje jezgre od sferi?ne ili osne simetrije; povezana je s kolektivnim gibanjima nukleona. Ona dovodi do pobuđenja
valentnih
nukleona, ali i do
dinami?kih
deformacija
(
vibracija
) te
stati?kih
deformacija (
rotacija
). Za razvoj modela deformiranih jezgri zaslu?ni su
G. Alaga
te
A. N. Bohr
,
B. R. Mottelson
i
J. Rainwater
.
Kromodinami?ki model
atomske jezgre u
kvantnoj kromodinamici
je nakupina nukleona povezanih
jakom nuklearnom silom
zaostalom od
jakog međudjelovanja
među
kvarkovima
unutar pojedinih nukleona. Jaka nuklearna sila ne ovisi o
elektri?nome naboju
nukleona, to jest iste je jakosti između bilo koja dva nukleona (protona i protona, neutrona i neutrona ili protona i neutrona).
[2]
U atomskoj teoriji
materije
,
atom
se sastoji od atomske jezgre oko koje kru?e
elektroni
. Danas je op?enito priznato mi?ljenje da se atomska jezgra svih
kemijskih elemenata
sastoji od pozitivno nabijenih
protona
i
neutrona
koji nemaju
elektri?ni naboj
. ?estice koje se nalaze u atomskoj jezgri, to jest protoni i neutroni, zovu se zajedni?kim imenom
nukleoni
(
lat
.
nucleus
: jezgra). Neutron ima
masu
gotovo jednaku masi protona. Proton je jezgra
vodikovog
atoma, pa mu je masa jednaka masi atoma vodika. Broj protona u atomskoj jezgri koji se zove
atomski broj
, jednak je njezinom
elektri?nom naboju
i uvijek odgovara rednom broju kemijskog elementa u
periodnom sustavu
. Dakle atomskim brojem određena je vrsta kemijskog elementa.
U neutralnom atomu broj elektrona ?to kru?e oko jezgre jednak je broju protona u jezgri. Pozitivan naboj jednog protona jednako je velik kao negativan naboj elektrona. 1869. ruski kemi?ar
D. I. Mendeljejev
otkrio je zakonitost ponavljanja kemijskih svojstva elemenata kod pove?anja njihove atomske mase. On je tada sve poznate elemente poredao po rastu?im atomskim masama jedan iznad drugoga i sastavio periodi?ku tablicu. Mendeljejev je dokazao da svaki kemijski element ima određen sastav atoma koji ozna?uje atomska masa i mjesto u periodnom sustavu elemenata.
Broj protona
P
i neutrona
N
u jezgri određuje atomsku masu
A
određenog elementa, to jest:

i zove se
maseni broj
atoma. Na primjer jezgra
helija
sastoji se od dva protona i dva neutrona. Prema tome je
elektri?ni naboj
jezgre i
redni broj
helija 2, a
relativna atomska masa
4. Oko atomske jezgre kru?e negativno nabijeni elektroni, a broj elektrona jednak je broju protona u jezgri.
No kod istog broja protona u jezgri mogu postojati razli?ite koli?ine neutrona. Dva atoma koji imaju isti broj protona, a razli?iti broj neutrona, imaju skoro ista kemijska svojstva i isti redni broj, ali razli?ite atomske mase. Takvi se elementi koji imaju isti redni broj, a razli?itu atomsku masu, zovu izotopi. Tako na primjer postoji
klor
koji ima redni broj 17, to jest njegova jezgra sadr?i 17 protona, dok mu je atomska masa 35, ?to zna?i da jezgra njegova atoma sadr?i 18 neutrona (17 + 18 = 35). Međutim, postoji i klor s atomskom masom 37, to jest jezgra njegova atoma sadr?i 20 neutrona (17 + 20 = 37). Obi?an klor koji se nalazi u spojevima u prirodi ima atomsku masu 35,46, ?to zna?i da je on smjesa tih dvaju izotopa koji su u njemu zastupani u omjeru 3 : 1, to jest:

Prvi izotop klora pi?emo simboli?ki
17
Cl
35
, a drugi
17
Cl
37
. Gornji broj uz kemijski simbol elementa zna?i relativnu atomsku masu tog elementa, a donji - broj protona u jezgri tog elementa, odnosno njegov redni broj. I
vodik
ima svoje izotope:
1
H
1
obi?ni vodik,
1
H
2
te?ki vodik ili
deuterij
i
1
H
3
tricij
.
Ovakvi izotopi nađeni su gotovo kod svih kemijskih elemenata. Tako
uranij
, koji je najva?niji u dobivanju
nuklearne energije
, ima 5 izotopa. Uranij ima redni broj 92, a njegovi izotopi imaju atomske mase 234, 235, 237, 238 i 239. U prirodnom uraniju najja?e je zastupljen izotop s atomskom masom 238. Ima ga 137 puta vi?e nego izotopa s atomskom masom 235. Ostalih njegovih izotopa ima jo? i manje. Izotopi se danas vrlo mnogo primjenjuju u medicini, tehnici i privredi, a naro?ito su veoma va?ni u proizvodnji nuklearne energije. Odjeljivanje izotopa vr?i se centrifugiranjem, destilacijom, difuzijom i tako dalje.
Da se jezgra atoma koja se sastoji od pozitivno nabijenih protona ne razleti, jer se istoimeni elektri?ni naboji međusobno odbijaju, uzrok su privla?ne sile koje vladaju, između protona i neutrona. To su takozvane sile jezgre ili
osnovne sile
koje, iako su vrlo velike, djeluju samo na vrlo male daljine, to jest u dimenzijama atomske jezgre. Tuma?enje tih sila spada danas u glavne probleme atomske fizike.
[3]
Sastav atomskih jezgara
[
uredi
|
uredi kod
]
Iskustvena potvrda
Rutherfordove
jednad?be, u?vrstila je pretpostavku da između
alfa-?estica
i atomskih jezgara vladaju poznate
Coulombove sile
. Na osnovu toga mo?e se prora?unati kako blizu jezgri dopre alfa-?estica koja se otklanja pod određenim kutom. ?estice vrlo velikih
brzina
mogu do?i sasvim blizu tako da je ispitana Coulombova sila sve do udaljenosti 10
-14
metara
. Dođu li izvanredno brze alfa-?estice jo? na ve?u blizinu atomskoj jezgri, slika s pokusa ne proizlazi vi?e iz odbojnog Coulombova potencijala. Između alfa-?estica i jegri javljaju se nove sile, koje znatno prevladavaju Coulombov elektri?ni potencijal. Po Rutherfordu mo?emo kao polumjer atomske jezgre odrediti onu udaljenost kod koje prestaje između alfa-?estica i atomske jezgre vrijediti Coulombova odbojna sila. Taj polumjer iznosi za najte?e atomske jezgre oko 10
-14
metara.
Bez obzira na to kakve su sile između atomskih jezgara na velikim i malim udaljenostima, osnovno na?elo
mehanike
:
zakon o odr?anju impulsa i energije
, moraju vrijediti za sve
srazove
. Predo?imo sebi alfa-?esticu, koja udari o neku drugu atomsku jezgru. Prije sraza ima alfa-?estica
impuls sile
m
1
?
v
, gdje je
m
1
masa
alfa-?estice, a
v
njena
brzina
prije sraza. Kad udari u atomsku jezgru, prenosi dio svojeg impulsa i poprima impuls
m
1
?
v
’. Po zakonu o odr?anju impulsa mora impuls alfa-?estice prije sraza biti jednak zbroju impulsa obiju ?estica poslije sraza:

Ovu vektorsku jednad?bu mo?emo pisati u komponentama u smjeru osi
y
i
x
:


Od prvobitnog smjera otklonjena je alfa-?estica za kut
θ
1
, a jezgra za kut
θ
2
. Prva nam je jednad?ba sistema ka?e da je prvobitni impuls alfa-?estice jednak zbroju impulsa obiju ?estica u prvobitnom smjeru. Druga jednad?ba ka?e da se impulsi obiju ?estica, okomiti na prvobitni smjer, poni?tavaju.
Prema zakonu o odr?anju energije mora
kineti?ka energija
alfa-?estica prije sraza biti jednaka zbroju kineti?kih energija obiju ?estica poslije sraza:

Srazove između alfa-?estica i jezgri mo?emo motriti u
Wilsonovoj komori
. Alfa-?estice poznate brzine dolaze do
radioaktivne tvari
i prolaze kroz plin komore. Tad se ?esto opazi da se staza neke alfa-?estice savije, a od mjesta pregiba odleti druga ?estica. Brzine obiju ?estica mogu se izmjeriti, a isto tako i kutovi njihovih staza s prvobitnim smjerom. Unesu li se vrijednosti iz pokusa za
v
’,
v
”,
θ
1
i
θ
2
u jednad?bu impulsa i energije, uvijek se nalazi da su jednad?be ispunjene. Zakoni o odr?anju impulsa i energije vrijede strogo za sve srazove.
Brzine ?estica nakon sraza dadu se mjeriti pomo?u savijanja u magnetskom polju ili iz duljine i debljine staze. Ali one se mogu i ukloniti iz zadnje dvije jednad?be. Tad nam preostaje jo? jedna jednad?ba, u kojoj dolaze mase ?estica i kutovi otklona:

Iz te jednad?be mo?e se prema izmjerenim kutovima
θ
1
i
θ
2
izra?unati masa udarene jezgre. Ta je metoda vrlo prikladna da se ustanovi koja je atomska jezgra u Wilsonovoj komori zadobila udarac.
?esto je najzgodnije da se promatraju sredi?nji srazovi. Tad alfa-?estica i jezgra lete u prvobitnom smjeru. U gornjim jednad?bama moramo staviti
θ
1
= 0 i
θ
2
= 0. Iz zakona o odr?anju impulsa i energije:


mo?emo isklju?ivanjem odmah izra?unati brzinu koju dobiva atomska jezgra pri srazu:

Na primjer kod udarca alfa- ?estice na
proton
(atom
vodika
) dobivamo:

To zna?i da je brzina protona 60% ve?a od prvobitne brzine alfa-?estice. No sredi?nje udareni protoni imaju najve?u brzinu. Ta najve?a brzina mo?e se mjeriti i prema mjerenjima je zaista 1,6 puta ve?a od po?etne brzine alfa-?estice. Zadnja jednad?ba omogu?uje nam da, mjere?i najve?e brzine udarenih atomskih jezgri, izra?unamo njihove mase. To je jedna od najboljih metoda da se utvrde nepoznate atomske jezgre u Wilsonovoj komori.
Pri to?nijem ispitivanju prolaza alfa-?estica kroz Wilsonovu komoru bili su ipak otkriveni i protoni s mnogo ve?im brzinama nego ?to bi to odgovaralo sredi?njem srazu. Paradoks se objasnio kad je Rutherford opazio da ti brzi protoni dolaze i onda kad alfa-?estice prolaze kroz tvari u kojima nema vodika. Rutherford je pustio alfa-?estice kroz ?isti
du?ikov
plin
i na veliko iznenađenje opazio da se od alfa-?estica odvaja staza jednog protona. Rutherford je odmah ispravno protuma?io da se tu događa pretvorba atomskih jezgara, alfa-?estica prodre u du?ikovu jezgru, a jedan proton biva izba?en. Kemijskim simbolima mo?emo tu reakciju pisati:

Gornji indeksi ozna?uju masu atomskih jezgri, a donji njihov naboj ili redni broj elementa. Primitkom jedne alfa-?estice i gubitkom jednog protona pove?ava se masa du?ikove jezgre za 3, a naboj za 1, pa iz du?ika dobivamo
kisikov
izotop
s atomskom te?inom 17.
Sad je bilo jasno, za?to se javljaju i protoni ve?ih energija nego ?to bismo ih dobili sredi?njim srazom alfa-?estica. Vi?ak energije protona potje?e od energije atomske jezgre. Reakcije atomskih jezgri mogu te?i s dobitkom ili gubitkom energije, a tu razliku u energijama nose izba?ene ?estice. Pretvorbe atomskih jezgri iznijele su na vidjelo da su protoni sastavni dijelovi svih atomskih jezgri. No vidi se odmah da pored njih moraju u izgradnji jezgri sudjelovati i druge ?estice. Dva protona dala bi dodu?e naboj helijeve jezgre, ali ta jezgra ima 4 puta ve?u masu od protona. No koje su jo? ?estice pored protona u atomskim jezgrama?
W. Bothe
i Herbert Becker su 1930. opazili da pri obasjavanju lakih elemenata alfa-?esticama nastaje neko vrlo prodorno zra?enje. Malo kasnije na?li su
I. Joliot-Curie
i
F. Joliot-Curie
da nove zrake bivaju jako apsorbirane u tvarima koje obiluju
vodikom
. Iz tih tvari nove zrake izbijaju protone s brzinama oko desetine
brzine svjetlosti
. Kakva je priroda tih zraka? Chadwick je malo kasnije ispitivao djelovanje zraka u Wilsonovoj komori. Zagonetne zrake nisu se vidjele u Wilsonovoj komori - znak da ne nose
elektri?ni naboj
. No opet to nisu mogle biti ni
gama zrake
. U Wilsonovoj komori vidi se kako lake jezgre, kao protoni, helijeve,
litijeve
,
berilijeve
i
ugljikove
jezgre, zadobivaju sna?ne udarce, ?to se ne mo?e objasniti djelovanjem
elektromagnetskih valova
.
J. Chadwick
je objasnio ova opa?anja hipotezom o novoj vrsti ?estica -
neutronima
. Te ?estice nemaju elektri?nog naboja pa ne
ioniziraju
i ne vide se u Wilsonovoj komori. Brzinu i masu nevidljivih ?estica mo?emo prora?unati tako da motrimo najve?e brzine udarenih atoma. Chadwick je mjerio najve?e brzine udarenih protona i
du?ikovih
atoma. Za omjer najve?ih brzina protona i du?ikovih jezgri dobiva se prema:

gdje je:
x
-
masa
neutrona. Najve?e brzine udarenih protona su oko 7 puta ve?e od najve?ih brzina du?ikovih atoma. Za masu neutrona dobiva se odatle vrijednost 1. Neutroni, dakle, imaju otprilike istu masu kao i protoni. Time se direktno obja?njava za?to nove zrake izbacuju sna?no protone iz tvari bogatih vodikom. Kao kod sraza biljarskih kugli, tako i tu mogu neutroni najja?e pokrenuti jednako te?ke protone.
Iste godine kad je otkriven neutron, postavili su
D. D. Ivanjenko
i
W. Heisenberg
hipotezu, da su atomske jezgre građene od protona i neutrona. Ova hipoteza odr?ala se i kasnije i temelj je ?itave
nuklearne fizike
. Pri razbijanju jezgara nalazimo uvijek protone, neutrone ili lake jezgre, a nikada ne elektrone i pozitrone.
Vidjeli smo da su atomske te?ine pribli?no cijeli brojevi. Zaokru?ene relativne atomske te?ine, kao ?iste cijele brojeve bez fizi?ke dimenzije, ozna?it ?emo s
A
.
Atomska te?ina
A
pokazuje ukupan broj sastavnih dijelova jezgre, a redni broj
Z
daje broj protona. Svaka atomska jezgra određena je s ta dva podatka:
A
i
Z
. Nađene su, ipak, i razli?ite atomske jezgre s istim
A
i
Z
, ali po svemu se ?ini da se tu radi o dva razli?ita
kvantna
stanja iste jezgre. Mi ?emo odsad pretpostaviti da atomska te?ina i redni broj jednozna?no opisuju vrstu atomske jezgre. Atomske jezgre s jednakim brojem protona, a razli?itom masom, zovemo
izotopima
. Atomske jezgre s jednakim brojem ?estica zovu se izobare.
Atomskih jezgara ima mnogo vi?e od
kemijskih elemenata
, jer neki kemijski elementi imaju i preko 10 razli?itih izotopa. Mo?e se grafi?ki dobiti lijep pregled nad svim jezgrama tako da pojedine jezgre nanesemo kao to?ke u kri?aljku, kod koje apscisa određuje broj protona, a ordinata broj neutrona. Iz polo?aja jezgre u tablici mo?e se odmah razabrati od koliko je protona i neutrona građena. Izvu?ena dijagonala na tablici ozna?uje one jezgre kod kojih je broj protona jednak broju neutrona. Ispod dijagonale broj je protona ve?i od broja neutrona, a iznad dijagonale prete?e broj neutrona u jezgri.
Ve? kratki pregled nad poznatim jezgrama odmah pokazuje da u prirodi nisu ostvarene sve mogu?e kombinacije između protona i neutrona. Kod jezgri je broj protona pribli?no jednak broju neutrona. Kod lakih jezgri vrijedi ovaj zakon vrlo to?no. Naj?e??e jezgre u prirodi, kao
helij
2
He
4
,
ugljik
6
C
12
,
du?ik
7
N
14
,
kisik
8
O
16
, magnezij
12
Mg
24
,
silicij
14
Si
28
,
sumpor
16
S
32
,
kalcij
20
Ca
40
, građene su od jednakog broja protona i neutrona. Dolaze i izotopi tih jezgri, kod kojih je ta simetrija između protona i neutrona za jednu ili dvije ili tri ?estice naru?ena, ali se ipak sve te jezgre gomilaju oko dijagonale kod koje je broj protona jednak broju neutrona. Ta pribli?no ostvarena simetrija između broja neutrona i protona jedan je od temeljnih zakona fizike jezgre, i mi ?emo morati tra?iti razlog te simetrije. Kod te?ih jezgri prevladava sve vi?e broj neutrona nad brojem protona. Suvi?ak neutrona nad protonima iznosi kod te?kih jezgri po vi?e desetaka. "Rijeka" jezgri zavr?ava s
uranijem
, koji ima elektri?ni naboj 92 i masu 238. Broj neutrona kod te jezgre jednak je razlici između mase i naboja, dakle 238 - 92 = 146. Suvi?ak neutrona nad protonima iznosi kod toga glavnog uranijevog izotopa 54. Simetrija je tu ve? znatno naru?ena.
[4]
- ↑
atom
.
Hrvatska enciklopedija
. Leksikografski zavod Miroslav Krle?a. 2019.
- ↑
nuklearna fizika
.
Hrvatska enciklopedija
. Leksikografski zavod Miroslav Krle?a. 2019.
- ↑
Velimir Kruz: "Tehni?ka fizika za tehni?ke ?kole", "?kolska knjiga" Zagreb, 1969.
- ↑
Ivan Supek
: "Nova fizika", ?kolska knjiga Zagreb, 1966.