 Os dimeros de
acidos carboxilicos
poden formarse en fase de vapor.
Os dimeros de
acidos carboxilicos
poden formarse en fase de vapor.
Un
dimero
e unha entidade quimica que consta de duas moleculas (unidades
monomeras
) estruturalmente similares unidas entre si por enlaces fortes ou febles,
covalentes
ou
intermoleculares
. As veces as duas moleculas son identicas (
homodimero
) e outras son distintas (
heterodimero
). A union das duas moleculas para formar o dimero denominase dimerizacion
[
1
]
, e o inverso da dimerizacion xeralmente se chama disociacion. Analogamente, falase de heterodimerizacion e homodimerizacion.
 Modelo do dimero da
galactosa-1-fosfato uridililtransferase
(
GALT
) de
E. coli
en complexo con UDP-galactosa. Poden verse ions potasio, cinc, e ferro como esferas de cor purpura, gris e bronce.
Modelo do dimero da
galactosa-1-fosfato uridililtransferase
(
GALT
) de
E. coli
en complexo con UDP-galactosa. Poden verse ions potasio, cinc, e ferro como esferas de cor purpura, gris e bronce.
En
bioquimica
, un dimero e un complexo macromolecular formado por duas moleculas, xeralmente
proteinas
ou
acidos nucleicos
, normalmente unidos de forma non
covalente
. As
clorofilas
do
centro de reaccion
dos
fotosistemas
forman tamen un dimero.
Nas proteinas os dimeros son un tipo de
estrutura cuaternaria
. Os homodimeros estan formados por duas moleculas identicas; un exemplo e a
ciclooxixenase
(COX). Os heterodimeros estan formados por duas moleculas diferentes; un exemplo e a tubulina, formada por monomeros de alfa e beta
tubulina
.
A maioria dos dimeros en bioquimica non estan conectados por enlaces covalentes. Un exemplo de heterodimero unido de forma non covalente e o
encima
transcriptase inversa
, que esta composto por duas cadeas polipeptidicas diferentes.
[
2
]
Os dimeros unidos covalentemente (por
pontes disulfuro
) son mais raros; un exemplo e a proteina homodimera
NEMO
.
[
3
]
Algunhas proteinas contenen dominios especializados que facilitan a dimerizacion, chamados dominios de dimerizacion. Un estudo atopou que as interfaces polas que se unen os homodimeros e heterodimeros son algo diferentes. Nos homodimeros hai en total mais residuos de aminoacidos e pontes de hidroxeno, ainda que a densidade de pontes de hidroxeno por residuo e maior nos heterodimeros. Nas interfaces de heterodimeros hai mais residuos cargados e
hidrofilicos
e nos homodimeros predominan os
hidrofobicos
.
[
4
]
A dimerizacion ou a disociacion poden facer cambiar o estado funcional da proteina de activo a inactivo ou viceversa. Por exemplo a
glicoxeno fosforilase
existe como monomero inactivo e so se activa cando se dimeriza.
[
5
]
Os
dimeros de pirimidinas
formanse por
reaccion fotoquimica
a partir de
bases nitroxenadas
pirimidinicas
do
ADN
. Esta reaccion causa
mutacions
no ADN, que poden ser
carcinoxenas
e orixinar
cancro de pel
.
Os
acidos carboxilicos
forman dimeros por formacion de
pontes de hidroxeno
entre o hidroxeno acido e o oxixeno
carbonilico
en condicions anhidro. Por exemplo, o
acido acetico
forma un dimero en fase de gas, no que as unidades monomeras se unen por pontes de hidroxeno. En condicions especiais, a maioria das moleculas que contenen
grupos OH
forman dimeros (por exemplo o
dimero de auga
).
O borano ("BH
3
") aparece como o dimero
diborano
(B
2
H
6
), debido a alta
acidez de Lewis
do centro de
boro
.
Os
excimeros
e
exciplexos
son estruturas
excitadas
de curta duracion. Por exemplo, os
gases nobres
non forman dimeros estables, pero forman os excimeros Ar
2
*, Kr
2
* e Xe
2
* en condicions de altas presions e estimulacion electrica.
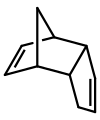 O dimero do
ciclopentadieno
ainda que pode non ser distinguible facilmente nunha inspeccion inicial.
O dimero do
ciclopentadieno
ainda que pode non ser distinguible facilmente nunha inspeccion inicial.
Os dimeros moleculares formanse a miudo pola reaccion de dous compostos identicos, como por exemplo: 2A → A-A. Neste exemplo, o
monomero
"A" dise que se dimeriza para dar o dimero "A-A". Un exemplo real son os
diaminocarbenos
, que se dimerizan dando un
tetraaminoetileno
:
- 2 C(NR
2
)
2
→ (R
2
N)
2
C=C(NR
2
)
2
Os
carbenos
son moi reactivos e forman enlaces doadamente.
O
diciclopentadieno
e un dimero asimetrico de duas moleculas de
ciclopentadieno
que reaccionaron pola
reaccion de Diels-Alder
para dar o produto. Sometido a calor sofre a reaccion inversa (retro-Diels-Alder) para dar os dous monomeros iguais:
- C
10
H
12
→ 2 C
5
H
6
Moitos elementos non metalicos aparecen como moleculas diatomicas e as veces falase delas denominandoas dimeros:
hidroxeno
,
nitroxeno
,
oxixeno
, os
haloxenos
(
fluor
,
cloro
,
bromo
e
iodo
). O
mercurio
parece como mercurio(I) cation (Hg
2
+
), formalmente un heterodimero.
No contexto da quimica de
polimeros
, "dimero" tamen se refire ao grao de polimerizacion 2, en relacion coa estequiometria das reaccions de condensacion. Un exemplo serian os
disacaridos
, formados por dous
monosacaridos
. Por exemplo, a
celobiosa
e un dimero de
glicosa
, ainda que na reaccion se produce auga:
- 2C
6
H
12
O
6
→ C
12
H
22
O
11
+ H
2
O
Aqui, o dimero ten unha estequiometria diferente a do par de monomeros.
- ↑
"IUPAC "Gold Book" definition"
. Consultado o
2009-04-30
.
- ↑
Sluis-Cremer N, Hamamouch N, San Felix A, Velazquez S, Balzarini J, Camarasa MJ (2006). "Structure-activity relationships of [2',5'-bis-O-(tert-butyldimethylsilyl)-beta-D-ribofuranosyl]- 3'-spiro-5' '-(4' '-amino-1' ',2' '-oxathiole-2' ',2' '-dioxide)thymine derivatives as inhibitors of HIV-1 reverse transcriptase dimerization".
J. Med. Chem.
49
(16): 4834?41.
PMID
16884295
.
doi
:
10.1021/jm0604575
.
- ↑
Herscovitch M, Comb W, Ennis T, Coleman K, Yong S, Armstead B, Kalaitzidis D, Chandani S, Gilmore TD (2008).
"Intermolecular disulfide bond formation in the NEMO dimer requires Cys54 and Cys347"
.
Biochem. Biophys. Res. Commun.
367
(1): 103?8.
PMC
2277332
.
PMID
18164680
.
doi
:
10.1016/j.bbrc.2007.12.123
.
- ↑
Cui Zhanhua, Jacob Gah-Kok Gan, Li lei, Meena Kishore Sakharkar, and Pandjassarame Kangueane. Protein subunit interfaces: heterodimers versus homodimers
Bioinformation. 2005; 1(2): 28?39. Published online 2005 August 11. PMCID: PMC1891636
[1]
- ↑
Browner MF, Fletterick RJ (1992). "Phosphorylase: a biological transducer".
Trends in Biochemical Science
17
(2): 66?71.
PMID
1566331
.
doi
:
10.1016/0968-0004(92)90504-3
.