| Boro
←
Carbono
→
Nitrogeno
|
|---|
|
|
|
Tabla completa
?
Tabla ampliada
|

A la derecha, fragmento de carbono vitrificado de 570 g. A la izquierda, pequeno cubo de grafito (1 cm
3
).
|
| Informacion general
|
|---|
| Nombre
,
simbolo
,
numero
|
Carbono, C, 6.
|
|---|
| Serie quimica
|
No metales
|
|---|
| Grupo
,
periodo
,
bloque
|
14
,
2
,
p
|
|---|
| Masa atomica
|
12,0107
u
|
|---|
| Configuracion electronica
|
[
He
] 2
s
2
2
p
2
|
|---|
| Dureza Mohs
|
1-2 (grafito)
10 (diamante)
|
|---|
| Electrones
por
nivel
|
2, 4
|
|---|
| Apariencia
|
Negro (grafito)
Incoloro (diamante)
|
|---|
| Propiedades atomicas
|
|---|
| Radio medio
|
70
pm
|
|---|
| Electronegatividad
|
2,55
(
escala de Pauling
)
|
|---|
| Radio atomico
(calc)
|
67
pm
(
radio de Bohr
)
|
|---|
| Radio covalente
|
77
pm
|
|---|
| Radio de van der Waals
|
170
pm
|
|---|
| Estado(s) de oxidacion
|
4
, 2
|
|---|
| Oxido
|
Acido debil
|
|---|
| 1.ª
energia de ionizacion
|
1086,5
kJ/mol
|
|---|
| 2.ª
energia de ionizacion
|
2352,6 kJ/mol
|
|---|
| 3.ª
energia de ionizacion
|
4620,5 kJ/mol
|
|---|
| 4.ª
energia de ionizacion
|
6222,7 kJ/mol
|
|---|
| 5.ª
energia de ionizacion
|
37 831,1 kJ/mol
|
|---|
| 6.ª
energia de ionizacion
|
47 277,1 kJ/mol
|
|---|
| Lineas espectrales
|
 |
|---|
| Propiedades fisicas
|
|---|
| Estado ordinario
|
Solido
(
no magnetico
)
|
|---|
| Densidad
|
2267
kg/m
3
|
|---|
| Punto de fusion
|
Diamante
: 3 823 343 K (3 823 070 °C)
Grafito
: 3800 K (3527 °C)
|
|---|
| Punto de ebullicion
|
Grafito: 5100
Diamante: 8,750,900
|
|---|
| Entalpia de vaporizacion
|
Grafito; sublima: 711
kJ/mol
|
|---|
| Entalpia de fusion
|
Grafito;
sublima
: 105
kJ/mol
|
|---|
| Varios
|
|---|
| Estructura cristalina
|
hexagonal
|
|---|
| Calor especifico
|
710
J
/(
K
·
kg
)
|
|---|
| Conductividad electrica
|
61×10
3
S
/
m
|
|---|
| Conductividad termica
|
129
W/(K·m)
|
|---|
| Velocidad del sonido
|
Diamante: 18.350
m/s
a 293,15
K
(20
°C
)
|
|---|
| Isotopos mas estables
|
|---|
|
Articulo principal:
Isotopos del carbono
|
|
|
| Valores en el
SI
y
condiciones normales de presion y temperatura
, salvo que se indique lo contrario.
|
|
Este articulo trata sobre un elemento quimico. Para la letra latina con el mismo simbolo, vease
C
.
El
carbono
(del
latin
,
carbo
, 'carbon') es un
elemento quimico
con
simbolo
C
,
numero atomico
6
y
masa atomica
12,01
. Es un
no metal
y
tetravalente
, disponiendo de 4 electrones y 6 protones para formar enlaces quimicos
covalentes
. Tres
isotopos del carbono
se producen de forma natural, los estables
12
C
y
13
C
y el
isotopo radiactivo
14
C
, que decae con una
vida media
de unos 5730 anos.
[
1
]
El carbono es uno de los
pocos elementos conocidos desde la antiguedad
,
[
2
]
y es el pilar basico de la
quimica organica
. Esta presente en la Tierra en estado de cuerpo simple (
carbon
y
diamantes
), de
compuestos inorganicos
(CO
2
y CaCO
3
) y de
compuestos organicos
(
biomasa
,
petroleo
y
gas natural
). Tambien se han sintetizado muchas nuevas estructuras basadas en el carbono:
carbon activado
,
negro de humo
,
fibras
,
nanotubos
,
fullerenos
y
grafeno
.
El carbono es el 15.º elemento mas abundante en la corteza terrestre,
[
3
]
y el cuarto elemento mas
abundante en el universo en masa
despues del
hidrogeno
, el
helio
y el
oxigeno
. La abundancia del carbono, su diversidad unica de
compuestos organicos
y su inusual capacidad para formar
polimeros
a las temperaturas comunmente encontradas en la
Tierra
, permite que este elemento sirva como componente comun de
toda la vida conocida
. Es el segundo elemento mas abundante en el
cuerpo humano
en masa (aproximadamente el 18,5%) despues del oxigeno.
[
4
]
Los atomos de carbono pueden unirse de diferentes maneras, denominadas
alotropos del carbono
, reflejo de las condiciones de formacion. Los mas conocidos que ocurren naturalmente son el
grafito
, el
diamante
y el
carbono amorfo
.
[
5
]
Las
propiedades fisicas
del carbono varian ampliamente con la forma alotropica. Por ejemplo, el grafito es
opaco
y negro, mientras que el diamante es altamente
transparente
. El grafito es lo suficientemente blando como para formar una raya en el papel (de ahi su nombre, del verbo griego "γρ?φειν" que significa 'escribir'), mientras que el diamante es el material natural mas duro conocido. El grafito es un buen
conductor electrico
mientras que el diamante tiene una baja
conductividad electrica
. En condiciones normales, el diamante, los
nanotubos de carbono
y el
grafeno
tienen las
conductividades termicas
mas altas de todos los materiales conocidos. Todos los alotropos del carbono son
solidos
en condiciones normales, siendo el grafito la forma
termodinamicamente estable
. Son quimicamente resistentes y requieren altas temperaturas para reaccionar incluso con oxigeno.
El
estado de oxidacion
mas comun del carbono en los
compuestos inorganicos
es +4, mientras que +2 se encuentra en el
monoxido de carbono
y en complejos
carbonilos
de
metales de transicion
. Las mayores fuentes de carbono inorganico son las
calizas
,
dolomitas
y
dioxido de carbono
, pero cantidades significativas se producen en depositos organicos de
carbon
,
turba
,
petroleo
y
clatratos de metano
. El carbono forma un gran numero de compuestos, mas que cualquier otro elemento, con casi diez millones de compuestos descritos hasta la fecha
[
6
]
(con 500.000 compuestos nuevos por ano), siendo sin embargo ese numero solo una fraccion del numero de compuestos teoricamente posibles bajo condiciones estandar. Por esta razon, a menudo el carbono se ha descrito como el ≪rey de los elementos≫.
[
7
]
La combustion del carbono en todas sus formas ha sido la base del desarrollo tecnologico desde tiempos prehistoricos. Los materiales basados en el carbono tienen aplicaciones en numerosas areas de vanguardia tecnologica:
materiales compuestos
,
baterias de iones de litio
,
descontaminacion del aire y del agua
,
electrodos
para
hornos de arco
, en la
sintesis de aluminio
, etc.
Caracteristicas
[
editar
]
El carbono es un elemento notable por varias razones. Sus formas
alotropicas
incluyen, una de las sustancias mas blandas (el grafito) y una de las mas duras (el diamante) y, desde el punto de vista economico, es de los materiales mas baratos (carbon) y uno de los mas caros (diamante). Mas aun, presenta una gran afinidad para enlazarse quimicamente con otros atomos pequenos, incluyendo otros atomos de carbono con los que puede formar largas cadenas, y su pequeno
radio atomico
le permite formar enlaces multiples. Asi, con el
oxigeno
forma el
dioxido de carbono
, vital para el crecimiento de las
plantas
(ver
ciclo del carbono
); con el
hidrogeno
forma numerosos compuestos denominados genericamente
hidrocarburos
, esenciales para la industria y el transporte en la forma de
combustibles fosiles
; y combinado con
oxigeno
e hidrogeno forma gran variedad de compuestos como, por ejemplo, los
acidos grasos
, esenciales para la vida, y los
esteres
que dan sabor a las frutas; ademas es vector, a traves del
ciclo carbono-nitrogeno
, de parte de la
energia
producida por el
Sol
.
[
8
]
Estados alotropicos
[
editar
]
 Grafito (izquierda) y diamante (derecha), dos alotropos del carbono.
Grafito (izquierda) y diamante (derecha), dos alotropos del carbono.
 Estructura del grafito
Estructura del grafito
Se conocen cinco formas alotropicas del carbono, ademas del amorfo:
grafito
,
diamante
,
fullereno
,
grafeno
y
carbino
.
[
9
]
Una de las formas en las cuales se encuentra el carbono es el grafito, caracterizado por tener sus atomos "en los vertices de hexagonos que tapizan un plano",
[
10
]
es de color negro, opaco y blando, y es el material del cual esta hecha la parte interior de los lapices de madera. El grafito tiene exactamente los mismos atomos del diamante, pero por estar dispuestos en diferente forma tienen distintas propiedades fisicas y quimicas. Los diamantes naturales se forman en lugares donde el carbono ha sido sometido a grandes presiones y altas temperaturas. Su estructura es tetraedrica, que da como resultado una red tridimensional y a diferencia del grafito tiene un grado de dureza alto: 10 Mohs. Los diamantes se pueden crear artificialmente, sometiendo el grafito a temperaturas y presiones muy altas. El precio del grafito es menor al de los diamantes naturales, pero si se han elaborado adecuadamente tienen la misma dureza, color y transparencia.
La forma amorfa es esencialmente grafito, pero no llega a adoptar una estructura cristalina macroscopica. Esta es la forma presente en la mayoria de los
carbones
y en el hollin.
 Disposicion geometrica de los orbitales hibridos sp
2
.
Disposicion geometrica de los orbitales hibridos sp
2
.
A presion normal, el carbono adopta la forma del
grafito
, en la que cada atomo esta unido a otros tres en un plano compuesto de celdas hexagonales; este estado se puede describir como tres
electrones
de valencia en
orbitales
hibridos planos sp² y el cuarto en el orbital
p
.
Las dos formas de grafito conocidas alfa (hexagonal) y beta (romboedrica) tienen propiedades fisicas identicas. Los grafitos naturales contienen mas del 30 % de la forma beta, mientras que el grafito sintetico contiene unicamente la forma alfa. La forma alfa puede transformarse en beta mediante procedimientos mecanicos, y esta recristalizar en forma alfa al calentarse por encima de 1000
°C
.
 Estructura del diamante
Estructura del diamante
Debido a la deslocalizacion de los
electrones
del
orbital pi
, el grafito es
conductor
de la electricidad, propiedad que permite su uso en procesos de
electroerosion
. El material es blando y las diferentes capas, a menudo separadas por atomos intercalados, se encuentran unidas por
enlaces de Van de Waals
, siendo relativamente facil que unas deslicen respecto de otras, lo que le da utilidad como
lubricante
.
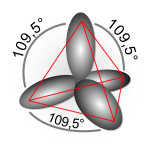 Disposicion geometrica de los orbitales hibridos sp
3
.
Disposicion geometrica de los orbitales hibridos sp
3
.
A muy altas presiones, el carbono adopta la forma del
diamante
, en el cual cada atomo esta unido a otros cuatro atomos de carbono, encontrandose los 4 electrones en orbitales sp³, como en los hidrocarburos. El diamante presenta la misma
estructura
cubica que el
silicio
y el
germanio
y, gracias a la resistencia del
enlace quimico
carbono-carbono, es, junto con el
nitruro de boro
, la sustancia mas
dura
conocida. La transicion a grafito a temperatura ambiente es tan lenta que es indetectable. Bajo ciertas condiciones, el carbono cristaliza como
lonsdaleita
, una forma similar al diamante pero hexagonal.
El orbital hibrido sp
1
que forma
enlaces covalentes
solo es de interes en
quimica
, manifestandose en algunos compuestos, como por ejemplo el
acetileno
.
 Fullereno C
60
.
Fullereno C
60
.
Los
fullerenos
fueron descubiertos hace 15 anos
[
10
]
tienen una estructura similar al grafito, pero el empaquetamiento hexagonal se combina con pentagonos (y en ciertos casos, heptagonos), lo que curva los planos y permite la aparicion de estructuras de forma
esferica
,
elipsoidal
o
cilindrica
. El constituido por 60 atomos de carbono, que presenta una estructura tridimensional y geometria similar a un balon de futbol, es especialmente estable. Los fullerenos en general, y los derivados del C
60
en particular, son objeto de intensa investigacion en quimica desde su descubrimiento a mediados de los 1980.
A esta familia pertenecen tambien los
nanotubos de carbono
, que pueden describirse como capas de grafito enrolladas en forma cilindrica y rematadas en sus extremos por hemiesferas (fulerenos), y que constituyen uno de los primeros productos industriales de la
nanotecnologia
.
Aplicaciones
[
editar
]
El principal uso industrial del carbono es como un componente de hidrocarburos, especialmente los combustibles fosiles (
petroleo
y
gas natural
). Del primero se obtienen, por
destilacion
en las
refinerias
,
gasolinas
,
queroseno
y
aceites
, siendo ademas la materia prima empleada en la obtencion de
plasticos
. El segundo se esta imponiendo como
fuente de energia
por su combustion mas limpia. Otros usos son:
- El isotopo radiactivo
carbono-14
, descubierto el 27 de febrero de 1940, se usa en la
datacion radiometrica
.
- El
grafito
se combina con
arcilla
para fabricar las minas de los
lapices
. Ademas se utiliza como aditivo en lubricantes. Las pinturas anti-radar utilizadas en el camuflaje de vehiculos y aviones militares estan basadas igualmente en el grafito, intercalando otros compuestos quimicos entre sus capas. Es negro y blando. Sus atomos estan distribuidos en capas paralelas muy separadas entre si. Se forma a menos presion que el diamante. Aunque parezca dificil de creer, un diamante y la mina de un lapicero tienen la misma composicion quimica: carbono.
- El
diamante
es transparente y muy duro. En su formacion, cada atomo de carbono esta unido de forma compacta a otros cuatro atomos. Se originan con temperaturas y presiones altas en el interior de la tierra. Se emplea para la construccion de
joyas
y como material de corte aprovechando su dureza.
- Como elemento de aleacion principal de los
aceros
.
- En varillas de proteccion de
reactores nucleares
.
- Las pastillas de
carbon
se emplean en
medicina
para absorber las toxinas del sistema digestivo y como remedio de la
flatulencia
.
- El carbon activado se emplea en sistemas de filtrado y purificacion de agua.
- El carbon amorfo ("
hollin
") se anade a la
goma
para mejorar sus propiedades mecanicas. Ademas se emplea en la formacion de electrodos (p. ej. de las
baterias
). Obtenido por sublimacion del grafito, es fuente de los fullerenos que pueden ser extraidos con disolventes organicos.
- Los fullerenos se emplean en medicina, se ha probado que un derivado soluble en agua del C
60
inhibe a los virus de inmunodeficiencia humana VIH-1 y VIH-2.
[
10
]
- La
fibra de carbono
(obtenido generalmente por termolisis de fibras de poliacrilato) debido a que son de alta resistencia se anade a resinas de poliester, obteniendose los materiales denominados
fibras de carbono
, son empleadas para fabricar raquetas de tenis.
- La fibra de carbono tambien se utiliza para la elaboracion de bicicletas de gama alta, logrando un menor peso, mayor resistencia y mejor geometria.
- Las propiedades quimicas y estructurales de los
fullerenos
, en la forma de
nanotubos
, prometen usos futuros en el incipiente campo de la nanotecnologia.
Historia
[
editar
]
El carbono fue descubierto en la prehistoria y ya era conocido en la antiguedad, a pesar de que en esta la manufacturaban mediante la
combustion incompleta
de materiales organicos. Los ultimos alotropos conocidos, los fullerenos (C
60
), fueron descubiertos como subproducto en experimentos realizados con gases moleculares en la decada de los 80. Se asemejan a un balon de futbol, por lo que coloquialmente se les llama futbolenos.
Newton
, en 1704, intuyo que el diamante podia ser combustible, pero no se consiguio quemar un diamante hasta 1772 en que
Lavoisier
demostro que en la reaccion de combustion se producia CO
2
.
Tennant
demostro que el diamante era carbono puro en 1797. El isotopo mas comun del carbono es el
12
C; en 1961 este isotopo se eligio para reemplazar al isotopo oxigeno-16 como base de los pesos atomicos, y se le asigno un peso atomico de 12.
Los primeros compuestos de carbono se identificaron en la materia viva a principios del siglo
XIX
, y por ello el estudio de los compuestos de carbono se llamo quimica organica.
Abundancia y obtencion
[
editar
]
El carbono no se creo durante el
Big Bang
porque hubiera necesitado la
triple colision
de
particulas alfa
(
nucleos atomicos
de
helio
) y el Universo se expandio y enfrio demasiado rapido para que la probabilidad de que ello aconteciera fuera significativa. Donde si ocurre este proceso es en el interior de las
estrellas
(en la fase
RH (Rama horizontal)
) donde este elemento es abundante, encontrandose ademas en otros cuerpos celestes como los cometas y en las atmosferas de los planetas. Algunos
meteoritos
contienen diamantes microscopicos que se formaron cuando el
Sistema Solar
era aun un
disco protoplanetario
.
En combinaciones con otros elementos, el carbono se encuentra en la atmosfera terrestre y disuelto en el agua, y acompanado de menores cantidades de
calcio
,
magnesio
y
hierro
forma enormes masas
rocosas
(
caliza
,
dolomita
,
marmol
, etc).
El grafito se encuentra en grandes cantidades en
Rusia
,
Estados Unidos
,
Mexico
,
Groenlandia
y la
India
.
Los diamantes naturales se encuentran asociados a
rocas volcanicas
(
kimberlita
y
lamproita
). Los mayores depositos de diamantes se encuentran en el
Africa
(
Sudafrica
,
Namibia
,
Botsuana
,
Republica del Congo
y
Sierra Leona
).
[
11
]
Existen ademas depositos importantes en
Canada
,
Rusia
,
Brasil
y
Australia
.
[
cita requerida
]
Compuestos inorganicos
[
editar
]
El mas importante
oxido
de carbono es el
dioxido de carbono
(CO
2
), un componente minoritario de la atmosfera terrestre (del orden del 0,04 % en peso) producido y usado por los seres vivos (ver
ciclo del carbono
). En el agua forma trazas de
acido carbonico
(H
2
CO
3
) ?las burbujas de muchos refrescos? pero, al igual que otros compuestos similares, es inestable, aunque a traves de el pueden producirse
iones
carbonato estables por
resonancia
. Algunos
minerales
importantes, como la
calcita
, son carbonatos.
Los otros oxidos son el
monoxido de carbono
(CO) y el mas raro
suboxido de carbono
(C
3
O
2
). El monoxido se forma durante la combustion incompleta de materias organicas y es incoloro e inodoro. Dado que la molecula de CO contiene un enlace triple, es muy polar, por lo que manifiesta una acusada tendencia a unirse a la
hemoglobina
, formando un nuevo compuesto muy peligroso denominado Carboxihemoglobina, impidiendoselo al oxigeno, por lo que se dice que es un
asfixiante
de sustitucion. El ion
cianuro
(CN
?
), tiene una estructura similar y se comporta como los iones
haluro
.
Con
metales
, el carbono forma tanto
carburos
como
acetiluros
, ambos muy
acidos
. A pesar de tener una
electronegatividad
alta, el carbono puede formar carburos covalentes como es el caso de
carburo de silicio
(SiC) cuyas propiedades se asemejan a las del
diamante
.
Isotopos
[
editar
]
En 1961 la
IUPAC
adopto el
isotopo
12
C
como la base para la
masa atomica
de los elementos quimicos.
El
carbono-14
es un
radioisotopo
con un
periodo de semidesintegracion
de 5730 anos que se emplea de forma extensiva en la datacion de especimenes organicos.
Los isotopos naturales y estables del carbono son el
12
C (98,89 %) y el
13
C
(1,11 %). Las proporciones de estos isotopos en un ser vivo se expresan en variacion (±‰) respecto de la referencia VPDB (
Vienna Pee Dee Belemnite
, fosiles
cretacicos
de
belemnites
, en
Carolina del Sur
). El δC-13 del CO
2
de la
atmosfera terrestre
es ?7‰. El carbono fijado por
fotosintesis
en los tejidos de las
plantas
es significativamente mas pobre en
13
C que el CO
2
de la atmosfera.
La mayoria de las plantas presentan valores de δC-13 entre ?24 y ?34‰. Otras plantas acuaticas, de desierto, de marismas saladas y hierbas tropicales, presentan valores de δC-13 entre ?6 y ?19‰ debido a diferencias en la reaccion de fotosintesis. Un tercer grupo intermedio constituido por las
algas
y
liquenes
presentan valores entre ?12 y ?23‰. El estudio comparativo de los valores de δC-13 en plantas y organismos puede proporcionar informacion valiosa relativa a la cadena alimenticia de los seres vivos.
Precauciones
[
editar
]
 Obrero en la planta de
negro de carbon
en
Sunray, Texas
(foto por
John Vachon
, 1942)
Obrero en la planta de
negro de carbon
en
Sunray, Texas
(foto por
John Vachon
, 1942)
Los compuestos de carbono tienen un amplio rango de
toxicidad
. El
monoxido de carbono
, presente en los gases de escape de los motores de combustion y el
cianuro
(CN) son
extremadamente toxicos
para los mamiferos, entre ellos las personas. Los
gases
organicos
eteno
,
etino
y
metano
son
explosivos e inflamables
en presencia de aire. Por el contrario, muchos otros compuestos no son toxicos sino esenciales para la vida.
El carbono puro tiene una
toxicidad
extremadamente baja para los humanos y puede ser manejado e incluso ingerido en forma segura en la forma de
grafito
o
carboncillo
. Es resistente a la disolucion y ataque quimico, incluso en los contenidos acidificados del
tracto digestivo
. Esto resulta en que una vez que entra a los tejidos corporales lo mas probable es que permanezcan alli en forma indefinida. El
negro de carbon
fue probablemente el primer
pigmento
en ser usado para hacer
tatuajes
y se encontro que
Otzi el hombre del hielo
tenia tatuajes hechos con carbon que sobrevivieron durante su vida y 5200 anos despues de su muerte.
[
12
]
Sin embargo, la inhalacion en grandes cantidades del polvo de carbon u hollin (negro de carbon) puede ser peligroso, al irritar los tejidos del
pulmon
y causar una enfermedad conocida como
neumoconiosis de los mineros del carbon
. De forma similar el polvo de diamante usado como un abrasivo puede ser danino si se ingiere o inhala. Tambien las microparticulas de carbon producidas por los gases de escape de los
motores diesel
se pueden acumular en los pulmones al ser inhaladas.
[
13
]
En estos ejemplos, los efectos daninos pueden resultar de la contaminacion de las particulas de carbon con elementos quimicos organicos o de
metales pesados
mas que del carbon en si mismo.
Generalmente el carbono tiene baja toxicidad para casi toda la
vida en la Tierra
, sin embargo, para algunas criaturas es toxico - por ejemplo, las
nanoparticulas
de carbon son
toxinas
mortales para la
Drosophila
.
[
14
]
Tambien el carbono se puede quemar vigorosa y brillantemente en la presencia de aire a alta temperatura, como en el caso del
Incendio de Windscale
, el que fue causado por la repentina liberacion de
energia Wigner
acumulada en el nucleo de grafito. Grandes acumulaciones de carbon, que han permanecido inertes por centenares de millones de anos en la ausencia de
oxigeno
, pueden
incendiarse espontaneamente
cuando son expuestas al aire, como por ejemplo en los desechos de las
minas de carbon
.
Entre la gran variedad de compuestos de carbono se pueden incluir
venenos
letales tales como la
tetradotoxina
, la
ricina
lectina
obtenida de las semillas de
ricino
(
Ricinus communis
), el
cianuro
(CN
?
) y el
envenenamiento por monoxido de carbono
.
Vease tambien
[
editar
]
Referencias
[
editar
]
- ↑
≪Carbon ? Naturally occurring isotopes≫
. WebElements Periodic Table
. Consultado el 9 de octubre de 2008
.
- ↑
≪History of Carbon≫
. Archivado desde
el original
el 1 de noviembre de 2012
. Consultado el 10 de enero de 2013
.
- ↑
Vease el articulo de la Wikipedia en ingles ≪Abundance of elements in Earth's crust≫, que recoge las estimaciones de varios autores.
- ↑
≪Biological Abundance of Elements≫
. The Internet Encyclopedia of Science
. Consultado el 9 de octubre de 2008
.
- ↑
≪World of Carbon ? Interactive Nano-visulisation in Science & Engineering Education (IN-VSEE)≫
. Archivado desde
el original
el 5 de octubre de 2008
. Consultado el 9 de octubre de 2008
.
- ↑
Chemistry Operations (15 de diciembre de 2003).
≪Carbon≫
. Los Alamos National Laboratory. Archivado desde
el original
el 13 de septiembre de 2008
. Consultado el 9 de octubre de 2008
.
- ↑
Deming, Anna (2010).
≪King of the elements?≫
.
Nanotechnology
21
.
doi
:
10.1088/0957-4484/21/30/300201
. Consultado el 15 de noviembre de 2016
.
- ↑
Carbono. Galilei
- ↑
≪Enlace externo a carbinos≫
.
- ↑
a
b
c
Gasque, Laura.
El elemento con multiples personalidades
.
- ↑
≪Carbono≫
.
- ↑
Dorfer, Leopold; Moser, M; Spindler, K; Bahr, F; Egarter-Vigl, E; Dohr, G (1998). ≪5200-year old acupuncture in Central Europe?≫.
Science
282
(5387): 242-243.
Bibcode
:
1998Sci...282..239D
.
PMID
9841386
.
doi
:
10.1126/science.282.5387.239f
.
- ↑
Donaldson, K; Stone, V; Clouter, A; Renwick, L; MacNee, W (2001).
≪Ultrafine particles≫
.
Occupational and Environmental Medicine
58
(3): 211-216.
PMC
1740105
.
PMID
11171936
.
doi
:
10.1136/oem.58.3.211
.
- ↑
Carbon Nanoparticles Toxic To Adult Fruit Flies But Benign To Young
ScienceDaily (Aug. 17, 2009)
Enlaces externos
[
editar
]