| P53
|
|
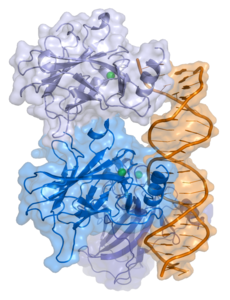
| Bander-/Oberflachenmodell von p53 an DNA nach
PDB
1TUP
|
|
Vorhandene Strukturdaten:
1a1u
,
1aie
,
1c26
,
1gzh
,
1hs5
,
1kzy
,
1olg
,
1olh
,
1pes
,
1pet
,
1sae
,
1saf
,
1sag
,
1sah
,
1sai
,
1saj
,
1sak
,
1sal
,
1tsr
,
1tup
,
1uol
,
1ycs
,
2ac0
,
2ady
,
2ahi
,
2ata
,
2b3g
,
2bim
,
2bin
,
2bio
,
2bip
,
2biq
,
2fej
,
2gs0
,
2h1l
,
2j1w
,
2j1x
,
2j1y
,
2j1z
,
2j20
,
2j21
,
2ocj
,
3sak
|
| Eigenschaften des menschlichen Proteins
|
| Masse
/Lange
Primarstruktur
|
393 Aminosauren
|
| Kofaktor
|
Zn
2+
|
| Isoformen
|
2
|
| Bezeichner
|
| Gen-Namen
|
TP53
; LFS1; TRP53; p53
|
| Externe IDs
|
|
| Vorkommen
|
| Homologie-Familie
|
TP53
|
| Ubergeordnetes
Taxon
|
Wirbeltiere
|
Das
Protein
p53
ist in vielen
Typen
von entarteten Zellen in erhohter Menge messbar. Es ist auch in normal wachsenden Zellen vorhanden. In
ruhenden Zellen
ist p53 jedoch kaum oder gar nicht zu finden. In vielen
Tumortypen
ist das fur p53
kodierende
Gen
mutiert
. In manchen, aber nicht allen Tumoren, scheint das Protein als
Tumorsuppressor
zu wirken. p53 spielt eine Rolle bei der Regulation des
Zellzyklus
, wo es die Aktivitat einer Anzahl von Genen bremst. Zudem ist es in allen
Wirbeltieren
zu finden.
[1]
p53 wurde 1979 unabhangig voneinander von Albert B. DeLeo,
David P. Lane
und
Arnold Levine
entdeckt.
[2]
[3]
Der humane Tumorsuppressor p53 reguliert als
Transkriptionsfaktor
nach
DNA-Schadigung
die Expression von
Genen
, die an der Kontrolle des Zellzyklus, an der Induktion der
Apoptose
(des
programmierten Zelltods
) oder an der
DNA-Reparatur
beteiligt sind. Aufgrund dieser Eigenschaft wird p53 in der Literatur als ?Wachter des
Genoms
“ bezeichnet.
[4]
Die besondere medizinische Bedeutung erklart sich aus dem Befund, dass p53 in 50 % aller menschlichen Tumoren mutiert ist. Der Verlust der p53-Funktion spielt daher eine kritische Rolle bei der Entstehung von
Krebs
, ist jedoch nicht dessen ursachlicher Ausloser. p53 wurde aufgrund seiner Bedeutung 1993 zum ?Molekul des Jahres“ gewahlt.
p53 erhielt seinen Namen aufgrund der scheinbaren
Molekularmasse
von 53
kDa
auf einem
SDS-PAGE
-Gel.
Das dazugehorige Gen, das
TP53
-Tumorsuppressor-Gen, liegt auf dem
Chromosom 17p13.1
. Um es von dem Protein zu unterscheiden, wird es kursiv geschrieben (TP53 ist die offizielle Bezeichnung fur menschliches p53-Protein). Das p53-Protein ist von Natur aus instabil, wird aber regelmaßig ?nachgebildet“. Kommt es in der DNA jedoch zu Schaden, etwa einem Doppelstrangbruch, die eine
Replikation
oder eine
Mitose
fehlerhaft ablaufen lassen wurden, so wird p53 innerhalb von 30 Minuten
posttranslational
stabilisiert, wodurch sich p53 in der Zelle akkumuliert.
Die Akkumulation von p53 hat viele Folgen. So werden einerseits DNA-Reparatur-Mechanismen in Gang gesetzt, andererseits wird der Zellzyklus gestoppt. Letzteres geschieht dadurch, dass p53 als Transkriptionsfaktor die Produktion des Proteins
p21
induziert. p21 wiederum hemmt sowohl den Cyclin D/CDK4/6-Komplex als auch den Cyclin E/CDK2-Komplex. Diese werden eigentlich benotigt, um einen vom Protein
pRB
gebundenen weiteren Transkriptionsfaktor (E2F) freizusetzen, der den Zellzyklus weiterfuhren wurde. Die Zelle bekommt also durch p53 Zeit, sich selbst zu reparieren, bevor sie sich teilt. Ist die DNA wieder in Ordnung, so sinkt der p53-Spiegel wieder, p21 wird nicht mehr transkribiert und nach einer Weile geht der Zellzyklus weiter.
Wird p53 jedoch zu stark angehauft und kommen weitere Faktoren hinzu, so aktiviert p53 Gene der Bcl2-Familie (insbesondere den Apoptose-Regulator BAX), die wiederum in Form einer Signalkaskade
Caspasen
auslosen und so zur
Apoptose
(programmierter Zelltod) fuhren. Demnach ist p53 wie eine Art Bremse, die notig ist, um Zellen vom unkontrollierten Wachstum und weiterer Schadigung abzuhalten, und deren Mutation zu verstarkter Zellteilung fuhrt.
Eine andere Funktion von p53 ist, dass es offensichtlich das menschliche Schwangerschaftshormon
hCG
steuert, wie Wissenschaftler der
Universitat Leipzig
nachweisen konnten.
[5]
p53 ist ein Schlusselprotein mit enormer Bedeutung. Ein Defekt hat demnach große Schadwirkung. Nach heutigem Kenntnisstand sind es im Allgemeinen
Punktmutationen
, die zu einem Funktionsverlust fuhren. Als Folge dieses Verlustes ist weder ein Anhalten des
Zellzyklus
zur DNA-Reparatur noch die Einleitung der Apoptose moglich. Die Zellen beginnen sich auch mit Schaden in der DNA unkontrolliert zu teilen, es kommt zur Tumorbildung. Ferner fuhrt der Verlust des funktionsfahigen p53 zu einem Verlust der Synthesefahigkeit von Cytochrom-C-Oxidase 2. Dadurch kann die Cytochrom-C-Oxidase-2 Untereinheit nicht mehr in den Cytochrom-C-Oxidase-Proteinkomplex (Komplex IV der Atmungskette) eingebaut werden. Die Krebszelle verliert zwar den Stoffwechsel der aeroben Atmung, geht aber zur Energiegewinnung in die anaerobe Glykolyse uber.
[6]
Im Folgenden eine Liste der Krankheiten, die ausschließlich oder hauptsachlich auf Mutationen in
TP53
(dem p53-Gen) zuruckzufuhren sind.
Beim
Glioblastoma multiforme
, WHO °IV, ist das p53-Gen ebenfalls mutiert: beim primaren GBM <30 %, beim sekundaren (durch Progression eines niedergradigen Glioms wie des diffusen Astrozytoms WHO °II oder des anaplastischen Astrozytoms WHO °III) GBM >65 % sowie beim
Riesenzellglioblastom
30 bis 40 %.
[9]
Patienten, die mit dem
Li-Fraumeni-Syndrom
geboren werden, haben eine angeborene Mutation in
TP53
. So kommt es bei Menschen mit dieser Mutation schon in fruhester Kindheit zu diversen Tumoren, wie
Brustkrebs
,
Leukamie
,
Hirntumoren
und vieles mehr. Ursache fur den Krebs ist jedoch vermutlich nicht die Mutation von
TP53
selbst, sondern die hohe Zellteilungsrate wahrend des embryonalen Wachstums, trotz Defekten in der DNA, sodass Schaden sich akkumulieren und weitere Gene fur die Regulierung des Zellwachstums geschadigt werden konnen. Wie Heidelberger Forscher im Jahre 2012 in der Fachzeitschrift
Cell
beschrieben, weisen
Tumoren
in Patienten mit angeborenen
TP53
-
Mutationen
daruber hinaus gehauft Merkmale von katastrophalen Chromosomenumlagerungen (
Chromothripsis
) auf.
TP53
-Mutationen konnten entweder Ausloser dieser massiven
Erbgutschaden
sein oder den Zelltod mittels
Apoptose
, trotz massiver Zerstorung der
Chromosomenstruktur
, verhindern.
[10]
Da jede
Rontgenuntersuchung
oder
Chemotherapie
die Mutationsrate erhoht, ist sowohl die Diagnose, als auch die Behandlung von Patienten mit Li-Fraumeni-Syndrom besonders schwierig.
Neben spontan auftretenden Mutationen gibt es auch andere Ursachen fur Schaden an p53 beziehungsweise seinen Funktionen. So gibt es tumorinduzierende
Viren
(sogenannte
Onkoviren
), die p53 hemmen, abbauen oder dessen naturlichen Abbau beschleunigen. Diese Strategie nutzen die Viren, da auch virale Erkrankungen eine Apoptose auslosen konnen und somit die Viren an ihrer Weiterverbreitung hindern wurden.
Weiterhin kann p53 durch chemische Stoffe geschadigt werden, zum Beispiel durch das im
Tabakrauch
enthaltene
Benzo[
a
]pyren
oder durch
Aflatoxin
. Diese Stoffe hinterlassen charakteristische Merkmale in der geschadigten DNA und konnen dadurch als Verursacher identifiziert werden.
Versuche an Fruchtfliegen deuten darauf hin, dass eine kunstlich reduzierte Aktivitat des Anti-Tumor-Proteins sich bei den Versuchstieren auf die Lebensdauer positiv auswirkt.
[11]
Verhalt sich das Protein jedoch aktiver als normal (uberaktiv), so
altern
die behandelten Fruchtfliegen wesentlich schneller als gewohnlich.
[12]
Bei Mausen wurde der gleiche Sachverhalt beobachtet.
[13]
Der Mechanismus selbst ist jedoch bislang ungeklart.
Bei der (haufig schnellen) Bildung von
Geweihen
und Hornern von
Horntragern
verhindert p53 uberschießendes Wachstum; zugleich haben die Tiere im Vergleich zu anderen
Saugetieren
eine funffach niedrige Krebserkrankungsrate.
[14]
- H. Kessler
, J. Buchner u. a.:
p53 ? ein naturlicher Krebskiller: Einsichten in die Struktur und Therapiekonzepte.
In:
Angewandte Chemie.
Band 118, 2006, S. 6590?6611.
doi:10.1002/ange.200600611
- Pierre Hainaut, Klas Wiman (Hrsg.):
25 Years of p53 Research.
Kluwer Academic Publishers, 2005,
ISBN 1-4020-2920-9
- T. Stiewe:
The p53 family in differentiation and tumorigenesis.
In:
Nature Reviews Cancer
, Band 7, Nummer 3, Marz 2007, S. 165?168.
doi:10.1038/nrc2072
.
PMID 17332760
. (Review).
- G. Ferbeyre, S. W. Lowe:
The price of tumour suppression?
In:
Nature
, Band 415, Nummer 6867, Januar 2002, S. 26?27;
doi:10.1038/415026a
.
PMID 11780097
.
- M. Lacroix, R. A. Toillon, G. Leclercq:
p53 and breast cancer, an update.
In:
Endocrine-Related Cancer
, Band 13, Nummer 2, Juni 2006, S. 293?325;
doi:10.1677/erc.1.01172
.
PMID 16728565
. (Review).
- A. B. DeLeo, G. Jay, E. Appella, G. C. Dubois, L. W. Law, L. J. Old:
Detection of a transformation-related antigen in chemically induced sarcomas and other transformed cells of the mouse.
In:
PNAS
, Band 76, Nummer 5, Mai 1979, S. 2420?2424.
PMID 221923
.
PMC 383613
(freier Volltext).
- Ingo B. Runnebaum
:
Das p53-Gen ist ein Tumorsuppressor und Zellzyklusregulator in Brustkrebszellen.
Habilitationsschrift, Universitat Ulm, 1997.
- ↑
PROSITE documentation PDOC00301.
Swiss Institute of Bioinformatics
(SIB),
abgerufen am 20. September 2011
(englisch).
- ↑
D. P. Lane, L. V. Crawford:
T antigen is bound to a host protein in SV40-transformed cells.
In:
Nature
, Band 278, Nummer 5701, Marz 1979, S. 261?263;
PMID 218111
.
- ↑
D. I. Linzer, A. J. Levine:
Characterization of a 54K dalton cellular SV40 tumor antigen present in SV40-transformed cells and uninfected embryonal carcinoma cells.
In:
Cell
, Band 17, Nummer 1, Mai 1979, S. 43?52;
PMID 222475
.
- ↑
D. P. Lane:
Cancer. p53, guardian of the genome.
In:
Nature
, Band 358, Nummer 6381, Juli 1992, S. 15?16;
doi:10.1038/358015a0
.
PMID 1614522
.
- ↑
Landes Bioscience 1. November 2011
- ↑
S. Matoba, J. G. Kang, W. D. Patino, A. Wragg, M. Boehm, O. Gavrilova, P. J. Hurley, F. Bunz, P. M. Hwang:
p53 regulates mitochondrial respiration.
In:
Science
, Band 312, Nummer 5780, Juni 2006, S. 1650?1653;
doi:10.1126/science.1126863
,
PMID 16728594
.
- ↑
R. F. Boynton u. a.:
Loss of heterozygosity involving the APC and MCC genetic loci occurs in the majority of human esophageal cancers.
Proc. Nat. Acad. Sci. 89/-/1992. S. 3385?3388.
PMID 1565631
- ↑
F. Chakrani u. a.:
Mutations clustered in exon 5 of the p53 gene in primary nasopharyngeal carcinomas from southeastern Asia.
Int. J. Cancer 61/-/1995. S. 316?320.
PMID 7729941
- ↑
Riede, Werner, Schaefer:
Allgemeine und spezielle Pathologie.
5. komplett uberarbeitete Auflage. Thieme Verlag
- ↑
T. Rausch et al.:
Genome sequencing of pediatric medulloblastoma links catastrophic DNA rearrangements with TP53 mutations
. In:
Cell
, 2012, 148, S. 59?71;
PMID 22265402
- ↑
J. Bauer u. a. in
Current Biology
- ↑
G. Ferbeyre, S. W. Lowe:
Aging: The price of tumour suppression?
In:
Nature
, 415, 2002, S. 26?27
- ↑
S. D. Tyner u. a.:
p53 mutant mice that display early ageing-associated phenotypes.
In:
Nature
, 415, 2002, S. 45?53.
doi:10.1038/415045a
PMID 11780111
- ↑
Y. Wang et al.:
Genetic basis of ruminant headgear and rapid antler regeneration
. In:
Science
, 2019, 364eaav6335;
doi:10.1126/science.aav6335
,
PMID 31221830