| Ketone
|

|
| R
1
und R
2
sind organische Reste (Alkyl, Aryl o. a.). Die Carbonylgruppe ist
blau
markiert.
|
Ketone
sind
chemische Verbindungen
, die als
funktionelle Gruppe
eine nicht endstandige
Carbonylgruppe
(>C=O) enthalten. Eine Ketongruppe [C?C(O)?C] enthalt drei Kohlenstoffatome. Alle Ketone enthalten mindestens drei Kohlenstoffatome. Im Gegensatz zu den
Aldehyden
ist hier der Carbonylkohlenstoff in beide Bindungsrichtungen mit Kohlenstoffatomen verbunden. Ketone kann man als
Oxidationsprodukte
sekundarer
Alkohole
auffassen. Die von den
Alkanen
ableitbaren Ketone nennt man auch
Alkanone
. Entsprechend bezeichnet man die auf
Alkene
und
Alkine
zuruckzufuhrenden Ketone als
Alkenone
(siehe
Enone
) bzw.
Alkinone
. Das einfachste Keton ist
Aceton
. Ein einfaches
aromatisches
Keton ist
Benzophenon
(Diphenylketon). Ein gemischtes Keton ist
Acetophenon
(Methylphenylketon). Physiologisch entstehen
bestimmte Ketone
als Stoffwechselprodukt in der Leber.
Nach der
IUPAC
-
Nomenklatur
erhalten Ketone das
Suffix
-on, sofern die Carbonylgruppe die im Molekul enthaltene Gruppe mit hochster
Prioritat
ist. Entsprechend heißt das vom
Propan
abgeleitete Keton
Propanon
(CH
3
?CO?CH
3
,
Trivialname: Aceton
). Bei Ketonen mit mehr als drei C-Atomen befindet sich die Carbonylgruppe in der Stammkette und erhalt die kleinstmogliche Nummer, diese kann entweder vor dem Namen oder, bei komplizierteren Molekulen unumganglich, direkt vor der Endung -on stehen. Beispielsweise heißt: CH
3
?CH
2
?CH
2
?CO?CH
3
2-Pentanon
oder Pentan-2-on.
Falls die Carbonylgruppe nicht die hochste Prioritat besitzt, verwendet man das
Prafix
Oxo-. Zum Beispiel heißt CH
3
?CO?CH
2
?CHO 3-Oxobutanal.
Sehr haufig tragen die Ketone jedoch Namen, welche aus der Bezeichnung der
Alkylreste
gefolgt von der Endung -keton bestehen (
Radikofunktionelle Nomenklatur
). So wird
Butanon
auch Methylethylketon (MEK) genannt. Falls der eine Substituent eine
Phenylgruppe
ist, ist die Endung
-phenon
gebrauchlich, wie zum Beispiel bei
Acetophenon
.
Niedermolekulare Ketone sind farblose, leichtbewegliche Flussigkeiten und aufgrund der Polaritat der Carbonylgruppe in Wasser loslich. Niedermolekulare Ketone zeichnen sich durch einen meist angenehmen, fruchtigen
Geruch
aus. Hohermolekulare Ketone sind feste Stoffe.
Ketone besitzen auf Grund des
+I-Effekts
der Alkylsubstituenten am Carbonyl-Kohlenstoffatom eine niedrigere Reaktionsfreudigkeit als Aldehyde und neigen nicht zur
Polymerisation
. Im Unterschied zu den Aldehyden erfolgt mit Ketonen keine Reaktion bei der
Fehling-Probe
, da die Ketongruppe unter Erhalt des Kohlenstoffgerusts nicht weiter oxidiert werden kann.
Ketone gehen, ahnlich wie
Aldehyde
,
Additions-
und
Kondensationsreaktionen
ein.
Ketone (R
1
, R
2
, R
3
=
Organyl
-Rest) stehen mit ihrer
tautomeren Form
, den
Enolen
im Gleichgewicht (
Keto-Enol-Tautomerie
), wenn an das α-Kohlenstoffatom ein Wasserstoffatom gebunden ist:
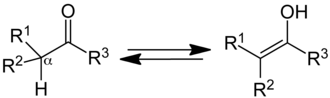 Keto-Enol-Tautomerie
Keto-Enol-Tautomerie
Zum Schutz gegen unerwunschte Reaktionen werden Ketone mit
Diolen
zu
Vollacetalen
(siehe
Schutzgruppe
) umgesetzt:
 Bildung von Vollacetalen
Bildung von Vollacetalen
Bei der Umsetzung des Vollacetals mit Wasser entsteht
saurekatalysiert
wieder das Keton, d. h. die Schutzgruppe wird abgespalten.
Ketone lassen sich im Gegensatz zu den Aldehyden nur unter drastischen Reaktionsbedingungen
oxidativ
angreifen. Dabei wird eine Bindung zwischen Carbonylkohlenstoff und einem Nachbarkohlenstoff gespalten. Die entstehenden Molekulbruchstucke sind
Carbonsauren
.
In
IR-Spektren
von Ketonen und
Aldehyden
findet man die charakteristische Bande der C=O-Valenzschwingung im Bereich von 1690 bis 1750 cm
?1
.
- K. Peter C. Vollhardt, Neil E. Schore:
Organische Chemie.
4. Auflage. Wiley-VCH, Weinheim 2005,
ISBN 3-527-31380-X
.
- ↑
Joachim Buddrus:
Grundlagen der Organischen Chemie
. 4. Auflage, Walter de Gruyter Verlag, Berlin 2011,
ISBN 978-3-11-024894-4
, S. 479.