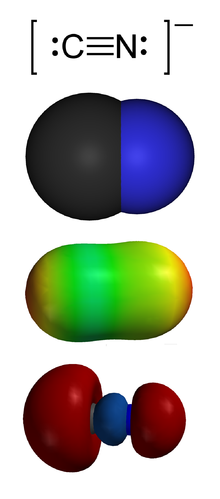 Diverses representacions de l'io cianur
Diverses representacions de l'io cianur
Un
cianur
es un
compost quimic
que conte el
grup ciano
, -
C
≡
N
. El terme cianur es refereix sovint a sals de l'
anio
CN
-
, gran part de les quals son toxiques.
Els cianurs els produeixen certs
bacteris
,
fongs
, i
algues
i es troben en un gran nombre de
plantes
. Es troben cianurs, pero en petites quantitats, en certes
llavors
i pinyols de fruits, per exemple, en les llavors de les pomes,
mango
,
pressec
, i
ametlles amargants
.
[1]
En les plantes, els cianurs normalment estan enllacats amb molecules de sucres en la forma de
glucosids
cianogenics i defensen la planta de les agressions dels
herbivors
. Les plantes tropicals que son font de la
tapioca
tambe contenen glucosids cianogenics.
[2]
[3]
El
radical cianur
, CN· s'ha identificat en l'
espai interestel·lar
.
[4]
El
cianur d'hidrogen
es produeix per la
combustio
o
pirolisi
de certs materials sota condicions deficients en
oxigen
. Per exemple es pot detectar en el fum del
tabac
. Certs plastics, especialment els derivats d'
acrilonitril
, alliberen cianur d'
hidrogen
quan s'escalfen o es cremen.
[5]
Quimica de coordinacio
[
modifica
]
L'
anio
cianur es un potent
lligand
per a molts
metalls de transicio
.
[6]
L'alta afinitat dels metalls per aquest anio pot ser atribuit a la seva
carrega
negativa, compacitat i capacitat de participar en enllacos n. Els complexos ben coneguts inclouen:
- hexacianurs [M(CN)?]
3?
(M = Ti, V, Cr, Mn, Fe, Co), amb forma d'
octaedre
;
- els tetracianurs, [M(CN)₄]
2?
(M = Ni, Pd, Pt), de geometria planar quadrada;
- els dicianurs [M(CN)₂]
?
(M = Cu, Ag, Au), de geometria linear.
El
pigment
de color blau fosc
Blau de Prussia
, usat per a fer
blueprints
, deriva dels complexos de cianur de ferro. El
blau de Prussia
pot produir cianur d'hidrogen si s'exposa a acids forts.
Certs
enzims
, per exemple les
hidrogenases
, contenen un lligand cianur unit al
ferro
en els seus llocs actius. La
biosintesi
del cianur en les [NiFe]-hidrogenases procedeix del fosfat de
carbamoil
el qual es converteix
tiocianatde
cisteinail
, el donador CN
?
.
[7]
L'io cianur, potencialment letal, actua com a
toxic
a traves de la inhibicio del complex
citocrom c oxidasa
i, per tant, bloquejant la
cadena transportadora d'electrons
, sistema central del proces de
respiracio cel·lular
. Si be la seva efectivitat a baixes
concentracions
es fulminant, l'individu mor sota dolorosos
espasmes
i
convulsions
que poden trigar des de deu
segons
a uns
minuts
. Tambe es conegut per la seva denominacio militar AN (per al
cianur d'hidrogen
, HCN) i CK (per al
clorur de cianogen
, NCCl).
Durant la
Segona Guerra Mundial
s'utilitza un
insecticida
fet a base de cianur, el
Zyklon B
, per a matar
essers humans
a les cambres de gas.
- ↑
≪
ToxFAQs for Cyanide
≫.
Agency for Toxic Substances and Disease Registry
, juliol 2006. [Consulta: 28 juny 2008].
- ↑
Vetter
, J. ≪Plant cyanogenic glycosides≫.
Toxicon
, 38, 1, 2000, pag. 11?36.
DOI
:
10.1016/S0041-0101(99)00128-2
.
PMID
:
10669009
.
- ↑
Jones
, D. A. ≪Why are so many food plants cyanogenic?≫.
Phytochemistry
, 47, 2, 1998, pag. 155?162.
DOI
:
10.1016/S0031-9422(97)00425-1
.
PMID
:
9431670
.
- ↑
Pieniazek
, Piotr A.; Bradforth, Stephen E.; Krylov, Anna I. ≪
Spectroscopy of the Cyano Radical in an Aqueous Environment
≫ (PDF).
The journal of physical chemistry. A
. Department of Chemistry,
University of Southern California
[[[Los Angeles]],
California
90089-0482], 110, 14, 07-12-2005, pag. 4854?65. Arxivat de l'
original
el 2008-09-11.
DOI
:
10.1021/jp0545952
.
PMID
:
16599455
[Consulta: 23 novembre 2011].
Arxivat
2008-09-11 a
Wayback Machine
.
- ↑
Anon
. ≪
Facts about cyanide:Where cyanide is found and how it is used
≫.
CDC Emergency preparedness and response
. Centers for Disease Control and Prevention, 27-01-2004. Arxivat de l'
original
el 15 d'abril 2010. [Consulta: 13 abril 2010].
- ↑
Sharpe, A. G. The Chemistry of Cyano Complexes of the Transition Metals; Academic Press: London, 1976
- ↑
Reissmann
, Stefanie; Elisabeth Hochleitner, Haofan Wang, Athanasios Paschos, Friedrich Lottspeich, Richard S. Glass and August Bock ≪
Taming of a Poison: Biosynthesis of the NiFe-Hydrogenase Cyanide Ligands
≫.
Science
, 299, 5609, 2003, pag. 1067?1070.
DOI
:
10.1126/science.1080972
.
PMID
:
12586941
[Consulta: 28 juny 2008].