 Metilen ? najjednostavniji karben.
Metilen ? najjednostavniji karben.
Karben
je
molekula
koja sadr?i neutralni atom
ugljika
sa
valencijom
dva i dva nedijele?a valencijska
elektrona
. Op?a formula je R-(C
:
)-R' ili R=C
:
.
[1]
[2]
[3]
[4]
Naziv "karben" mo?e se također odnositi i na posebni spoj H
2
C
:
, zvani
metilen
, roditeljski
hidrid
od kojeg su formalno izvedeni svi ostali karbenski spojevi.
[5]
Karbeni su podijeljeni ili kao
jednostruko
ili
trostruko stanje
, ovisno o njihovoj elektronskoj strukturi. Ve?ina karbena su vrlo kratkog vijeka, iako su poznati i kao
uporni ili perzistentni karbeni
. Jedan dobro prou?eni karben je
dihlorokarben
Cl
2
C:
, koji mo?e nastati
in situ
iz
hloroforma
i jake
baze
.
 Jednostruki i trostruki karben.
Jednostruki i trostruki karben.
Postoje dvije klase karbena:
jednostruki
(monopletni) i
trostruki ili tripletni
. Monopletni karbeni su parno
spinovani
. Na jeziku
teorije valentne veze
, molekula usvaja
sp
2
hibridnu strukturu
. Trojni karbeni imaju dva nesparena
elektrona
. Ve?ina karbenas imaju nelinearno tripletno osnovno stanje, osim onih koji imaju
du?ik
,
kisik
ili atome
sumpora
i halogenida direktno vezanih na dvovalentni ugljik.
Karbeni se nazivaju unipletnim ili tripletnim, ovisno o elektronskom
spinu
koji posjeduju. Trojni karbeni su
paramagnetni
i mogu se uo?iti prema
rezonancnoj spektroskopiji elektronskog spina
, ako potraju dovoljno dugo. Ukupan spin jednostrukih karbena je nula, trojnih je jedan (u jedinicama
 ). Uglovi veze su 125-140° za tripletni metilen, a 102° za jednostruki (kako je određeno
EPR
-om). Tripletni karbeni su op?enito stabilni u gasovitom stanju, dok se jednopstruki ?e??e javljaju u vodenom mediju.
Ugljikovodici trojnih karbena obi?no imaju energiju od 8
kcal
/
mola
, ni?u nego jednostruki. Op?enito re?eno, triplet je stabilnije stanje (
osnovno stanje
), a jednostrukost je
pobuđeno stanje
.
Supstituenti
koji mogu donirati
elektronske parove
mogu stabilizirati jednostruko stanje, delokaliziraju?i par u praznu p-orbitalu. Ako je
energija
jednostrukog stanja dovoljno smanjena, zapravo ?e postati osnovno stanje.
). Uglovi veze su 125-140° za tripletni metilen, a 102° za jednostruki (kako je određeno
EPR
-om). Tripletni karbeni su op?enito stabilni u gasovitom stanju, dok se jednopstruki ?e??e javljaju u vodenom mediju.
Ugljikovodici trojnih karbena obi?no imaju energiju od 8
kcal
/
mola
, ni?u nego jednostruki. Op?enito re?eno, triplet je stabilnije stanje (
osnovno stanje
), a jednostrukost je
pobuđeno stanje
.
Supstituenti
koji mogu donirati
elektronske parove
mogu stabilizirati jednostruko stanje, delokaliziraju?i par u praznu p-orbitalu. Ako je
energija
jednostrukog stanja dovoljno smanjena, zapravo ?e postati osnovno stanje.
Ne postoje odr?ive strategije za stabilizaciju tripleta. Karben zvani 9-
fluoreniliden
je pokazao da brzo uspostavlja
uravnote?avaju?u
mje?avinu unipletnog i tripletnog stanja s oko 1,1 kcal/mol (4,6 kJ/mol) energijske razlike.
[6]
Međutim, sporno je da li su diaril karbeni, kao ?to je
fluoren
karben, jer se kod pravih karbenia elektroni mogu delokalizirati do te mjere da postaju
biradikali
. Eksperimenti
in silico
pokazuju da trojni karbeni mogu biti
termodinami?ki
saveznik stabilizacije
elektropozitivnosti
heteroatoma, kao ?to su
silil
i
sililoksi
karbeni, a posebno trifluorosilil karbeni.
[7]
 Dodavanje karbena na alkene.
Dodavanje karbena na alkene.
Jednostruki i trojni karbeni pokazuju razli?itu reaktivnost. Jednostruki uglavnom sudjeluju u
heletropskim reakcijama
ili kao
elektrofili
ili
nukleofili
. Jednostruki karbeni sa nepopunjenom p-orbitalom bi trebalo da budi elektrofilni. Trojni karbeni mogu se smatrati
diradikalima
, a u?estvuju u stepenasto radikalnim dodacima. Trojni karbeni prolaze i kroz
reaktivni međuproizvod
sa dva nesparena elektrona, dok jednostruki karben mo?e reagirati u jednom
usklađenom
koraku.
Zbog ova dva na?ina reaktivnosti, reakcije jednostrukog metilena su
stereospecifi?ne
, dok je trojni metilen
stereoselektivan
. Ova razlika se mo?e koristiti za probe u poznavanju prirode karbena. Naprimjer, reakcija metilena proizvedenog iz
fotolize
od
diazometana
sa
cis
-
2-buten
ili sa
trans
-
2-buten
, od kojih svaki daje jedan diastereomer 1,2-dimetilciklopropanskog proizvoda:
cis
od
cis
i
trans
od
trans
, ?to dokazuje da je metilen jednostruk.
[8]
Ako je metilen triplet, ne bi se moglo o?ekivati da proizvod zavisi od po?etne geometrija alkena, ve? on predstavlja identi?nu mje?avinu.
Reaktivnost određenih karbena zavisi od
supstituenatske
grupe. Njihova reaktivnost mo?e uticati putem
metala
. Neke od reakcija karbena mogu se u?initi putem
umetanja (insercije) u vezu C-H
, skeletnim preuređenjem i dopunom dvostruke veze.
Karbeni se mogu podijeliti na nukleofilne, elektrofilne ili ambifilne. Naprimjer, ako je supstituent u mogu?nosti da donira par elektrona, karben najvjerovatnije ne?e biti elektrofilan.
Alkil
karbeni ume?u se mnogo selektivnije od metilena, koji ne pravi razliku između primarne, sekundarne i tercijarne C-H veze.
.
 Umetanje karbena.
Umetanje karbena.
Karbenska C-H insercija
je drugi uobi?ajeni oblik karbenskih reakcija. Karben se u osnovi ugrađuje u postoje?u vezu. Redoslijed prednosti je naj?e??e:
- 1. X-H veza, gdje nema ugljika,
- 2. C-H veza
- 3. C-C veza X.
Insercija mo?e ali ne mora i?i u jednom koraku.
Intramolekulske
reakcije insercija ispoljavaju novi sintetski rastvori, dok kruta struktura daje prednost za događanje takvog umetanja. Kada je mogu?a unutarmolekulska insercija, nema
međumolekulskog
umetanja. U fleksibilnoj strukturi, nastajanje peto?lanog prstena se de?ava lak?e nego kao kod ?esto?lanog. Oba i inter- i intra- umetanja su dostupna stanja asimetri?ne indukcije, izborom hiralnih liganada na metalnim centrima.
 Unutarmolekulska reakcija karbena.
Unutarmolekulska reakcija karbena.
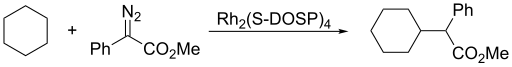 Međumolekulska reakcija karbena.
Međumolekulska reakcija karbena.
Alkilidenski karbeni su primamljivi po tome ?to nude stvaranje
ciklopentenskih
polovina. Za generiranje alkilidenskih karbena,
ketoni
mogu biti izlo?eni
trimetilsilil
diazometanu
.
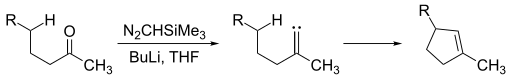 Alkilidenski karben.
Alkilidenski karben.
- Metod koji se ?iroko primjenjuje za organske sinteze je inducirana eliminacija
halogenida
od gem-dihalida pomo?u
organolitij-reagensa
. Ostaje neizvjesno kako se pod tim uslovima stvaraju slobodni karbeni ili metal-karbenskikompleks. Ipak, ovi metalokarbeni (ili karbenoidi) daju o?ekivane organske proizvode.
- R
2
CBr
2
+ BuLi → R
2
CLi(Br) + BuBr
- R
2
CLi(Br) → R
2
C + LiBr
- Za ciklopropanacije u
Simmons-Smith reakciju
, uklju?en je
cink
. Specijalizirani ali pou?an slu?aj, alfa-halo?ivini spojevi mogu biti izolirani i odvojeni termolizom (toplotnim razlaganjem). Na primjer, "Seyferthov reagens" oslobađa CCl
2
, uz grijanje.
- C
6
H
5
HgCCl
3
→ CCl
2
+ C
6
H
5
HgCl
- Naj?e??e, karbeni se stvaraju od
diazoalkana
, putem kojeg su katalizirani
fotolitski
, termo- ili
prelazni metali
. Katalizatori obi?no imaju
rodij
i
bakar
.
Bamford-Stevens reakcija
daje karbene u aprotonskim otapalima i karbenijum ion u protonskim otapalima.
- Eliminacija HX iz haloformi (CHX
3
) pomo?u baza mogu?a je u uslovima prijelazne fazne
katalize
.
- Fotoliza
diazirina
i
epoksida
se zakođer mo?e primijeniti. Diazirini su cikli?ni oblici diazoalkana. Neki mali prstenovi lahko izazivaju
fotoekscitaciju
(svjetlosno podra?ivanje). Fotoliza epoksida daje
karbonilne
spojeve kao sporedne proizvode. Sa
asimetri?nim
epoksidima mogu potencijalno nastati dva razli?ita karbonilna spoja. Priroda supstituenata obi?no daje prednost nastanku jednog karbonilnog spoja preko drugog. Jedna od C-O veza ?e imati izra?eniju osobinu dvostruke veze i na taj na?in ?e biti ja?a i sa manje ?anse da se probije. Rezonanca strukture mo?e se izvesti kako bi se utvrdilo koji dio ?e doprinijeti nastanku vi?e karbonila. Kada je jedan supstituent
alkil
i jo?
aril
, aril-supstituirani ugljik se obi?no otpu?ta kao karbenski fragment.
- Karbeni su intermedijeri u
Wolffovom preuređenju
.
?iroka je skala primjene karbena u industrijskoj proizvodnji
tetrafluoroetilena
, prekursora
teflona
. Tetrafluoroetilen nastaje preko međuproizvoda
difluorokarbena
:
[9]
- CHClF
2
→ CF
2
+ HCl
- 2 CF
2
→ F
2
C=CF
2
- ^
Voet D, Voet J. . (1995).
Biochemistry, 2nd Ed
. Wiley,
http://www.wiley.com/college/math/chem/cg/sales/voet.html
.
CS1 odr?avanje: upotreba parametra authors (
link
)
- ^
Atkins P., de Paula J. (2006).
Physical chemistry, 8th Ed
. San Francisco: W. H. Freeman.
ISBN
0-7167-8759-8
.
- ^
Whitten K.W., Gailey K. D. and Davis R. E. (1992).
General chemistry, 4th Ed
. Philadelphia: Saunders College Publishing.
ISBN
0-03-072373-6
.
- ^
Petrucci R. H., Harwood W. S., Herring F. G. (2002).
General Chemistry, 8th Ed
. New York: Prentice-Hall.
ISBN
0-13-014329-4
.
CS1 odr?avanje: vi?e imena: authors list (
link
)
- ^
Hoffmann, Roald
(2005).
Molecular Orbitals of Transition Metal Complexes
. Oxford. str. 7.
ISBN
0-19-853093-5
.
CS1 odr?avanje: nepreporu?eni parametar (
link
)
- ^
Grasse, P. B.; Brauer, B. E.; Zupancic, J. J.; Kaufmann, K. J.; Schuster, G. B. (1983). "Chemical and physical properties of fluorenylidene: equilibration of the singlet and triplet carbenes".
Journal of the American Chemical Society
.
105
(23): 6833.
doi
:
10.1021/ja00361a014
.
- ^
Nemirowski, A; Schreiner, P. R. (novembar 2007). "Electronic Stabilization of Ground State Triplet Carbenes".
J. Org. Chem
.
72
(25): 9533?9540.
doi
:
10.1021/jo701615x
.
PMID
17994760
.
- ^
Skell, P. S.; Woodworth, R. C. (1956). "Structure of Carbene, Ch2".
Journal of the American Chemical Society
.
78
(17): 4496.
doi
:
10.1021/ja01598a087
.
- ^
Bajzer, W. X. (2004). "Fluorine Compounds, Organic".
Kirk-Othmer Encyclopedia of Chemical Technology
. John Wiley & Sons.
doi
:
10.1002/0471238961.0914201802011026.a01.pub2
.
|
|---|
| |
|---|
Samo jedan
element
osim
C, H, O
| |
|---|
Ostale
| |
|---|
|
|