Валентлы?
(от
лат.
val?ns
≪к?ск? эй?≫;
рус.
Валентность
) ?
атом
барлы??а килтерг?н химик б?йл?нешт?р и??бе, й?ки атомдар ?аны бирелг?н элементты? атомын ?уша й?ки алмаштыра ала.
Валентлы? терминыны? этимология?ы 1424 йылдан, ?илми текста ≪экстракт≫, ≪препарат≫ м???н??енд? ?улланыла башла?андан бирле к???тел?. Заманса билд?л?м? сикт?ренд? ?улланыу 1884 йылда терк?лг?н (нем.
Valenz
). 1789 йылда Уильям Хиггинс матд?л?р?е? ва? ки??кс?л?ре ара?ында б?йл?нешт?р барлы?ы фаразлан?ан ?илми хе?м?т ба?тырып сы?ара.
[1]
.
 Эдуард Франкленд ? х??ерге валентлы? т?ш?нс??ен? ниге? ?алыусы
Эдуард Франкленд ? х??ерге валентлы? т?ш?нс??ен? ниге? ?алыусы
Л?кин валентлы? феномены тулы?ынса ра?лан?ан т?ш?нс?не 1852 йылда химик Эдуард Франкленд т??дим ит?. Ул ошо м?лг? бул?ан б?т? теориялар?ы ??м фараздар?ы йыя ??м ?айтанан ?арай
[2]
.
Т?рл? металдар?ы? тулыланыу ??л?тен к???теп ??м органик сы?арылма металдар?ы? составын органик булма?ан берл?шм?л?р составы мен?н са?ыштырып, Франкленд ≪берл?ше? к?с?≫ (берл?ше? ауырлы?ы) тура?ында т?ш?нс? индер?. Был валентлы? тура?ында?ы т??лим?тк? ниге? булып тора. Франкленд ?ай?ы бер закондар урынлаштыр?а ла, уны? идеялары ??еш? алмай.
Валентлы? теория?ын т?????? Фридрих Август Кекуле х?л иткес роль уйнай. 1857 йылда ул углеродты? д?рт ниге?ле (д?рт атомлы) элемент булыуын к?р??т?, ??м уны? и? ябай берл?шм??е булып СН
4
метан тора. Атомдар?ы? валентлы?ы тура?ында?ы к??аллау?арыны? ха?лы?ына ышан?ан Кекуле улар?ы ??ене? органик химия д?реслеген? индер?: автор фекеренс?, ниге?лелек ? атомды? фундаменталь ??енс?леге, атом ауырлы?ы ке?ек ?к даими ??м ??г?рм?й тор?ан ??енс?лек. 1858 йылда Кекуле идеяларына тап килг?н ?араштар Арчибальд Скотт Купер тарафынан ≪Я?ы химик теория тура?ында≫?ы м???л?л? телг? алына.
1861 йылды? сентябренд? А. М. Бутлеров валентлы? теория?ына м??им ??т?м?л?р индер?. Ул ирекле атом ??м баш?алар мен?н берл?шк?н атом ара?ында?ы аны? айырманы к?р??т?.. Бутлеров о?шаш к?ст?р?е тулы?ынса фай?аланыу ??м ≪я?ынлы? к?с?рг?неше≫, й??ни молекулала?ы атомдар?ы? ??-ара йо?онто?о ар?а?ында барлы??а килг?н б?йл?нешт?р?е? энергетик я?тан эквивалент?ы? булыуы тура?ында т?ш?нс? индер?.Ошо ??-ара йо?онто ????мт??енд? атомдар, структура?ына ?арап, т?рл? ≪химик ?имм?тк?≫ эй? була. Бутлеров теория?ы органик берл?шм?л?р?е? изомерлы?ына ??м улар?ы? реакция?а ине?ен? ?а?ылышлы бик к?п факттар?а а?латма бирерг? м?мкинлек бир?.
Молекуланы?
к?рг??м? ??р?тен т?ш?р?? м?мкинлеге л? валентлы? теория?ыны? ?ур ??т?нл?г? була. 1860-сы йылдар?а т??ге молекуляр моделд?р барлы??а кил?. 1864 йылда у? А. Браун структуралы формулалар?ы улар?а урынлаш?ан ??м атомдар ара?ында химик б?йл?неште билд?л??се ?ы?ы?тар мен?н тоташтырыл?ан элементтар символдары бул?ан т???р?кт?р р??ешенд? фай?аланыр?а т??дим ит?; ?ы?ы?тар ?аны атом валентлы?ына тап кил?.1865 йылда А. фон Гофман т??ге шар стерженле моделд?р к?р??т?, улар?а атомдар ролен крокет шар?ары алмаштарыа. 1866 йылда Кекуле д?реслегенд? тетраэдр конфигурация?ы бул?ан стереохимик моделд?р?е? ??р?тт?ре ба?ыла.
Т???? валентлы? бер?меге итеп
водород
атомыны? валентлы?ы ?абул ител?. Икенсе элементты? валентын ??ен? ?ушыл?ан й?ки был икенсе элементты? бер атомын алмаштыр?ан водород атомдары ?аны мен?н к?р??терг? м?мкин. Шул р??ешле билд?л?нг?н валентлы? водород берл?шм?л?ренд? валентлы? й?ки водород буйынса валентлы? тип атала: HCl, H
2
O, NH
3
, CH
4
м???л?н,
хлор?ы?
водород буйынса валентлы?ы ? 1-г?, кислородты?ы ? 2-г?, азотты?ы ? 3-к?, углеродты?ы ? 4-к? тиге?.
Кислородты?
валентлы?ы, ?а?и?? булара?, икег? тиге?. Шу?а к?р?, теге й?ки был элементты? кислород берл?шм??е составын й?ки формула?ын белеп, уны? валентлы?ын был элементты? бер атомын тоташтыра ал?ан кислород
атомдарыны?
икел?т? ?аны итеп билд?л?рг? м?мкин. Шул р??ешле билд?л?нг?н валентлы? элементты? кислород берл?шм?л?ренд?ге валентлы?ы й?ки кислород буйынса валентлы?ы тип атала: м???л?н, K
2
O, CO,
N
2
O
3
, SiO
2
, SO
3
берл?шм?л?ренд?
калий?ы?
кислород буйынса валентлы?ы ? 1-г?,
углеродты?ы
? 2-г?,
азотты?ы
? 3-к?,
кремний?ы?ы
? 4-к?,
к?к?ртт?к?
? 6-?а тиге?.
К?пселек элементтар?а кислород ??м водород берл?шм?л?ренд? валентлы?ты? м???н??е т?рл?с?: м???л?н, водород буйынса к?к?ртт?? (H
2
S) валентлы?ы ? 2-г?, ? кислород буйынса ? 6-?а (SO
3
). Бынан тыш, элементтар?ы? к?бе?е т?рл? берл?шм?л?р?? т?рл? валентлы?ты (?ай?ы бер элементтар?ы? гидридтары ла, оксидтары ла булмауы м?мкин) к?р??т?. М???л?н, углерод кислород мен?н ике оксид барлы??а килтер?: СО монооксид углероды ??м CO
2
углерод диоксиды Углерод монооксидында углерод валентылы?ы ? 2-г?, ? диоксидта 4-к? тиге? (?ай?ы бер элементтар шулай у? пероксидтар барлы??а килтер? ала). Тикшерелг?н ми?алдар?ан к?рене?енс?, элементты? валентлы?ын, ?а?и?? булара?, бер ?ан ??м/й?ки ысул мен?н ба?алау м?мкин т?гел.
Химик б?йл?неш теория?ы барлы??а килг?нд?н алып ≪валентлы?≫ т?ш?нс??е ?и?елерлек эволюция кисер?. ?леге ва?ытта уны? аны? ф?нни а?латма?ы ю?, шу?а к?р? ф?нни лексиканан тулы?ынса тиерлек ?ы?ыры?лап сы?арыл?ан ??м башлыса методик ма?сатта фай?аланыла.
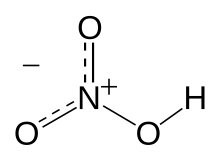 HNO3 молекула?ында ковалентлы б?йл?нешт?р булдырыу?ы? резонанс моделе
HNO3 молекула?ында ковалентлы б?йл?нешт?р булдырыу?ы? резонанс моделе
Ниге???, химик элементтар?ы? валентлы?ында, ????тт?, уны? ирекле атомдарыны? билд?ле бер ?анда ковалент б?йл?нешт?р барлы??а килтере?г? ??л?тлелеге (тарыра? м???н?л? ? уны? ??л?тлелек ?лс?ме) а?латыла. Ковалент б?йл?нешле берл?шм?л?р?? атомдар?ы? валентлы?ы барлы??а килг?н ике электрон ике ???кле б?йл?нешт?р ?аны мен?н билд?л?н?. 1927 йылда В. Гайтлер ??м Ф. Лондон т??дим итк?н локаль валентлы? б?йл?нешт?ре теория?ында тап ошондай алым ?абул ител?. ?г?р атомда
n
пар?ы? электрондар ??м
m
б?ленм?г?н электрон пар?ар бар ик?н, был атом баш?а атомдар мен?н
n + m
ковалент б?йл?нешт?р барлы??а килтере?е м?мкин
[3]
. Максималь валентлы?ты ба?ала?анда гипотетик ≪яр?ыулы≫ (валентлы?) х?лене? электрон конфигурация?ынан сы?ып эш ител?. М???л?н, бор, углерод, азот атомыны? максималь валентлы?ы ? 4 (м???л?н, [BF4],CH4 ??м [NH4]+),
фосфор
? 5 (PCl5),
к?к?рт
? 6 (H2SO4), ?
хлор
? 7 (Cl2O7).
Атом барлы??а килтер? ал?ан б?йл?нешт?р ?аны уны? д?й?м электрон пар?ары (молекуляр ике электрон болот) барлы??а киле?г? бар?ан пар?ы? электрондары ?анына тиге?. Ковалентлы б?йл?неш донор-акцептор механизмы яр?амында ла барлы??а кил? ала. Ике осра?та ла б?йл?неш барлы??а килтерг?н полярлы? и??пк? алынмай, шунлы?тан валентлы? там?а?ы? була ? окисланыу торошонан айырмалы р??ешт? ы??ай ?а, кире л? була алмай (N2, NO2, NH3 ??м [NH4]+).
 Этан молекула?ыны? структур формула?ы
Этан молекула?ыны? структур формула?ы
Водород ??м кислород буйынса валентлы?тан тыш, был элемент атомдарыны? бер-бере?е й?ки баш?а элементтар атомдары мен?н берл?ше? ??л?те ?ай?ы бер осра?тар?а элементты? окисланыу д?р?ж??ен ковалентлы?ты асы?лар?а ??м баш?а ысулдар мен?н тиге?л?рг? м?мкин. Был характеристикалар я?ын ??м хатта ?ан я?ынан тура килерг? м?мкин, л?кин бер-бере?ен? тождество булма??а тейеш
[4]
. М???л?н, N2 азотыны? изоэлектрон молекулаларында CO углерод оксиды ??м цианид ионы CN?, ?сл?т? б?йл?неш баш?ара (й??ни ??р атомды? валентлы?ы ? 3), л?кин элементтар?ы? окисланыу д?р?ж??е ? 0, +2, +2, +3 ??м ?3. Этан молекула?ында (??р?тте ?ара) углерод к?пселек органик берл?шм?л?р??ге ке?ек тетравалентлы, ? окисланыу д?р?ж??е ?3.
Был бигер?к т? делокализациялан?ан химик б?йл?нешле молекулалар?а ?а?ыла; м???л?н, азот кислота?ында азотты? окисланыу д?р?ж??е +5, ? азотты? валентлы?ы 4-т?н ю?ары була алмай. К?п кен? м?кт?п д?реслект?рен?н билд?ле ?а?и?? ? ≪Элементты? максималь валентлы?ы ?ан я?ынан Периодик таблицала?ы т?рк?м номерына тиге?≫ ? тик окисланыу д?р?ж??ен? ген? ?арай. ≪Даими валентлы?≫ ??м ≪??г?ре?с?н валентлы?≫ т?ш?нс?л?ре л? башлыса окисланыу д?р?ж??ен к???? тота.
Ете поляр (семиполярные) ??м донор-акцепторлы (датив) б?йл?нешт?р асылда ≪икел?т?≫ б?йл?нешт?р булып тора, с?нки улар барлы??а килг?нд? ике процесс та бара: электронды? к?сереле?е (ионлы элемт?не? барлы??а киле?е) ??м электрондар?ы? д?й?мл?штереле?е (ковалентлы б?йл?неште? барлы??а киле?е).
?г?р ике электронлы ике ???кле б?йл?неш моделен ?улланыу м?мкин булма?а
[5]
??м ковалентлы берл?шм?л?р ю? ик?н, валентлы? т?ш?нс??ен ?улланыр?а ярамай. Валентлы? кластер берл?шм?л?рен, бороводородтар?ы, карборндар?ы, затлы газ берл?шм?л?рен ??м баш?алар?ы тасуирлау ?с?н ?улланылмай. М???л?н, ?елтеле металл катиондары краун-эфирлы комплекстар?а улар?ы? окисланыу ким?лен?н валентлы? к?пк? ю?арыра? к?р??т?.
Ионлы кристалл т???л?ш? бул?ан берл?шм?л?р?е тасуирлау ?с?н валентлы? ?улланыу д?р?? булма? ине. ?йт?йек, натрий хлориды NaCl кристаллында ??р ион Na+й?ки Cl ? ? бер?мек к???н?кте? ???ге ? к?рше иондар?ы? реаль ?аны ? координация ?аны ? 6, ? окисланыу д?р?ж??ен? ярашлы р??ешт? +1 ??м ?1 т?шкил ит?. Локалл?штерелг?н электрон пар?ар б?т?нл?й ю?.
Х??ерге химияла молекуляр орбиталдар ысулы ???ем ?улланыла, улар?а атомды? валентлы?ы т?ш?нс??е аналогтары ю?
[4]
.Шул у? ва?ытта химик б?йл?неште? к?плеге т?ш?нс??е барлы??а киле?се б?йл?нешт?р ?анына хас. Ике электрон молекуляр орбиталь мен?н бер??м б?йл?неште асы?лау тик экстремаль, локалл?штерелг?н осра?та ?ына м?мкин
[6]
. Квант химия?ында валентлы? т?ш?нс??ене? молекулала?ы атом характеристика?ы булара? аналогы ю?, ? ?улланыл?ан спин-валентлы? т?ш?нс??е айырым атом?а ?арай
[7]
Элментты? ковалентлы?ы
(элементтар?ы? валент м?мкинлект?ре ?лс?ме; ?ый?ырышлы?ы) пар?ы? электрондар?ы? д?й?м ?аны мен?н билд?л?н?
[8]
атомды?
нормаль
??м
яр?ыу
х?лд? (
матд? атомы электрондарыны? я?тылы? т?ш?? й?ки баш?а юл мен?н т?ь?ирл?неп, беренсе стационар х?лд?н икенсе стационар х?лг? к?се?е
), икенсе т?рл? ?йтк?нд?, атом барлы??а килтерг?н ковалентлы б?йл?нешт?р ?аны (углерод 2s22p2 II ковалентлы, ? яр?ы?ан х?лд? C*2s12p3 IV-ковалентлы; шулай итеп, CO ??м CO2-л? валентлы? ? II й?ки IV, ? ковалентлы? ? II ??м/й?ки IV). , Азотты? N2, NH3, Al≡N ??м Сa = N-C≡N молекулаларында кислород коваленты ? 3-к?, H2O ??м CO2 молекулаларында кислород ковалентлы?ы ? 2-г?, CH
4
, СО2 молекулаларында ??м (алмас) кристалында углерод ковалентлы?ы ? 4-к? тиге?.
Классик й?ки кванттан ?у??ы химик са?ылышта ике атомлы молекулалар?ы? электрон йотоу спектрынан бирелг?н энергия?ында оптик (валентлы?) электрондар ?анын билд?л?рг? м?мкин
[9]
. Был ысул?а ярашлы, корреляция тура ?ы?ы?тарыны? ауышлы? м?й?ш? тангенсыны? кире д??м?ле валентлы электрондар пар?ары ?анына тап кил?
[10]
.
Ошо берл?шм?л? валентлы? (стехиометрик), уны? атомдарыны? моляр масса?ы ??м уны? эквивалент масса?ы ара?ында туранан-тура атом теория?ынан барлы??а килг?н ≪эквивалент масса≫ т?ш?нс??ен билд?л??се ябай нисб?т бар.
Элементты? был берл?шм?л?ге
стехиометрик валентлы?ы
[11]
уны? атомдарыны? молекуляр масса?ына тиге? (г/моль), элементты? эквивалент масса?ына (г/моль) б?ленг?н :

V ? Стехиометрик валентлы?;
M ? Молекуляр масса (г/моль);
E ? Эквивалентлы масса (г/моль);
М???л?н, -углеродты? стехиометрик валентлы?ы CO 12 (г/моль) /6 (г/моль) = 2, ? CO2 12 /3 = 4.
Органик булма?ан химияла
к?п осра?та элементты? валентлы? т?ш?нс??е билд?лелеген ю?алта: был д??м?л берл?ше??е? химик т???л?ш?н беле?г? б?йле, к?п осра?та ул т?рк?м номерынан к?бер?к булыуы м?мкин (таблица
ПСХЭ
). Органик булма?ан химияла ????тт? ? окисланыу д?р?ж??е, ?
органик химияла
валентлы? т?ш?нс??е ?улланыла, с?нки органик булма?ан матд?л?р?е? к?бе?е молекуляр булма?ан, ? органик химияла молекуляр т???л?шл?. Был ике т?ш?нс? ?ан я?ынан тура кил?? л?, улар?ы тиге?л?рг? ярамай. Шулай у? ≪валентлы электрондар≫ термины, й??ни атом ядро?ы мен?н ны? б?йл?нм?г?нд?ре, йышыра? тыш?ы электрондар, ки? ?улланыла. Шулай у? ≪
валентлы электрондар
>≫ термины, й??ни атом ядро?ы мен?н ны? б?йл?нм?г?нд?ре, йышыра? тыш?ы электрондар, ки? ?улланыла.
Элементтар?ы? валентлы?ы буйынса берл?шм?л?р?е? ысын формулаларын т???рг? м?мкин, ??м, кире?енс?, ысын формулалар?ан сы?ып, был берл?шм?л?р?? элементтар?ы? валентлы?ын билд?л?рг? м?мкин. Шул у? ва?ытта бер элементты? валентлы? ?абатланды?ы уны? атомдары ?анына икенсе элементты? валентлы?ы ?абатланды?ына тиге? тиг?н принципты и?т? тотор?а к?р?к. М???л?н, азот оксиды (III) формула?ын т???? ?с?н химик там?аны? ??т?н? валентлы?тарын я?ып ?уялар

 . И? б?л?к?й урта? б?лене?сене билд?л?п ??м уны тейешле валентлы??а б?леп, азотты? кислород?а ?арата атом нисб?тен алабы?, атап ?йтк?нд?, 2:3. Ошонан сы?ып, азот (III) оксиды формула?ы ?
. И? б?л?к?й урта? б?лене?сене билд?л?п ??м уны тейешле валентлы??а б?леп, азотты? кислород?а ?арата атом нисб?тен алабы?, атап ?йтк?нд?, 2:3. Ошонан сы?ып, азот (III) оксиды формула?ы ?
 .
.
Ошо р??ешле валентлы?ты билд?л?? ?с?н кире?енс? эшл?й??р.
- ↑
Partington, J.R.
A Short History of Chemistry
. ? Dover Publications, Inc, 1989. ?
ISBN 0-486-65977-1
.
- ↑
Frankland E.
On a New Series of Organic Bodies Containing Metals. // Phil. Trans. 1852. Vol. 142. P. 417?444.
- ↑
Неорганическая химия / Б. Д. Степин, А. А. Цветков ; Под ред. Б. Д. Степина. ? М.: Высш. шк., 1994. ? С. 71?72
- ↑
4,0
4,1
Валентность атомов в молекулах / Корольков Д. В. Основы неорганической химии. ? М.: Просвещение, 1982. ? С. 126
- ↑
Развитие учения о валентности. Под ред.
Кузнецова В. И.
М.: Химия, 1977. стр.19.
- ↑
Татевский В. М.
Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. Глава 3.
- ↑
Татевский В. М.
Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. Глава 3.
- ↑
в том числе в донорно-акцепторной связи
- ↑
Серов Н. В. Электронные термы простых молекул // Оптика и спектроскопия, 1984, Т.56, вып.3, с. 390?406.
- ↑
Ionov S.P. and Kuznetsov N.T. Excited and Ionized and States of H2 in Terms of the Structural Thermodynamic Model// Russian Journal of Inorganic Chemistry Vol. 50, No. 2, February 2005, pp. 233?237
- ↑
В предположении что Валентность неизвестна, но известны молекулярная масса и эквивалентная масса соединения.
- Окисланыу д?р?ж??е
- Координация ?аны
- Л. Паулинг
Природа химической связи. М., Л.: Гос. НТИ хим. литературы, 1947.
- Картмелл, Фоулс. Валентность и строение молекул. М.: Химия, 1979. 360 с.]
- Коулсон Ч.
Валентность. М.: Мир, 1965.
- Маррел Дж., Кеттл С., Теддер Дж.
Теория валентности. Пер. с англ. М.: Мир. 1968.
(недоступная ссылка)
- Развитие учения о валентности. Под ред.
Кузнецова В. И.
М.: Химия, 1977. 248с.
- Валентность атомов в молекулах / Корольков Д. В. Основы неорганической химии. ? М.: Просвещение, 1982. ? С. 126.