 Dmitri Mendelejef
, die vader van die moderne periodieke tabel. Portret deur
Ilja Repin
.
Dmitri Mendelejef
, die vader van die moderne periodieke tabel. Portret deur
Ilja Repin
.
 Mendelejef se periodieke tabel uit sy boek.
Mendelejef se periodieke tabel uit sy boek.
Die
periodieke tabel
is 'n voorstelling van die bekende
chemiese elemente
, gerangskik volgens hul
atoomgetal
, elektronkonfigurasie en chemiese eienskappe. Elemente word gerangskik volgens toenemende atoomgetal (die getal
protone
). Die standaardvorm van die tabel bestaan uit ’n rooster van 18 x 7 blokkies, wat die hoofdeel vorm, plus ’n kleiner deel van twee rye onderaan.
Die tabel kan ook verdeel word in vier reghoekige blokke: die
s-blok
links, die
p-blok
regs, die
d-blok
in die middel en die
f-blok
daaronder. Die rye van die tabel word
periodes
genoem en die kolomme van die s-, d- en p-blok
groepe
; sommige van hulle het name soos
halogene
of
edelgasse
. Aangesien die periodieke tabel chemiese tendense behels, kan dit gebruik word om die verhouding tussen eienskappe van die elemente af te lei en om die eienskappe van nuwe, nog onontdekte elemente of sinteties vervaardigde elemente te voorspel.
Hoewel periodieke tabelle vantevore bestaan het, word
Dmitri Mendelejef
oor die algemeen beskou as die vader van die huidige tabel, wat hy in 1869 gepubliseer het. Dit is die eerste een wat algemeen aanvaar is. Hy het die tabel ontwikkel om tendense in die eienskappe van die destyds bekende elemente te illustreer. Hy het ook van die eienskappe van toe nog onbekende elemente voorspel na aanleiding van lee ruimtes in die tabel. Die meeste van sy voorspellings het korrek blyk te wees toe die elemente later ontdek is. Mendelejef se periodieke tabel is sedertdien uitgebrei en verfyn met die ontdekking of sintetiese vervaardiging van nog nuwe elemente en die ontwikkeling van nuwe teoretiese modelle om chemiese gedrag te verduidelik.
Alle elemente van 1 (
waterstof
) tot 118 (
oganesson
) is al ontdek of sinteties vervaardig. Die elemente van 1 tot 98 (
kalifornium
) bestaan natuurlik, hoewel sommige net in klein hoeveelhede voorkom en aanvanklik ontdek is toe hulle sinteties vervaardig is. Die elemente na 98 is sinteties vervaardig in
laboratoriums
. Die vervaardiging van elemente na oganesson word beplan en voortdurende debatte word gevoer oor hoe die periodieke tabel verander sal moet word as enige sulke elemente bykom.
Uitleg
So lyk die huidige periodieke tabel van bekende chemiese elemente. Elemente waarvan die atoomgetal in rooi aangedui word, is sinteties vervaardig. Die eienskappe van elemente op ’n liggrys agtergrond is onbekend.
| Groep
→
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
| ↓
Periode
|
|
| 1
|
Waterstof
1
H
1,008
|
|
Helium
2
He
4,0026
|
| 2
|
Litium
3
Li
6,94
|
Berillium
4
Be
9,0122
|
|
Boor
5
B
10,81
|
Koolstof
6
C
12,011
|
Stikstof
7
N
14,007
|
Suurstof
8
O
15,999
|
Fluoor
9
F
18,998
|
Neon
10
Ne
20,180
|
| 3
|
Natrium
11
Na
22,990
|
Magne-
sium
12
Mg
24,305
|
|
Alumi-
nium
13
Al
26,982
|
Silikon
14
Si
28,085
|
Fosfor
15
P
30,974
|
Swael
16
S
32,06
|
Chloor
17
Cl
35,45
|
Argon
18
Ar
39,948
|
| 4
|
Kalium
19
K
39,098
|
Kalsium
20
Ca
40,078
|
Skandium
21
Sc
44,956
|
Titaan
22
Ti
47,867
|
Vanadium
23
V
50,942
|
Chroom
24
Cr
51,996
|
Mangaan
25
Mn
54,938
|
Yster
26
Fe
55,845
|
Kobalt
27
Co
58,933
|
Nikkel
28
Ni
58,693
|
Koper
29
Cu
63,546
|
Sink
30
Zn
65,38
|
Gallium
31
Ga
69,723
|
Germa-
nium
32
Ge
72,630
|
Arseen
33
As
74,922
|
Seleen
34
Se
78,971
|
Broom
35
Br
79,904
|
Kripton
36
Kr
83,798
|
| 5
|
Rubidium
37
Rb
85,468
|
Stronsium
38
Sr
87,62
|
Yttrium
39
Y
88,906
|
Sirko-
nium
40
Zr
91,224
|
Niobium
41
Nb
92,906
|
Molib-
deen
42
Mo
95,95
|
Tegne-
sium
43
Tc
[97]
|
Rutenium
44
Ru
101,07
|
Rodium
45
Rh
102,91
|
Palladium
46
Pd
106,42
|
Silwer
47
Ag
107,87
|
Kadmium
48
Cd
112,41
|
Indium
49
In
114,82
|
Tin
50
Sn
118,71
|
Antimoon
51
Sb
121,76
|
Telluur
52
Te
127,60
|
Jodium
53
I
126,90
|
Xenon
54
Xe
131,29
|
| 6
|
Sesium
55
Cs
132,91
|
Barium
56
Ba
137,33
|
*
|
Hafnium
72
Hf
178,49
|
Tantaal
73
Ta
180,95
|
Wolfram
74
W
183,84
|
Renium
75
Re
186,21
|
Osmium
76
Os
190,23
|
Iridium
77
Ir
192,22
|
Platinum
78
Pt
195,08
|
Goud
79
Au
196,97
|
Kwik
80
Hg
200,59
|
Tallium
81
Tl
204,38
|
Lood
82
Pb
207,2
|
Bismut
83
Bi
208,98
|
Polonium
84
Po
[209]
|
Astaat
85
At
[201]
|
Radon
86
Rn
[222]
|
| 7
|
Frankium
87
Fr
[223]
|
Radium
88
Ra
[226]
|
* *
|
Ruther-
fordium
104
Rf
[267]
|
Dubnium
105
Db
[268]
|
Sea-
borgium
106
Sg
[269]
|
Bohrium
107
Bh
[270]
|
Hassium
108
Hs
[270]
|
Meit-
nerium
109
Mt
[278]
|
Darm-
stadtium
110
Ds
[281]
|
Ront-
genium
111
Rg
[282]
|
Koperni-
kium
112
Cn
[285]
|
Nihonium
113
Nh
[286]
|
Flero-
vium
114
Fl
[289]
|
Mosko-
vium
115
Mc
[290]
|
Liver-
morium
116
Lv
[293]
|
Tennes-
sien
117
Ts
[294]
|
Oganes-
son
118
Og
[294]
|
|
| *
Lantaniede
|
Lantaan
57
La
138,91
|
Serium
58
Ce
140,12
|
Praseodi-
mium
59
Pr
140,91
|
Neodi-
mium
60
Nd
144,24
|
Prome-
tium
61
Pm
[145]
|
Sama-
rium
62
Sm
150,36
|
Euro-
pium
63
Eu
151,96
|
Gadoli-
nium
64
Gd
157,25
|
Terbium
65
Tb
158,93
|
Dispro-
sium
66
Dy
162,50
|
Holmium
67
Ho
164,93
|
Erbium
68
Er
167,26
|
Tulium
69
Tm
168,93
|
Ytterbium
70
Yb
173,05
|
Lutesium
71
Lu
174,97
|
| * *
Aktiniede
|
Aktinium
89
Ac
[227]
|
Torium
90
Th
232,04
|
Protakti-
nium
91
Pa
231,04
|
Uraan
92
U
238,03
|
Neptu-
nium
93
Np
[237]
|
Pluto-
nium
94
Pu
[244]
|
Ameri-
kium
95
Am
[243]
|
Curium
96
Cm
[247]
|
Berke-
lium
97
Bk
[247]
|
Kalifor-
nium
98
Cf
[251]
|
Einstei-
nium
99
Es
[252]
|
Fermium
100
Fm
[257]
|
Mendele-
vium
101
Md
[258]
|
Nobelium
102
No
[259]
|
Lawren-
sium
103
Lr
[266]
|
Standaardatoomgewig
A
r, std
(E) Ca: 40,078
? amptelike kort waarde, afgerond (geen onsekerheid)
- Po: [209] ?
massagetal
van die stabielste
isotoop
Alle weergawes van die periodieke tabel bevat net chemiese elemente, nie samestellings of
elementere deeltjies
nie. Elke chemiese element het ’n unieke atoomgetal wat ooreenstem met die getal protone in sy kern. Die meeste elemente het ’n verskillende aantal
neutrone
in verskillende atome, en die variasies word
isotope
genoem.
Koolstof
het byvoorbeeld drie isotope wat in die natuur voorkom: al sy atome het ses protone en die meeste het ook ses neutrone, maar sowat 1 persent het sewe neutrone en ’n baie klein aantal het agt neutrone. Isotope word nooit apart in periodieke tabelle aangetoon nie; hulle word altyd saam as een element gegroepeer.
In die standaardmodel word die elemente gelys in volgorde van toenemende atoomgetalle. ’n Nuwe periode (ry) begin wanneer ’n nuwe elektronskil sy eerste elektron het. Groepe (kolomme) word bepaal deur die elektronkonfigurasie van die atoom; elemente met dieselfde getal elektrone in ’n spesifieke subskil val in dieselfde kolom (
suurstof
en
seleen
is byvoorbeeld in dieselfde kolom omdat albei vier elektrone in die buitenste p-subskil het). Elemente met soortgelyke chemiese eienskappe val gewoonlik in dieselfde groep in die periodieke tabel, hoewel elemente in dieselfde periode in die f-blok, en in ’n mate in die d-blok, geneig is om ook soortgelyke eienskappe te he. Dit is dus relatief maklik om die chemiese eienskappe van ’n element te voorspel as die eienskappe van die omringende elemente bekend is.
[1]
Sedert 2012 bevat die periodieke tabel 118 bevestigde chemiese elemente. Altesaam 98 kom in die natuur voor, waarvan 84 oorspronklik is. Die ander 14 natuurlike elemente kom net voor in
vervalreekse
van oorspronklike elemente.
[2]
Alle elemente van
einsteinium
(99) tot oganesson (118) word erken al is hulle sinteties vervaardig en kom hulle nie in die natuur voor nie.
Groepering
Groepe
’n "Groep" of "familie" is ’n vertikale kolom in die periodieke tabel. Elemente in dieselfde groep het ooreenstemmende chemiese eienskappe. Byvoorbeeld die verbindings met waterstof in kolom 17 het die formule
HX
: HF, HCl, HBr, HI, terwyl in kolom 16 dit juis
H
2
X
is:
H
2
O
,
H
2
S
,
H
2
Se
,
H
2
Te
. In een kolom toon van die eienskappe ’n duidelike tendens met die toename van die atoomgetal.
[3]
In sommige dele van die tabel, soos in die d- en f-blok, kan horisontale ooreenkomste egter net so belangrik of duideliker wees as vertikale ooreenkomste.
[4]
[5]
[6]
Die groepe word van 1-18 genommer, van die linkerkantse kolom (die
alkalimetale
) tot die regterkantse kolom (die
edelgasse
).
[7]
Voorheen is hulle in Romeinse syfers gemerk.
Elemente in dieselfde groep neig om patrone te toon in
atoomradius
,
ionisasie-energie
en
elektronegatiwiteit
. Van bo na onder in ’n groep neem die atoomradius van die elemente toe; elektrone kom dus verder van die kern af voor. Van bo na onder neem die ionisasie-energie af, want dit is makliker om ’n elektron te verwyder omdat die atome se verbinding nie so sterk is nie. Net so neem elektronegatiwiteit af van bo na onder.
[8]
Daar is egter uitsonderings op die reel, soos in groep 11, waar die elektronegatiwiteit verder af in die groep toeneem.
Periodes
’n "Periode" is ’n horisontale ry in die periodieke tabel. Hoewel vertikale ooreenkomste gewoonlik groter is, is daar dele van die tabel waar die horisontale ooreenkomste groter is, soos in die f-blok, waar die
lantaniede
en
aktiniede
twee duidelike horisontale reekse elemente is.
[9]
 Die verskillende blokke in die periodieke tabel.
Die verskillende blokke in die periodieke tabel.
Elemente in dieselfde periode toon tendense in die atoomradius, ionisasie-energie en elektronegatiwiteit. Van links na regs in die tabel neem die atoomradius gewoonlik af. Dit gebeur omdat elke opeenvolgende element ’n bykomende proton en elektron het, wat veroorsaak dat die elektron meer deur die kern aangetrek word.
[10]
Dit veroorsaak dat die ionisasie-energie van links na regs toeneem: hoe meer die elektrone deur die kern aangetrek word, hoe meer energie is nodig om ’n elektron te verwyder. Net so neem elektronegatiwiteit van links na regs toe.
[8]
Elektronaffiniteit toon ook ’n tendens. Metale (links) het gewoonlik ’n laer elektronaffiniteit as die nie-metale (regs), met die uitsondering van die edelgasse.
[11]
Blokke
Vanwee die belangrikheid van die buitenste elektronskil word die verskillende areas van die periodieke tabel soms "blokke" genoem, waarvan die name verwys na die subskil met die "laaste" elektron. Die s-blok bevat die eerste twee groepe (alkalimetale en aardalkalimetale) sowel as waterstof en
helium
. Die p-blok bevat die laaste ses groepe: van 13 tot 18, onder meer die metalloides. Die d-blok bevat groep 3 tot 12, onder meer al die oorgangsmetale. Die f-blok, wat gewoonlik onderaan die res van die tabel aangetoon word, bevat die lantaniede en aktiniede.
[12]
Variasies
Die lantaniede en aktiniede word gewoonlik onderaan die res van die periodieke tabel aangetoon, soos heel bo.
[13]
Dit is bloot om estetiese en praktiese redes. Hulle kan ook deel van die hooftabel vorm en op hul regte plek as deel van die sesde en sewende periode ingevoeg word om ’n bree tabel te vorm, soos onder aangedui:
Periodieke eienskappe
Talle eienskappe van die elemente, soos die atoomradius, die ionisasie-energie, die elektronegativiteit, die smeltpunte en so meer vertoon 'n periodieke gedrag en die tabel kan gebruik word om dit in kaart te bring.
Elektronegativiteit
Hierdie belangrike kenmerk van 'n element se eienskappe bepaal hoofsaaklik watter bindings die element met ander elemente kan vorm. Langs die hoofdiagonaal van
frankium
(linksonder) na
fluoor
(regsbo) neem die waarde van die elektronegatiwiteit toe, maar daar is ook party eilande met taamlik hoe waardes (sien wolfram, goud, lood).
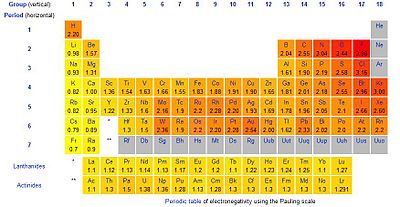 Elektronegatiwiteit van die elemente
Elektronegatiwiteit van die elemente
Smeltpunt
Veral in die
d-blok
kan elemente 'm hoe smeltpunt bereik maar die diagonale groep van die
metalloiede
het ook hoe smeltpunte.
 Smeltpunte van die elemente
Smeltpunte van die elemente
Geskiedenis
Die periodieke tabel is oorspronklik ontwerp sonder kennis van die inwendige bou van die atoom. Die elemente is gerangskik volgens hul atoommassa. Die Duitser
Johann Wolfgang Doberreiner
was die eerste wat opgemerk het dat daar ’n golfbeweging ontstaan het in die eienskappe. Hy het
triade
van ooreenkomstige elemente onderskei. Die Engelsman
John Alexander Reina Newlands
het ontdek daar bestaan ’n reelmatigheid in elke 8 elemente, maar hy is bespot toe hy die vermoede uitspreek dat dit vergelykbaar met die oktawe in musiek kon wees. Uiteindelik het die Duitser
Lothar Meyer
en die Rus Dmitri Mendelejef die eerste perodieke tabel gepubliseer. Daarby het hulle die massa van
telluur
en
jodium
omgeruil. Dit het die ooreenstemming van tendense verbeter. Na die koms van die golfmeganika het dit duidelik geword dat hierdie stap geregverdig was.
Sien ook
Verwysings
- ↑
Gray, p. 6
- ↑
Emsley, John (2011).
Nature's Building Blocks: An A-Z Guide to the Elements
(New uitg.). New York, NY: Oxford University Press.
ISBN
978-0-19-960563-7
.
- ↑
Messler, R. W. (2010).
The essence of materials for engineers
. Sudbury, MA: Jones & Bartlett Publishers. p. 32.
ISBN
0-7637-7833-8
.
- ↑
Bagnall, K. W. (1967), "Recent advances in actinide and lanthanide chemistry", in Fields, PR; Moeller, T,
Advances in chemistry, Lanthanide/Actinide chemistry
,
71
, American Chemical Society, pp. 1?12,
doi
:
10.1021/ba-1967-0071
- ↑
Day, M. C.; Selbin, J. (1969).
Theoretical inorganic chemistry
(2de uitg.). New York, MA: Reinhold Book Corporation. p. 103.
ISBN
0-7637-7833-8
.
- ↑
Holman, J.; Hill, G. C. (2000).
Chemistry in context
(5de uitg.). Walton-on-Thames: Nelson Thornes. p. 40.
ISBN
0-17-448276-0
.
- ↑
Leigh, G. J. (1990).
Nomenclature of Inorganic Chemistry: Recommendations 1990
. Blackwell Science.
ISBN
0-632-02494-1
.
- ↑
8,0
8,1
Moore, p. 111
- ↑
Stoker, Stephen H. (2007).
General, organic, and biological chemistry
. New York: Houghton Mifflin. p. 68.
ISBN
978-0-618-73063-6
.
OCLC
52445586
.
- ↑
Mascetta, Joseph (2003).
Chemistry The Easy Way
(4th uitg.). New York: Hauppauge. p. 50.
ISBN
978-0-7641-1978-1
.
OCLC
52047235
.
- ↑
Kotz, John; Treichel, Paul; Townsend, John (2009).
Chemistry and Chemical Reactivity, Volume 2
(7de uitg.). Belmont: Thomson Brooks/Cole. p. 324.
ISBN
978-0-495-38712-1
.
OCLC
220756597
.
- ↑
Jones, Chris (2002).
d- and f-block chemistry
. New York: J. Wiley & Sons. p. 2.
ISBN
978-0-471-22476-1
.
OCLC
300468713
.
- ↑
Gray, p. 11
Bibliografie
- Ball, Philip (2002).
The Ingredients: A Guided Tour of the Elements
. Oxford: Oxford University Press.
ISBN
0-19-284100-9
.
- Chang, Raymond (2002).
Chemistry
(7th uitg.). New York: McGraw-Hill Higher Education.
ISBN
0-07-112072-6
.
- Gray, Theodore (2009).
The Elements: A Visual Exploration of Every Known Atom in the Universe
. New York: Black Dog & Leventhal Publishers.
ISBN
978-1-57912-814-2
.
- Huheey, JE; Keiter, EA; Keiter, RL.
Principles of structure and reactivity
(4th uitg.). New York: Harper Collins College Publishers.
ISBN
0-06-042995-X
.
- Moore, John (2003).
Chemistry for Dummies
. New York: Wiley Publications. p. 111.
ISBN
978-0-7645-5430-8
.
OCLC
51168057
.
- Scerri, Eric (2007).
The periodic table: Its story and its significance
. Oxford: Oxford University Press.
ISBN
0-19-530573-6
.
- Scerri, Eric R. (2011).
The periodic table: A very short introduction
. Oxford: Oxford University Press.
ISBN
978-0-19-958249-5
.
- Venable, F P (1896).
The development of the periodic law
. Easton PA: Chemical Publishing Company.
Eksterne skakels